Содержание
- 2. Основные термины занятия (часть 2) Качественный и количественный состав молекулы - Qualitative and quantitative composition of
- 3. Основные термины занятия (часть 3) Явление - effect Образование нескольких веществ - The formation of several
- 4. Основные термины занятия (часть 4) Число частиц - The number of particles Количество вещества - Amount
- 5. План занятия: Часть I Молекулы. Химические формулы. Молекулярные массы. Простые и сложные вещества. Валентность элементов. Моль.
- 6. Молекулы. При соединении атомов образуются молекулы.
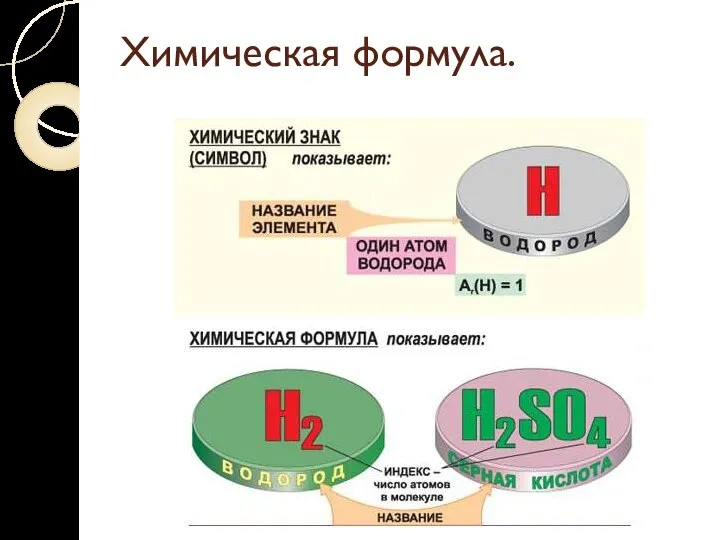
- 7. Химическая формула. Химическая формула - условное обозначение химического состава и структурыи структуры соединенийи структуры соединений с
- 8. Химическая формула.
- 9. Химическая формула.
- 10. Молекулярные массы. Масса любой молекулы равна сумме образующих ее атомов. Mr – относительная молекулярная масса. Рассчитайте
- 11. Молекулярные массы. Mr величина безразмерная! По формуле вещества можно рассчитать массовую долю каждого химического элемента, который
- 12. Массовая доля химического элемента в веществе.
- 13. Простые и сложные вещества. Все вещества делятся на простые и сложные. Простые Сложные
- 14. Простые и сложные вещества. Простые вещества имеют: Молекулярное строение: (фтор, хлор, азот, кислород) Атомное строение (железо,
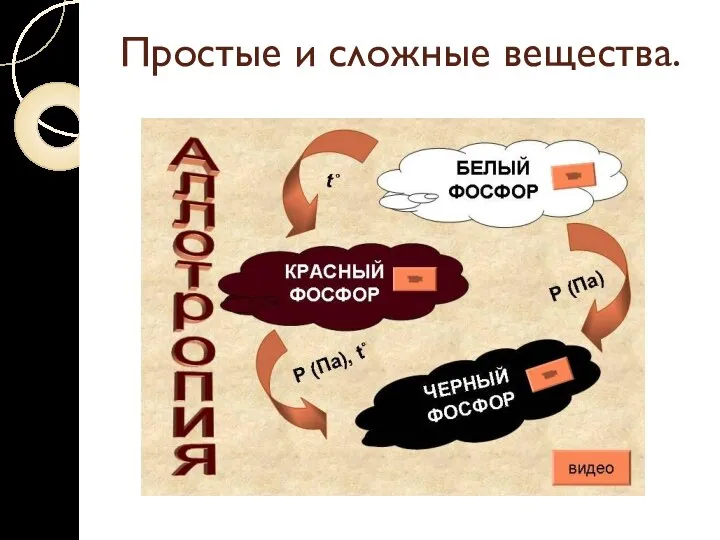
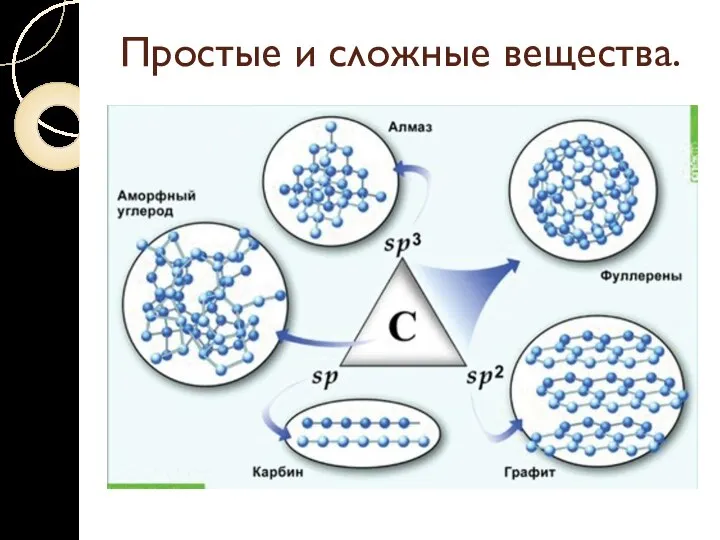
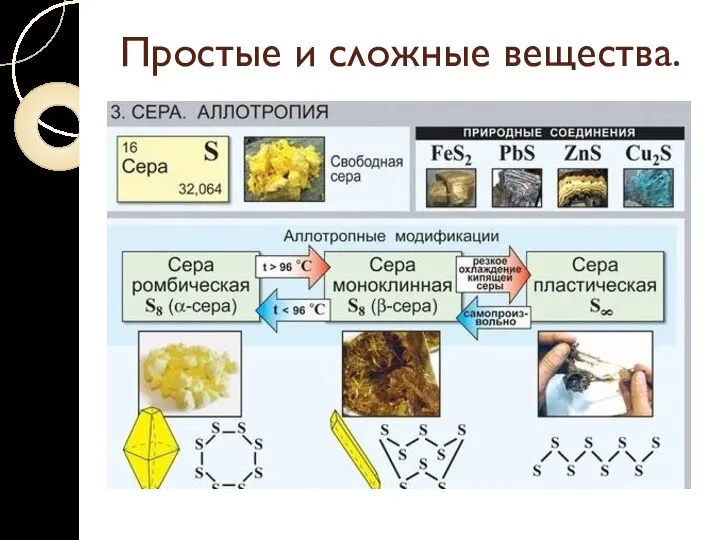
- 15. Простые и сложные вещества. Аллотропия – явление образования нескольких простых веществ одним элементом. Разные простые вещества,
- 16. Простые и сложные вещества.
- 17. Простые и сложные вещества.
- 18. Простые и сложные вещества.
- 19. Простые и сложные вещества. Сложные вещества.
- 20. Валентность элементов. Валентность обозначается римскими цифрами: I, II, III, IV, V, VI, VII, VIII
- 21. Валентность элементов. Элементы с постоянной валентностью I: H, F, щелочные металлы: Li, Na, K – образуют
- 22. Валентность элементов. Атомы этих элементов в разных соединениях могут образовывать разное число химических связей.
- 23. Валентность элементов.
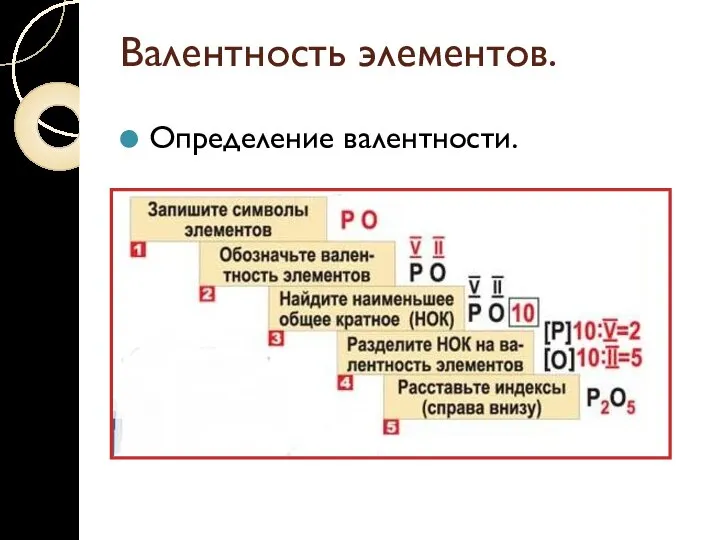
- 24. Валентность элементов. Определение валентности.
- 25. Наименьшее общее кратное (НОК) Наименьшее общее кратное двух целых чисел m и n есть наименьшее натуральное
- 26. Валентность элементов. Правило валентности: Определить валентность элементов в соединениях: PH3, P2O5 ,H2S, SiH4
- 27. Моль. Молярная масса. Единицей количества вещества является моль. Аа Рассчитаем сколько атомов С содержится в 12г
- 28. Моль. Молярная масса. Один моль любого вещества содержит столько молекул, сколько содержится в 12 граммах углерода!
- 29. Моль. Молярная масса. Если вещество состоит из молекул, то 1 моль это молекул этого вещества. Если
- 30. Моль. Молярная масса.
- 31. Моль. Молярная масса. Задача: Решение:
- 32. Моль. Молярная масса. Масса одного моля вещества называется молярной массой. Молярная масса выражается в г/моль.
- 33. Моль. Молярная масса. Определим молярные массы: Водорода Глюкозы Железа Зная молярную массу вещества М, можно рассчитать
- 35. Скачать презентацию



























 Алканы. Этан - C₂H₆
Алканы. Этан - C₂H₆ Кремний и его соединения
Кремний и его соединения Исследовательская работа Химические средства в быту
Исследовательская работа Химические средства в быту Арены. 10 класс
Арены. 10 класс Химический состав клетки. Неорганические вещества клетки
Химический состав клетки. Неорганические вещества клетки Химия-технологиялық процестеріндегі негізгі заңдылықтары. Технологиялық процестерідегі тепетеңдік
Химия-технологиялық процестеріндегі негізгі заңдылықтары. Технологиялық процестерідегі тепетеңдік Пресс - конференция «Карбоновые кислоты в природе, химические свойства, применение.»
Пресс - конференция «Карбоновые кислоты в природе, химические свойства, применение.» Презентация Строение и свойства циклоалканов.
Презентация Строение и свойства циклоалканов.  Органічні сполуки в побуті
Органічні сполуки в побуті Гидроксид магния. Mg(OH)2
Гидроксид магния. Mg(OH)2 Гидролиз. Применение
Гидролиз. Применение Определение формул органических веществ
Определение формул органических веществ Обменные реакции в растворах электролитов
Обменные реакции в растворах электролитов Кислотные и основные свойства органических соединений
Кислотные и основные свойства органических соединений Атомы. Молекулы. Ионы
Атомы. Молекулы. Ионы Карбоновые кислоты
Карбоновые кислоты Способы получения полимеров (Лекция 3)
Способы получения полимеров (Лекция 3) Гранулометрический метод контроля
Гранулометрический метод контроля Закономерности изменения металлических и неметаллических свойств элементов в периодах и группах (8 класс)
Закономерности изменения металлических и неметаллических свойств элементов в периодах и группах (8 класс) Төменгі фосфориттерден азот – фосфорлы тыңайтқыштар алу технологиясын әзірлеу
Төменгі фосфориттерден азот – фосфорлы тыңайтқыштар алу технологиясын әзірлеу Негізгі топша элементтерінің химиясы
Негізгі топша элементтерінің химиясы Эндогенная серия. Магматическая группа
Эндогенная серия. Магматическая группа Алканы. Предельные углеводороды. Парафины. Насыщенные углеводороды
Алканы. Предельные углеводороды. Парафины. Насыщенные углеводороды Химиялық кинетика
Химиялық кинетика Ток в жидкостях. Закон электролиза. Гальваностегия. Гальванопластика
Ток в жидкостях. Закон электролиза. Гальваностегия. Гальванопластика Тканые армирующие материалы
Тканые армирующие материалы Обмен липидов
Обмен липидов Презентация по Химии "Презентация Химический состав растений" - скачать смотреть
Презентация по Химии "Презентация Химический состав растений" - скачать смотреть