Содержание
- 2. Список рекомендуемой литературы 1. Основная литература: 1.1. Тимофеев В.С., Серафимов Л.А. Принципы технологии основного органического и
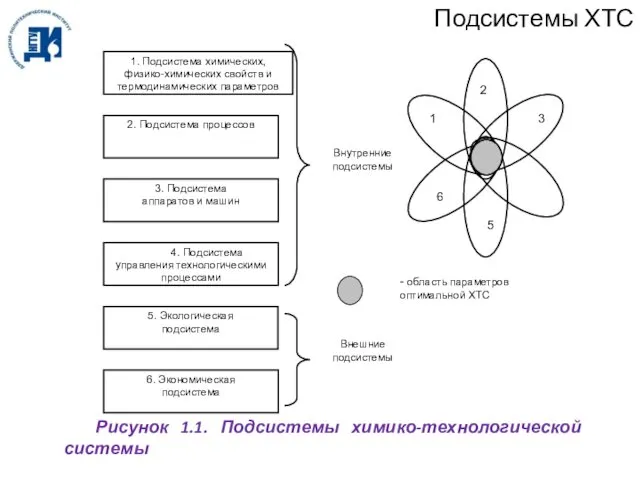
- 3. Подсистемы ХТС Рисунок 1.1. Подсистемы химико-технологической системы
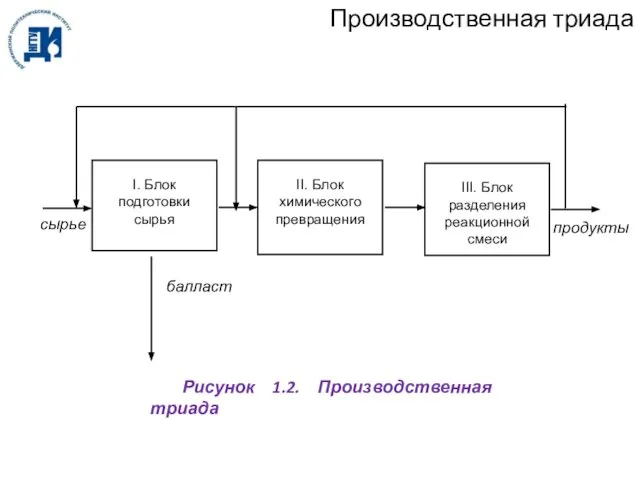
- 4. Рисунок 1.2. Производственная триада Производственная триада
- 5. Подсистема разделения При разработке технологии разделения необходимо решить следующие основные технологические задачи: 1. Определить последовательность выделения
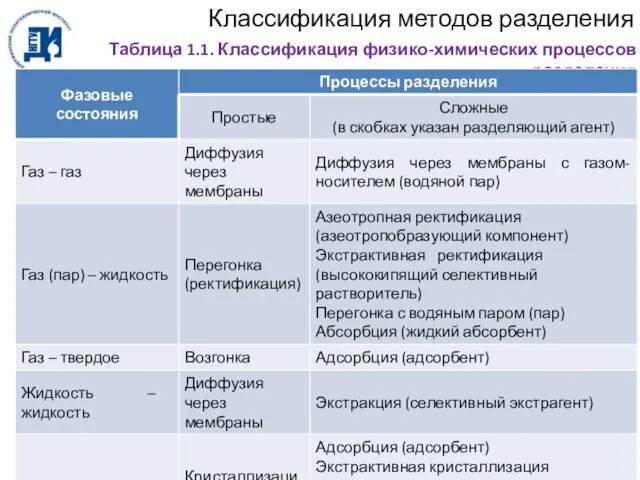
- 6. Классификация методов разделения Таблица 1.1. Классификация физико-химических процессов разделения
- 7. Массообменные процессы Процессами массообмена называют такие процессы, в которых основную роль играет перенос вещества из одной
- 8. Массообменные процессы 4. Адсорбция – избирательное поглощение газов, паров или растворенных в жидкости веществ твердым поглотителем,
- 9. Общее понятие о растворах Параметры состояния – любая величина, присущая телу, изменение которой определяется только начальным
- 10. Общее понятие о растворах Термодинамической системой называется произвольная система, выделенная из окружающей среды и изучаемая методами
- 11. Общее понятие о растворах Гетерогенной называется система, состоящая из двух или более различных гомогенных частей. Гомогенные
- 12. Общее понятие о растворах Гомогенная система или фаза гетерогенной системы, состоящая из нескольких чистых веществ, называется
- 13. Способы выражения состава смеси Мольная доля показывает, какая часть молекул смеси принадлежит данному компоненту: где ni
- 14. Способы выражения состава смеси Между различными способами выражения состава смеси существует вполне определенная связь. Так, количество
- 15. Способы выражения состава смеси Таблица 2.1. Способы выражения состава смеси* * ρi – плотность компонента i.
- 16. Фазовое равновесие. Условия равновесия фаз Равновесным называется такое состояние системы, которое может быть сохранено неизменным сколь
- 17. Фазовое равновесие. Условия равновесия фаз Уравнение Ван-дер-Ваальса–Сторонкина содержит всю информацию о гетерогенной системе в равновесных условиях
- 18. Фазовое равновесие. Условия равновесия фаз Частные производные от изобарно-изотермического потенциала по числу молей одного из компонентов
- 19. Фазовое равновесие. Условия равновесия фаз Для качественных исследований используется также уравнение для нулевого потенциала (уравнение Гиббса-Дюгема),
- 20. Фазовое равновесие. Условия равновесия фаз Равенство температур сосуществующих фаз принято называть условиями термического равновесия, равенство давлений
- 21. Химический потенциал идеальных и реальных растворов Идеальными растворами называют растворы, в которых предполагается отсутствие взаимодействий между
- 22. Химический потенциал индивидуального идеального газа Рассмотрим термодинамическую систему, представляющую собой идеальный газ. Химический потенциал идеального газа
- 23. Химический потенциал компонента идеальных растворов Если общее давление газовой смеси невелико, то каждый газ будет оказывать
- 24. Химический потенциал компонента идеальных растворов Для идеальных жидких растворов применим закон Рауля: парциальное давление насыщенного пара
- 25. Химический потенциал компонента реальных растворов Для реальных растворов все рассмотренные зависимости неприменимы. Химический потенциал компонента реального
- 26. Химический потенциал компонента реальных растворов Понятие фугитивности применимо к любому агрегатному состоянию вещества. Фугитивность измеряется в
- 27. Правило фаз Гиббса Правило фаз Гиббса устанавливает связь между числом компонентов системы n, числом фаз r,
- 28. Правило фаз Гиббса Для чистого вещества n = 1 и в однофазном состоянии (r = 1)
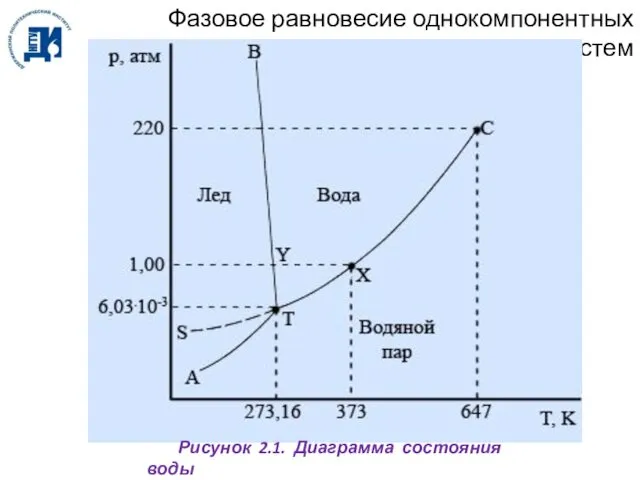
- 29. Фазовое равновесие однокомпонентных систем Рисунок 2.1. Диаграмма состояния воды
- 30. Области фазовой диаграммы, ограниченные кривыми, соответствуют тем условиям (температурам и давлениям), при которых устойчива только одна
- 31. Диаграмма состояния воды Кривая ВТ представляет собой кривую плавления. Она показывает, как давление влияет на температуру
- 32. Зависимость давления от температуры. Уравнение Антуана В настоящее время предложено большое количество уравнений, определяющих зависимость давления
- 33. Фазовое равновесие двухкомпонентных систем. Азеотропные и зеотропные смеси Азеотропная смесь – смесь двух или более жидкостей,
- 34. Константа фазового равновесия жидкость–пар Константа фазового равновесия жидкость–пар Ki – отношение мольной доли компонента в паре
- 35. Расчет бинарных систем жидкость–пар Для бинарного раствора мольная доля более летучего, т.е. низкокипящего, компонента (НКК) в
- 36. Теоретические основы процессов дистилляции и ректификации Дистилляция – перегонка, испарение жидкости с последующим охлаждением и конденсацией
- 37. Теоретические основы процессов дистилляции и ректификации Фракционная дистилляция (или дробная перегонка) – разделение многокомпонентных жидких смесей
- 38. Законы Коновалова Законы Коновалова (или Гиббса–Коновалова) устанавливают связи между изменениями состава, давления и температуры в двойных
- 39. Законы Коновалова Рисунок 3.1. Диаграмма равновесия T–x–y для системы бензол–толуол
- 40. Законы Коновалова Откладывая по оси ординат температуры кипения и составы жидкой фазы, получаем линию ТВБ, называемую
- 41. Законы Коновалова Как видно из рисунка 3.1, по мере увеличения в смеси содержания НКК температура кипения
- 42. Законы Коновалова 2. Температура кипения раствора возрастает (уменьшается) при увеличении концентрации того компонента, содержание которого в
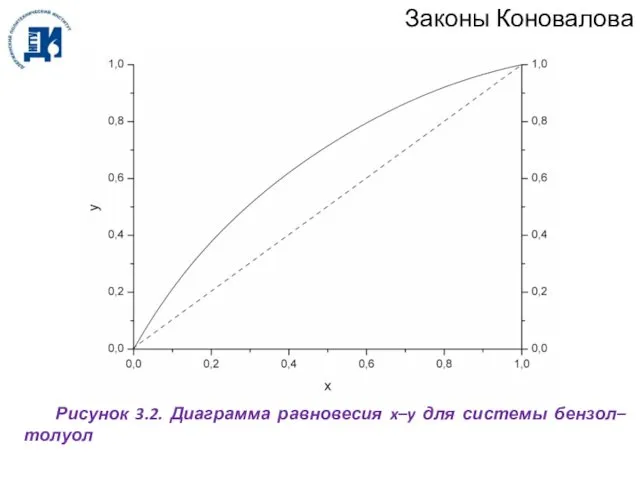
- 43. Законы Коновалова Рисунок 3.2. Диаграмма равновесия x–y для системы бензол–толуол
- 44. Законы Коновалова Второй закон Коновалова справедлив для фаз любой природы: если температура и давление сосуществования двух
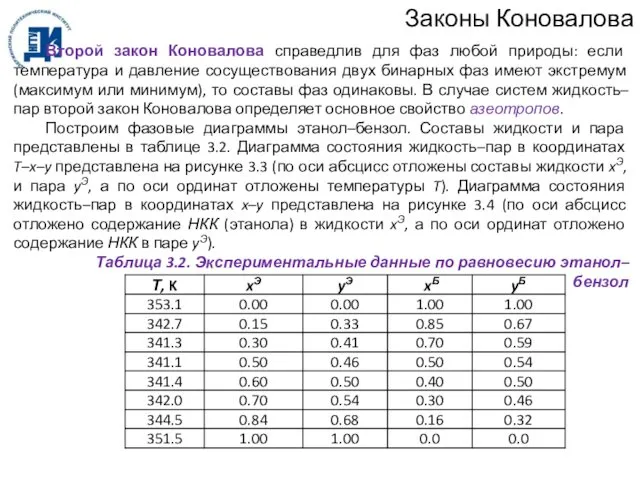
- 45. Законы Коновалова Рисунок 3.3. Диаграмма равновесия T–x–y для системы этанол–бензол
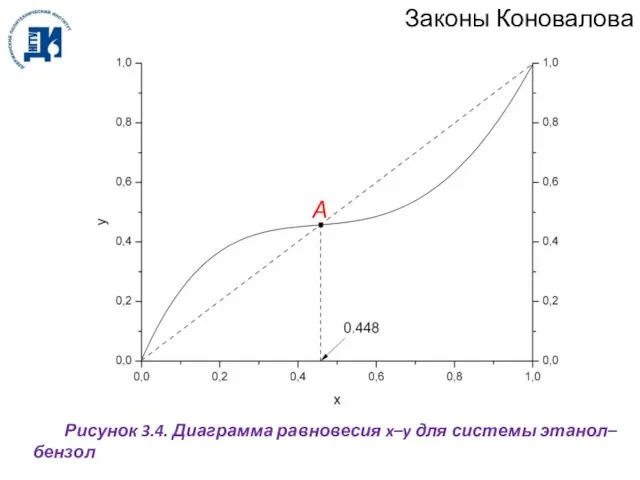
- 46. Законы Коновалова Рисунок 3.4. Диаграмма равновесия x–y для системы этанол–бензол
- 47. Законы Коновалова В азеотропной точке А составы фаз равны x = y. Поскольку y – x
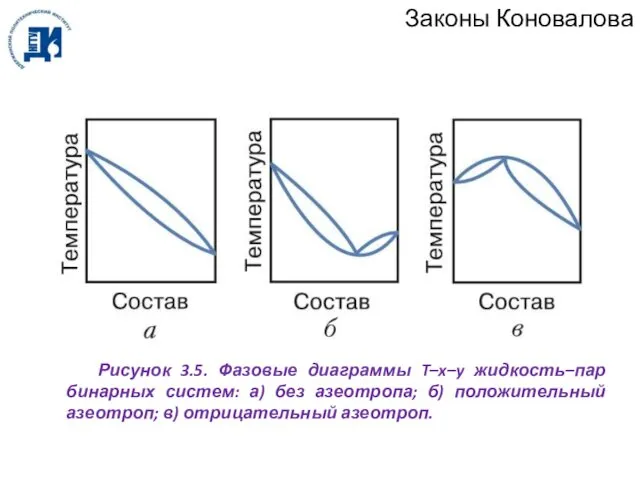
- 48. Законы Коновалова Рисунок 3.5. Фазовые диаграммы T–x–y жидкость–пар бинарных систем: а) без азеотропа; б) положительный азеотроп;
- 49. Законы Коновалова Таким образом, разделение азеотропных смесей на два чистых компонента путем перегонки невозможно, т.к. одним
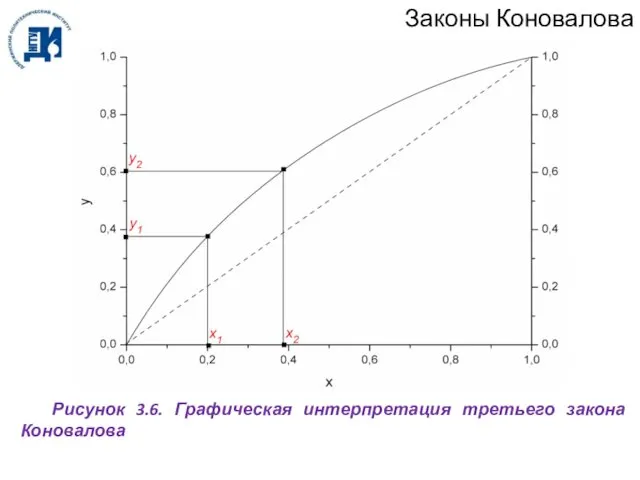
- 50. Законы Коновалова Рисунок 3.6. Графическая интерпретация третьего закона Коновалова
- 51. Законы Вревского Если законы Коновалова характеризуют изменение состояния равновесия бинарных систем при изобарных или изотермических условиях,
- 52. Законы Вревского Второй закон Вревского: – для систем с положительным азеотропом при повышении температуры (давления) в
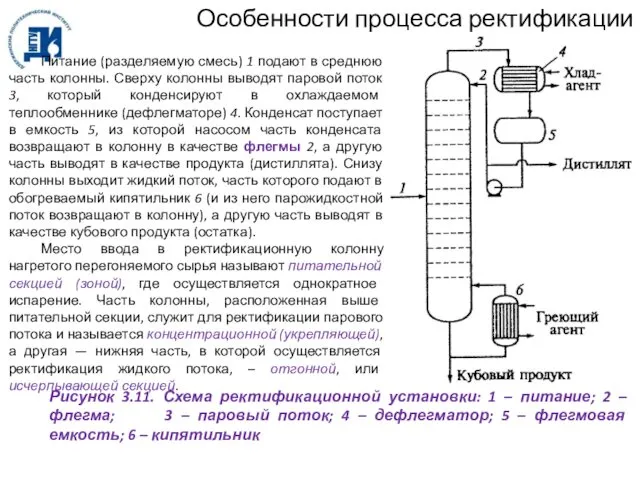
- 53. Особенности процесса ректификации Ректификацией называют процесс тепло- и массообмена между состоящими из одинаковых компонентов потоками неравновесных
- 54. Особенности процесса ректификации Однократное частичное испарение позволяет получить в виде пара смесь, обогащенную более легкими компонентами.
- 55. Особенности процесса ректификации Рисунок 3.11. Схема ректификационной установки: 1 – питание; 2 – флегма; 3 –
- 56. 1. Простые колонны обеспечивают разделение исходной смеси (сырья) на два продукта: ректификат (дистиллят), выводимый с верха
- 57. Особенности процесса ректификации Нерегулярные насадки Кольца Рашига Кольца Палля Седла Берля Регулярные насадки а – Mellapack
- 58. Особенности процесса ректификации Выбор конкретной схемы и рабочих параметров процессов перегонки определяется технико-экономическими и технологическими расчетами
- 59. Обычно КПД тарелок составляет от 0.3 до 0.8. Он существенно зависит от ряда факторов: нагрузки колонны,
- 60. Особенности процесса ректификации В наиболее обобщенной форме разделительные свойства перегоняемого сырья принято выражать коэффициентом относительной летучести
- 61. Выбор давления и температурного режима в ректификационной колонне При принятых значениях флегмового числа, числа и типа
- 62. Выбор давления и температурного режима в ректификационной колонне По величине давления колонны ректификации, применяемые на промышленных
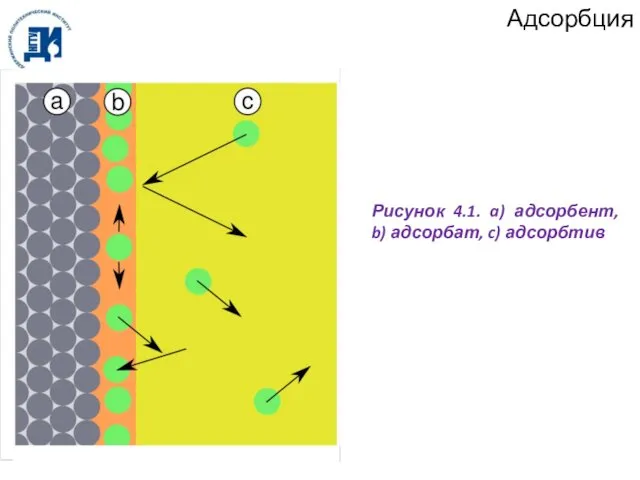
- 63. Адсорбция Адсорбция – частный случай более общего явления, называемого сорбцией. Сорбция – это поглощение веществ, входящих
- 64. Адсорбция Рисунок 4.1. a) адсорбент, b) адсорбат, c) адсорбтив
- 65. Адсорбция Классификация адсорбции по агрегатному состоянию фаз. В зависимости от агрегатного состояния сопредельных фаз различают следующие
- 66. Физическая и химическая адсорбция Типичная физисорбция протекает без переноса или обобществлении электронов, т.е. за счет межмолекулярного
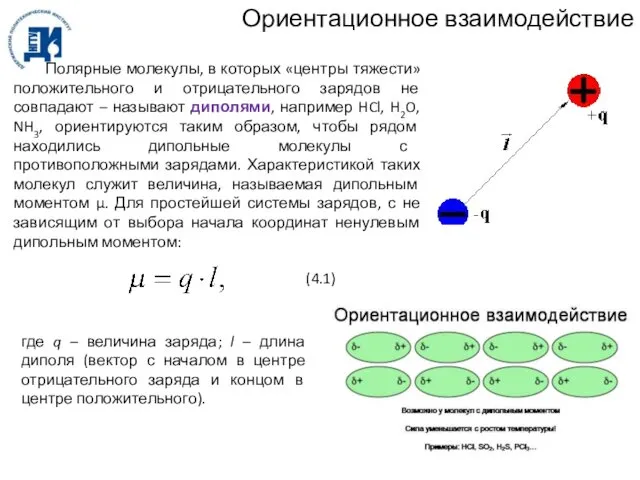
- 67. Ориентационное взаимодействие Полярные молекулы, в которых «центры тяжести» положительного и отрицательного зарядов не совпадают – называют
- 68. Индукционное взаимодействие Межмолекулярное взаимодействие, вызванное поляризацией нейтральной молекулы под действием постоянного диполя. Наведение диполя – индуцирование
- 69. Дисперсионное взаимодействие Взаимодействие, вызванное между мгновенно наведенными диполями в неполярных молекулах в результате флуктуаций при движении
- 70. Физическая и химическая адсорбция В отличие от физической (неактивированной и нелокализованной) адсорбции, хемособция является активированной (локализованной).
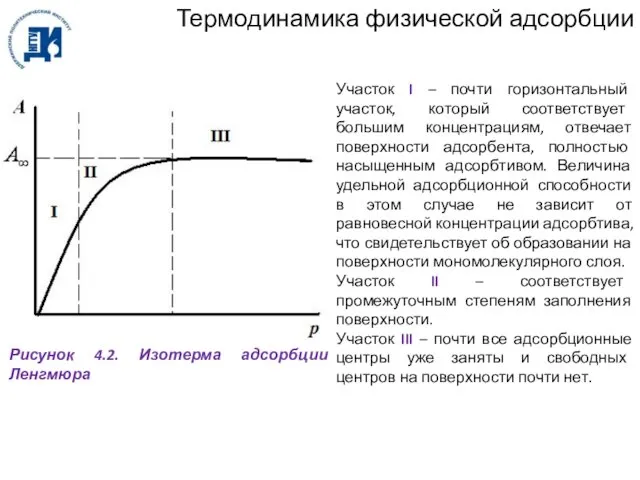
- 71. Термодинамика физической адсорбции Строгая теория изотермы адсорбции была создана Ленгмюром. По модели Ленгмюра все атомы поверхности
- 72. Термодинамика физической адсорбции При адсорбционном равновесии скорость адсорбции равна скорости десорбции. При этом скорость адсорбции пропорциональна
- 73. Термодинамика физической адсорбции Рисунок 4.2. Изотерма адсорбции Ленгмюра Участок I – почти горизонтальный участок, который соответствует
- 74. Термодинамика физической адсорбции Адсорбционный коэффициент b связан с термодинамическими величинами выражением: (4.8) где ΔS – энтропия
- 75. Термодинамика физической адсорбции Дифференциальная теплота адсорбции q равна убыли энтальпии dH при изменении адсорбции a на
- 76. Активные угли Основная доля промышленных адсорбентов приходится на активные угли. Активные угли – высокопористые адсорбенты на
- 77. Силикагели Одним из наиболее распространенных в промышленной практике минеральных адсорбентов является силикагель, обладающий достаточно развитой пористостью.
- 78. Активный оксид алюминия Другим типом неорганических адсорбентов, широко применяемых в технике для осушки различных сред и
- 79. Цеолиты Цеолиты – алюмосиликаты, содержащие в своем составе оксиды щелочных и щелочноземельных металлов. Общая химическая формула
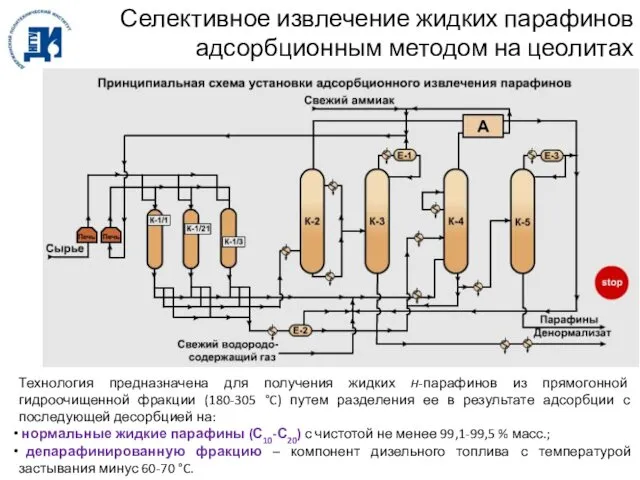
- 80. Селективное извлечение жидких парафинов адсорбционным методом на цеолитах Технология предназначена для получения жидких н-парафинов из прямогонной
- 81. Наряду с установками «Парекс» на многих нефтеперерабатывающих предприятиях России и нашли свое применение технологии: установка «Молекс»:
- 82. Теоретические основы процесса абсорбции Абсорбцией называют процесс поглощения газов или паров из газовых или парогазовых смесей
- 83. 3. Очистка газа от примесей вредных компонентов. Такая очистка осуществляется, прежде всего, с целью удаления примесей,
- 84. Физическая абсорбция Зависимость растворимости газа от давления при небольших концентрациях газа в растворе и небольших давлениях
- 85. Физическая абсорбция При этом фугитивность компонента газовой смеси может быть рассчитана по уравнению: (5.3) где y2
- 86. Физическая абсорбция Если раствор нагревается при смешении газа с жидкостью, то ΔH В широком интервале температур
- 87. Химическая абсорбция При хемосорбции молекулы газа, растворенного в жидкости, вступают в реакцию с активным компонентом абсорбента.
- 88. Одним из наиболее простых случаев равновесия газ–жидкость при хемосорбции является равновесие при следующих условиях: – в
- 89. Физико-химические свойства абсорбентов и требования к ним Абсорбционная емкость растворителя. Решающим свойством растворителя являются растворимость в
- 90. Физико-химические свойства абсорбентов и требования к ним Температура кипения в значительной мере определяется требованиями к давлению
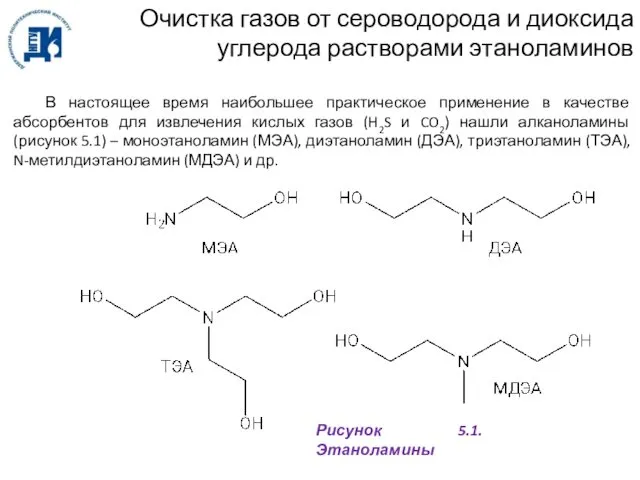
- 91. Очистка газов от сероводорода и диоксида углерода растворами этаноламинов В настоящее время наибольшее практическое применение в
- 92. Очистка газов от сероводорода и диоксида углерода растворами этаноламинов Основные реакции, протекающие при абсорбции кислых газов
- 93. Теоретические основы процесса жидкостной экстракции Под жидкостной экстракцией понимают процесс перехода одного или нескольких растворенных веществ
- 94. 1. Экстракцию можно использовать вместо методов непосредственного разделения смесей (например, вместо ректификации), если последние стоят дороже.
- 95. г) Удешевление процесса концентрирования растворов выпариванием. Так, бензойная кислота может быть выделена из разбавленных водных растворов
- 96. Теоретические основы процесса жидкостной экстракции г) Удешевление процесса концентрирования растворов выпариванием. Так, бензойная кислота может быть
- 97. Выбор экстрагента (растворителя) Экстрагенты классифицируют по разным признакам. Например, по химическому характеру различают три класса экстрагентов:
- 99. Скачать презентацию

















































































 Арены и ароматичность
Арены и ароматичность АЛОТРОПНІ ФОРМИ КАРБОНУ АВТОР: НАЗАРЕНКО МАКСИМ ВОЛОДИМИРОВИЧ 9-А КЛАС,ГІМНАЗІЯ №32 ПЕЧЕРСЬКИЙ РАЙОН, М. КИЇВ ПЕДАГОГІЧНИЙ КЕ
АЛОТРОПНІ ФОРМИ КАРБОНУ АВТОР: НАЗАРЕНКО МАКСИМ ВОЛОДИМИРОВИЧ 9-А КЛАС,ГІМНАЗІЯ №32 ПЕЧЕРСЬКИЙ РАЙОН, М. КИЇВ ПЕДАГОГІЧНИЙ КЕ Препараты гормонов стероидной структуры
Препараты гормонов стероидной структуры Закон постоянства углов Стено
Закон постоянства углов Стено Растворы. Общая характеристика растворов
Растворы. Общая характеристика растворов Арены. Бензол
Арены. Бензол Обмен веществ и энергии, основа существования клетки
Обмен веществ и энергии, основа существования клетки КАЛЬЦИЙ И ЕГО СОЕДИНЕНИЯ 9 класс МКОУ «СОШ № 85» г. Тайшет Иркутской обл. Учитель: Никитюк Л.Ф.
КАЛЬЦИЙ И ЕГО СОЕДИНЕНИЯ 9 класс МКОУ «СОШ № 85» г. Тайшет Иркутской обл. Учитель: Никитюк Л.Ф. Пены. Пенообразование
Пены. Пенообразование Введение в титриметрический анализ. Кислотно-основное титрование
Введение в титриметрический анализ. Кислотно-основное титрование Щелочные металлы
Щелочные металлы Ковалентная химическая связь
Ковалентная химическая связь Элементы группы VII B
Элементы группы VII B Мыс айналымы
Мыс айналымы Презентация по Химии "Разнообразие кристаллов и их выращивание" - скачать смотреть
Презентация по Химии "Разнообразие кристаллов и их выращивание" - скачать смотреть  Модифицирование структуры полисахаридов гидрофобными заместителями: твердофазный синтез, исследование структуры и свойств
Модифицирование структуры полисахаридов гидрофобными заместителями: твердофазный синтез, исследование структуры и свойств Макроэлементы и микроэлементы
Макроэлементы и микроэлементы Виды изомерии у моносахаридов
Виды изомерии у моносахаридов Презентация по теме «Металлы» «Уран» Работа Садковского Ивана 9 «В»
Презентация по теме «Металлы» «Уран» Работа Садковского Ивана 9 «В» Хімічний склад і використання мінералів
Хімічний склад і використання мінералів Характеристика элементов VIIA-группы (галогены)
Характеристика элементов VIIA-группы (галогены) Электролиз: опыты к заданиям ЕГЭ
Электролиз: опыты к заданиям ЕГЭ Биосинтез жирных кислот и триацилглицеролов. Обмен липидов. (Лекция 13)
Биосинтез жирных кислот и триацилглицеролов. Обмен липидов. (Лекция 13) Аттестационная работа. Методическая разработка фрагмента урока химии с элементами исследовательской деятельности
Аттестационная работа. Методическая разработка фрагмента урока химии с элементами исследовательской деятельности Электрохимические методы. (Лекция 3)
Электрохимические методы. (Лекция 3) Электролиз. Урок химии 11 класс
Электролиз. Урок химии 11 класс Переработка нефти. (10 класс)
Переработка нефти. (10 класс) Сплавы, растворы и смеси. Задачи на концентрвцию
Сплавы, растворы и смеси. Задачи на концентрвцию