Содержание
- 2. План лекции Общие положения; Способы выражения концентраций раствора; Электролитическая диссоциация, рН раствора; Гидролиз солей.
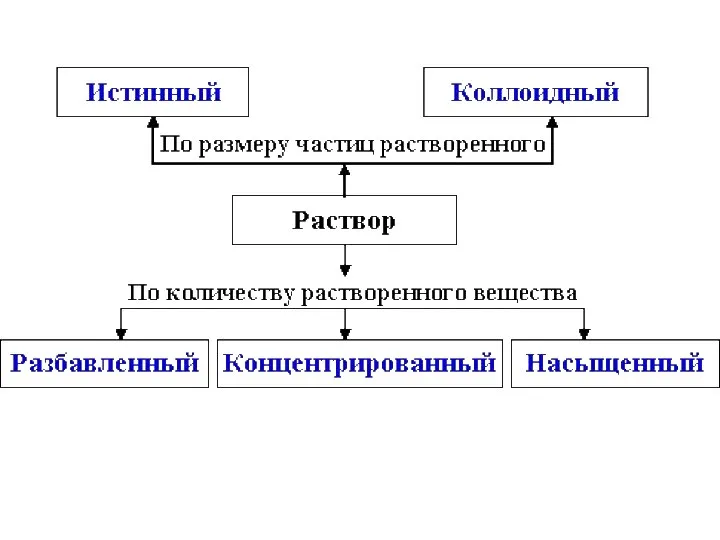
- 4. Растворимость Таблица растворимости Хорошо растворимые (более 10 г в-ва в 1 л воды) Малорастворимые (от 0,01
- 5. 5 % водный раствор HCl 100 г раствора содержит 5 г HCl и 95 г растворителя
- 7. Молярная концентрация (Молярность), СМ, [моль/л] – число молей растворенного вещества n, содержащегося в 1 л раствора
- 8. , [моль/л]
- 9. Определите массу нитрата натрия, которая требуется для приготовления 2 л децимолярного раствора (0,1 м). В 1
- 10. Нормальная концентрация эквивалента (Нормальность), CН, [моль/л] − число эквивалентов растворенного вещества nэ, содержащихся в 1 л
- 11. , [моль/л]
- 12. 0,75 н р-р H2SO4 или CН = 0,75 моль/л р-ра H2SO4 в 1 л р-ра –
- 13. Моляльная концентрация (Моляльность), Cm, [моль/кг] – число молей растворенного вещества n, приходящихся на 1 кг растворителя
- 14. , [моль/кг]
- 15. 2 m раствор H2SO4 2 моля приходятся на 1000 г растворителя Cm × М приходятся на
- 16. Титр Т, [г/мл] Показывает количество г растворенного вещества m, содержащегося в 1 мл раствора V: ,
- 17. Способы выражения концентраций растворов
- 18. Закон эквивалентов для растворов Объемы реагирующих веществ обратно пропорциональны их нормальностям:
- 19. Закон эквивалентов для растворов
- 20. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ NaCl ⇄ Na+ + Cl– KA ⇄ K+ + A¯ Катион Анион диссоциация Степень
- 22. Константа диссоциации Кдис(СН3СООН) = 1,8⋅10–5 Кдис (НСN) = 8⋅10–10 СН3СООН ⇄ СН3СОО– + Н+
- 23. Электролитическая диссоциация воды где [H+], [OH–] и [H2O] – молярные концентрации частиц в воде. Н2О ⇄
- 24. Ионное произведение воды: Нейтральная среда [H+] = [OH–] = 10–7 Кислая среда [H+] > 10–7 >
- 25. Водородный показатель pH = –lg[H+] [H+] = 10–7 pH = –lg10–7 = 7 нейтральная среда pH
- 26. [H+] = 10–2 моль/л pH = ? pH = –lg[H+] = –lg10–2 = 2 кис. ср.
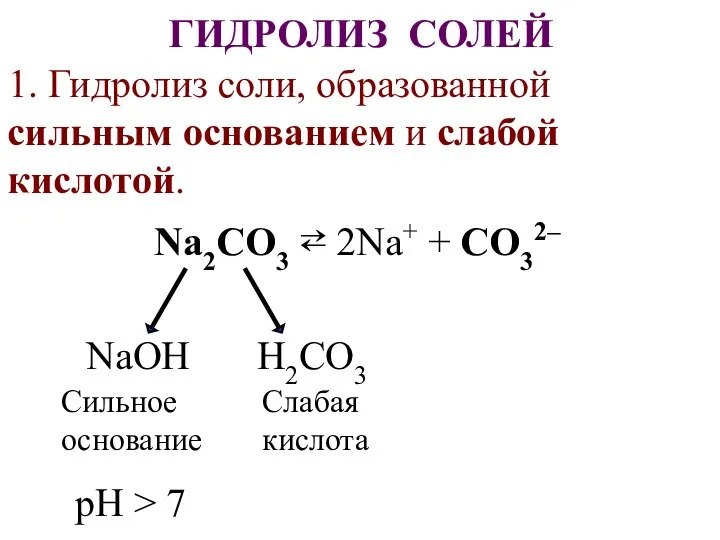
- 27. ГИДРОЛИЗ СОЛЕЙ 1. Гидролиз соли, образованной сильным основанием и слабой кислотой. Na2CO3 ⇄ 2Na+ + CO32–
- 28. I ст. CO32– + H+OН– ⇄ HCO3– + OН– Na2CO3 + H2O ⇄ NaHCO3 + NaOН
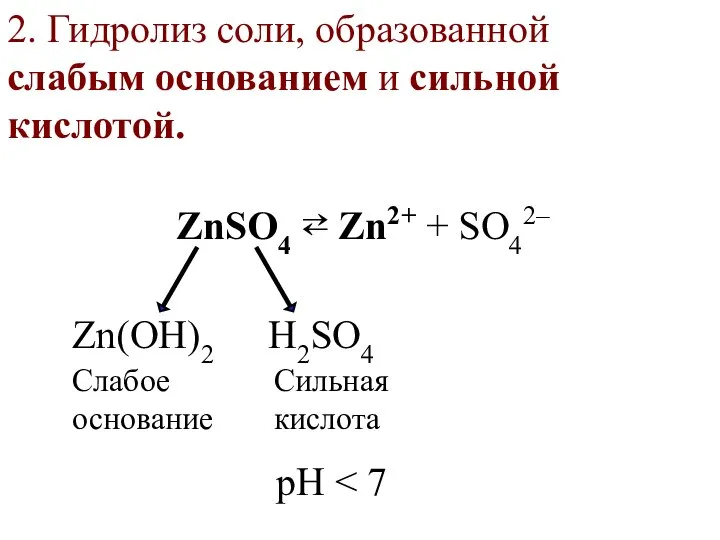
- 29. 2. Гидролиз соли, образованной слабым основанием и сильной кислотой. ZnSO4 ⇄ Zn2+ + SO42– Zn(OН)2 H2SO4
- 30. I ст. Zn2+ + H+OН– ⇄ ZnOH+ + Н+ 2ZnSO4 + 2H2O ⇄ (ZnOH)2SO4 + H2SO4
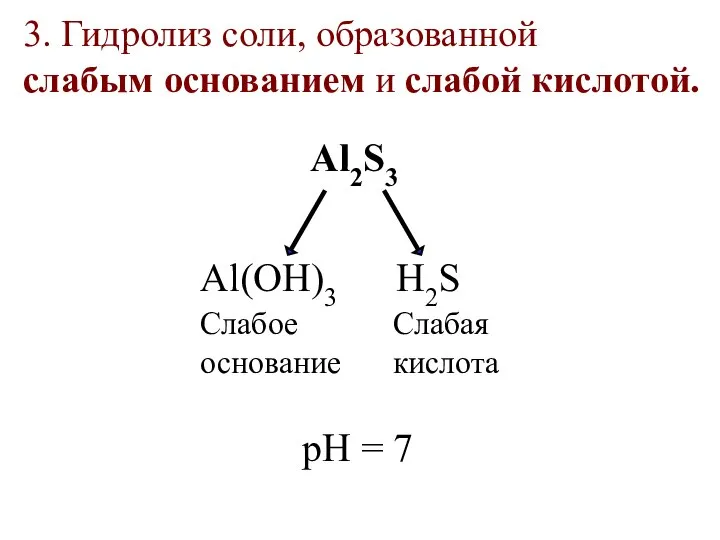
- 31. 3. Гидролиз соли, образованной слабым основанием и слабой кислотой. Al2S3 Al(OН)3 H2S Слабое основание Слабая кислота
- 32. Al2S3 + 6H2O ⇄ 2Al(OH)3↓ + 3H2S↑ 2Al3+ + 3S2– + 6H2O ⇄ 2Al(OH)3↓ + 3Н2S↑
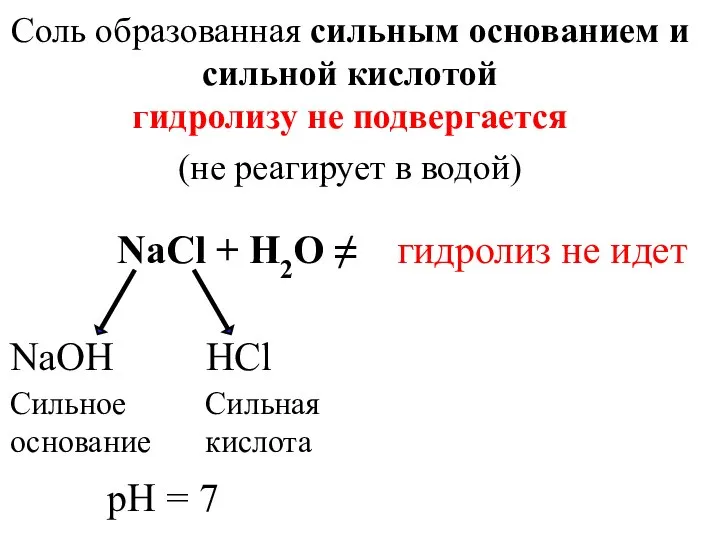
- 33. Соль образованная сильным основанием и сильной кислотой гидролизу не подвергается (не реагирует в водой) NaCl +
- 35. Скачать презентацию




![Молярная концентрация (Молярность), СМ, [моль/л] – число молей растворенного вещества n,](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396475/slide-6.jpg)
![, [моль/л]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396475/slide-7.jpg)

![Нормальная концентрация эквивалента (Нормальность), CН, [моль/л] − число эквивалентов растворенного вещества](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396475/slide-9.jpg)
![, [моль/л]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396475/slide-10.jpg)

![Моляльная концентрация (Моляльность), Cm, [моль/кг] – число молей растворенного вещества n,](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396475/slide-12.jpg)
![, [моль/кг]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396475/slide-13.jpg)

![Титр Т, [г/мл] Показывает количество г растворенного вещества m, содержащегося в](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396475/slide-15.jpg)






![Электролитическая диссоциация воды где [H+], [OH–] и [H2O] – молярные концентрации](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396475/slide-22.jpg)
![Ионное произведение воды: Нейтральная среда [H+] = [OH–] = 10–7 Кислая](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396475/slide-23.jpg)
![Водородный показатель pH = –lg[H+] [H+] = 10–7 pH = –lg10–7](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396475/slide-24.jpg)
![[H+] = 10–2 моль/л pH = ? pH = –lg[H+] =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396475/slide-25.jpg)
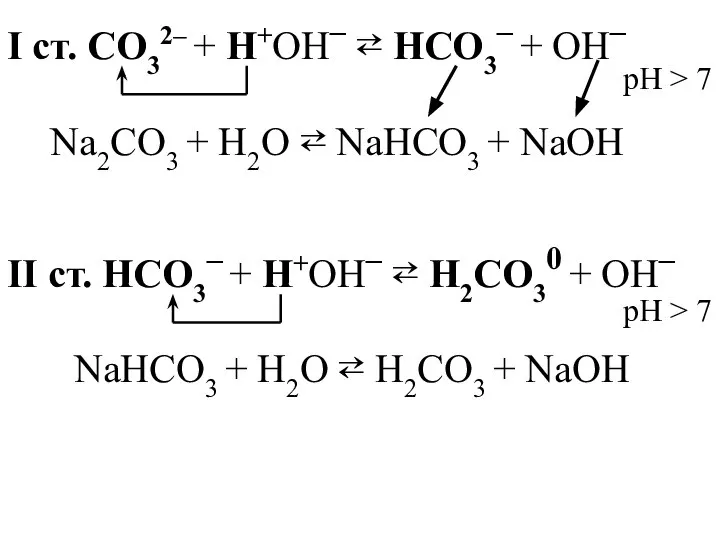
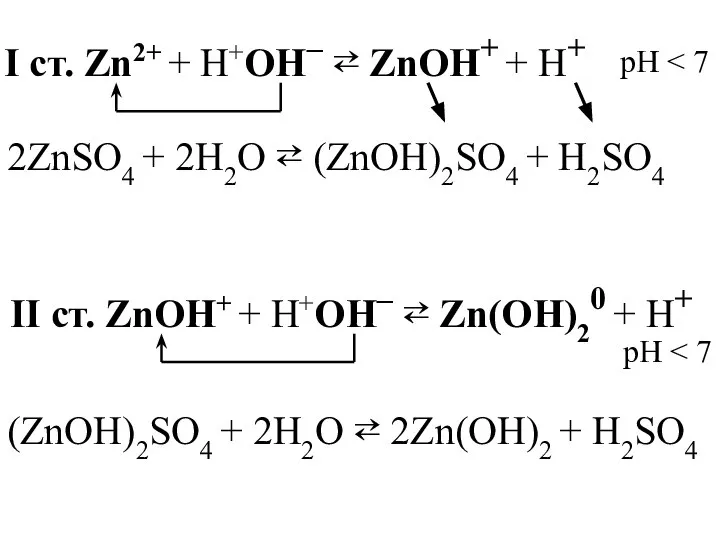
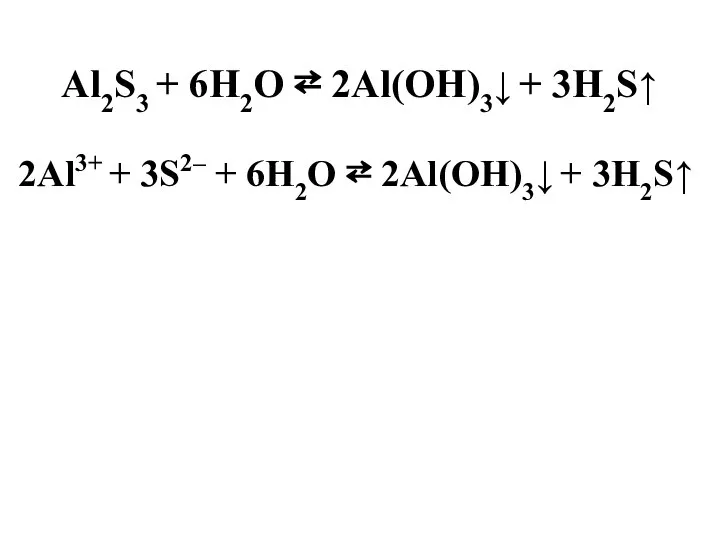
 Металлы и сплавы
Металлы и сплавы ИЗВЕСТНЫЕ УЧЕНЫЕ – ХИМИКИ Немного из истории химии
ИЗВЕСТНЫЕ УЧЕНЫЕ – ХИМИКИ Немного из истории химии Геологические структуры МПИ. Группа доминерализационных структур
Геологические структуры МПИ. Группа доминерализационных структур Allgemeine Chemie für PharmazeutInnen
Allgemeine Chemie für PharmazeutInnen Алкины. 10 класс
Алкины. 10 класс Физические свойства элементов
Физические свойства элементов Гидролиз. Методы его получения и применения
Гидролиз. Методы его получения и применения Ученые химики. Выполнила ученица 10 кл. Трофимова Настя
Ученые химики. Выполнила ученица 10 кл. Трофимова Настя Жидкостно-сцинтилляционная спектроскопия
Жидкостно-сцинтилляционная спектроскопия Многоатомные спирты
Многоатомные спирты Алканы. Гомологи, изомеры, номенклатура.
Алканы. Гомологи, изомеры, номенклатура.  Валидация титриметрических методик анализа
Валидация титриметрических методик анализа Электролитическая диссоциация
Электролитическая диссоциация Кислородосодержащие органические соединения (2 часть)
Кислородосодержащие органические соединения (2 часть) Методы разделения и концентрирования. Хроматографические методы
Методы разделения и концентрирования. Хроматографические методы Основные этапы первичного процесса переработки нефти
Основные этапы первичного процесса переработки нефти Синергизм и синергические системы
Синергизм и синергические системы Химические реакции. Типы химических реакций
Химические реакции. Типы химических реакций Требование к оформлению отчета лабораторной работы
Требование к оформлению отчета лабораторной работы ОБЩАЯ ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ ПОДГРУППЫ КИСЛОРОДА
ОБЩАЯ ХАРАКТЕРИСТИКА ЭЛЕМЕНТОВ ПОДГРУППЫ КИСЛОРОДА  Моделирование химических процессов
Моделирование химических процессов Поверхностное упрочнение деталей. (Лекция 11)
Поверхностное упрочнение деталей. (Лекция 11) Окисно-відновні процеси
Окисно-відновні процеси Кислород, его общая характеристика, нахождение в природе и получение (8 класс)
Кислород, его общая характеристика, нахождение в природе и получение (8 класс) «Разработка и реализация проекта по установлению фильтров для питьевых фонтанчиков в школе» Разработан: ОКУЛОВ АНДРЕЙ, ученик 10 к
«Разработка и реализация проекта по установлению фильтров для питьевых фонтанчиков в школе» Разработан: ОКУЛОВ АНДРЕЙ, ученик 10 к Штучні і синтетичні волокна
Штучні і синтетичні волокна  Современные и новейшие материалы
Современные и новейшие материалы Учитель химии МБОУ СОШ № 9 МО ЩР станица Новощербиновская Степучева Ольга Викторовна
Учитель химии МБОУ СОШ № 9 МО ЩР станица Новощербиновская Степучева Ольга Викторовна