Содержание
- 2. Непредельные углеводороды. Непредельные, или ненасыщенные, УВ содержат кратные углерод- углеродные связи (>C=C Непредельными называются углеводороды, в
- 3. Алкены ( олефины, этиленовые УВ) CnH2n, n>2 Алкены – это УВ, в молекулах которых два атома
- 4. Изомерия Для алкенов возможны 4 типа изомерии: Изомерия углеродной цепи Изомерия положения двойной связи Цис,- транс-
- 5. Номенклатура CnH2n ан -- ен или илен В качестве главной выбирают цепь, включающую двойную связь, даже
- 6. Физические свойства С2-С4 газы, С5-С16 жидкости, С>19 твердые, р Ткип.(н)>Tкип.(разв.) Ткип.(цис)>Tкип.(транс) Назад
- 7. Химические свойства Активны из-за наличия непрочной π- связи Характерны реакции присоединения Гидрирование( присоединение водорода) СН3-СН=СН2 +Н2→
- 8. Присоединение галогенводородов к несимметричным алкенам происходит по правилу В.В. Марковникова Правило Марковникова !!! При присоединении полярных
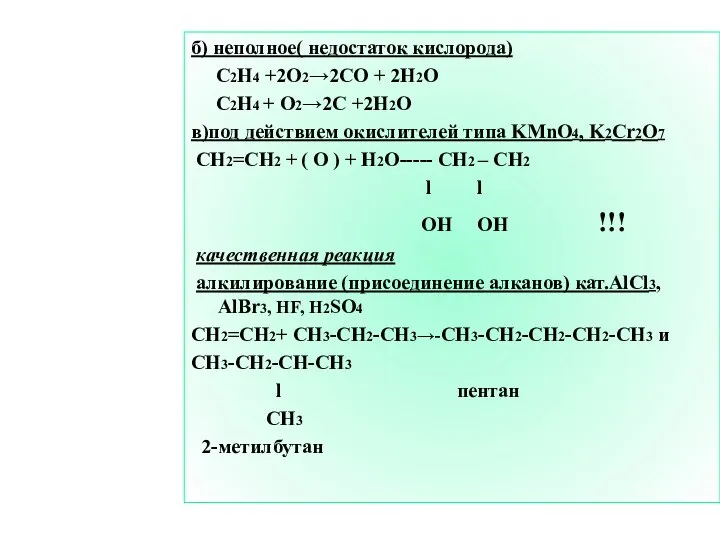
- 9. б) неполное( недостаток кислорода) C2H4 +2O2→2CO + 2H2O C2H4 + O2→2C +2H2O в)под действием окислителей типа
- 10. III.Реакции полимеризации. Процесс полимеризации алкенов открыт А.М.Бутлеровым. Полимеризацией называется процесс соединения одинаковых молекул (мономеров), протекающий за
- 11. Получение алкенов. 1)Крекинг нефтепродуктов С16Н34 --- С8Н18 + С8Н16( t ) 2) Дегидрирование алканов ( де
- 13. Скачать презентацию









 Установка изомеризации пентан гексановой фракции
Установка изомеризации пентан гексановой фракции Структура белка
Структура белка Предельные углеводороды
Предельные углеводороды Биологическая роль макро и микроэлементов. (Лекция 17)
Биологическая роль макро и микроэлементов. (Лекция 17) pH жидкостей, необходимых для человека Выполнили: Учащиеся 11 класса МОУ «СОШ №16» Самоделкин Василий Шадрин Константин
pH жидкостей, необходимых для человека Выполнили: Учащиеся 11 класса МОУ «СОШ №16» Самоделкин Василий Шадрин Константин  Мило та його склад
Мило та його склад  Растворение. Растворимость веществ.
Растворение. Растворимость веществ. Химия морской воды
Химия морской воды Теория диаграмм состояния
Теория диаграмм состояния Углеводы. Структура
Углеводы. Структура Биогеохимические эндемии и их профилактика
Биогеохимические эндемии и их профилактика Органикалық қосылыстар
Органикалық қосылыстар Бораты и силикаты как матрицы лазеров. Свойства и методы выращивания
Бораты и силикаты как матрицы лазеров. Свойства и методы выращивания Закономерности химических реакций
Закономерности химических реакций Азотная кислота
Азотная кислота Гидролиз солей
Гидролиз солей Химические свойства кислот.
Химические свойства кислот. Презентация по Химии "Спирты" - скачать смотреть _
Презентация по Химии "Спирты" - скачать смотреть _ Основные типы химических реакций
Основные типы химических реакций Презентация по химии Применение электролиза
Презентация по химии Применение электролиза  Классификация и ассортимент клея
Классификация и ассортимент клея Фосфор, фосфор оксидтері
Фосфор, фосфор оксидтері Выполнил учениц__ 9 «___» класса __________________
Выполнил учениц__ 9 «___» класса __________________  Химические свойства алкинов
Химические свойства алкинов Воздух. Состав воздуха. Реакция горения
Воздух. Состав воздуха. Реакция горения Химический элемент сера
Химический элемент сера Ionic polymerization
Ionic polymerization Неорганическая химия
Неорганическая химия