Содержание
- 2. Элементы V-A – группы
- 3. Элементы VА-группы. Азот Общая электронная формула: […] ns 2 (n–1)d 10np 3 Степени окисления: –III, 0,
- 4. Элементы VА-группы (все, кроме N) Общая электронная формула: […] ns 2 (n–1)d 10np 3 Степени окисления:
- 5. Простые в-ва N2, P4, As, Sb, Bi N≡N – молекулярное соединение в любом агрегатном состоянии, кроме
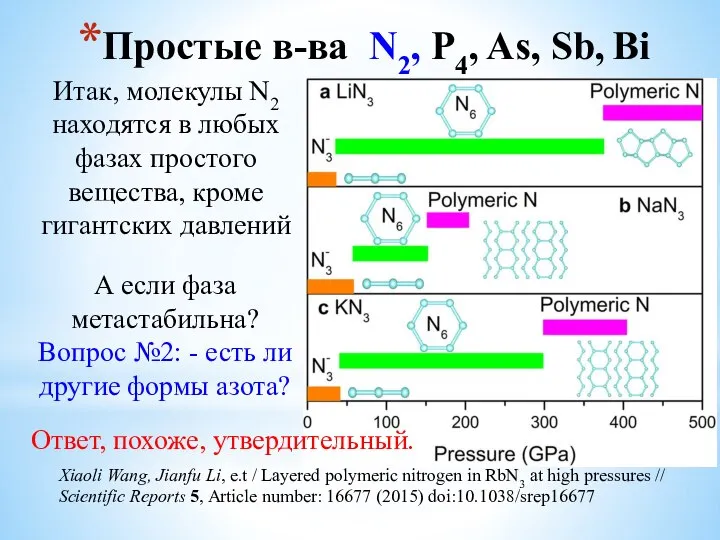
- 6. Простые в-ва N2, P4, As, Sb, Bi Итак, молекулы N2 находятся в любых фазах простого вещества,
- 7. Простые в-ва N2, P4, As, Sb, Bi Итак, молекулы N2 находятся в любых фазах простого вещества,
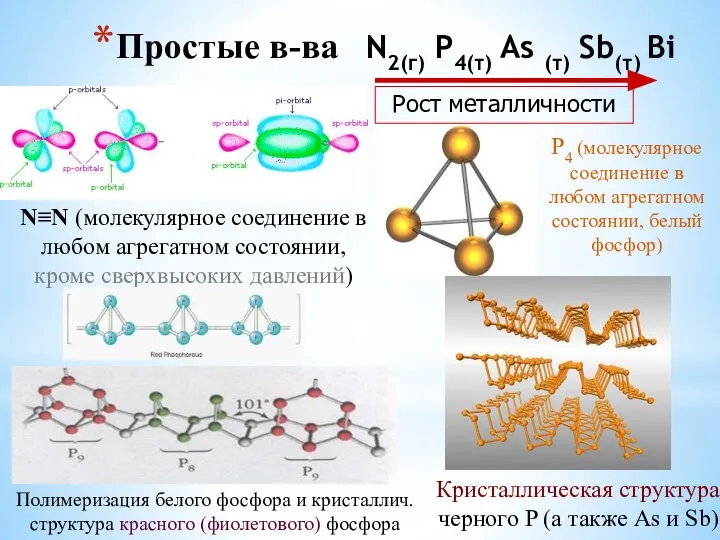
- 8. Простые в-ва N2(г) P4(т) As (т) Sb(т) Bi N≡N (молекулярное соединение в любом агрегатном состоянии, кроме
- 9. Тетраэдрические мотивы, сохраняющиеся в сложных соединениях P, As и Sb AsS, минерал реальгар As2S3, минерал аурипигмент
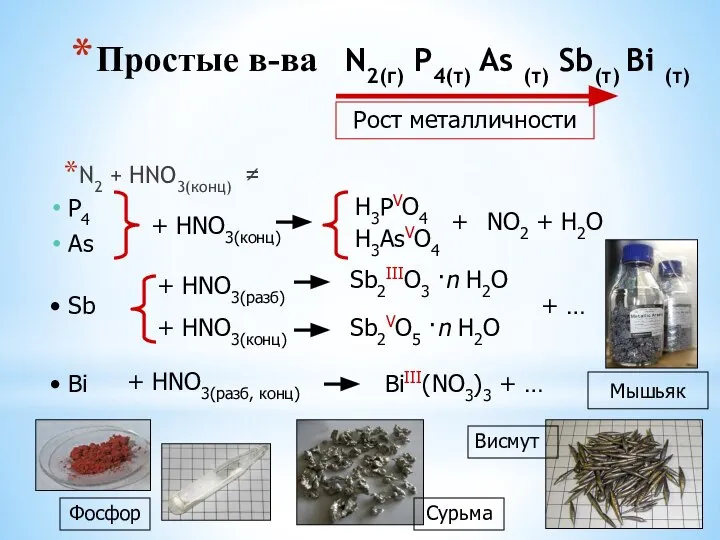
- 10. Простые в-ва N2(г) P4(т) As (т) Sb(т) Bi (т) N2 + HNO3(конц) ≠ P4 As +
- 11. Водородные соединения NH3 – уст. PH3 – неуст. AsH3 – SbH3 – (BiH3) Устойчивость убывает очень
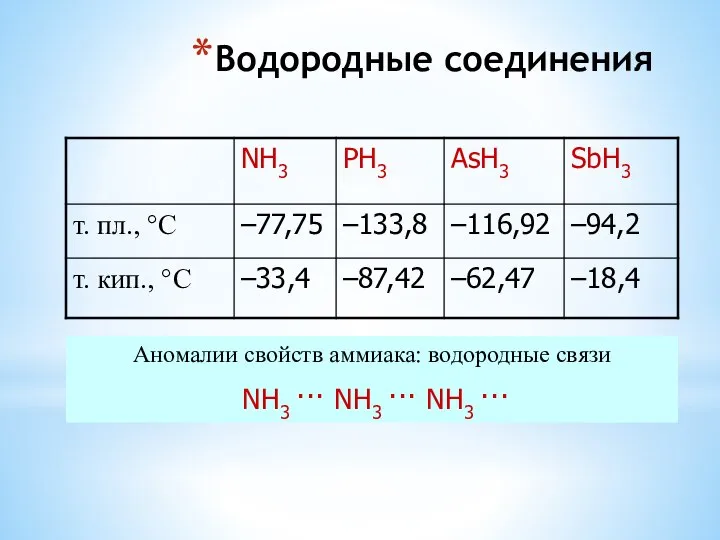
- 12. Водородные соединения Аномалии свойств аммиака: водородные связи NH3 ··· NH3 ··· NH3 ···
- 13. Гидроксиды, кислоты Э+III Э+V N P As Sb Bi HNO2 (слабая к-та) HNO3 (сильная к-та) HPO(OH)2
- 14. Оксиды
- 15. Степени окисления Ст. ок. +5: P, As, Sb N(+5), Bi(+5) – сильные окислители Ст. ок. +3:
- 16. Распространение в природе 12. P – 0,09 масс.% 16. N – 0,03 масс.% 47. As –
- 17. Азот, фосфор Нитратин (чилийская селитра) NaNO3 Нитрокалит (индийская селитра) KNO3 Нашатырь NH4Cl Апатит 3Ca3(PO4)2·Ca(Cl,OH,F)2 Фосфорит Ca3(PO4)2
- 18. Мышьяк, сурьма, висмут Реальгар As4S4 Аурипигмент As2S3 Арсенопирит FeAsS Тетраэдрит Cul2As4S13 Антимонит (сурьмяный блеск) Sb2S3 Висмутин
- 19. История открытия элементов Азот: 1772 г., Д. Резерфорд, Г.Кавендиш, 1769-1771 гг., К.Шееле, А.Л. Лавуазье Фосфор: 1669
- 20. Свойства азота N2 – бесцветный газ, без запаха и вкуса, т.пл. –210,0 °С, т.кип. –195,8 °С
- 21. Азот. Шкала степеней окисления N2O5, NO3−, HNO3, NaNO3, AgNO3 NO2, N2O4 N2O3, NO2−, HNO2, NaNO2, NF3
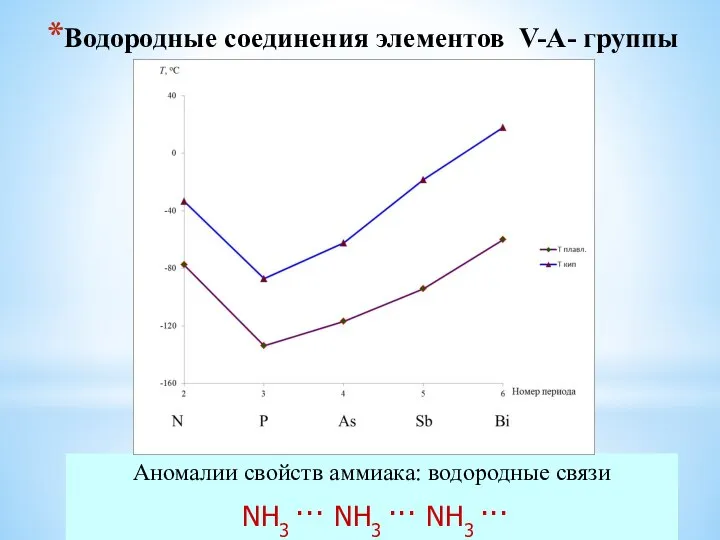
- 22. Водородные соединения элементов V-A- группы Аномалии свойств аммиака: водородные связи NH3 ··· NH3 ··· NH3 ···
- 23. Получение и применение азота В промышленности: фракционная дистилляция сжиженного воздуха (жидкий кислород остается в жидкой фазе).
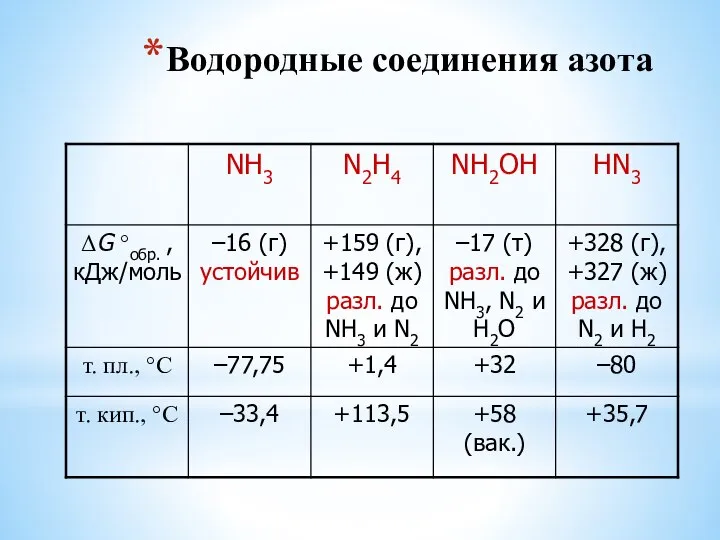
- 24. Водородные соединения азота
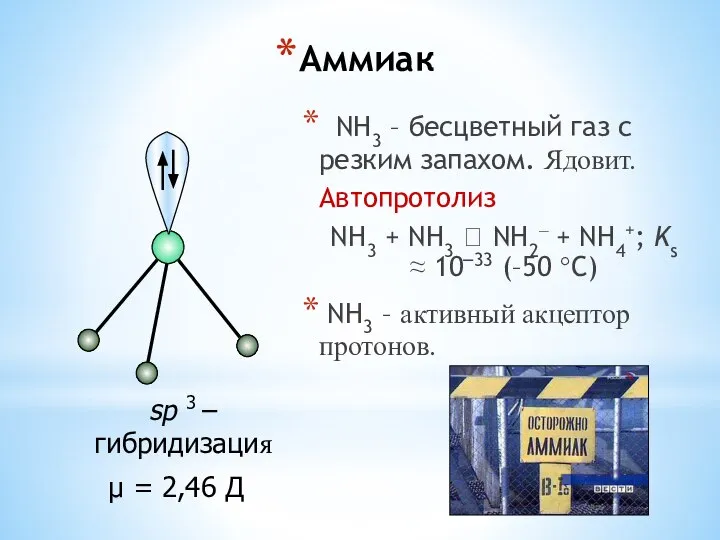
- 25. Аммиак NH3 – бесцветный газ с резким запахом. Ядовит. Автопротолиз NH3 + NH3 ⮀ NH2– +
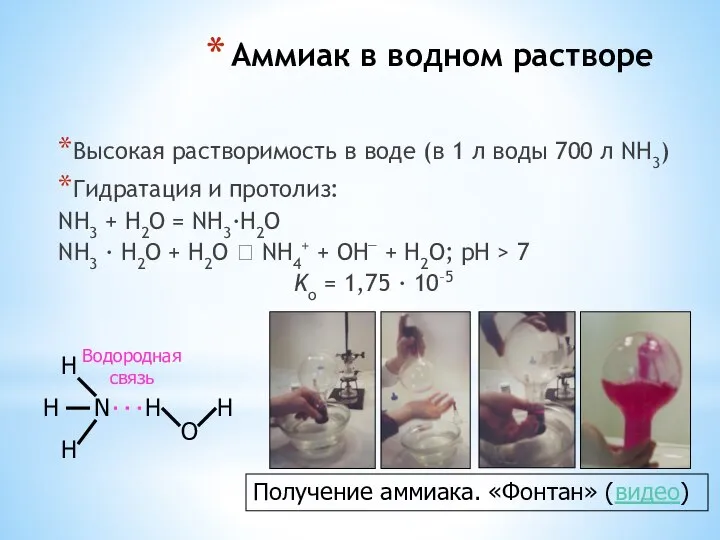
- 26. Аммиак в водном растворе Высокая растворимость в воде (в 1 л воды 700 л NH3) Гидратация
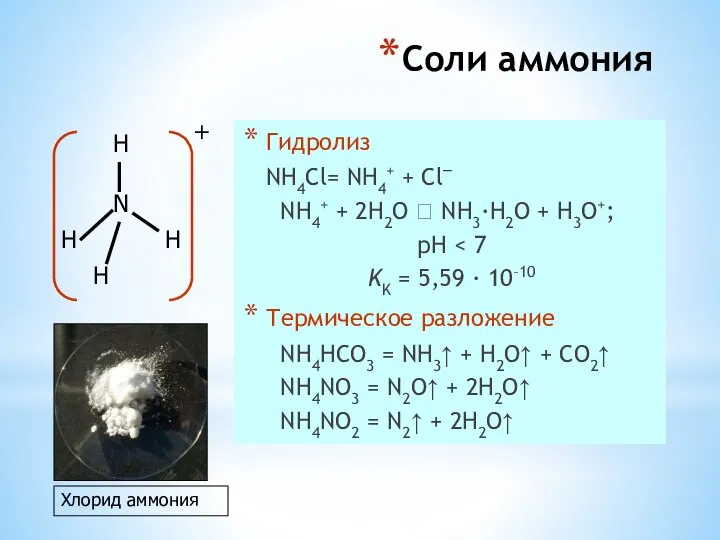
- 27. Соли аммония Гидролиз NH4Cl= NH4+ + Cl– NH4+ + 2H2O ⮀ NH3·H2O + H3O+; pH KK
- 28. Окислительно-восстановительные свойства Горение 4 NH3 + 3O2 = 2N2 + 6H2O (без кат.) 4 NH3 +
- 29. Получение аммиака В промышленности: N2 + 3H2 ⮀ 2NH3 + Q (300-500 °С, 300 атм, катализатор:
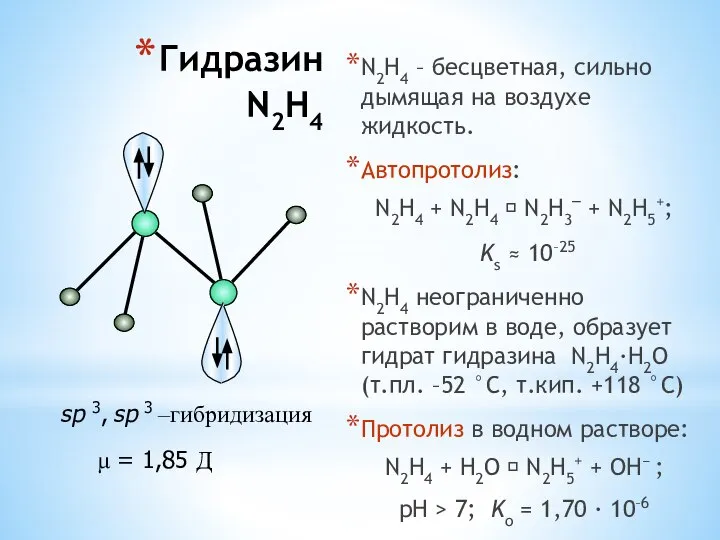
- 30. Гидразин N2H4 N2H4 – бесцветная, сильно дымящая на воздухе жидкость. Автопротолиз: N2H4 + N2H4 ⮀ N2H3–
- 31. Протоноакцепторные свойства N2H4 – акцептор протонов (две неподеленные пары электронов): N2H4 + H3O+ = N2H5+ +
- 32. Окислительно-восстановительные свойства гидразина Получение: 2NH3 + NaClO = N2H4 + NaCl + H2O Гидразин как восстановитель
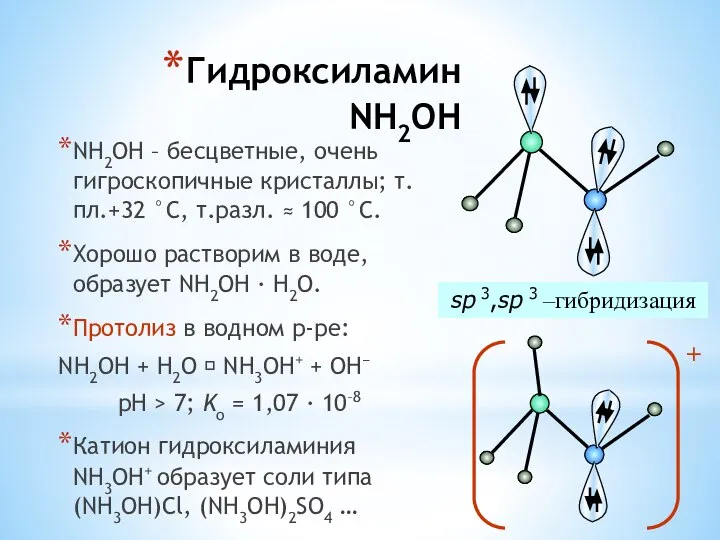
- 33. Гидроксиламин NH2OH NH2OH – бесцветные, очень гигроскопичные кристаллы; т.пл.+32 °С, т.разл. ≈ 100 °С. Хорошо растворим
- 34. Окислительно-восстановительные свойства гидроксиламина Гидроксиламин как восстановитель рН > 7: 2(NH2OH·H2O) + 2OH− −2e − = N2
- 35. Азидоводород HN3 HN3 – бесцветная летучая жидкость, неограниченно растворимая в воде (при содержании в растворе свыше
- 37. Скачать презентацию

![Элементы VА-группы. Азот Общая электронная формула: […] ns 2 (n–1)d 10np](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1398921/slide-2.jpg)
![Элементы VА-группы (все, кроме N) Общая электронная формула: […] ns 2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1398921/slide-3.jpg)




















 Бериллий. Строение элемента. Физические и химические свойства. Способы получения. Применение. Интересные факты. Опыты
Бериллий. Строение элемента. Физические и химические свойства. Способы получения. Применение. Интересные факты. Опыты Хром және оның қосылыстары
Хром және оның қосылыстары Металл и ржавчина: взаимодействие и способы защиты
Металл и ржавчина: взаимодействие и способы защиты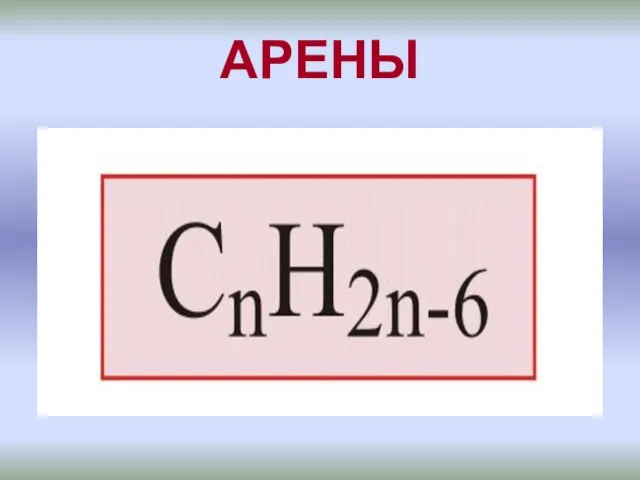 Бензоидные ароматические углеводороды - арены
Бензоидные ароматические углеводороды - арены Диссертация «Анализ и моделирование колебательно-вращательных спектров высокого разрешения молекулы двуокиси азота»
Диссертация «Анализ и моделирование колебательно-вращательных спектров высокого разрешения молекулы двуокиси азота» Отбор проб товаров для анализа. Химико-аналитический контроль
Отбор проб товаров для анализа. Химико-аналитический контроль Аттестационная работа. Задачи на смеси и сплавы
Аттестационная работа. Задачи на смеси и сплавы Способы получения полимеров (Лекция 3)
Способы получения полимеров (Лекция 3) Производство серной кислоты контактным способом
Производство серной кислоты контактным способом Предмет биоорганической химии. Классификация, строение, реакционная способность органических соединений
Предмет биоорганической химии. Классификация, строение, реакционная способность органических соединений Сульфиды. Лекция 8
Сульфиды. Лекция 8 The alkali metals
The alkali metals Классификация химических реакций
Классификация химических реакций Оксиды углероды
Оксиды углероды Презентация по химии Применение кислорода
Презентация по химии Применение кислорода Дисперсные системы. Коллоидные растворы
Дисперсные системы. Коллоидные растворы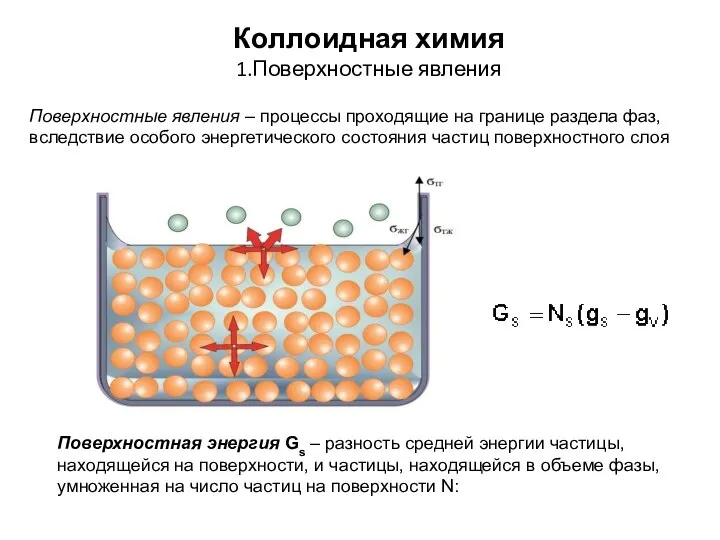 Коллоидная химия. Поверхностные явления
Коллоидная химия. Поверхностные явления Презентация по Химии "Степень окисления" - скачать смотреть
Презентация по Химии "Степень окисления" - скачать смотреть  Состав, строение, классификация кислот
Состав, строение, классификация кислот Стимулсезімтал сополимерлердің полимерлік комплексін зерттеу
Стимулсезімтал сополимерлердің полимерлік комплексін зерттеу Пральні порошки. Мила
Пральні порошки. Мила  Особенности строения, реакционной способности и методы синтеза галогенпроизводных углеводородов
Особенности строения, реакционной способности и методы синтеза галогенпроизводных углеводородов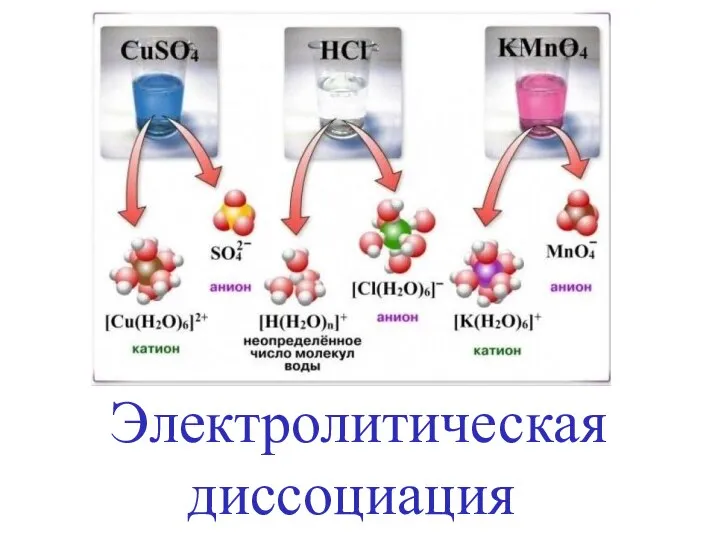 Электролитическая диссоциация
Электролитическая диссоциация Конструкционные функциональные волокнистые композиты
Конструкционные функциональные волокнистые композиты Окислительно-восстановительные реакции с участием органических веществ
Окислительно-восстановительные реакции с участием органических веществ Ионизирующее излучение и окружающая среда
Ионизирующее излучение и окружающая среда Елементи VІ групи головної підгрупи
Елементи VІ групи головної підгрупи Підготувала учениця 11-А класу Білецька Олеся
Підготувала учениця 11-А класу Білецька Олеся