Содержание
- 2. ПЛАН Основные понятия Классификация ОВР Составление уравнений окислительно-восстановительных реакций Распространенные окислители и восстановители Окислительно-восстановительная двойственность Влияние
- 3. Антуан Лоран Лавуазье 1743 – 1794 гг. Французский химик, член Парижской академии наук. Ввел в химию
- 4. Одним из первых сформулировал определение окислительно-восстановительных реакций как процесса переноса электронов русский химик Л. В. Писаржевский.
- 8. Основные понятия Степень окисления - заряд атома элемента в соединении, вычисленный исходя из предположения, что соединение
- 9. Постоянные степени окисления в соединениях проявляют: +1 все щелочные металлы ( Li, Na, K, Rb, Cs
- 10. Окислительно-восстановительные реакции - реакции, в ходе которых изменяются степени окисления вследствие перехода электронов от восстановителя к
- 11. Изменение степени окисления элемента - результат отдачи или присоединения электронов теми химическими соединениями, в которые входят
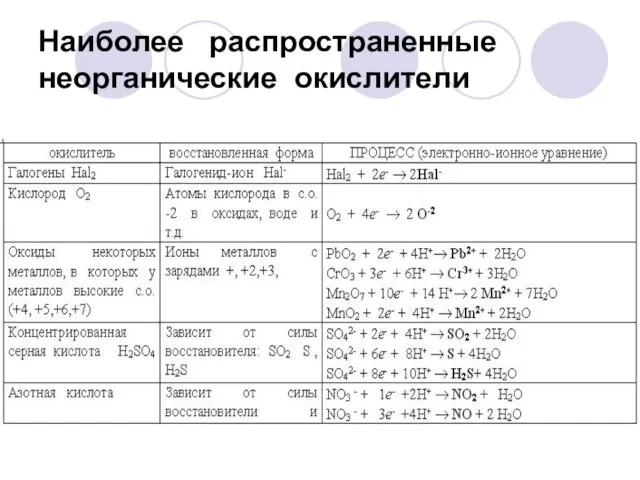
- 12. Наиболее распространенные неорганические окислители
- 19. Наиболее распространенные неорганические восстановители
- 20. Окислительно-восстановительная двойственность Окислительно-восстановительная двойственность – способность одного и того же вещества, в зависимости от реагентов и
- 21. Окислительно-восстановительная двойственность
- 23. Классификация ОВР
- 24. Межмолекулярные окислительно-восстановительные реакции – реакции, в которых окислитель и восстановитель находятся в разных веществах.
- 25. Внутримолекулярные окислительно-восстановительные реакции - реакции, в которых окислитель и восстановитель находятся в одном веществе, но представлены
- 26. Диспропорционирование - ОВР, в которых окислителем и восстановителем является один и тот же элемент, в одной
- 27. Конпропорционирование – ОВР, в которых окислителем и восстановителем является один и тот же элемент в разных
- 28. Составление уравнений окислительно-восстановительных реакций Электронный баланс - метод нахождения коэффициентов в уравнениях окислительно-восстановительных реакций, в котором
- 29. Составление уравнений окислительно-восстановительных реакций Электронно-ионный баланс (метод полуреакций) метод нахождения коэффициентов, в котором рассматривается обмен электронами
- 30. Зависимость направления протекания ОВР от среды а) Кислая среда, рН
- 31. Зависимость направления протекания ОВР от среды б) Нейтральная среда, рН =7
- 32. Зависимость направления протекания ОВР от среды в) Щелочная среда, рН>7
- 33. Эквивалент окислителя и эквивалент восстановителя – это часть моля, которая отвечает соответственно одному присоединенному или отданному
- 34. Электродный потенциал. Уравнение Нернста Если пластину любого металла погрузить в воду или раствор электролита, содержащий ионы
- 35. Эту разность электрических потенциалов или скачок потенциала на границе металл-раствор электролита называют электродным потенциалом. Величина электродного
- 36. где E0Me- стандартный электродный потенциал R- универсальная газовая постоянная F- постоянная Фарадея n - заряд иона
- 37. Потенциалы, измеренные при температуре равной 250С, Р=101,325кПа и концентрации ионов 1 моль/л называются стандартными электродными потенциалами
- 38. 1) чем меньше электродный потенциал металла Е0 ,тем легче он окисляется и труднее восстанавливается из своих
- 39. Связь с энергией Гиббса ∆G =-nEF Реакция возможна, только при ∆G 0
- 41. Понятие о гальваническом элементе Гальванический элемент – это устройство, в котором на основе ОВР получают электрический
- 42. H2S + Cl2 + H2O → K2Cr2O7 + H2S + H2SO4 → KClO3 + Na2SO3 →
- 44. Скачать презентацию







































 Radiation dosimetry
Radiation dosimetry Биоэнергетика. Часть первая
Биоэнергетика. Часть первая Валентность. Порядок действий при составлении химической формулы
Валентность. Порядок действий при составлении химической формулы Липиды. Классификация липидов
Липиды. Классификация липидов Класифікація вуглеводнів. Утворення ковалентних карбон-карбонових зв’язків у органічних сполуках. Види гібридизації електро
Класифікація вуглеводнів. Утворення ковалентних карбон-карбонових зв’язків у органічних сполуках. Види гібридизації електро Кислород
Кислород Фазовые диаграммы трехкомпонентных систем
Фазовые диаграммы трехкомпонентных систем Будова атома
Будова атома Переработка гидроминерального сырья
Переработка гидроминерального сырья Процессы нитрования
Процессы нитрования Карбонові кислоти. Насичені карбонові кислоти
Карбонові кислоти. Насичені карбонові кислоти Геохимия стабильных изотопов, Радиоуглеродный метод
Геохимия стабильных изотопов, Радиоуглеродный метод Презентация Угольная кислота
Презентация Угольная кислота Дисахариды, моносахариды
Дисахариды, моносахариды «Фосфор как элемент и вещество» урок химии 9 класс Мотайло М.В. учитель химии и биологии МОУ «Головчинская СОШ с УИОП» Белгородска
«Фосфор как элемент и вещество» урок химии 9 класс Мотайло М.В. учитель химии и биологии МОУ «Головчинская СОШ с УИОП» Белгородска Атомдар мен молекулалар
Атомдар мен молекулалар Понятие электрохимии. Процессы на границе металл – раствор. Электродные потенциалы. Гальванические элементы. Уравнение Нернста
Понятие электрохимии. Процессы на границе металл – раствор. Электродные потенциалы. Гальванические элементы. Уравнение Нернста Железо
Железо Предельные углеводороды
Предельные углеводороды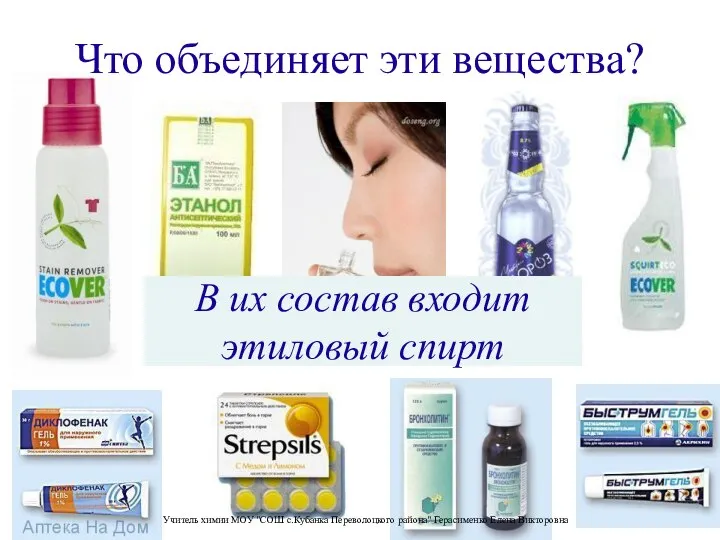 Что объединяет эти вещества?
Что объединяет эти вещества?  Презентация "Основания"
Презентация "Основания" Антибиотики. Действие антибиотиков
Антибиотики. Действие антибиотиков Важнейшие минералы
Важнейшие минералы Размерные эффекты. Причины и различные проявления размерных эффектов. Определение размерных эффектов
Размерные эффекты. Причины и различные проявления размерных эффектов. Определение размерных эффектов Хозяйственный механизм НГХК
Хозяйственный механизм НГХК Гліцерин (Гліцерол)
Гліцерин (Гліцерол) Классификация автомобильных масел
Классификация автомобильных масел Неорганические и органические основания.
Неорганические и органические основания.