Содержание
- 2. Окислительно-восстановительные реакции переход е от одних атомов (или ионов) к другим атомам, в результате которых изменяется
- 3. Окислительно-восстановительные реакции окисление - отдача е. восстановление - присоединение е. восстановитель - вещество, которое отдает е,
- 4. Окислительно-восстановительные реакции Число е, отдаваемых восстановителем, = числу е, присоединяемых окислителем.
- 5. Окислительно-восстановительные реакции Mg + Cl2 = MgCl2 Mg0 – 2е → Mg+2 - восстановитель (окисляется) Cl20
- 6. Окислительно-восстановительные реакции Вещество-окислитель и вещество-восстановитель называют сопряженной окислительно-восстановительной парой или системой.
- 7. Типы окислительно-восстановительных реакций межмолекулярные протекают с изменением степени окисления атомов в различных молекулах: Mg + Cl2
- 8. Типы окислительно-восстановительных реакций внутримолекулярные – сопровождаются изменением степени окисления различных атомов в одной и той же
- 9. Типы окислительно-восстановительных реакций диспропорционирования – протекают с одновременным изменением степени окисления атомов одного и того же
- 10. Метод электронного баланса подсчет числа отдаваемых и присоединяемых е проводится в соответствии со значениями степеней окисления
- 11. Метод электронного баланса KMnO4 + KI + H2SO4 → K2SO4 + MnSO4 + I2 + H2O
- 12. Метод электронного баланса Mn +7 + 5е → Mn +2 (восстановление) 2I -1 – 2е →
- 13. Метод электронного баланса Mn +7 + 5е → Mn +2 2 2I -1 – 2е
- 14. Метод электронного баланса 2KMnO4 + 10KI + H2SO4 → K2SO4 + 2MnSO4 + 5I2 + H2O
- 15. Метод электронного баланса суммарное уравнение: 2KMnO4 + 10KI + 8H2SO4 → 6K2SO4 + 2MnSO4 + 5I2
- 16. Ионно-электронный метод (метод полуреакций) - составление сокращенного ионного уравнения с участием ионов, участвующих в процессах окисления
- 17. Ионно-электронный метод K+ + MnO4- + K+ + I- + 2H+ + SO42- → 2K+ +
- 18. Ионно-электронный метод MnO4- + I- + 2H+ → Mn2+ + I2 + H2O
- 19. Ионно-электронный метод первая полуреакция: MnO4- + 8H+ + 5е → Mn2+ + 4H2O вторая полуреакция: 2I
- 20. Ионно-электронный метод MnO4- + 8H+ + 5е → Mn2+ + 4H2O 2 (восстановление) 2I - –
- 21. Ионно-электронный метод суммарное уравнение: 2KMnO4 + 10KI + 8H2SO4 → 6K2SO4 + 2MnSO4 + 5I2 +
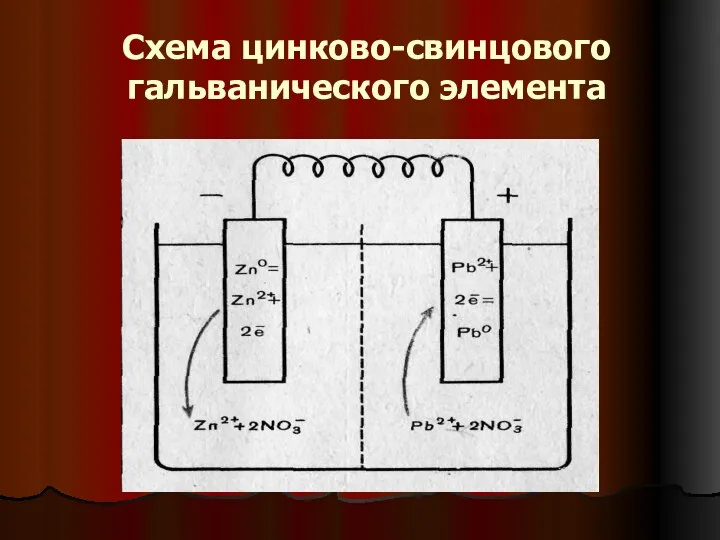
- 22. Схема цинково-свинцового гальванического элемента
- 23. В гальваническом элементе e идут от «-» полюса к «+» полюсу восстановительные процессы – на катоде
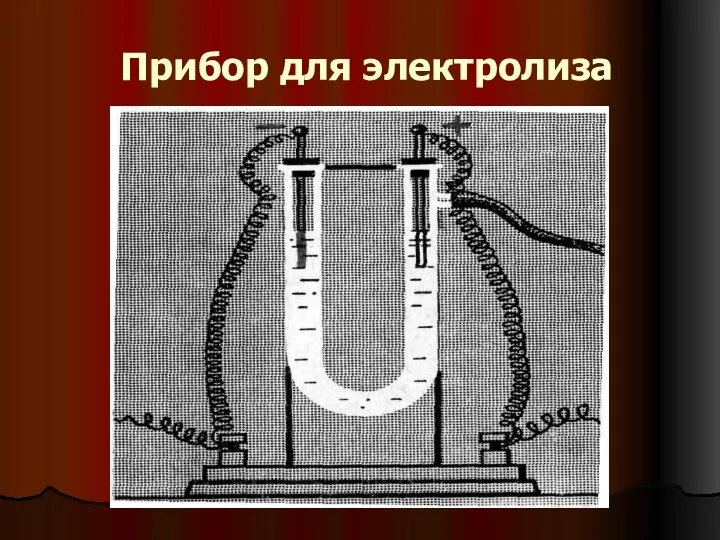
- 24. Прибор для электролиза
- 25. Электролиз – ОВР, протекающие на электродах при прохождении через раствор или расплав электролита электрического тока.
- 27. Скачать презентацию






















 Белый камень
Белый камень Непредельные углеводороды: этилен
Непредельные углеводороды: этилен Липиды
Липиды Презентация по химии Ферменты
Презентация по химии Ферменты  Periodic Table: It’s Elementary
Periodic Table: It’s Elementary Органическая химия. История развития
Органическая химия. История развития Дипломная работа. Тема: Получение гальванических покрытий на основе цинка
Дипломная работа. Тема: Получение гальванических покрытий на основе цинка Кобаламины(витамин В12) антианемический
Кобаламины(витамин В12) антианемический Фенолы. Простые эфиры
Фенолы. Простые эфиры Иондық емес флокулянттар
Иондық емес флокулянттар Химическая номенклатура
Химическая номенклатура Crystal defects
Crystal defects Биотехнология туралы түсінік
Биотехнология туралы түсінік Биогеохимия: основные понятия, история развития, практическое значение идей биогеохимии
Биогеохимия: основные понятия, история развития, практическое значение идей биогеохимии Набухание наполненных полимеров
Набухание наполненных полимеров Роль химической науки в производстве искусственной пищи
Роль химической науки в производстве искусственной пищи Презентация по Химии "Методы разделения и концентрирования" - скачать смотреть бесплатно
Презентация по Химии "Методы разделения и концентрирования" - скачать смотреть бесплатно Презентация по Химии "Химия и реклама" - скачать смотреть
Презентация по Химии "Химия и реклама" - скачать смотреть  Пиридин. Строение пиридина
Пиридин. Строение пиридина Гидролиз солей
Гидролиз солей Кам’яне вугілля Підготувала учениця 11а класу Нагайло Марта
Кам’яне вугілля Підготувала учениця 11а класу Нагайло Марта  Ванадий
Ванадий Макроэлементтер N,Cа,P
Макроэлементтер N,Cа,P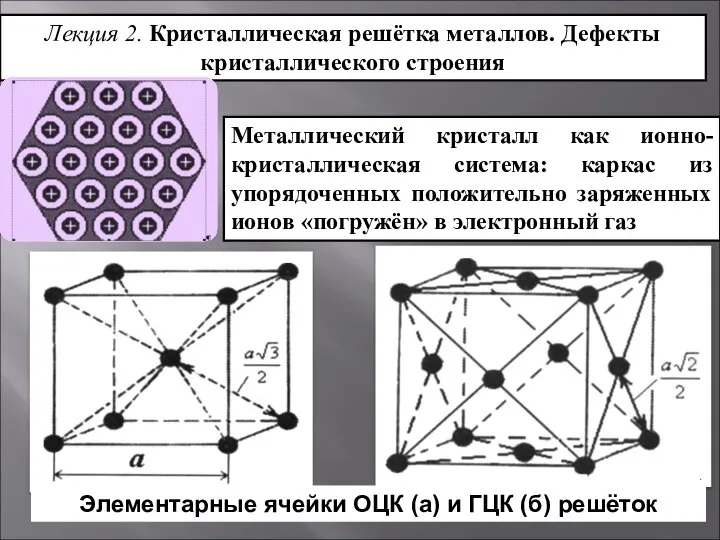 Кристаллическая решётка металлов. Дефекты кристаллического строения. Лекция 2
Кристаллическая решётка металлов. Дефекты кристаллического строения. Лекция 2 Пищевые кислоты Выполнил: Черепнин Евгений Группа: ТХ-921
Пищевые кислоты Выполнил: Черепнин Евгений Группа: ТХ-921  Теория Опарина
Теория Опарина Способы переработки нефти
Способы переработки нефти Методы разделения и концентрирования
Методы разделения и концентрирования