Содержание
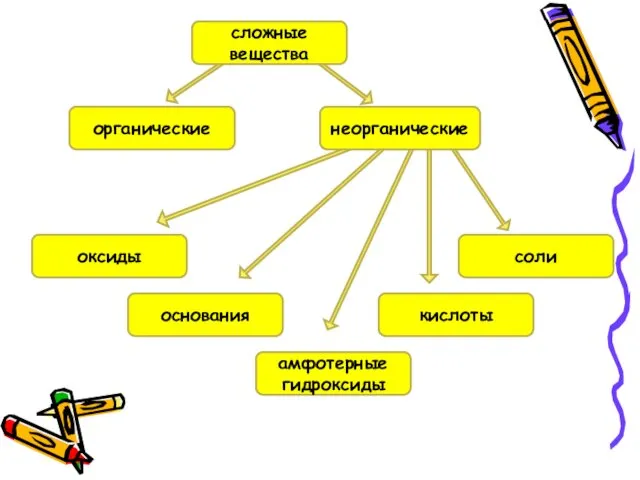
- 2. органические основания кислоты амфотерные гидроксиды соли оксиды неорганические сложные вещества
- 3. Me(OH)n ОСНОВАНИЯ - это сложные вещества, состоящие из ионов металлов и гидроксид-ионов Гидроксид-ион имеет суммарный заряд
- 4. - -
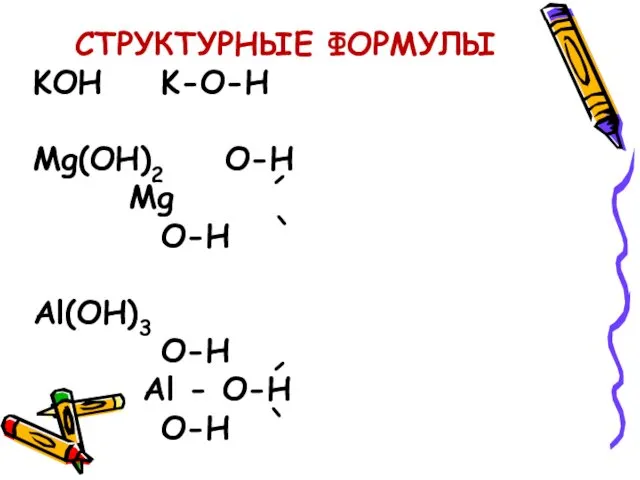
- 5. НОМЕНКЛАТУРА (НАЗВАНИЯ) ГИДРОКСИДОВ NaOH – гидроксид натрия читается «натрий-о-аш» Mg(OH)2 – гидроксид магния читается «магний-о-аш-дважды» Fe(OH)2
- 6. НОМЕНКЛАТУРА ГИДРОКСИДОВ Ca(OH)2 Al(OH)3 KOH CuOH Cu(OH)2
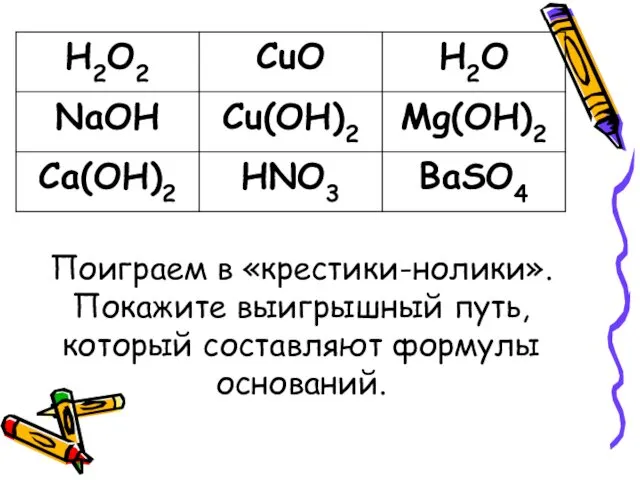
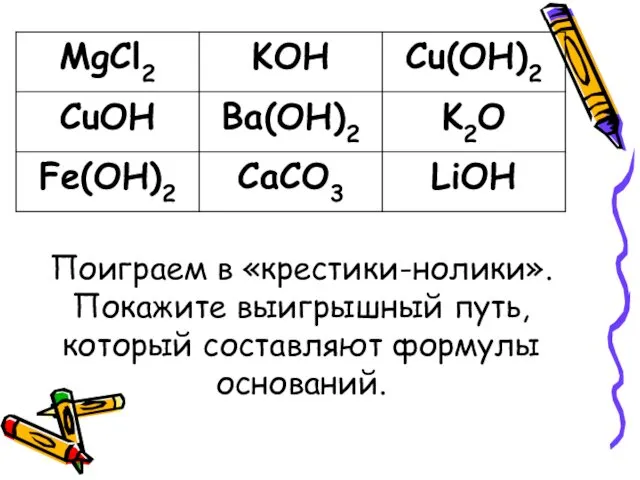
- 7. Поиграем в «крестики-нолики». Покажите выигрышный путь, который составляют формулы оснований.
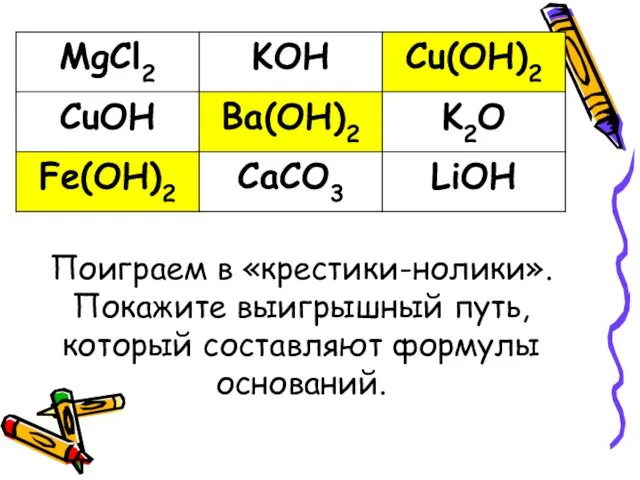
- 8. Поиграем в «крестики-нолики». Покажите выигрышный путь, который составляют формулы оснований.
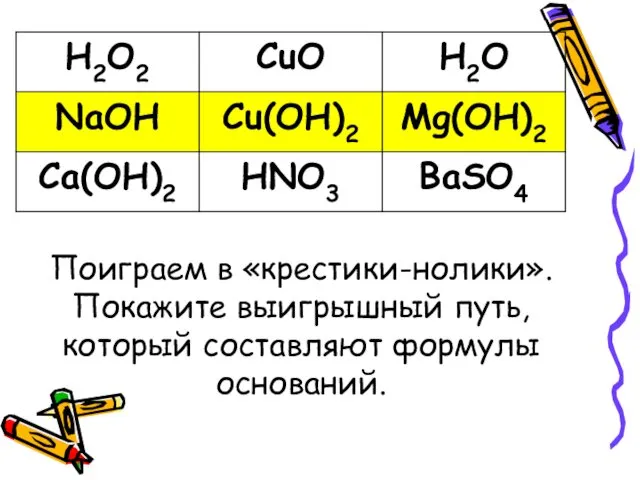
- 9. Поиграем в «крестики-нолики». Покажите выигрышный путь, который составляют формулы оснований.
- 10. Поиграем в «крестики-нолики». Покажите выигрышный путь, который составляют формулы оснований.
- 11. СОСТАВЛЕНИЕ ФОРМУЛ ГИДРОКСИДОВ
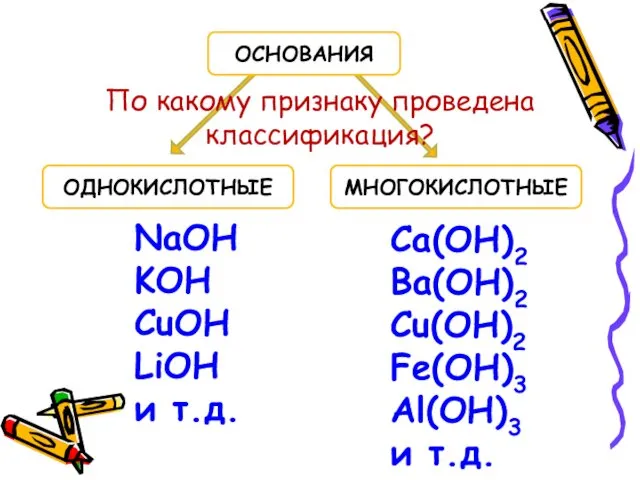
- 12. ОДНОКИСЛОТНЫЕ МНОГОКИСЛОТНЫЕ ОСНОВАНИЯ NaOH KOH CuOH LiOH и т.д. Ca(OH)2 Ba(OH)2 Cu(OH)2 Fe(OH)3 Al(OH)3 и т.д.
- 13. Подчеркните формулы оснований NaOHHClAl(OH)3FeCl2Ba(OH)2CO2Mg(OH)2Na2S Cu(OH)2SCa(OH)2Ca(NO3)2KOHMnSO4Fe(OH)2
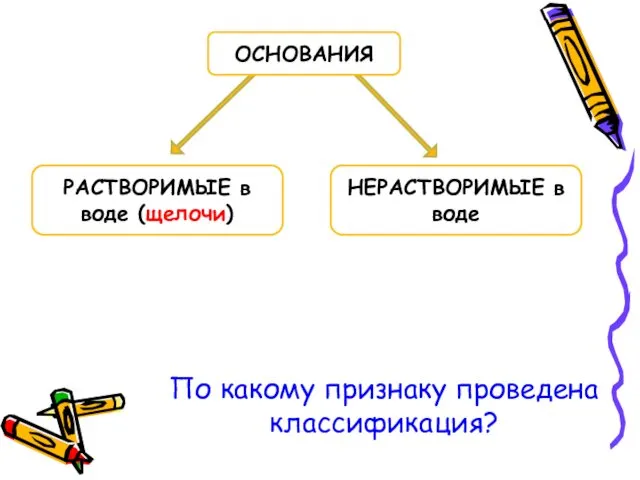
- 14. РАСТВОРИМЫЕ в воде (щелочи) НЕРАСТВОРИМЫЕ в воде ОСНОВАНИЯ По какому признаку проведена классификация?
- 15. ЗАДАЧА 1. Вычислите, какое количество вещества составляет 684 г гидроксида бария.
- 16. ЗАДАЧА 2. Определите массу 0,5 моль гидроксида кальция.
- 17. ЗАДАЧА 3. Определите, сколько молекул содержат: а) 100г NaOH, б) 20г NaOH, в) 8г NaOH.
- 18. Домашнее задание §20 – учить в тетради Стр. 118 Таблица 4 – переписать в тетрадь №1-6
- 21. Скачать презентацию










 Арены и ароматичность
Арены и ароматичность АЛОТРОПНІ ФОРМИ КАРБОНУ АВТОР: НАЗАРЕНКО МАКСИМ ВОЛОДИМИРОВИЧ 9-А КЛАС,ГІМНАЗІЯ №32 ПЕЧЕРСЬКИЙ РАЙОН, М. КИЇВ ПЕДАГОГІЧНИЙ КЕ
АЛОТРОПНІ ФОРМИ КАРБОНУ АВТОР: НАЗАРЕНКО МАКСИМ ВОЛОДИМИРОВИЧ 9-А КЛАС,ГІМНАЗІЯ №32 ПЕЧЕРСЬКИЙ РАЙОН, М. КИЇВ ПЕДАГОГІЧНИЙ КЕ Препараты гормонов стероидной структуры
Препараты гормонов стероидной структуры Закон постоянства углов Стено
Закон постоянства углов Стено Растворы. Общая характеристика растворов
Растворы. Общая характеристика растворов Арены. Бензол
Арены. Бензол Обмен веществ и энергии, основа существования клетки
Обмен веществ и энергии, основа существования клетки КАЛЬЦИЙ И ЕГО СОЕДИНЕНИЯ 9 класс МКОУ «СОШ № 85» г. Тайшет Иркутской обл. Учитель: Никитюк Л.Ф.
КАЛЬЦИЙ И ЕГО СОЕДИНЕНИЯ 9 класс МКОУ «СОШ № 85» г. Тайшет Иркутской обл. Учитель: Никитюк Л.Ф. Пены. Пенообразование
Пены. Пенообразование Введение в титриметрический анализ. Кислотно-основное титрование
Введение в титриметрический анализ. Кислотно-основное титрование Щелочные металлы
Щелочные металлы Ковалентная химическая связь
Ковалентная химическая связь Элементы группы VII B
Элементы группы VII B Мыс айналымы
Мыс айналымы Презентация по Химии "Разнообразие кристаллов и их выращивание" - скачать смотреть
Презентация по Химии "Разнообразие кристаллов и их выращивание" - скачать смотреть  Модифицирование структуры полисахаридов гидрофобными заместителями: твердофазный синтез, исследование структуры и свойств
Модифицирование структуры полисахаридов гидрофобными заместителями: твердофазный синтез, исследование структуры и свойств Макроэлементы и микроэлементы
Макроэлементы и микроэлементы Виды изомерии у моносахаридов
Виды изомерии у моносахаридов Презентация по теме «Металлы» «Уран» Работа Садковского Ивана 9 «В»
Презентация по теме «Металлы» «Уран» Работа Садковского Ивана 9 «В» Хімічний склад і використання мінералів
Хімічний склад і використання мінералів Характеристика элементов VIIA-группы (галогены)
Характеристика элементов VIIA-группы (галогены) Электролиз: опыты к заданиям ЕГЭ
Электролиз: опыты к заданиям ЕГЭ Биосинтез жирных кислот и триацилглицеролов. Обмен липидов. (Лекция 13)
Биосинтез жирных кислот и триацилглицеролов. Обмен липидов. (Лекция 13) Аттестационная работа. Методическая разработка фрагмента урока химии с элементами исследовательской деятельности
Аттестационная работа. Методическая разработка фрагмента урока химии с элементами исследовательской деятельности Электрохимические методы. (Лекция 3)
Электрохимические методы. (Лекция 3) Электролиз. Урок химии 11 класс
Электролиз. Урок химии 11 класс Переработка нефти. (10 класс)
Переработка нефти. (10 класс) Сплавы, растворы и смеси. Задачи на концентрвцию
Сплавы, растворы и смеси. Задачи на концентрвцию