Содержание
- 3. Простые вещества Металлы І группа главная подгруппа – щелочные металлы ІІ группа главная подгруппа – щелочноземельные
- 4. Металлы. Неметаллы
- 5. Физические свойства простых веществ
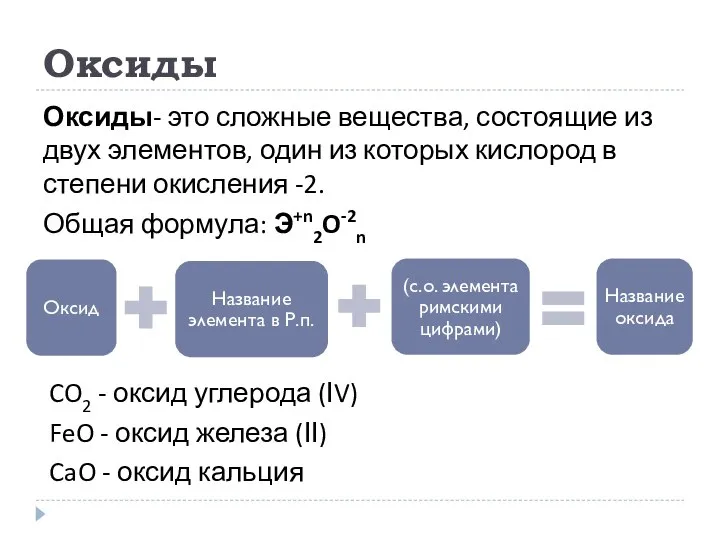
- 6. Оксиды Оксиды- это сложные вещества, состоящие из двух элементов, один из которых кислород в степени окисления
- 7. Оксиды 1) Несолеобразующие - CO, SiO, N2O, NO, NO2 2) Солеобразующие Основные – металлы со с.о.
- 8. Гидриды Гидриды - соединения водорода с металлами или менее электроотрицательными, чем водород, неметаллами. LiH, CaH2, AlH3
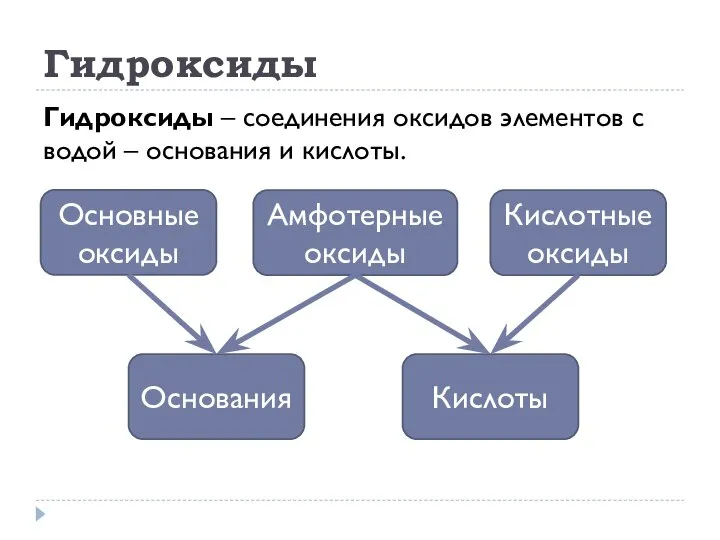
- 9. Гидроксиды Гидроксиды – соединения оксидов элементов с водой – основания и кислоты.
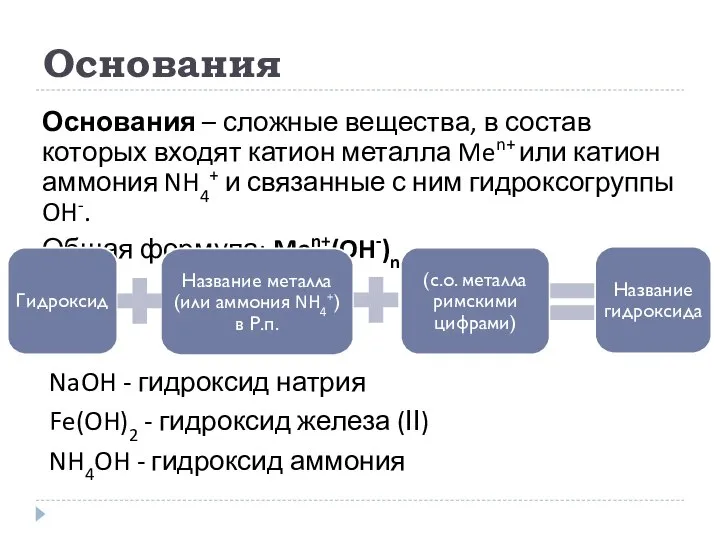
- 10. Основания Основания – сложные вещества, в состав которых входят катион металла Men+ или катион аммония NH4+
- 11. Основания По числу гидроксогрупп OH: Однокислотные – NaOH, KOH Двухкислотные – Ca(OH)2, Ba(OH)2 Многокислотные – Al(OH)3,
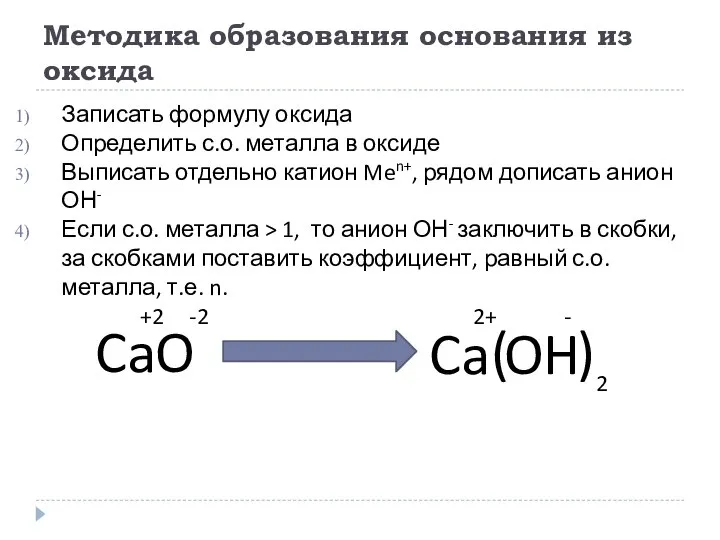
- 12. Методика образования основания из оксида Записать формулу оксида Определить с.о. металла в оксиде Выписать отдельно катион
- 13. Кислоты Кислоты – сложные вещества, молекулы которых состоят из атомов водорода Н+ и кислотных остатков Аm-.
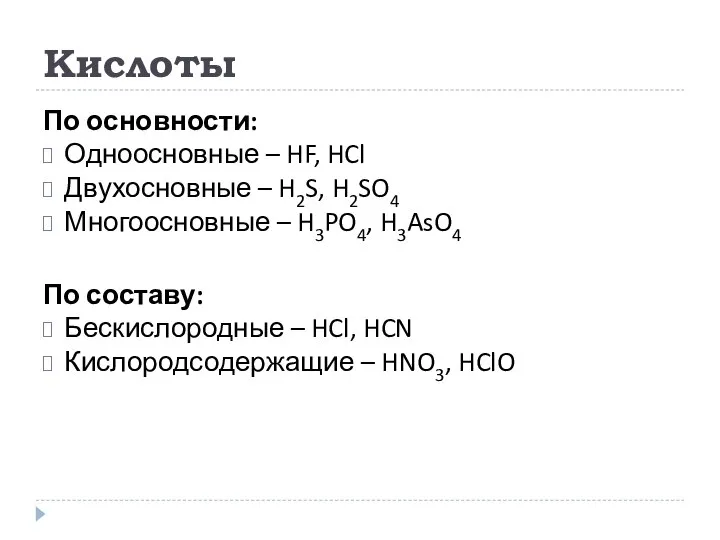
- 14. Кислоты По основности: Одноосновные – HF, HCl Двухосновные – H2S, H2SO4 Многоосновные – H3PO4, H3AsO4 По
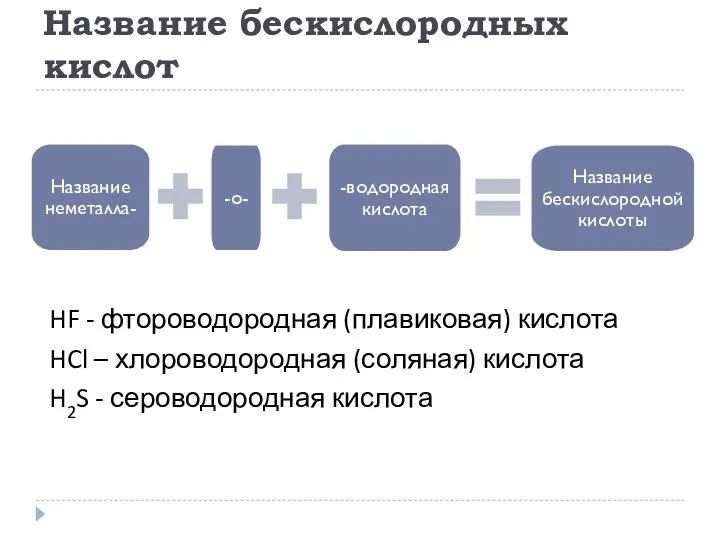
- 15. Название бескислородных кислот HF - фтороводородная (плавиковая) кислота HCl – хлороводородная (соляная) кислота H2S - сероводородная
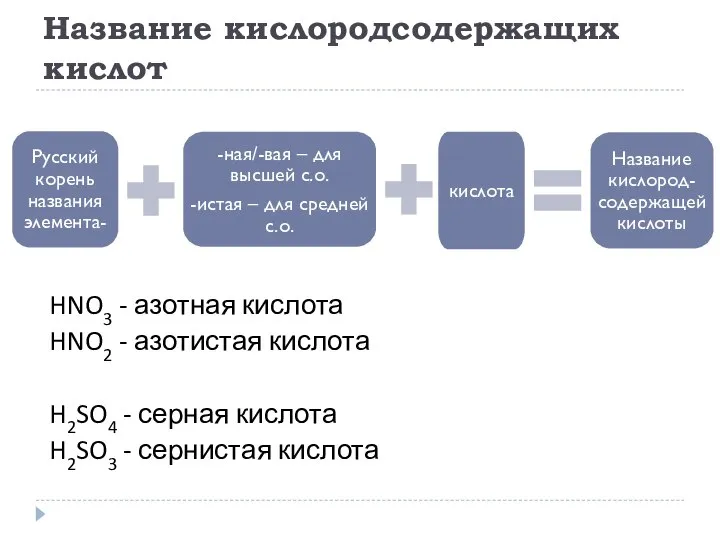
- 16. Название кислородсодержащих кислот HNO3 - азотная кислота HNO2 - азотистая кислота H2SO4 - серная кислота H2SO3
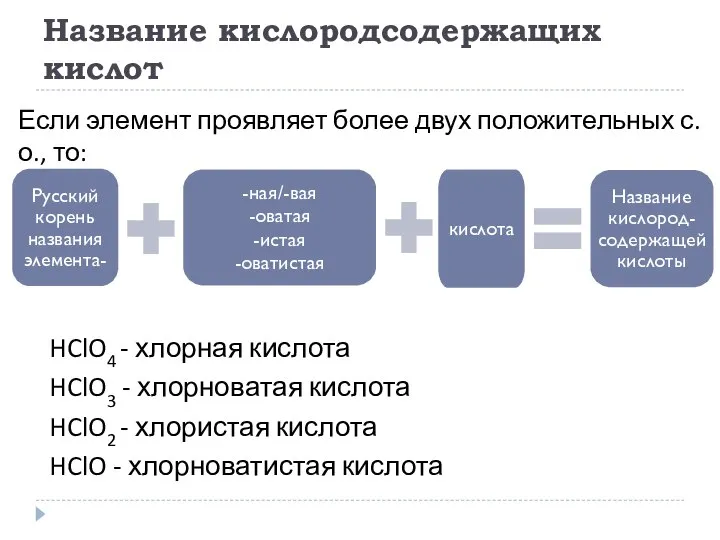
- 17. Название кислородсодержащих кислот HClO4 - хлорная кислота HClO3 - хлорноватая кислота HClO2 - хлористая кислота HClO
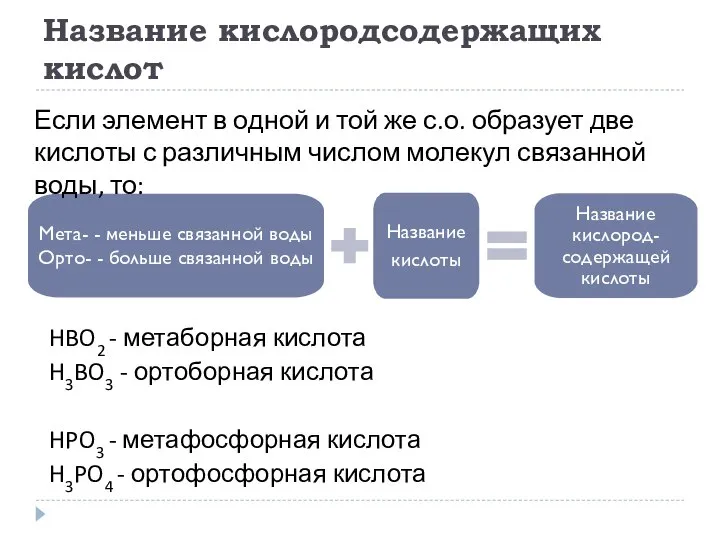
- 18. Название кислородсодержащих кислот HBO2 - метаборная кислота H3BO3 - ортоборная кислота HPO3 - метафосфорная кислота H3PO4
- 19. Методика образования кислоты из оксида Записать формулу оксида К оксиду алгебраически прибавить одну молекулу воды Сократить
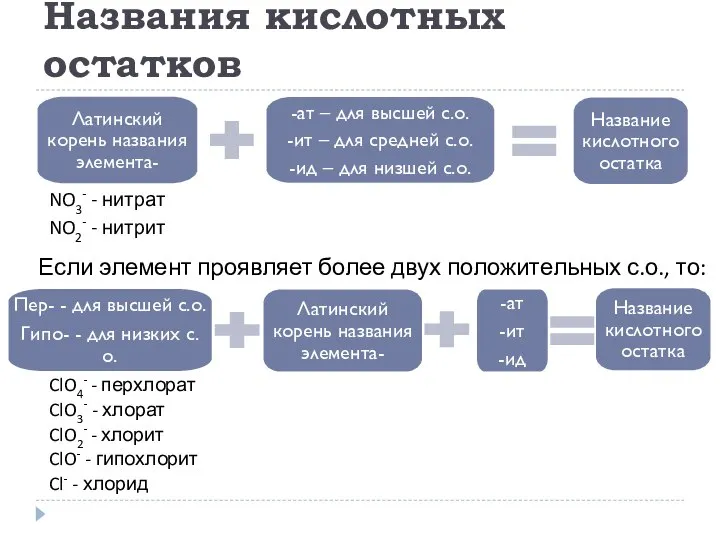
- 20. Названия кислотных остатков Если элемент проявляет более двух положительных с.о., то: ClO4- - перхлорат ClO3- -
- 21. Соли 1) Как продукты замены протонов в кислотах или гидроксогрупп в основаниях: Средние – KBr, CaSO4
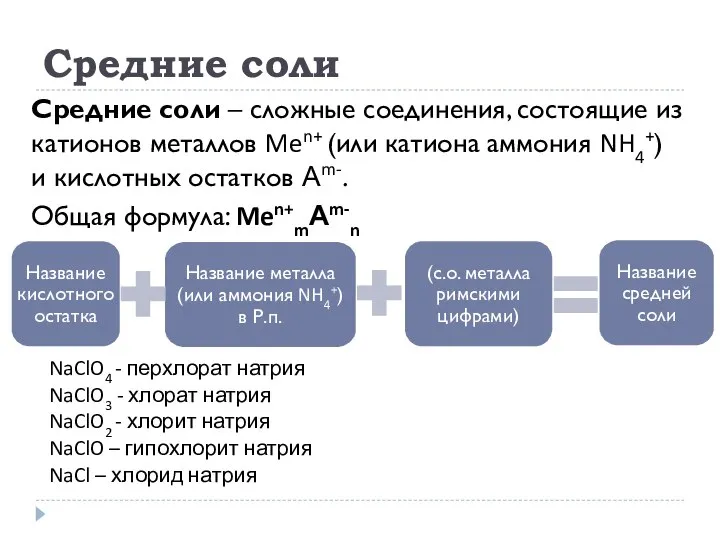
- 22. Средние соли Средние соли – сложные соединения, состоящие из катионов металлов Men+ (или катиона аммония NH4+)
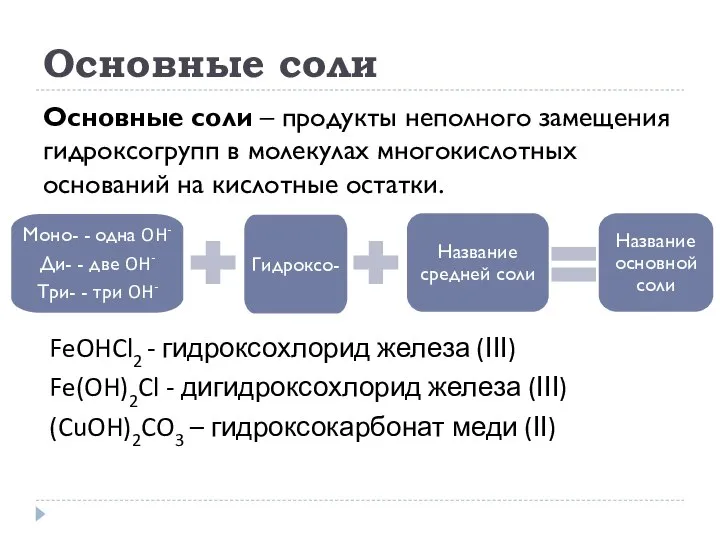
- 23. Основные соли Основные соли – продукты неполного замещения гидроксогрупп в молекулах многокислотных оснований на кислотные остатки.
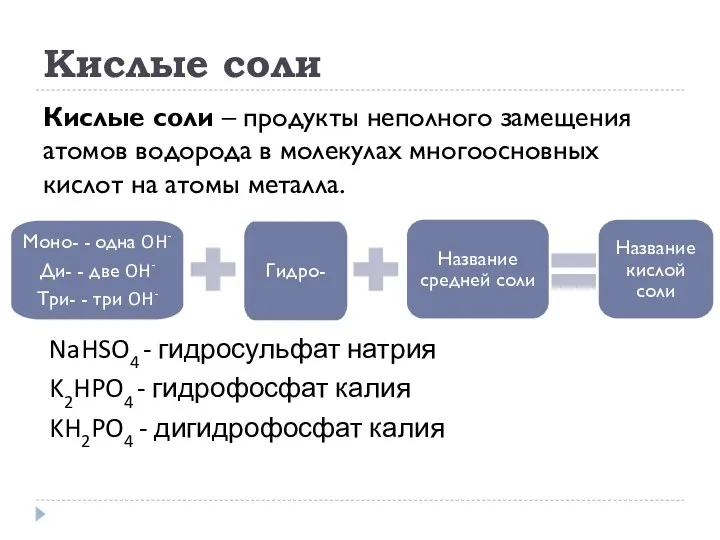
- 24. Кислые соли Кислые соли – продукты неполного замещения атомов водорода в молекулах многоосновных кислот на атомы
- 25. По числу присутствующих в структуре катионов и анионов Двойные соли – соли, содержащие два типа катионов.
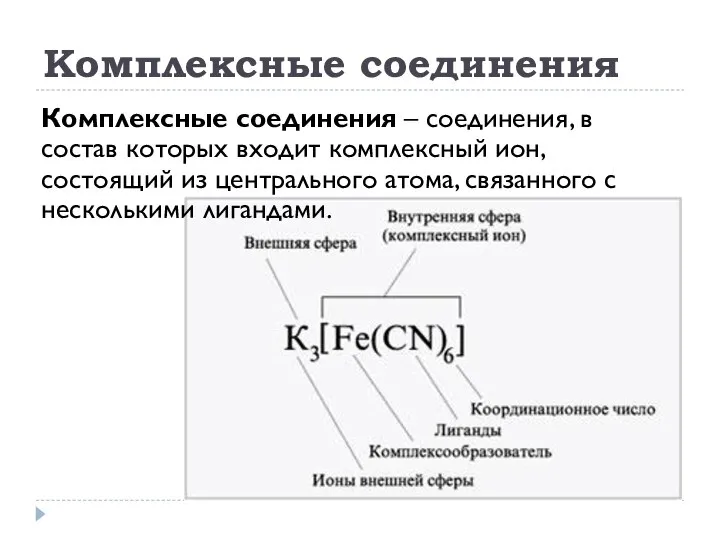
- 26. Комплексные соединения Комплексные соединения – соединения, в состав которых входит комплексный ион, состоящий из центрального атома,
- 28. Номенклатура комплексных соединений Если комплексный – анион: 1) Число лигандов (греческие числительные) 2) Латинское название лиганда
- 29. Номенклатура комплексных соединений Если комплексный – катион: 1) Число анионов внешней сферы 2) Латинское название анионов
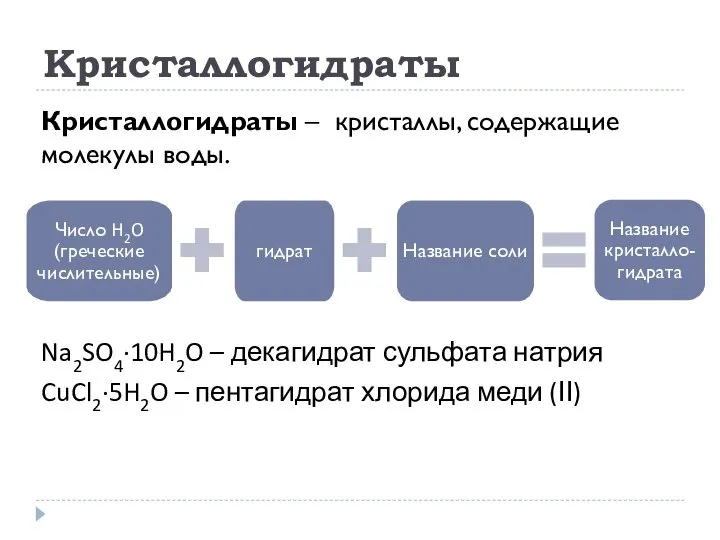
- 30. Кристаллогидраты Кристаллогидраты – кристаллы, содержащие молекулы воды. Na2SO4·10H2O – декагидрат сульфата натрия CuCl2·5H2O – пентагидрат хлорида
- 32. Скачать презентацию














 Этанол. Одноатомный спирт
Этанол. Одноатомный спирт Рекомендации по подготовке учащихся к выполнению заданий различного уровня сложности ЕГЭ по химии
Рекомендации по подготовке учащихся к выполнению заданий различного уровня сложности ЕГЭ по химии Гидролиз. Применение
Гидролиз. Применение Процессы формирования водородной плазмы в зоне резания
Процессы формирования водородной плазмы в зоне резания Презентация по Химии "Кремний" - скачать смотреть
Презентация по Химии "Кремний" - скачать смотреть  Сероводород. Польза или вред
Сероводород. Польза или вред Деградация пищевых и клеточных белков. (Лекция 1)
Деградация пищевых и клеточных белков. (Лекция 1) Магнитодиэлектрический эффект в нанокристаллическом мультиферроике BiFeO3
Магнитодиэлектрический эффект в нанокристаллическом мультиферроике BiFeO3 Способи та засоби припинення та запобігання процесів горіння. Припинення горіння методом охолодження. (Тема 15.24)
Способи та засоби припинення та запобігання процесів горіння. Припинення горіння методом охолодження. (Тема 15.24) Строение атома
Строение атома Факторы, влияющие на смещение химического равновесия (концентрация реагентов, температура, давление )
Факторы, влияющие на смещение химического равновесия (концентрация реагентов, температура, давление ) Тест по химии
Тест по химии ПОЧЕМУ СОЛИ СОЛЕНЫЕ ?
ПОЧЕМУ СОЛИ СОЛЕНЫЕ ? Применение эксклюзионной хроматографии в биологии
Применение эксклюзионной хроматографии в биологии Класс «оксиды»
Класс «оксиды» Уравнение состояния идеального газа. Решение задач
Уравнение состояния идеального газа. Решение задач Алканы
Алканы Применение серной кислоты
Применение серной кислоты Проведення електрофоретичного розділення ДНК в агарозному гелі
Проведення електрофоретичного розділення ДНК в агарозному гелі Резина и каучук
Резина и каучук № 15. Олигосахариды ПОЛИСАХАРИДЫ.
№ 15. Олигосахариды ПОЛИСАХАРИДЫ.  Презентация по Химии "Щелочные металлы" - скачать смотреть
Презентация по Химии "Щелочные металлы" - скачать смотреть  Предмет биоорганической химии. Классификация, строение, реакционная способность органических соединений
Предмет биоорганической химии. Классификация, строение, реакционная способность органических соединений Технология производства аминоальдегидных смол
Технология производства аминоальдегидных смол Периодическая система химических элементов Д.И.Менделеева Учитель химии МБОУ СОШ №37 г. Шахты Ростовской области Вабищевич М.В.
Периодическая система химических элементов Д.И.Менделеева Учитель химии МБОУ СОШ №37 г. Шахты Ростовской области Вабищевич М.В. "We know it only takes one critically short telomere to make a cell die, so it's clear that the more really short telomeres a person has the faster problems will develop.“ Carol Greider Образ жизни и длина теломер
"We know it only takes one critically short telomere to make a cell die, so it's clear that the more really short telomeres a person has the faster problems will develop.“ Carol Greider Образ жизни и длина теломер Solutions. Acid–base equilibrium in biological systems
Solutions. Acid–base equilibrium in biological systems Строение атома. Движение электрона в атоме
Строение атома. Движение электрона в атоме