Содержание
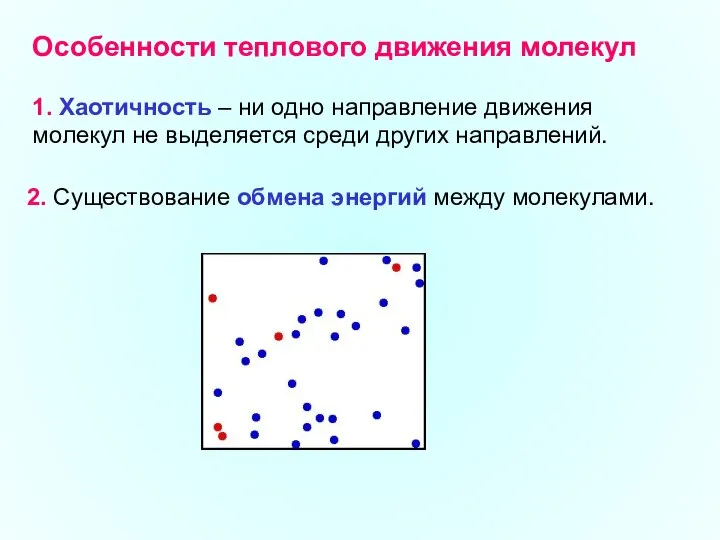
- 2. Особенности теплового движения молекул 1. Хаотичность – ни одно направление движения молекул не выделяется среди других
- 3. Необходимо учитывать вращательное движение молекул и число степеней свободы этих молекул. Молекулы многоатомных газов нельзя рассматривать
- 4. Для описания поступательного движения используются три независимых компоненты энергии: Для описания вращательного движения используются три независимых
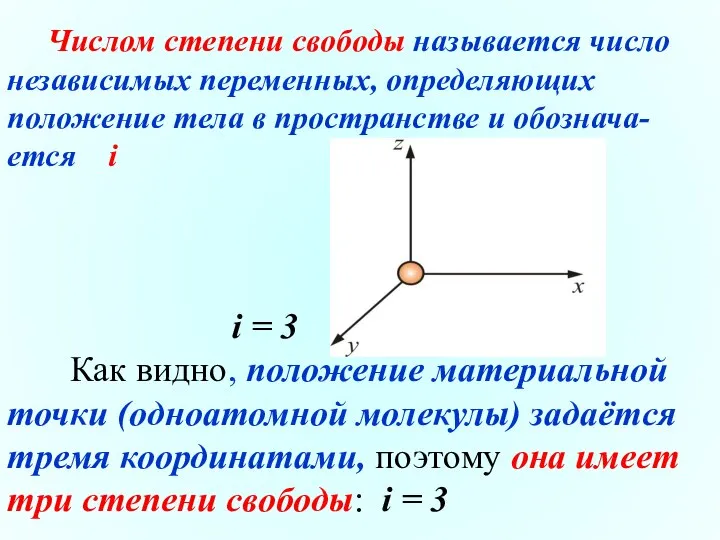
- 5. Числом степени свободы называется число независимых переменных, определяющих положение тела в пространстве и обознача-ется i i
- 6. У системы из N невзаимодействующих материальных точек имеется 3N степеней свободы. Если между 2-мя точками имеется
- 7. Многоатомная молекула может ещё и вращаться. Например, у двухатомных молекул вращательное движение можно разложить на два
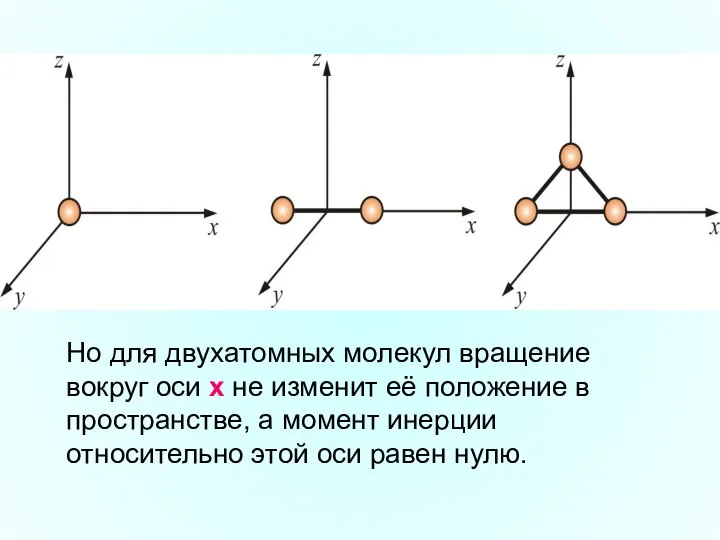
- 8. Но для двухатомных молекул вращение вокруг оси х не изменит её положение в пространстве, а момент
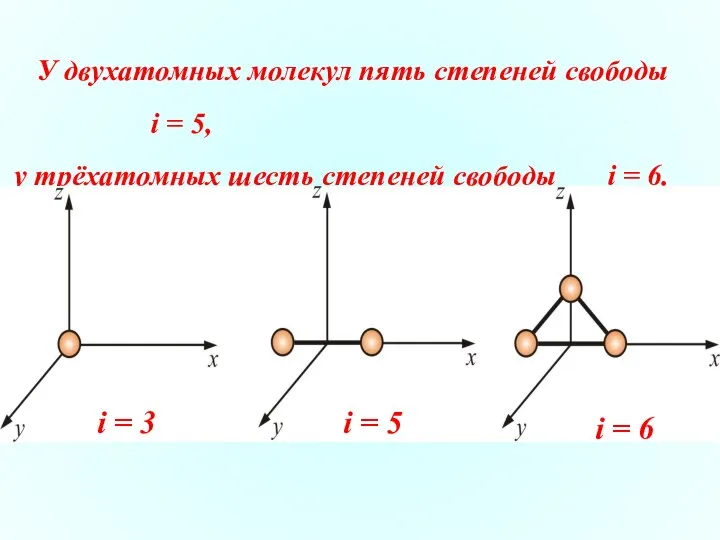
- 9. У двухатомных молекул пять степеней свободы i = 5, у трёхатомных шесть степеней свободы i =
- 10. У системы из N упруго связанных точек имеется 3N степеней свободы, из которых: 3 степени –
- 11. Теперь рассмотрим молекулы. При определении числа степеней свободы молекулы входящие в нее атомы надо рассматривать как
- 12. Если два атома в двухатомной молекуле связаны не жестко, а упруго, то расстояние между атомами может
- 14. При взаимных столкновениях молекул возможен обмен их энергиями и превращение энергии вращательного движения в энергию поступательного
- 15. Больцман доказал, что, средняя энергия приходящаяся на одну степень свободы равна Закон о равномерном распределении энергии
- 16. У одноатомной молекулы i = 3, тогда (4.4.2) для двухатомных молекул i = 5 (4.4.3) для
- 17. На среднюю кинетическую энергию молекулы, имеющей i-степеней свободы приходится (4.4.5) Это и есть закон Больцмана о
- 18. Характер и величина силы взаимодействия между молекулами зависят от расстояния между ними. Установлено, что на малых
- 19. колебательное движение молекул не является, вообще говоря, гармоническим, так как действующие на молекулы силы не удовлетворяют
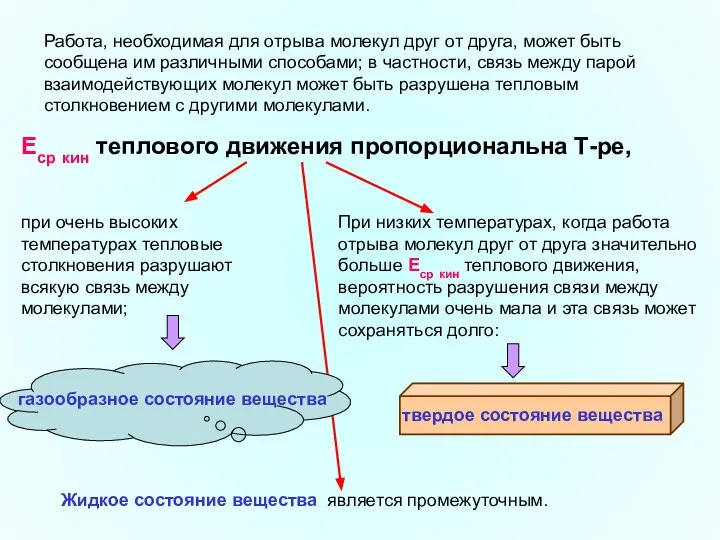
- 20. Работа, необходимая для отрыва молекул друг от друга, может быть сообщена им различными способами; в частности,
- 21. Агрегатные состояния и фазовые переходы. Равновесные и неравновесные состояния и процессы агрегатные состояния определяются соотношением величин
- 22. Выделяют два вида переходов вещества из одного состояния в другое 1) переходы, при которых меняются только
- 23. Термодинамической системой называется всякая физическая система, состоящая из большого числа частиц — атомов и молекул, которые
- 24. Для некоторых систем существуют такие состояния, называемые метастабильными, в которых эти системы могут находиться относительно долгое
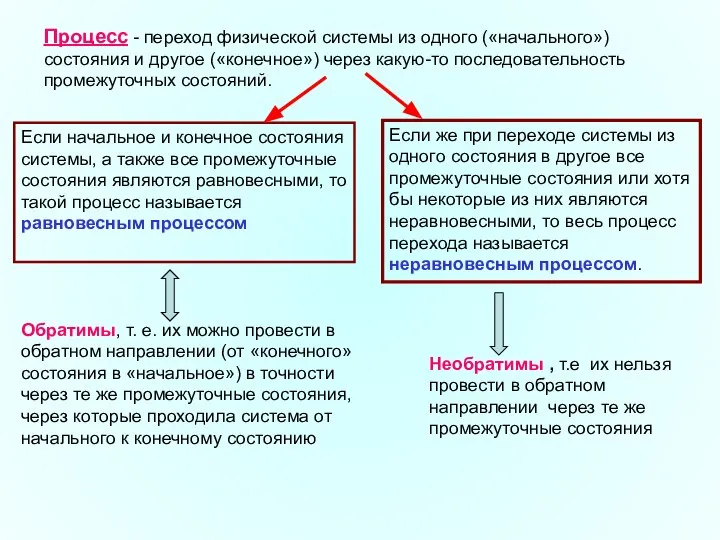
- 25. Процесс - переход физической системы из одного («начального») состояния и другое («конечное») через какую-то последовательность промежуточных
- 26. Основные условия, необходимые для того, чтобы процесс был обратимым 1) процесс должен протекать настолько медленно, чтобы
- 27. Внутренняя энергия термодинамической системы Внутренней энергией любого тела называется энергия этого тела за вычетом кинетической энергии
- 28. Внутренняя энергия системы является однозначной функцией ее состояния, т. е. в каждом определенном состоянии система обладает
- 29. Понятно, что в общем случае термодинамическая система может обладать как внутренней, так и механической энергией и
- 30. Способ передачи энергии, связанный с изменением внешних макропараметров системы, называется работой; без изменения внешних макропараметров, но
- 31. Изменение внутренней энергии ΔU при переходе системы из состояния 1 в состояние 2 не зависит от
- 32. Закон сохранения энергии для систем, в которых существенную роль играют тепловые процессы, называется первым началом термодинамики:
- 35. Скачать презентацию


























 Готовимся к экзамену по химии. 9 класс
Готовимся к экзамену по химии. 9 класс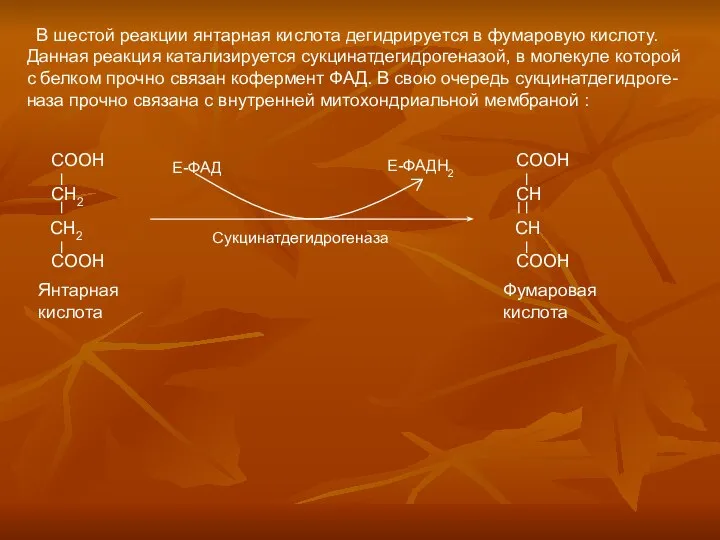 Аэробное окисление углеводов. (Часть 2)
Аэробное окисление углеводов. (Часть 2) Оксиды азота
Оксиды азота Классификация кислот
Классификация кислот Қатты күйдегі препараттар
Қатты күйдегі препараттар Полиамиды. Классификация по методу получения
Полиамиды. Классификация по методу получения Химический элемент платина
Химический элемент платина Щелочные металлы
Щелочные металлы Растворы (дисперсные системы)
Растворы (дисперсные системы) Тақырыпқа байланысты білімді жүйелеу
Тақырыпқа байланысты білімді жүйелеу II главная подгруппа ПС: Be, Mg, Ca, Sr, Ba, Ra
II главная подгруппа ПС: Be, Mg, Ca, Sr, Ba, Ra Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях
Выращивание кристалла медного купороса CuSO4*5Н2О в разных условиях Генетичний зв'язок
Генетичний зв'язок Презентация по Химии "РАСТВОРЫ" - скачать смотреть бесплатно
Презентация по Химии "РАСТВОРЫ" - скачать смотреть бесплатно Органічні розчинники. Їх застосування
Органічні розчинники. Їх застосування Получение этилена и опыты с ним. (Практическая работа 2)
Получение этилена и опыты с ним. (Практическая работа 2) Презентация по Химии "Ковалентная химическая связь" - скачать смотреть бесплатно
Презентация по Химии "Ковалентная химическая связь" - скачать смотреть бесплатно Основы химической термодинамики
Основы химической термодинамики Определение свободной поверхностной энергии тонких пленок оксидов
Определение свободной поверхностной энергии тонких пленок оксидов Внеурочная работа по химии. Краеведение
Внеурочная работа по химии. Краеведение Азотная кислота
Азотная кислота Жоғары температурағы асқын өткізгіштер
Жоғары температурағы асқын өткізгіштер Введение в биоорганическую химию. Пространственное и электронное строение органических соединений
Введение в биоорганическую химию. Пространственное и электронное строение органических соединений Исследовательская работа на тему: Удивительные свойства воды
Исследовательская работа на тему: Удивительные свойства воды “Кількість речовини. Молярна маса. Молярний об’єм” Урок хімії у 8 класі КЗ Верхівцевського НВК Учитель Кукса Наталія Миколаївна.
“Кількість речовини. Молярна маса. Молярний об’єм” Урок хімії у 8 класі КЗ Верхівцевського НВК Учитель Кукса Наталія Миколаївна.  Степень окисления
Степень окисления Презентация по Химии "Щавелевая кислота" - скачать смотреть
Презентация по Химии "Щавелевая кислота" - скачать смотреть  Количества вещества
Количества вещества