Содержание
- 2. Спирты Спиртами называются производные углеводородов, в которых один или несколько атомов водорода заменены на гидроксильньк группы.
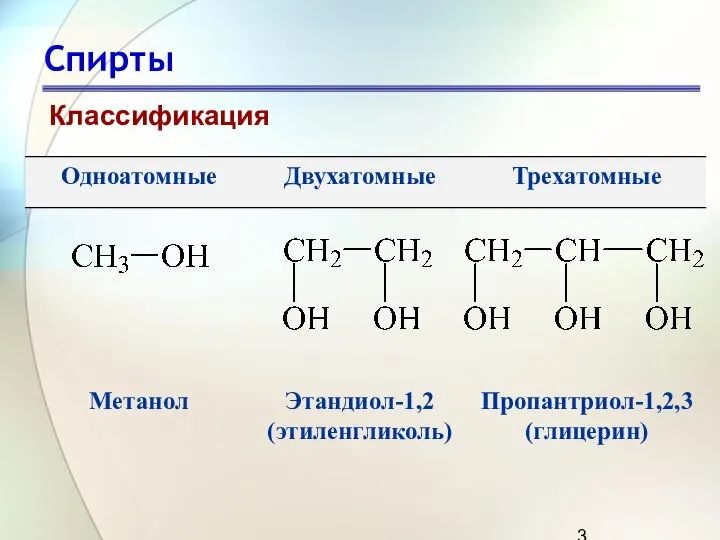
- 3. Спирты Классификация
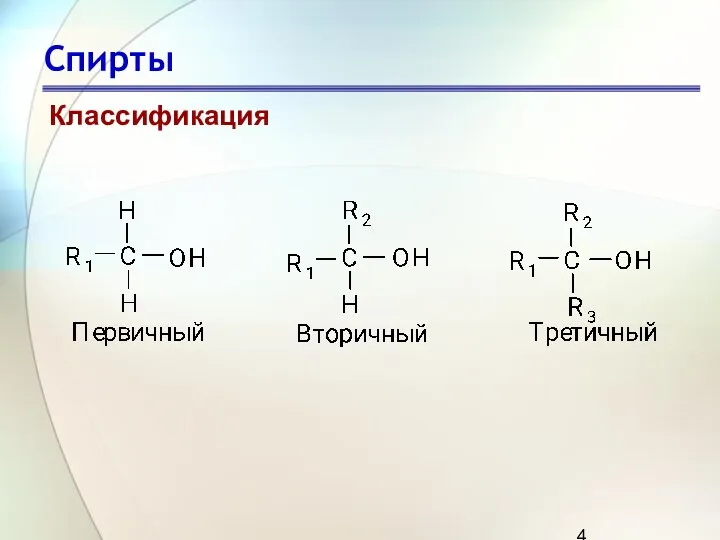
- 4. Спирты Классификация
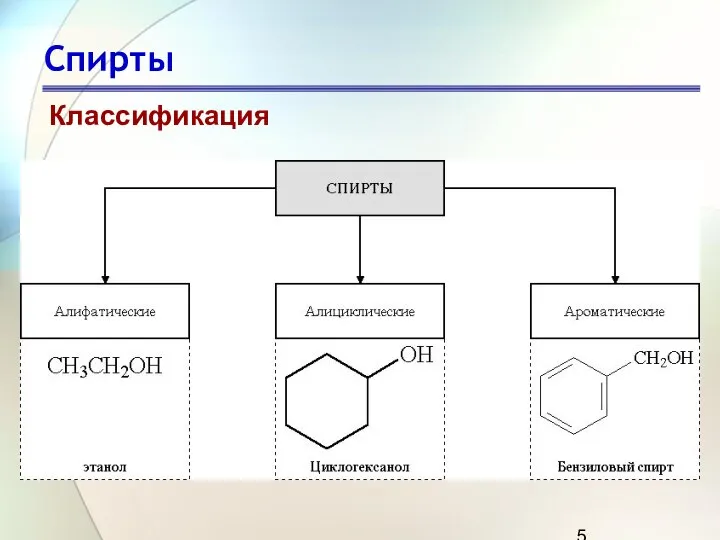
- 5. Спирты Классификация
- 6. Спирты Номенклатура и изомерия Этанол (этиловый спирт) Пропанол-1 (н-пропиловый спирт) Пропанол-2 (изопропиловый спирт)
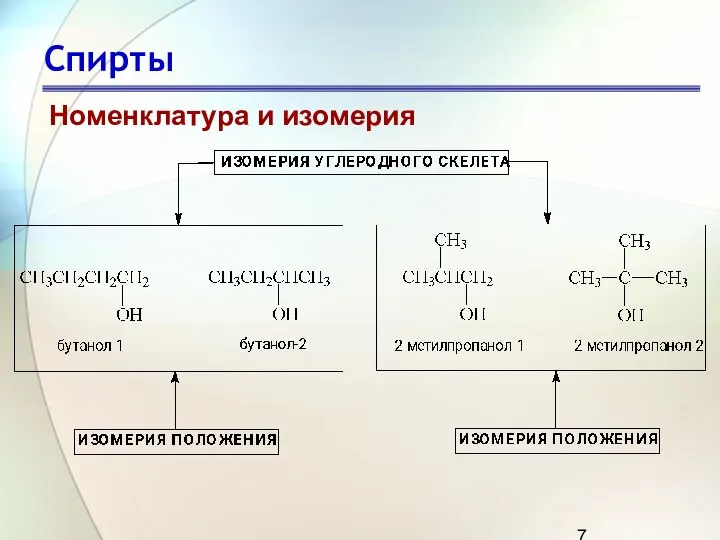
- 7. Спирты Номенклатура и изомерия
- 8. Спирты
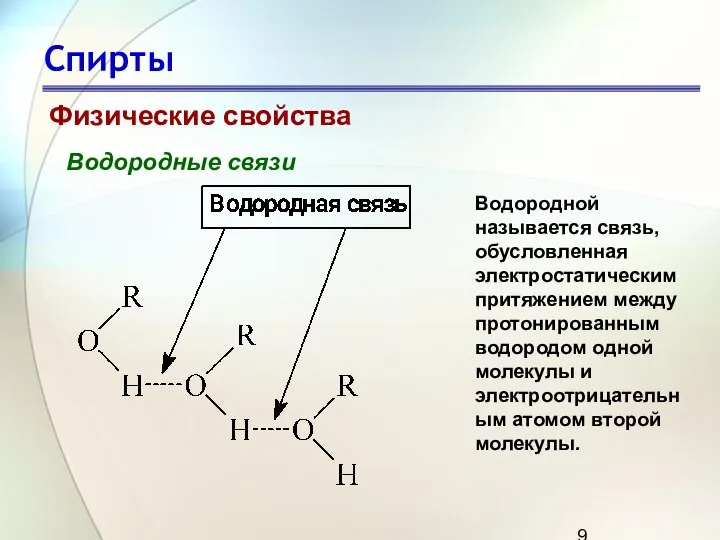
- 9. Спирты Физические свойства Водородные связи Водородной называется связь, обусловленная электростатическим притяжением между протонированным водородом одной молекулы
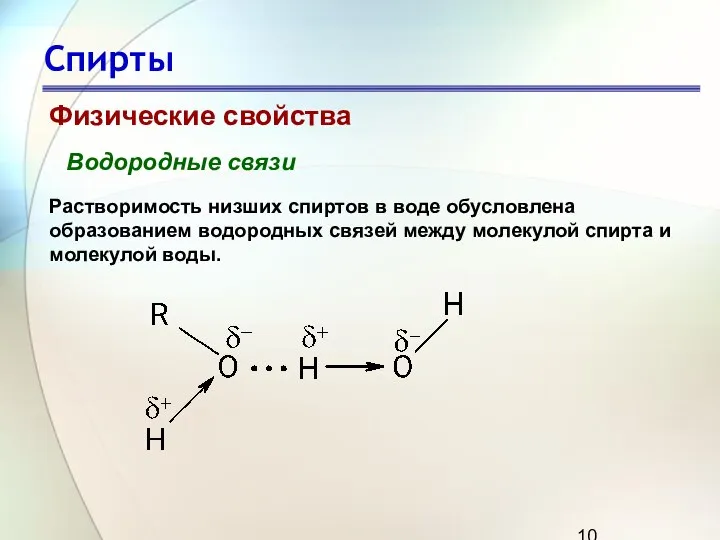
- 10. Спирты Физические свойства Водородные связи Растворимость низших спиртов в воде обусловлена образованием водородных связей между молекулой
- 11. Спирты Химические свойства 1. Кислотность спиртов В молекуле спирта содержится атом водорода, связанный с сильно электроотрицательным
- 12. Спирты Химические свойства 1. Кислотность спиртов
- 13. Спирты Химические свойства 1. Кислотность спиртов Алкоксиды (алкоголяты) нельзя получить реакцией спирта с гидроксидами металлов, их
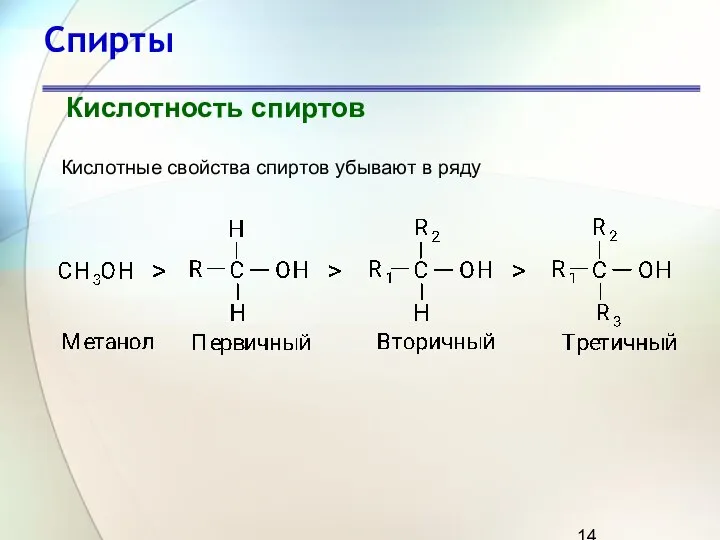
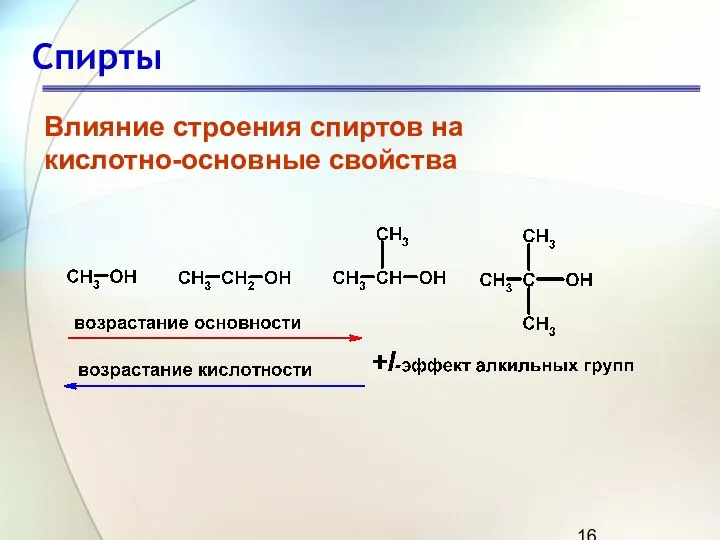
- 14. Спирты Кислотность спиртов Кислотные свойства спиртов убывают в ряду
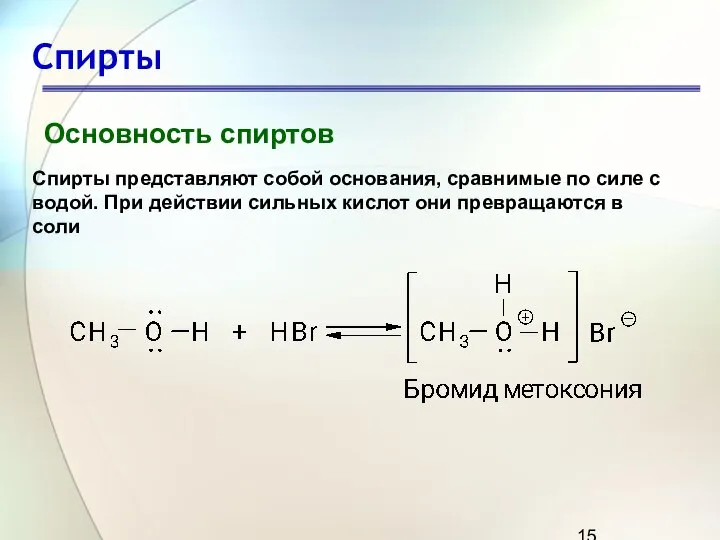
- 15. Спирты Основность спиртов Спирты представляют собой основания, сравнимые по силе с водой. При действии сильных кислот
- 16. Спирты Влияние строения спиртов на кислотно-основные свойства
- 17. Спирты Взаимодействие с магнийгалогеналкилами В этой реакции происходит замещение гидроксильного водорода на магнийгалоген и выделяется углеводород.
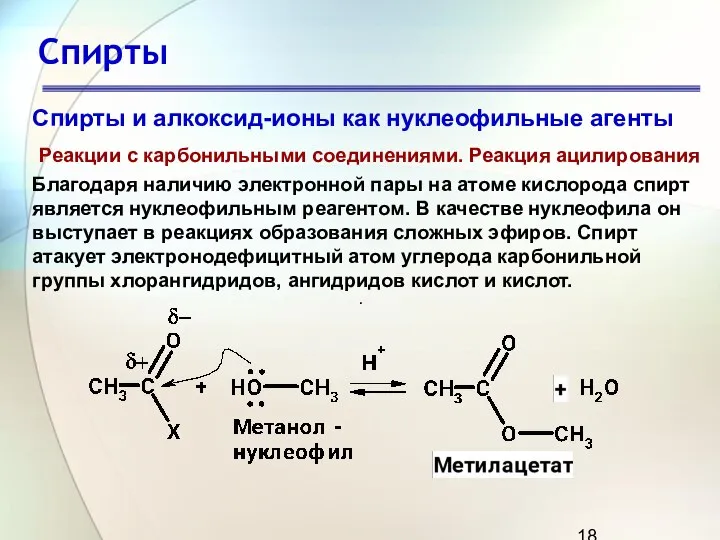
- 18. Спирты . Спирты и алкоксид-ионы как нуклеофильные агенты Реакции с карбонильными соединениями. Реакция ацилирования Благодаря наличию
- 19. Спирты . Реакции с карбонильными соединениями. Реакция ацилирования С карбоновыми кислотами спирты реагируют в присутствии кислотных
- 20. Спирты Реакция с участием связи R–OH Электроотрицательный кислород, оттягивая общую пару электронов связи . создает частичный
- 21. Спирты Реакции нуклеофильного замещения Реакции с галогеноводородами, образование алкилгалогенидов Спирты легко реагируют с галогеноводородами (HCl, HBr,
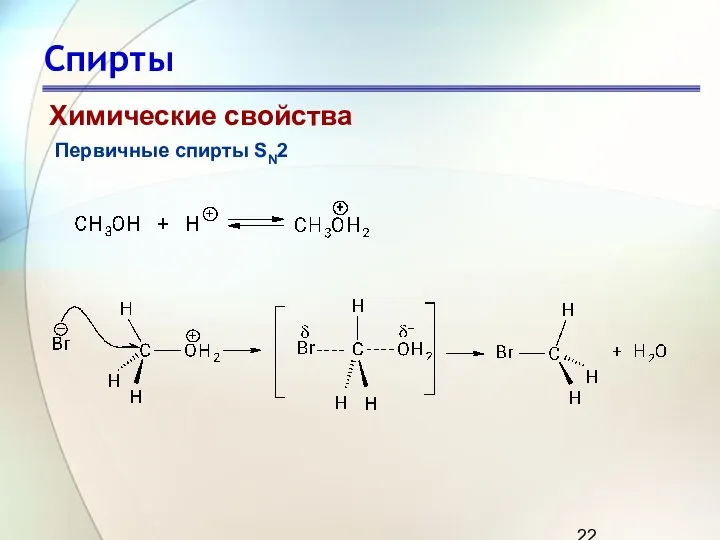
- 22. Спирты Химические свойства Первичные спирты SN2
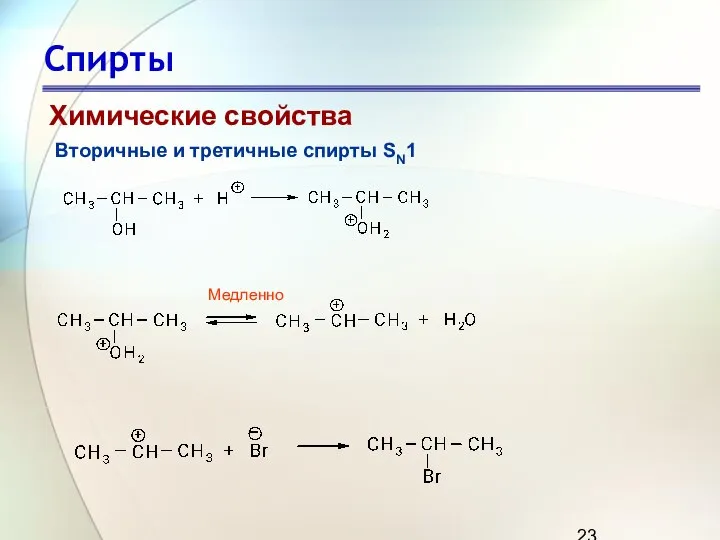
- 23. Спирты Химические свойства Вторичные и третичные спирты SN1 Медленно
- 24. Спирты Химические свойства Вторичные и третичные спирты SN1 Поскольку реакции замещения у вторичных и третичных спиртов
- 25. Спирты Химические свойства Реакционная способность спиртов по отношению к галогенводородам изменяется следующим образом: Бензиловый, аллиловый >
- 26. Спирты Реакции нуклеофильного замещения Реакция с галогенидами фосфора PCl5, PCl3, PBr3, PI3, тионилхлоридом SOCl2. Для получения
- 27. Спирты Реакции нуклеофильного замещения Межмолекулярная дегидратация спиртов. Получение простых эфиров Межмолекулярная дегидратация спиртов в присутствии каталитических
- 28. Спирты Синтез простых эфиров Важным методом получения простых эфиров является реакция алкоголятов с алкилгалогенидами (синтез Вильямсона)
- 29. Спирты Синтез простых эфиров Пример 1
- 30. Спирты Межмолекулярная дегидратация Вторичные и третичные спирты не подвергаются межмолекулярной дегидратации, а реагируют с образованием продуктов
- 31. Спирты Образование алкенов – внутримолекулярная дегидратация . Спирт превращается в алкен при температуре ~ 200 оС
- 32. Спирты Отщепление воды (дегидратация) протекает по правилу Зайцева – водород отщепляется от соседнего менее гидрированного атома
- 33. Спирты Реакции окисления Первичные спирты можно окислить до альдегидов действием К2Сr2О7, если одновременно с окислением вести
- 34. Спирты Реакции окисления Вторичные спирты окисляются до кетонов действием перманганата калия или хромовой кислотой. Дальнейшее окисление
- 35. Спирты Реакции окисления Третичные спирты в присутствии кислот превращаются в алкены, которые далее легко окисляются. В
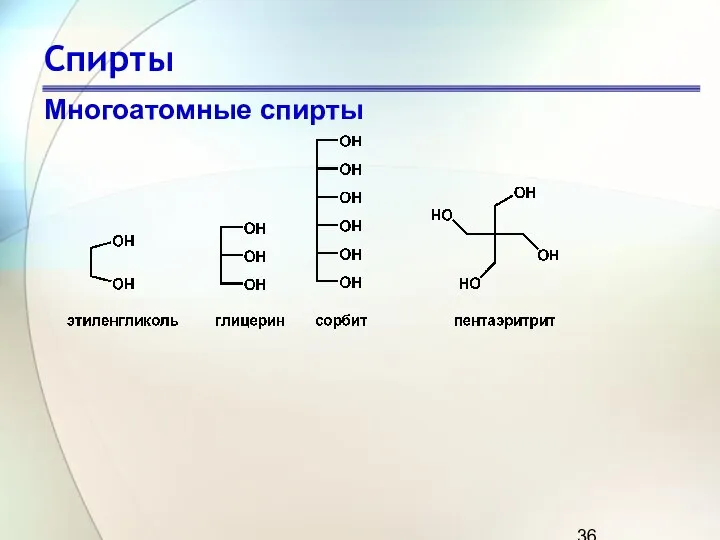
- 36. Спирты Многоатомные спирты
- 37. Спирты Многоатомные спирты При гидроксилировании алкенов получают вицинальные диолы. Простейший виц-диол – гликоль (этиленгликоль, 1,2-этандиол). Получают
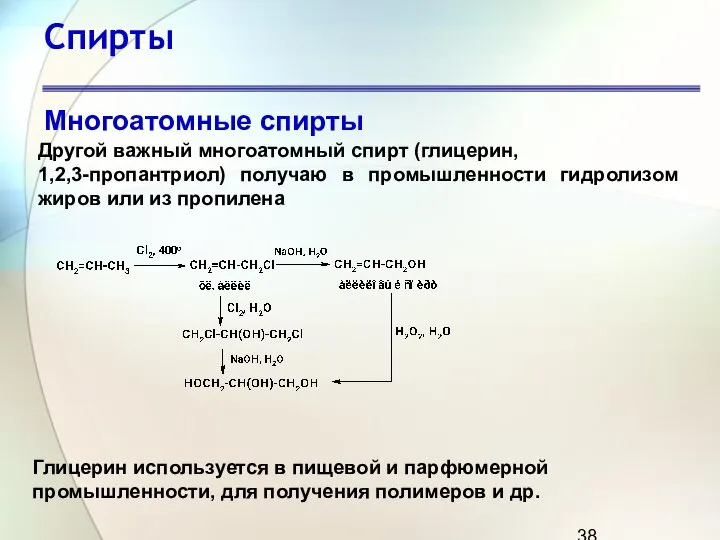
- 38. Спирты Многоатомные спирты Другой важный многоатомный спирт (глицерин, 1,2,3-пропантриол) получаю в промышленности гидролизом жиров или из
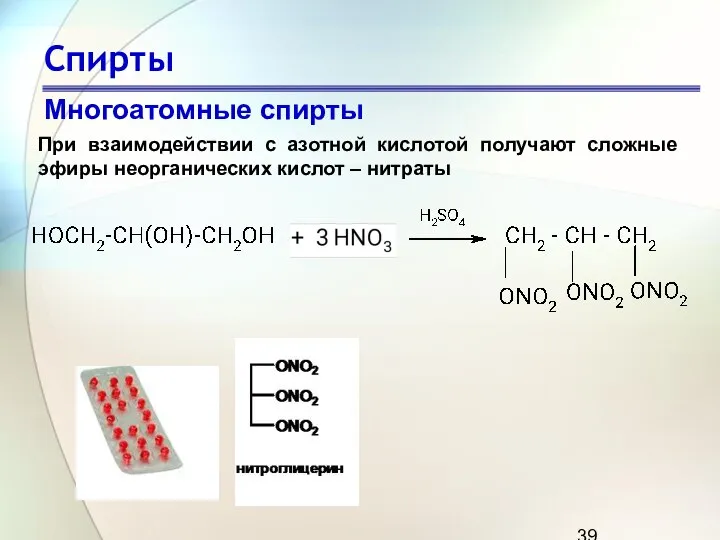
- 39. Спирты Многоатомные спирты При взаимодействии с азотной кислотой получают сложные эфиры неорганических кислот – нитраты
- 40. Спирты Способы получения 1. Гидратация алкенов (промышленный метод) Присоединение воды к алкенам происходит в присутствии кислых
- 41. Спирты Способы получения 2. Брожение сахаров Дрожжи сбраживают некоторые виды сахаров. Это сложный каталитический многостадийный распад
- 42. Спирты Способы получения 3. Гидролиз галогеналканов Гидролиз галогеналканов проводят при нагревании с водным раствором щелочей. Реакция
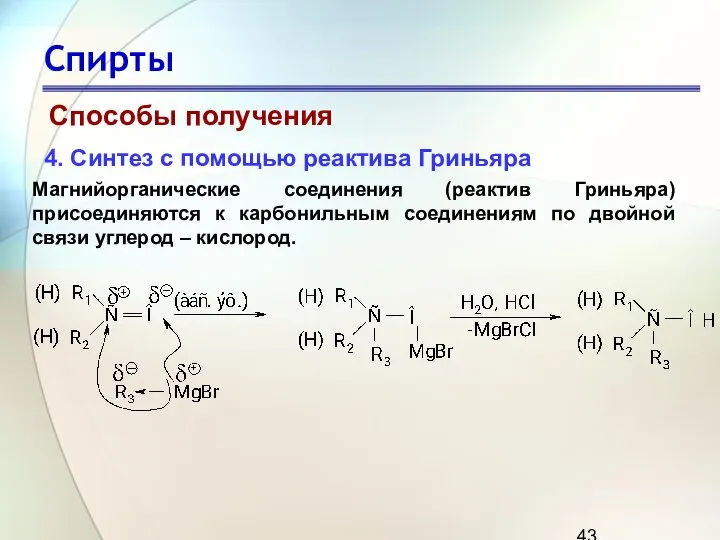
- 43. Спирты Способы получения 4. Синтез с помощью реактива Гриньяра Магнийорганические соединения (реактив Гриньяра) присоединяются к карбонильным
- 44. Спирты Способы получения 4. Синтез с помощью реактива Гриньяра Для синтеза первичных спиртов используют в качестве
- 46. Скачать презентацию



























 ОБЩАЯ ХИМИЯ 11 КЛАСС РАЗДЕЛ «ВЕЩЕСВА И ИХ СВОЙСТВА»
ОБЩАЯ ХИМИЯ 11 КЛАСС РАЗДЕЛ «ВЕЩЕСВА И ИХ СВОЙСТВА» Кислотность и основность рганических соединений. Инфракрасная спектроскопия
Кислотность и основность рганических соединений. Инфракрасная спектроскопия КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КУБАНСКИЙ МЕДИЦИНСКИЙ ИНСТИТУТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМ
КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КУБАНСКИЙ МЕДИЦИНСКИЙ ИНСТИТУТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМ Биогеотехнология
Биогеотехнология Скорость химической реакции (химическая кинетика )
Скорость химической реакции (химическая кинетика ) Реакционная способность твердых тел и способы ее регулирования
Реакционная способность твердых тел и способы ее регулирования Пестициды. Применение пестицидов
Пестициды. Применение пестицидов Валентность. Правила составления формул бинарных соединений
Валентность. Правила составления формул бинарных соединений Химические компоненты клетки. Неорганические компоненты
Химические компоненты клетки. Неорганические компоненты Презентация по Химии "Харчові добавки" - скачать смотреть бесплатно
Презентация по Химии "Харчові добавки" - скачать смотреть бесплатно Генетика человека с основами медицинской генетики.(Лекция 2)
Генетика человека с основами медицинской генетики.(Лекция 2) Гели (Студни)
Гели (Студни) Сероводород в природе. Получение сероводорода синтетическим способом
Сероводород в природе. Получение сероводорода синтетическим способом Операции термической обработки
Операции термической обработки Азотсодержащие органические соединения. Амины. Анилинароматический амин
Азотсодержащие органические соединения. Амины. Анилинароматический амин 9 класс Урок №7. Сложные эфиры. Жиры. Составитель презентации – учитель химии МОУ СОШ г. Холма Насонова Т.А.
9 класс Урок №7. Сложные эфиры. Жиры. Составитель презентации – учитель химии МОУ СОШ г. Холма Насонова Т.А. Анализ качества лекарственных веществ, определяемых методом комплексонометрии
Анализ качества лекарственных веществ, определяемых методом комплексонометрии Вторая группа главная подгруппа наряду с семейством щелочноземельных металлов включает и два типических элемента –бериллий и ма
Вторая группа главная подгруппа наряду с семейством щелочноземельных металлов включает и два типических элемента –бериллий и ма Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач в химии (ОГЭ, ЕГЭ, Олимпиады) Алмазы, искусственный и естественный рост
Алмазы, искусственный и естественный рост Своя Игра Химия
Своя Игра Химия Тұздар. Құрамы және химиялық қасиеттері
Тұздар. Құрамы және химиялық қасиеттері Основные виды и понятия курса органической химии в старшей школе
Основные виды и понятия курса органической химии в старшей школе Anionic Polymerization
Anionic Polymerization Ліпіди. Класифікація ліпідів
Ліпіди. Класифікація ліпідів Статья двумя способами. Приготовление катализатора
Статья двумя способами. Приготовление катализатора Chemical physics. Atomic structure
Chemical physics. Atomic structure Сплавы
Сплавы