Содержание
- 2. ПС элементов была предложена выдающимся русским химиком Д.И. Менделеевым в 1869 году
- 3. ПЕРИОДИЧЕСКИЙ ЗАКОН Свойства простых веществ и соединений, которые они образуют, находятся в периодической зависимости от величины
- 4. ПЕРИОДИЧЕСКИЙ ЗАКОН Периодический закон был сформулирован почти за полстолетия до открытия электрона! Сформулированный закон позволил: уточнить
- 5. ПС ЭЛЕМЕНТОВ ЧАСТО ИСПОЛЬЗУЕМАЯ В РОССИИ (короткопериодный вариант)
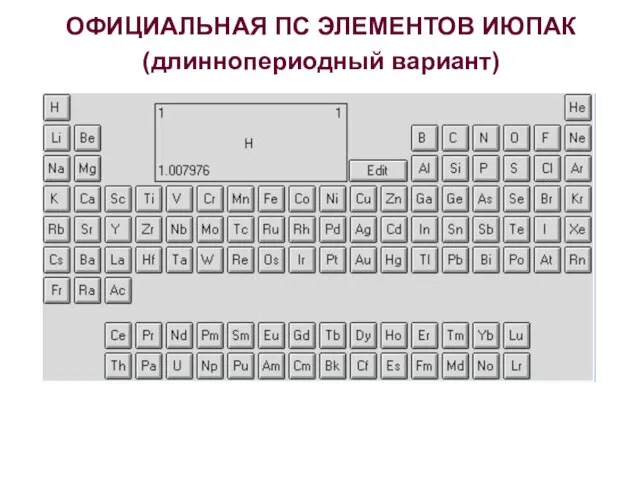
- 6. ОФИЦИАЛЬНАЯ ПС ЭЛЕМЕНТОВ ИЮПАК (длиннопериодный вариант)
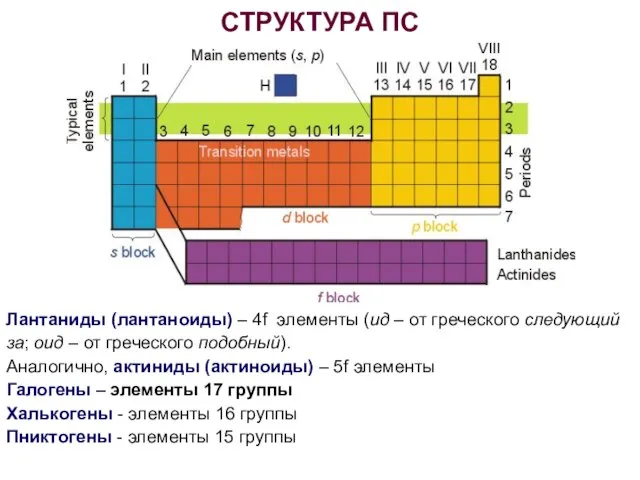
- 7. СТРУКТУРА ПС Лантаниды (лантаноиды) – 4f элементы (ид – от греческого следующий за; оид – от
- 8. Закономерности изменения свойств атомов и ионов К числу важнейших свойств элементов, определяемых электронным строением, относятся: радиусы;
- 9. Закономерности изменения свойств атомов и ионов Одна из основных характеристик атомов и ионов – их размеры.
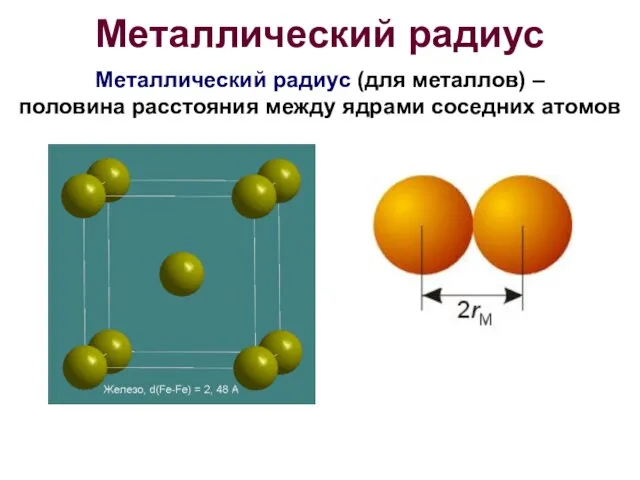
- 10. Металлический радиус Металлический радиус (для металлов) – половина расстояния между ядрами соседних атомов
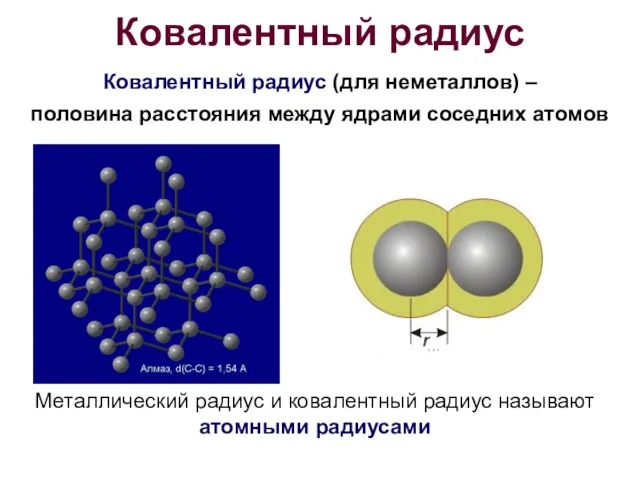
- 11. Ковалентный радиус Ковалентный радиус (для неметаллов) – половина расстояния между ядрами соседних атомов Металлический радиус и
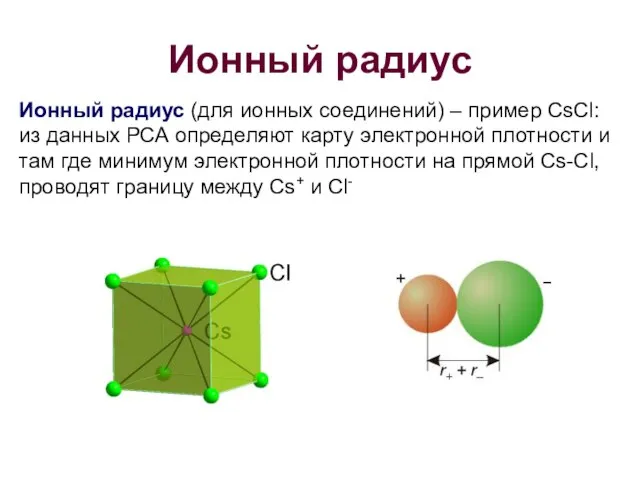
- 12. Ионный радиус Ионный радиус (для ионных соединений) – пример CsCl: из данных РСА определяют карту электронной
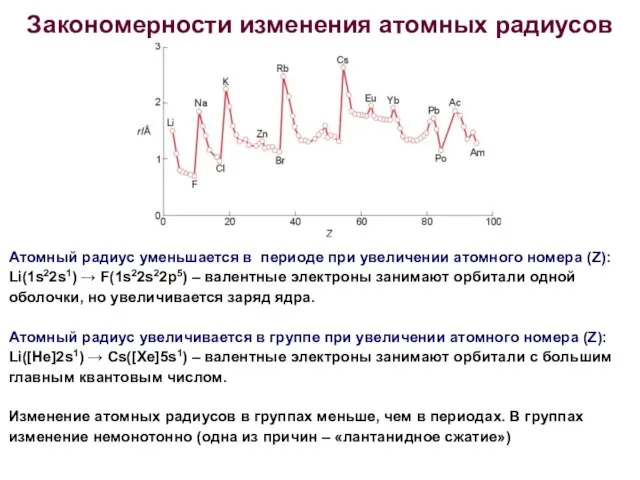
- 13. Закономерности изменения атомных радиусов Атомный радиус уменьшается в периоде при увеличении атомного номера (Z): Li(1s22s1) →
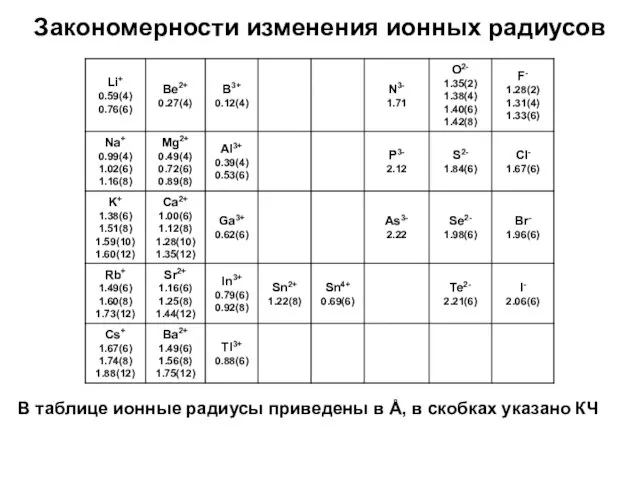
- 14. Закономерности изменения ионных радиусов В таблице ионные радиусы приведены в Å, в скобках указано КЧ
- 15. Закономерности изменения ионных радиусов Ионный радиус зависит от координационного окружения (КЧ) – чем больше КЧ, тем
- 16. Закономерности изменения ионных радиусов для переходных металлов В периоде: Ti2+ (1,00 Å) → Ni2+ (0,83 Å)
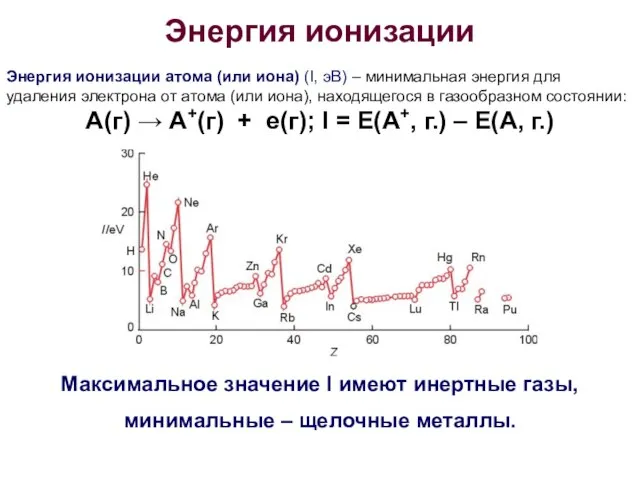
- 17. Энергия ионизации Энергия ионизации атома (или иона) (I, эВ) – минимальная энергия для удаления электрона от
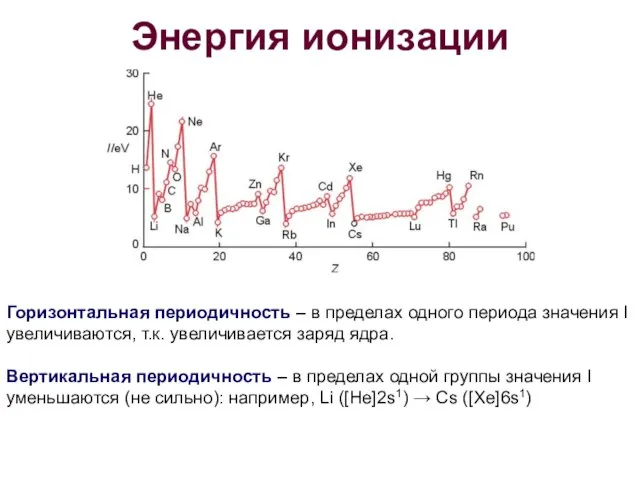
- 18. Энергия ионизации Горизонтальная периодичность – в пределах одного периода значения I увеличиваются, т.к. увеличивается заряд ядра.
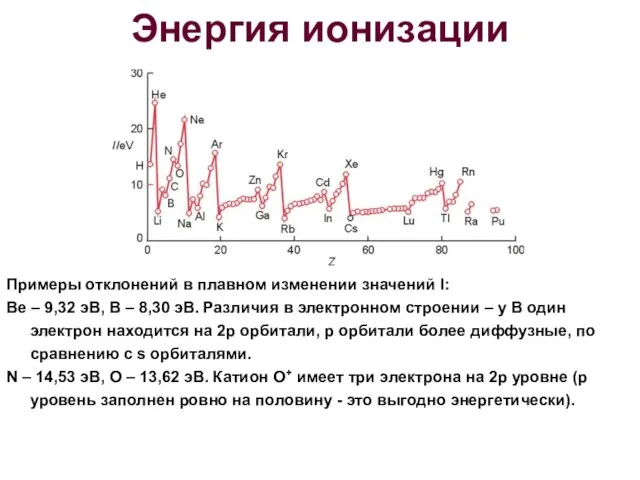
- 19. Энергия ионизации Примеры отклонений в плавном изменении значений I: Be – 9,32 эВ, В – 8,30
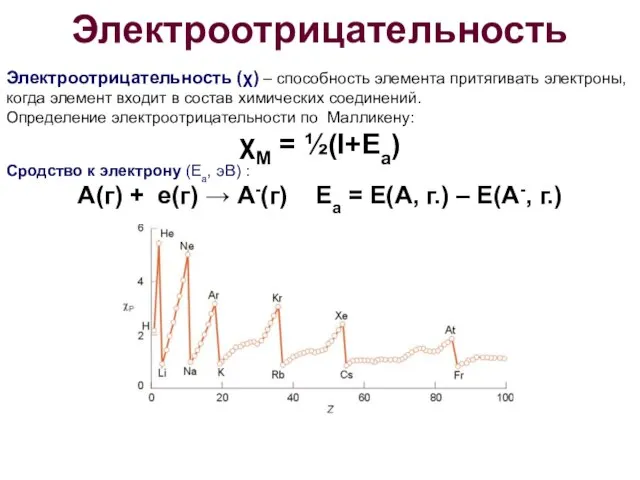
- 20. Электроотрицательность Электроотрицательность (χ) – способность элемента притягивать электроны, когда элемент входит в состав химических соединений. Определение
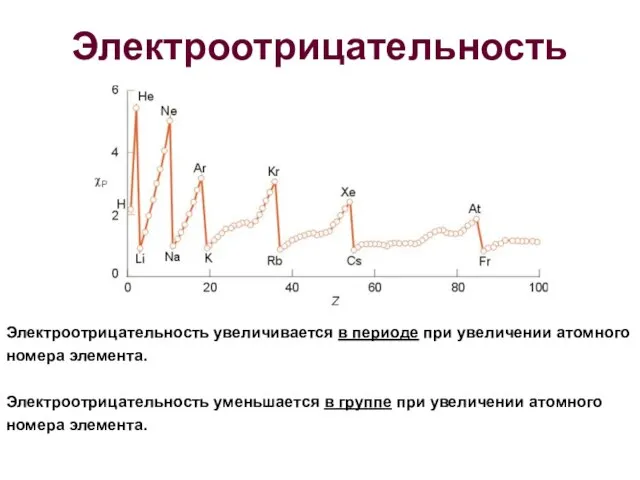
- 21. Электроотрицательность Электроотрицательность увеличивается в периоде при увеличении атомного номера элемента. Электроотрицательность уменьшается в группе при увеличении
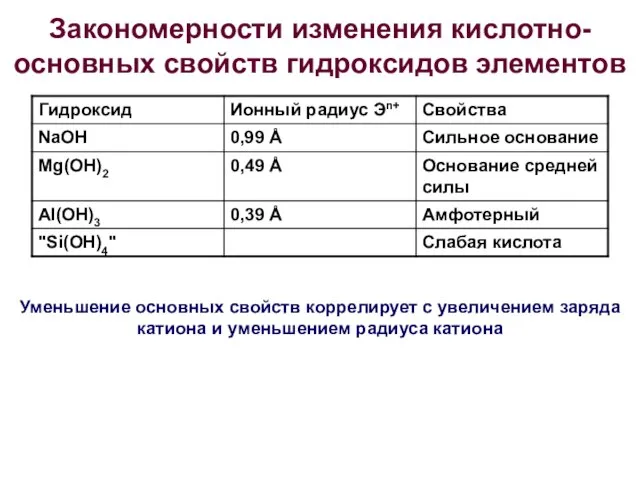
- 22. Закономерности изменения кислотно-основных свойств гидроксидов элементов Основные свойства: ЭОН → Э+ + ОН- Кислотные свойства: ЭОН
- 23. Закономерности изменения кислотно-основных свойств гидроксидов элементов Уменьшение основных свойств коррелирует с увеличением заряда катиона и уменьшением
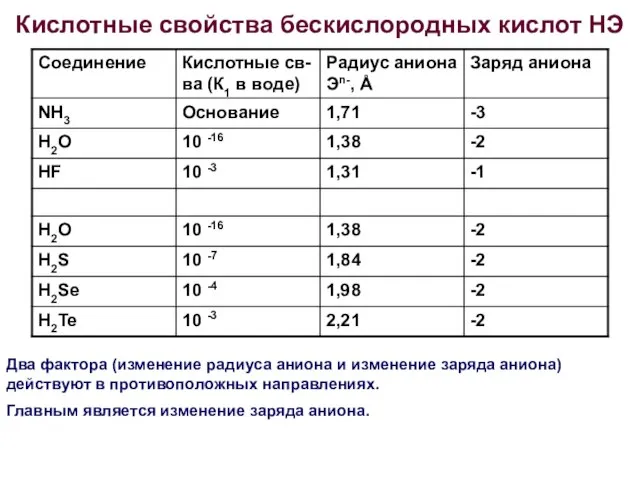
- 24. Кислотные свойства бескислородных кислот НЭ Два фактора (изменение радиуса аниона и изменение заряда аниона) действуют в
- 25. Эмпирическая корреляция между строением и силой кислоты (правила Полинга) Можно предсказать относительную силу кислот: для кислородсодержащих
- 26. Некоторые закономерности изменения окислительно-восстановительных свойств Э + 2е + 2Н+ → Н2Э (Э – халькоген) Окислительные
- 27. Окислительно-восстановительные свойства соединений элементов в высших степенях окисления Главные элементы – s и p: 14 группа:
- 29. Скачать презентацию












 Инсектициды на основе бакуловирусов
Инсектициды на основе бакуловирусов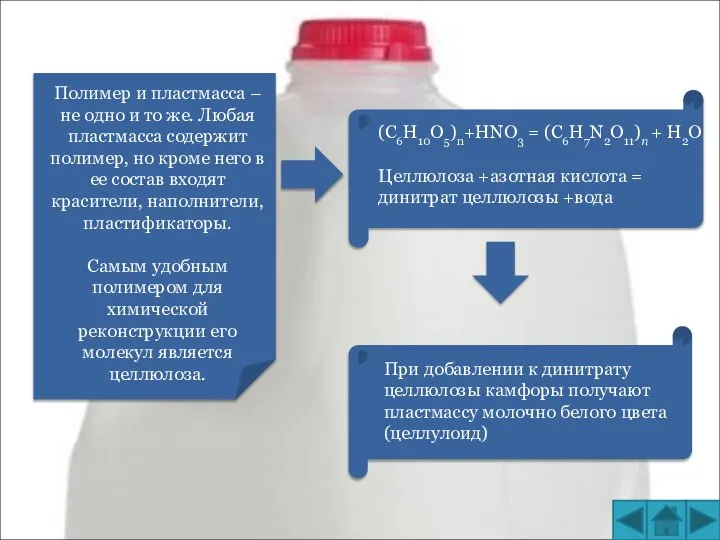 Полимер и пластмасса
Полимер и пластмасса Металлы в нашей жизни
Металлы в нашей жизни Сложные эфиры
Сложные эфиры Металлы и их соединения
Металлы и их соединения Властивості етанової (оцтової) кислоти
Властивості етанової (оцтової) кислоти Елементарний склад живих організмів
Елементарний склад живих організмів Структурно-механические свойства дисперсных систем
Структурно-механические свойства дисперсных систем Протеины: плюсы и минусы
Протеины: плюсы и минусы Излучение и поглощение света атомами. Виды спектров, спектральный анализ
Излучение и поглощение света атомами. Виды спектров, спектральный анализ Относительная атомная масса
Относительная атомная масса Биодизельное топливо
Биодизельное топливо Неметалічні елементи
Неметалічні елементи Бромды метил буының концентрациясын анықтау тәсілдемесі
Бромды метил буының концентрациясын анықтау тәсілдемесі Металлдардың кристалдық құрылымы
Металлдардың кристалдық құрылымы Поняття про лікарські препарати Підготували Стебко Марія, Бондар Аліна 11-Ф
Поняття про лікарські препарати Підготували Стебко Марія, Бондар Аліна 11-Ф  Закон постоянства состава веществ
Закон постоянства состава веществ Аргентум (Срібло)
Аргентум (Срібло) Мило. Синтетичні миючі засоби.
Мило. Синтетичні миючі засоби.  Растворы электролитов. Буферные растворы. Лекция 4
Растворы электролитов. Буферные растворы. Лекция 4 Аммиак. Физические и химические свойства. Получение и применение
Аммиак. Физические и химические свойства. Получение и применение Обмен железа и его нарушения
Обмен железа и его нарушения Презентация по Химии "Окислительно-восстановительные реакции" - скачать смотреть бесплатно
Презентация по Химии "Окислительно-восстановительные реакции" - скачать смотреть бесплатно Кетоны
Кетоны Альдегиды. Строение молекулы
Альдегиды. Строение молекулы Элементы третьего периода, периодической системы Д. И. Менделеева
Элементы третьего периода, периодической системы Д. И. Менделеева Нанохімія та нанотехнології
Нанохімія та нанотехнології Allgemeine Chemie für PharmazeutInnen
Allgemeine Chemie für PharmazeutInnen