Содержание
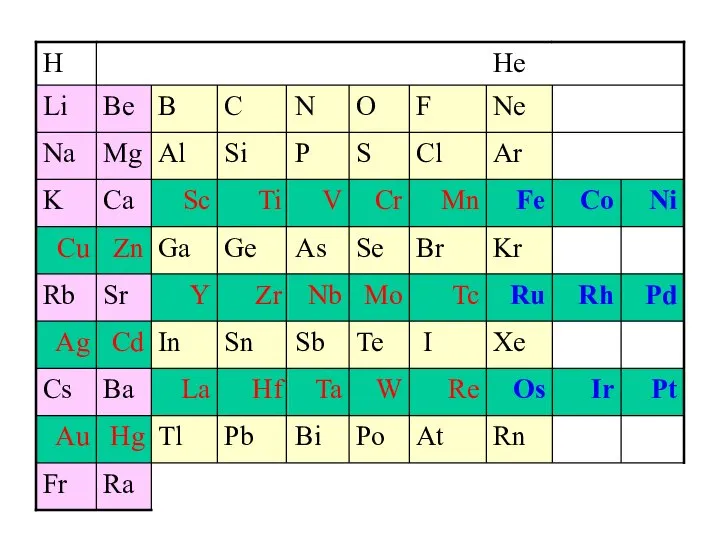
- 3. Главная подгруппа – инертные газы He, Ne, Ar, Kr, Xe, Rn 1s2 ns2np6 Побочная подгруппа –
- 4. Общая электронная формула: […] ns 0÷2 (n–1)d 6÷10
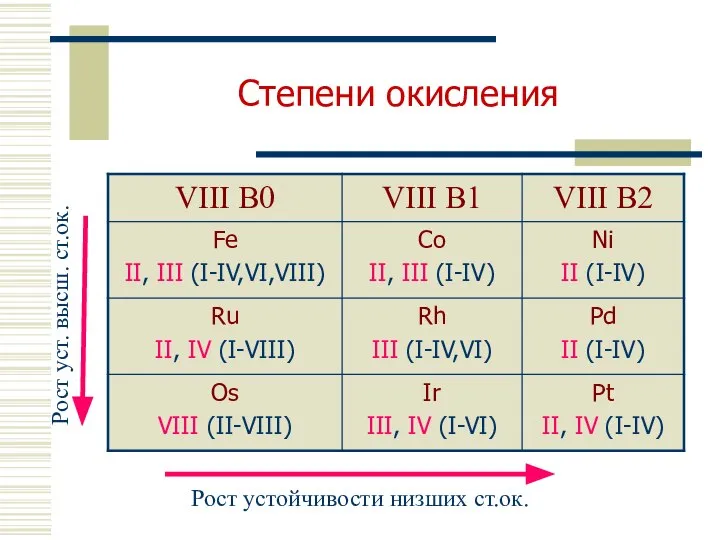
- 5. Степени окисления
- 6. Активность металлов
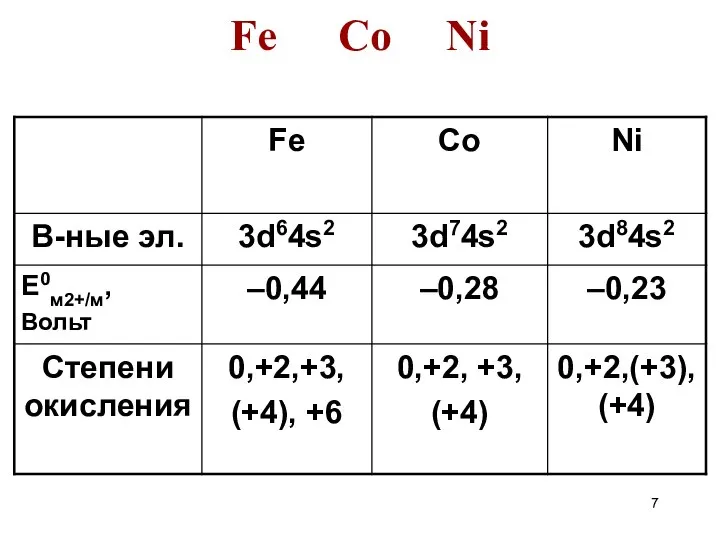
- 7. Fe Co Ni
- 8. Распространенность и минералы Fe – 4 место; Fe2O3 (гематит, красный железняк), Fe3O4 или (FeIIFe2III)O4 (магнетит, магнитный
- 9. Открытие элементов Fe – известно с древнейших времен, от лат. Ferreus – твердый. Со – 1735,
- 10. Получение В промышленности железо в основном (95%) выплавляют из руд в виде чугунов и сталей: 3Fe2O3
- 11. Получение Мировое производство чугуна ~ 1 000 000 000 тонн! ~ 1012 кг или ~ 100
- 12. Сплавы железа Чугун (2-5% углерода) т-ра плавления 1100-1200 0С; Серый чугун – углерод в виде пластинок
- 13. Алюминий используется для получения некоторых металлов. Этот метод называется алюминотермией. Метод основан на том, что порошкообразный
- 14. Получение Co и Ni Обжиг: 3CoS + 5O2 = Co3O4 + 3SO2 2Ni3S2 + 7O2 =
- 15. Свойства простых веществ Металлы реагируют с кислотами, железо легче, Co и Ni очень медленно: M +
- 16. Коррозия По отношению к воздуху и воде компактные Co, Ni и химически чистое Fe устойчивы. Однако,
- 17. Взаимодействие с O2: Fe + O2 (150 °C) → «Fe3O4» ≡ (FeIIFe2III)O4 Co + O2 (900
- 18. Соединения М2+ Оксиды: FeO↓ CoO↓ NiO↓ Гидроксиды: Fe(OH)2 ↓ (белый) Со(ОН)2 ↓ (розовый, синий) Ni(OH)2 ↓
- 19. Соединения М2+ Цвет кристаллогидратов обусловлен наличием [M(H2O)6]2+ и совпадает с цветом растворов: Fe – светлозеленый Co
- 20. Окисление М2+ кислородом в различных средах Щелочная среда: M(OH)3 + e = M(OH)2 + OH– (EoM3+/M2+)
- 21. Окисление М2+ кислородом в различных средах Кислая среда: M3+ + e = M2+ (EoM3+/M2 ) O2
- 22. Получение Co3+ и Ni3+ Co(OH)3 и Ni(OH)3 (NiO(OH)) получают действием более сильных окислителей: 2M(OH)2 + Br2
- 23. Соединения M3+ Оксиды и гидроксиды M2O3 и M(OH)3 обладают только основными свойствами Fe(OH)3 + 3HCl =
- 24. Соединения M3+ Простые соли M3+ характерны только для Fe Растворимые в воде: FeX3 (X = Cl–,
- 25. Соединения M3+ В водных растворах соли Fe3+ сильно гидролизованы, поэтому все растворы этих солей окрашены в
- 26. Соединения Fe6+ FeO3 – нет, H2FeO4 – нет Существуют соли: Na2FeO4 – растворима в воде, BaFeO4
- 27. Комплексы Fe K4[FeII(CN)6] – желтая кровяная соль; β6 ~ 1037, реактив на Fe3+ Берлинская лазурь KFeIII[FeII(CN)6]
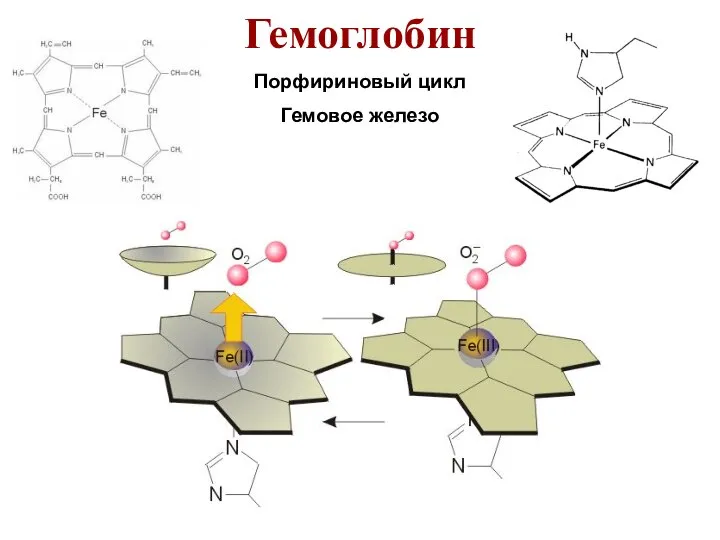
- 28. Гемоглобин Порфириновый цикл Гемовое железо
- 29. ПЛАТИНОВЫЕ МЕТАЛЛЫ
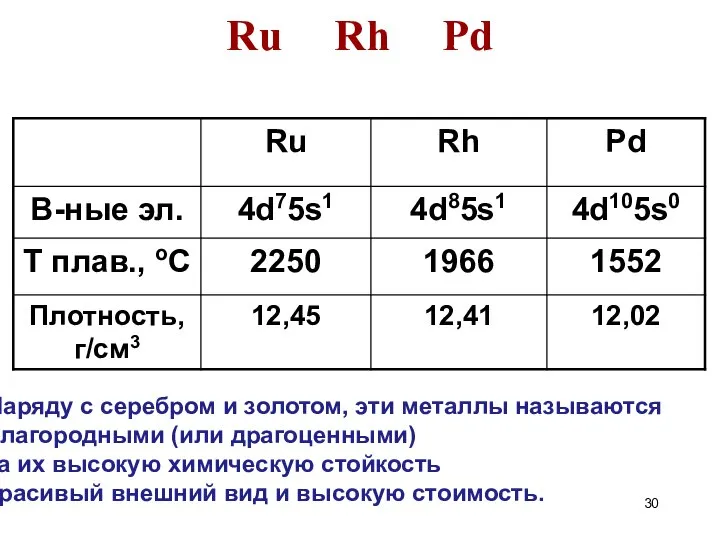
- 30. Ru Rh Pd Наряду с серебром и золотом, эти металлы называются благородными (или драгоценными) за их
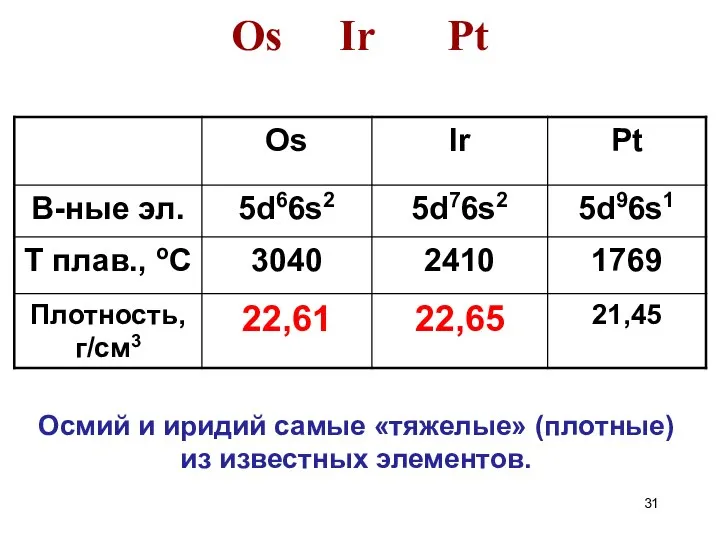
- 31. Os Ir Pt Осмий и иридий самые «тяжелые» (плотные) из известных элементов.
- 32. Распространенность и минералы Содержание платиновых металлов в земной коре: Pd – 71 место, Pt – 72
- 33. На долю вторичных источников платиновых металлов (лом, отработанные катализаторы и др.) приходится от 10 до 33%
- 34. ПЛАТИНОВЫЕ МЕТАЛЛЫ В ОТРАБОТАННОМ ЯДЕРНОМ ТОПЛИВЕ (ОЯТ)
- 35. Ru, Rh, Pd Реакторы на тепловых нейтронах (РТН) (топливо – UO2 (235U), глубина выгорания топлива –
- 36. ДИНАМИКА НАКОПЛЕНИЯ ПЛАТИНОВЫХ МЕТАЛЛОВ В ОЯТ
- 37. Антонио де Ульоа (1716 – 1795) – испанский морской офицер, физик и математик, которого не вполне
- 38. Наиболее крупные самородки Pt найдены на Среднем Урале, самый тяжелый - 9635 г.
- 39. Палладий (Pd) в честь астероида Паллада Родий (Rh) от греч. ροδον – розовый Выделены в 1803-1804
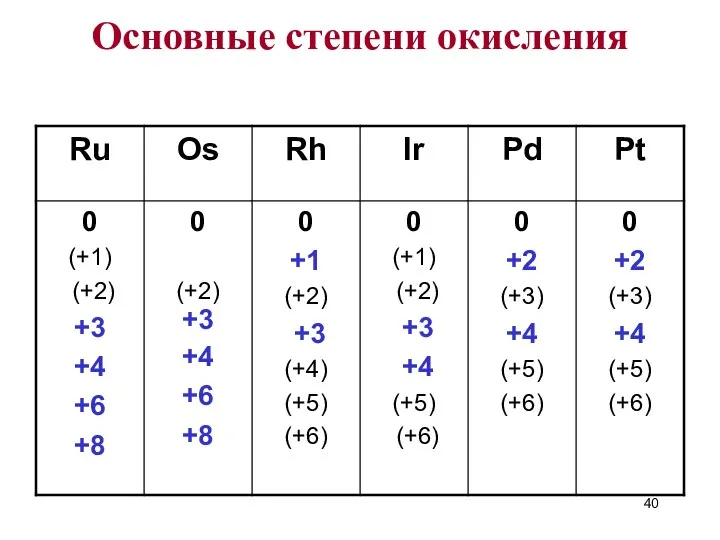
- 40. Основные степени окисления
- 41. Простые вещества Ru, Os, Rh, Ir – не растворимы в индивидуальных кислотах и их смесях. Pt
- 42. Pd 3Pd + 18HCl + 4HNO3 = 3H2[PdCl6] + 4NO↑+ 8H2O Pd + 4HNO3(конц.) = Pd(NO3)2
- 43. Все платиновые металлы можно перевести в растворимое состояние: 1. окислительным щелочным плавлением (t = 500-700оС) M
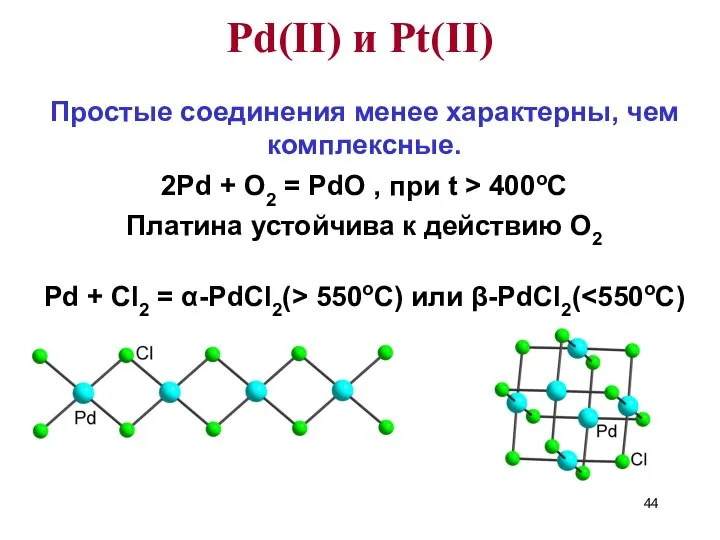
- 44. Простые соединения менее характерны, чем комплексные. 2Pd + O2 = PdO , при t > 400oC
- 45. Доминируют квадратные комплексы. [MX4]2– (X = Cl, Br, I, SCN, CN) [MX2L2] (L = NH3, NR3,
- 46. Галогениды Pd: PdF4 и (PdF3 – PdII[PdIVF6]) Pd + 2F2 = PdF4 (при t = 120
- 47. Множество термодинамически стабильных и кинетически инертных октаэдрических комплексов. Например синтезирован весь ряд от [PtCl6]2– ….. [PtClx(NH3)6–x]
- 48. Pt(V) и Pt(VI) Pt + 3F2 = PtF6 – при 200 оС и повышенном давлении фтора;
- 49. M + X2 = MX3 (при t > 400 oC ; X = Cl, Br, I)
- 50. Известно очень много комплексов, в основном октаэдрические и кинетически инертные. Нитритные комплексы широко используются при получении
- 51. Os(VIII): OsO4, молекулярная решетка, tпл=40оС, tк= 130оС Ru(VIII): RuO4, молекулярная решетка tпл=25оС, tк= 130оС Os +
- 52. Мировые запасы платиновых металлов ~56 тыс. тонн В мире в 2010 г. было добыто ~433 тонны
- 53. Россия – лидер по производству палладия (до 50%) ЮАР – 57%мирового производства платиновых металлов 1 Troy
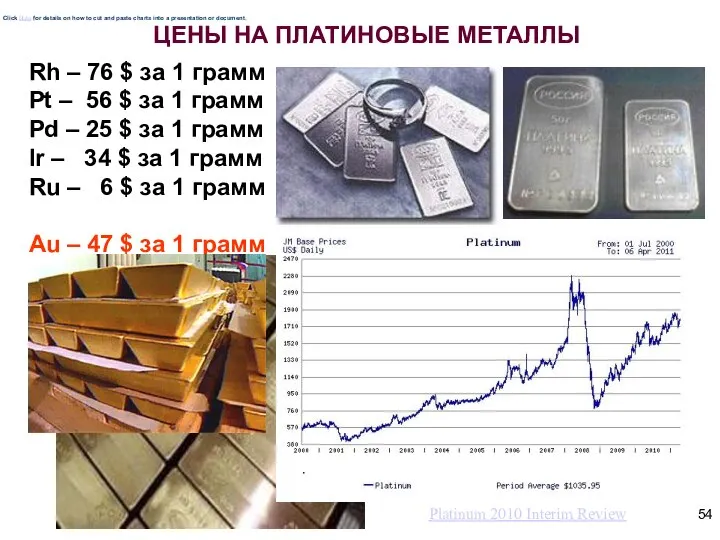
- 54. ЦЕНЫ НА ПЛАТИНОВЫЕ МЕТАЛЛЫ Rh – 76 $ за 1 грамм Pt – 56 $ за
- 55. Структура потребления платиновых металлов в 2010 году ПЛАТИНА (187 тонн) 40% - автокатализаторы 32% - ювелиры
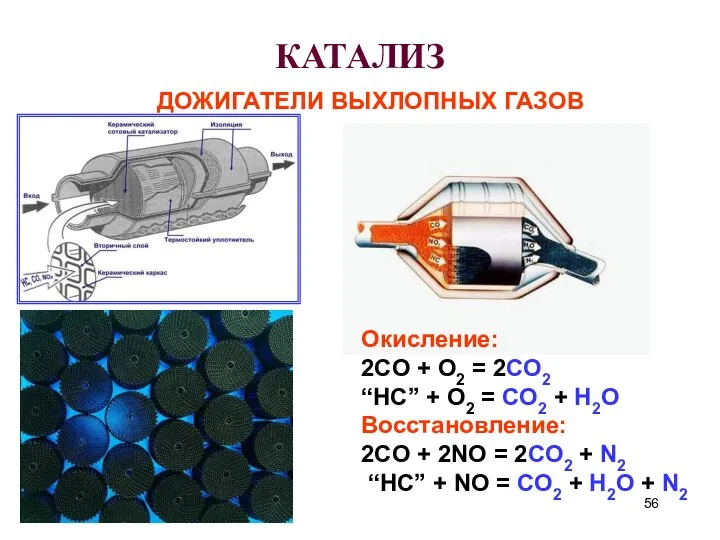
- 56. КАТАЛИЗ ДОЖИГАТЕЛИ ВЫХЛОПНЫХ ГАЗОВ Окисление: 2CO + O2 = 2CO2 “HC” + O2 = CO2 +
- 57. КАТАЛИЗ нефтехимия Каталитический риформинг - это каталитическая ароматизация тяжелых бензинов с целью повышения октанового числа (платина,
- 58. Ювелирная промышленность Платина не изнашивается и является надежной оправой для драгоценных камней. Многие знаменитые драгоценные камни
- 60. Промышленность Палладиевые конденсаторы Платино-родиевые фильеры Платинорованные мешалки Платина – конструкционный материал стекловаренных печей для производства высококачественного
- 61. Промышленность Иридиевые воронки Родиевая фольга для производства зеркал Иридиевый тигель Платина применяется в точных приборах. Из
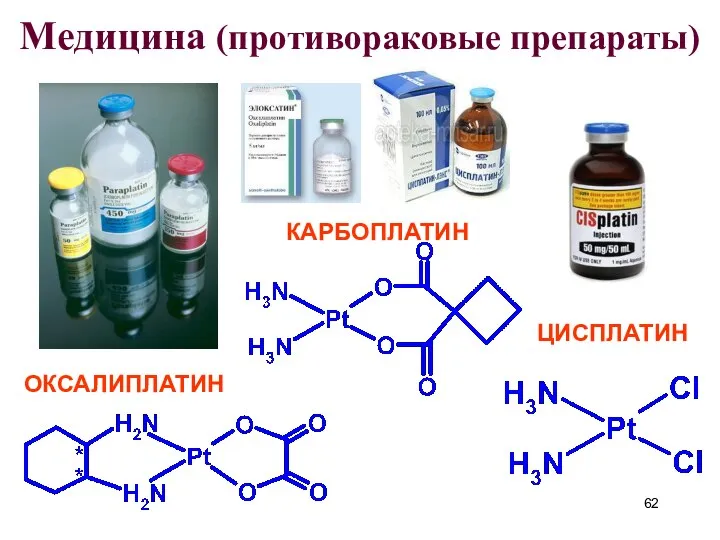
- 62. Медицина (противораковые препараты) КАРБОПЛАТИН ЦИСПЛАТИН ОКСАЛИПЛАТИН
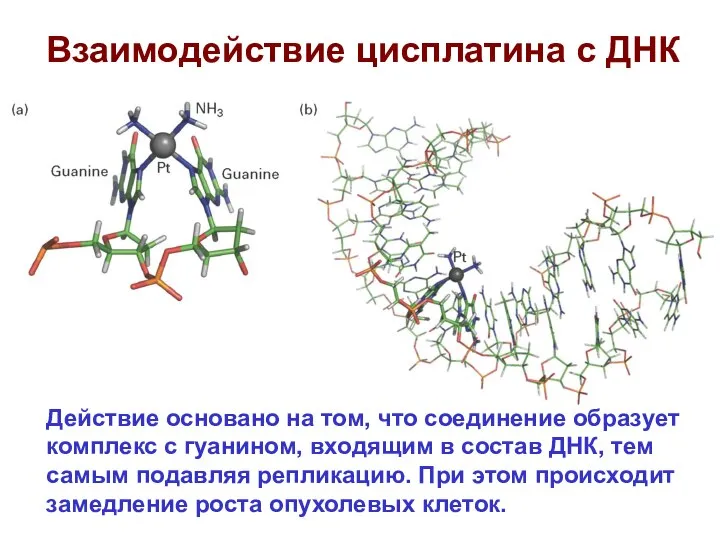
- 63. Взаимодействие цисплатина с ДНК Действие основано на том, что соединение образует комплекс с гуанином, входящим в
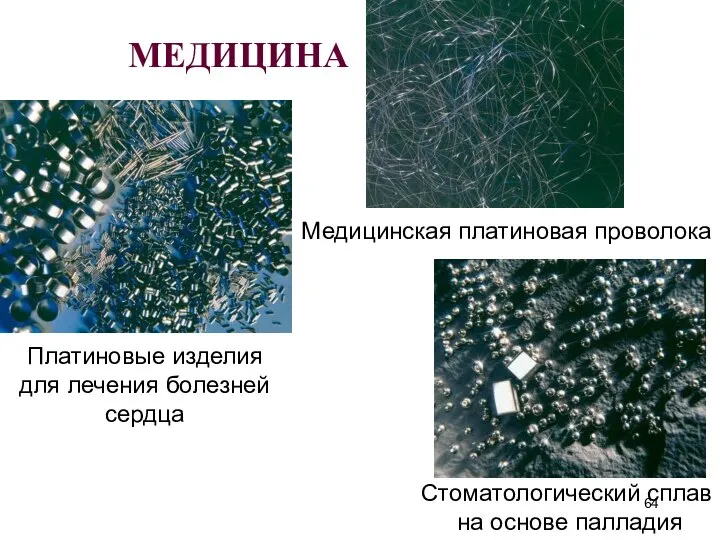
- 64. МЕДИЦИНА Платиновые изделия для лечения болезней сердца Стоматологический сплав на основе палладия Медицинская платиновая проволока
- 66. Скачать презентацию

![Общая электронная формула: […] ns 0÷2 (n–1)d 6÷10](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397749/slide-3.jpg)












![Соединения М2+ Цвет кристаллогидратов обусловлен наличием [M(H2O)6]2+ и совпадает с цветом](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397749/slide-18.jpg)







![Комплексы Fe K4[FeII(CN)6] – желтая кровяная соль; β6 ~ 1037, реактив](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397749/slide-26.jpg)










![Pd 3Pd + 18HCl + 4HNO3 = 3H2[PdCl6] + 4NO↑+ 8H2O](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397749/slide-41.jpg)

![Доминируют квадратные комплексы. [MX4]2– (X = Cl, Br, I, SCN, CN)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397749/slide-44.jpg)
![Галогениды Pd: PdF4 и (PdF3 – PdII[PdIVF6]) Pd + 2F2 =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397749/slide-45.jpg)













 Спін-спінова взаємодія в спектрах ямр
Спін-спінова взаємодія в спектрах ямр Полимеры
Полимеры  В таблиці я ― відомий елемент, Та літеру зміни з одного боку, Переконаєшся в один момент, Що я не елемент вже, а протока. Метаграми
В таблиці я ― відомий елемент, Та літеру зміни з одного боку, Переконаєшся в один момент, Що я не елемент вже, а протока. Метаграми  Физико-химические и электро-физические свойства А3В5. Сравнительный анализ
Физико-химические и электро-физические свойства А3В5. Сравнительный анализ Атомно – молекулярное учение
Атомно – молекулярное учение Нефть в США. История. Запасы и прогноз
Нефть в США. История. Запасы и прогноз Классификация электродов. (Лекция 4)
Классификация электродов. (Лекция 4) Сахароза
Сахароза Основные сведения о строении атома
Основные сведения о строении атома Растворение. Растворимость веществ в воде
Растворение. Растворимость веществ в воде Минеральные удобрения
Минеральные удобрения Ядерный магнитный резонанс. (Лекция 8)
Ядерный магнитный резонанс. (Лекция 8) Фазовые равновесия раствор-пар в двухкомпонентных системах из двух летучих жидкостей
Фазовые равновесия раствор-пар в двухкомпонентных системах из двух летучих жидкостей Щелочные металлы
Щелочные металлы Алканы и циклоалканы
Алканы и циклоалканы Полудрагоценные камни
Полудрагоценные камни Двойной электрический слой на границе раздела твердое тело. Раствор электролита
Двойной электрический слой на границе раздела твердое тело. Раствор электролита Презентация по Химии "Открытия и изобретения в химии" - скачать смотреть
Презентация по Химии "Открытия и изобретения в химии" - скачать смотреть  VI группа периодической системы Д.И. Менделеева
VI группа периодической системы Д.И. Менделеева Промышленная очистка воды
Промышленная очистка воды Перекисное окисление липидов
Перекисное окисление липидов Презентация Щелочные металлы
Презентация Щелочные металлы  Олимпиада по химии
Олимпиада по химии Группа галогенов в периодической системе
Группа галогенов в периодической системе Гидрокаталитические процессы
Гидрокаталитические процессы Полимеризация циклов. Сополимеризация
Полимеризация циклов. Сополимеризация Жувальна гумка Виконав учень 11-Б Надворний Ярослав
Жувальна гумка Виконав учень 11-Б Надворний Ярослав  Строение белков и их значение для организма “Жизнь – форма существования белковых тел.”
Строение белков и их значение для организма “Жизнь – форма существования белковых тел.”