Содержание
- 2. Механизмы образования ДЭС: а) преимущественная адсорбция одного вида ионов из раствора электролита на твердую фазу ;
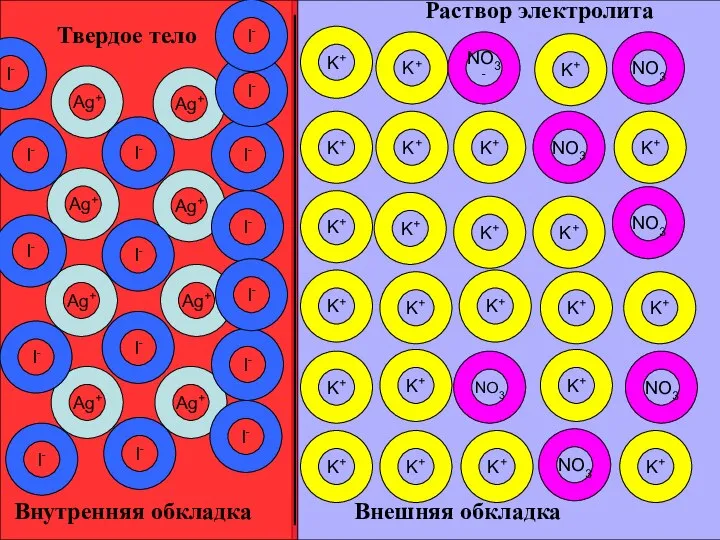
- 3. K+ K+ K+ Твердое тело Ag+ K+ Ag+ Ag+ Ag+ Ag+ Ag+ Ag+ I- I- I-
- 4. Правило Панета ─ Фаянса В достраивании кристаллической решетки внутренней обкладки ДЭС могут принимать участие только те
- 5. - Si – O - – H+ O - SI – O - – H+ O
- 6. (В.1) dG = - S*dT +V*dP + σ*ds + μ i*dni + φ*dq i При постоянных
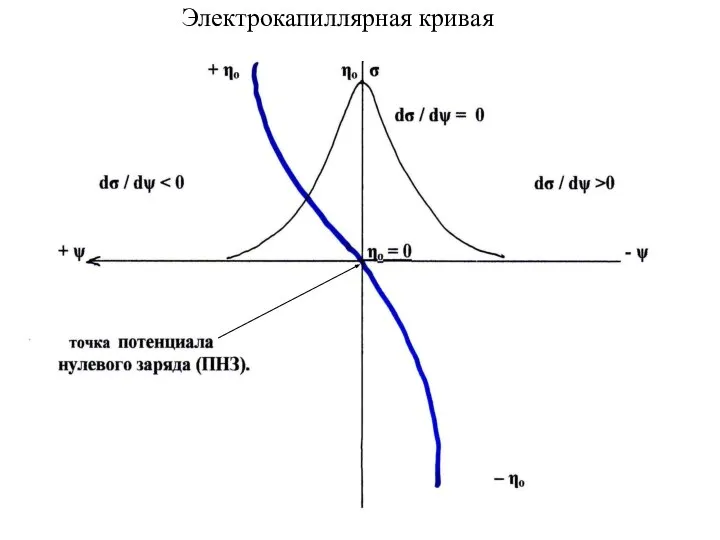
- 7. Электрокапиллярная кривая
- 8. Во всех теориях строения ДЭС действует принцип электронейтральности системы, т. е. заряд 1 см2 поверхности твердой
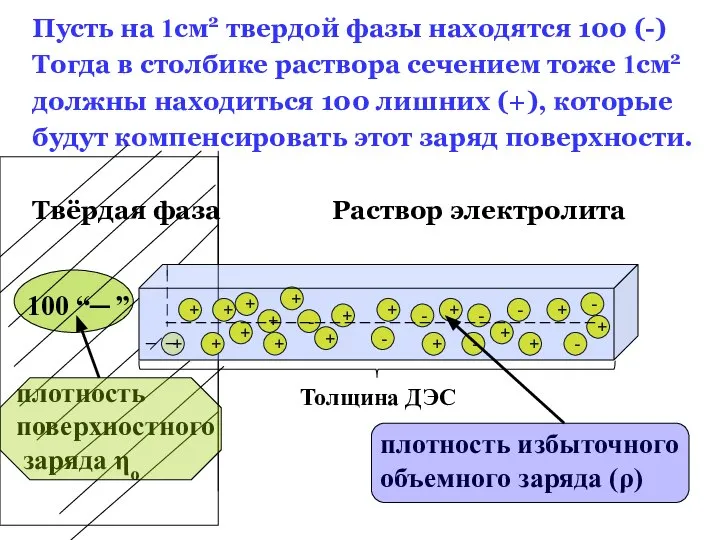
- 9. Пусть на 1см2 твердой фазы находятся 100 (-) Тогда в столбике раствора сечением тоже 1см2 должны
- 10. Поэтому во всех последующих рассуждениях мы будем рассматривать модель плоского ДЭС, считая что радиус кривизны поверхности
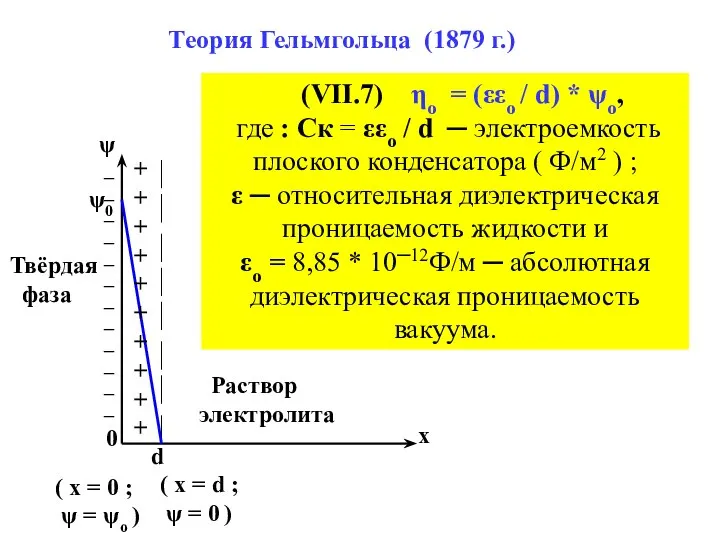
- 11. ψ0 ψ 0 x d + + + + + + + + + + _
- 12. Учитывая, что теория Гельмгольца создавалась за 5 лет до опубликования теории электролитической диссоциации С.Аррениуса, понятно что
- 13. ψ0 ψ 0 x + + + + + + + + + + _ _
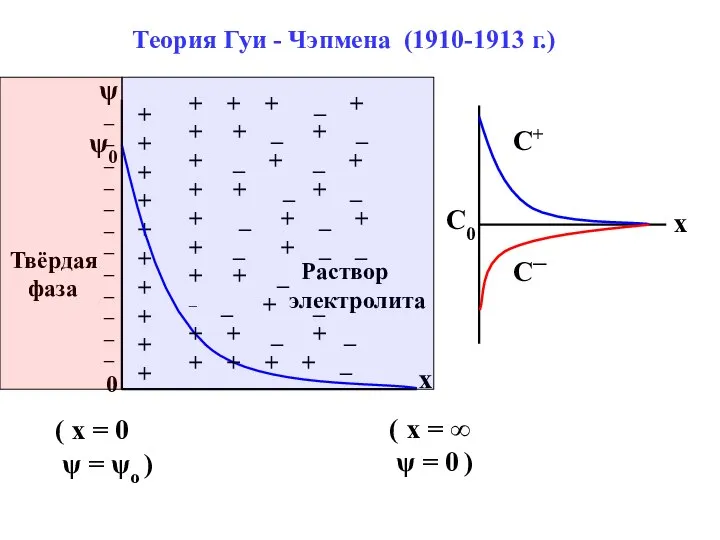
- 14. (VII.8) ηо= √ 2εε0RTCo *[exp( zFψо / 2RT) – exp(– zFψо / 2RT)], [exp( zF ψо
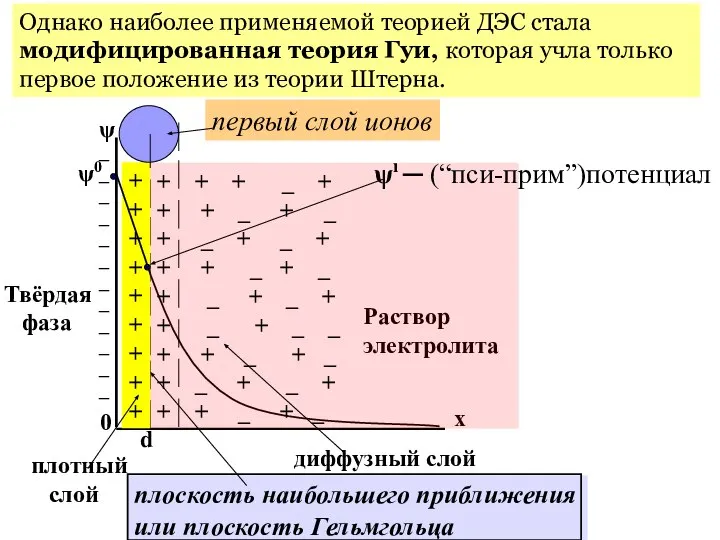
- 15. Для устранения указанных недостатков теории Гуи – Чепмена в 1924 г. Штерн предложил схему строения двойного
- 16. ─ η0 = + + z+*FГ∞ z─ *FГ∞ 1+[exp (Ф++ z+*Fψ1) / 2RT]/18c+ 1+[exp (Ф─+ z─*Fψ1)
- 17. ψ 0 x d + + + + + + + + + _ _ _
- 18. Для этой cхемы строения ДЭС применимо основное уравнение модифицированной теории Гуи (VII.8), но действует оно в
- 19. ψ0 ψ 0 x d + + + + + + + + + + _
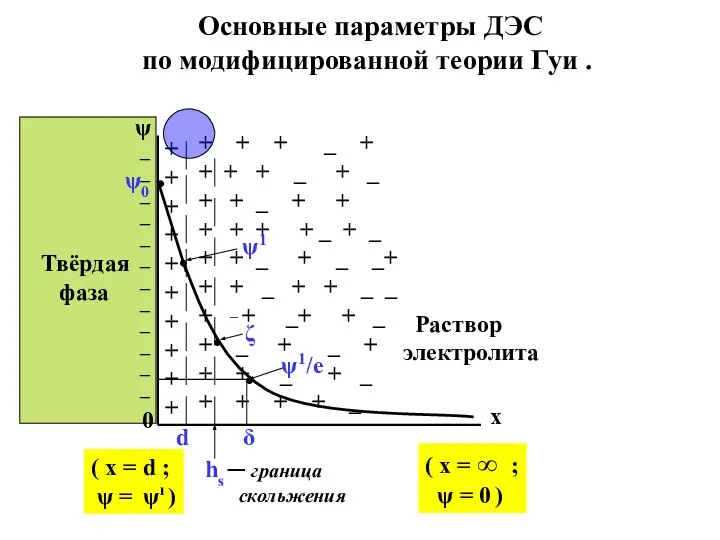
- 20. а) ψо - потенциал поверхности , т.е. разность потенциалов от плоскости наибольшего приближения ( х =
- 21. d) ζ − электрокинетический потенциал (или дзета – потенциал) относится только к движущейся части жидкости, поэтому
- 22. Ещё один важный параметр ДЭС : f) δ ─ это приведенная толщина диффузного слоя, т.е. такое
- 23. Влияние различных электролитов на параметрыДЭС. Сразу договоримся , что будем рассматривать одну и ту же дисперсную
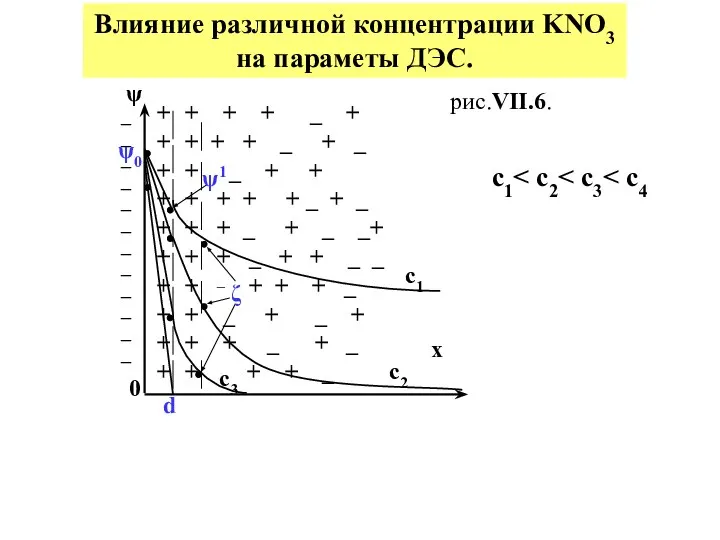
- 24. _ _ _ _ _ _ _ _ _ _ _ _ Влияние различной концентрации KNO3
- 25. Индифферентный электролит не изменяет величину ψo, зато абсолютные величины ψ1 , ζ и δ постепенно уменьшаются
- 26. Предположим, что на единице поверхности твердой фазы AgI находится 100 отрицательных зарядов. Пусть концентрация KNO3 будет
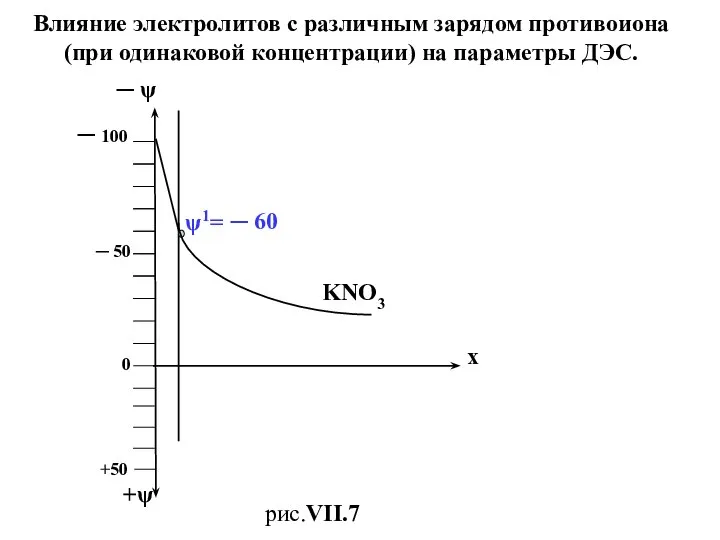
- 27. Влияние электролитов с различным зарядом противоиона (при одинаковой концентрации) на параметры ДЭС. ─ 100 ─ 50
- 28. Примем для простоты рассуждений , что размеры ионов K+ , Ca2+ и Al3+ одинаковы ( радиусы
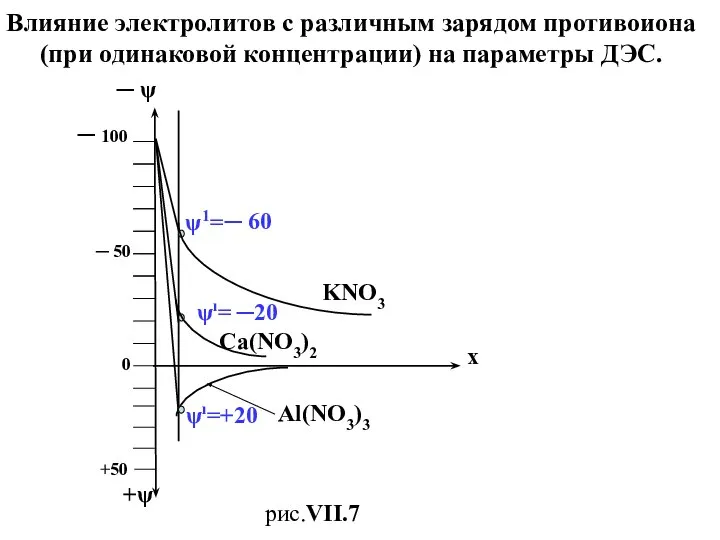
- 29. Влияние электролитов с различным зарядом противоиона (при одинаковой концентрации) на параметры ДЭС. ─ 100 ─ 50
- 30. На рис.VII.7 представлено только по одной кривой для каждого вида электролита. Понятно, что вместо одного рис.VII.7
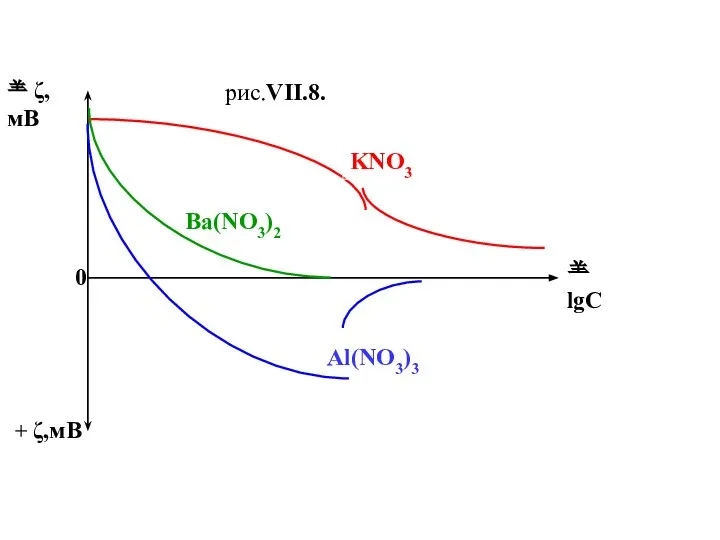
- 31. ζ,мВ + ζ,мВ lgC 0 рис.VII.8. KNO3 Ba(NO3)2 Al(NO3)3
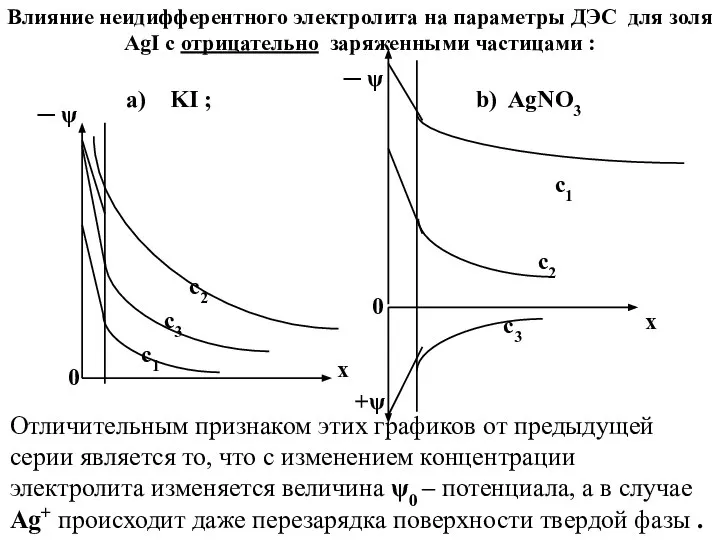
- 32. 2) Влияние электролитов, содержащих потенциал – определяющие ионы . При рассмотрении этого вопроса следует учесть ,
- 33. с2 с1 с3 x x ─ ψ ─ ψ 0 0 +ψ с2 с1 с3 Влияние
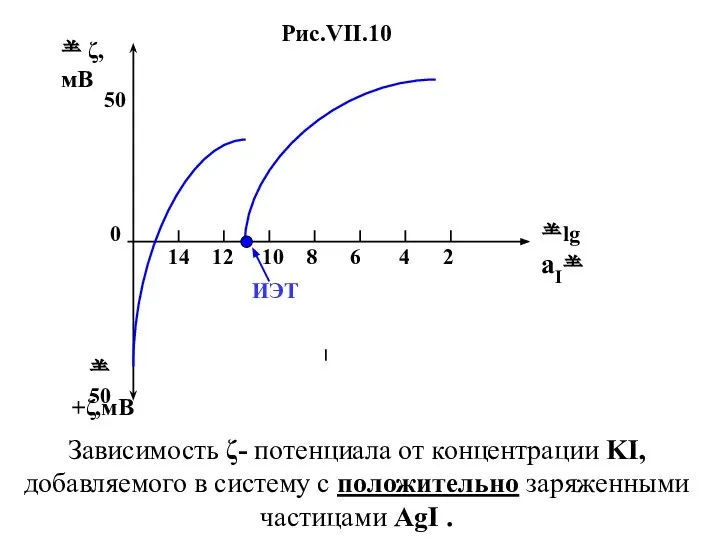
- 34. 14 12 10 8 6 4 2 0 50 50 +ζ,мВ ζ,мВ lg aI
- 35. На рис.VII.10 хорошо видно , что происходит перезарядка ДЭС , причем в отличие от ранее разобранного
- 36. Следует отметить, что поверхностный заряд также зависит от концентрации потенциал-определяющих ионов, только в этом случае речь
- 37. Электрокинетические явления . В первой группе причиной является приложенная к системе разность потенциалов, которая вызывает :
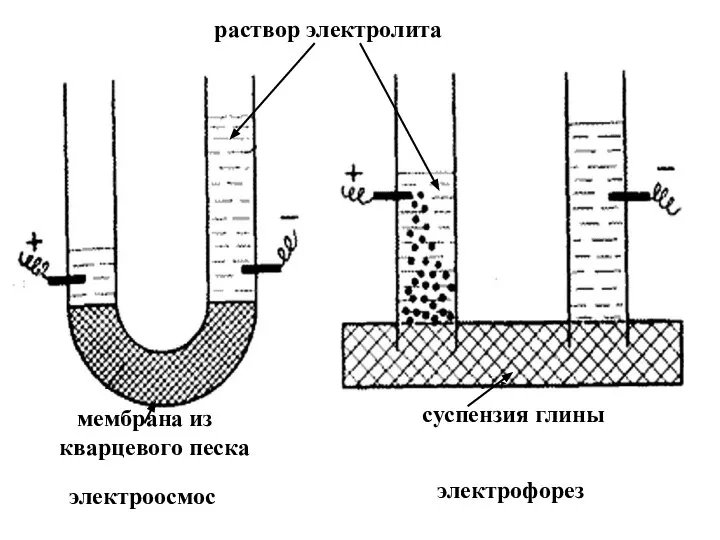
- 38. мембрана из кварцевого песка суспензия глины раствор электролита электроосмос электрофорез
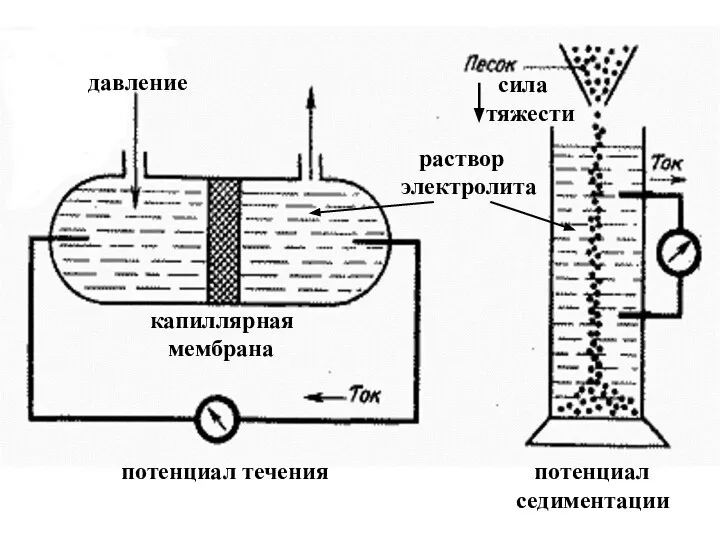
- 39. потенциал течения потенциал седиментации давление капиллярная мембрана сила тяжести раствор электролита
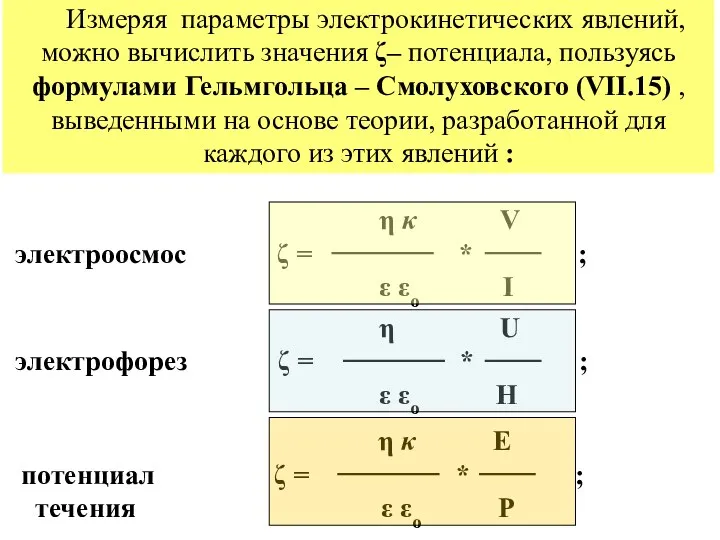
- 40. Измеряя параметры электрокинетических явлений, можно вычислить значения ζ– потенциала, пользуясь формулами Гельмгольца – Смолуховского (VII.15) ,
- 41. η – вязкость среды ; κ – удельная электропроводность раствора электролита ; ε и εо -
- 42. а) Значения ζ – потенциала , определенные различными методами , для одной и той же системы
- 43. b) поверхностная проводимость ; Мы уже указывали, что значения ζ – потенциала не должны зависеть от
- 44. Такая аномалия объясняется тем , что в формулах Гельмгольца ─ Смолуховского (VII.15) для расчетов были использованы
- 45. Таким образом, фактическая удельная электропроводность раствора в капилляре складывается из объемной электропроводности κv и поверхностной проводимости
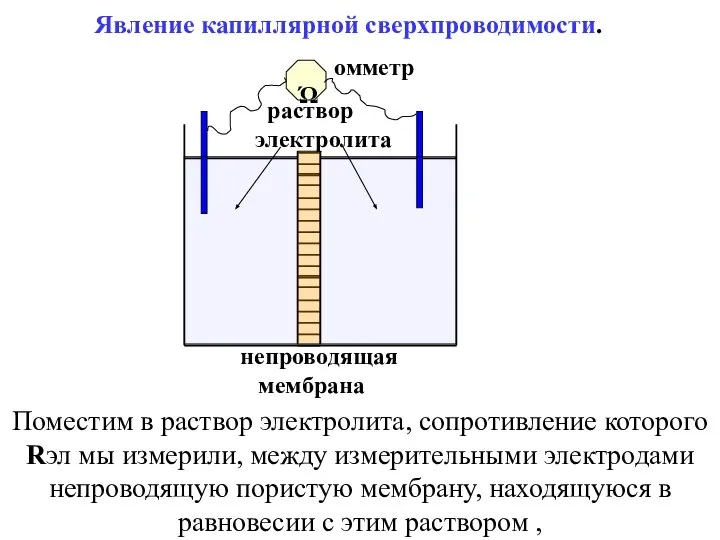
- 46. Явление капиллярной сверхпроводимости. раствор электролита непроводящая мембрана Ώ омметр Поместим в раствор электролита, сопротивление которого Rэл
- 47. Общее сопротивление такой системы R∑ должно увеличиться за счет замены части проводящего раствора электролита на непроводящий
- 48. В этом случае отношение сопротивлений системы с мембраной и без неё уже выразится формулой R∑ /
- 49. c) изменение чисел переноса ионов в порах капиллярной системы (мембраны) по сравнению со свободным раствором. Числом
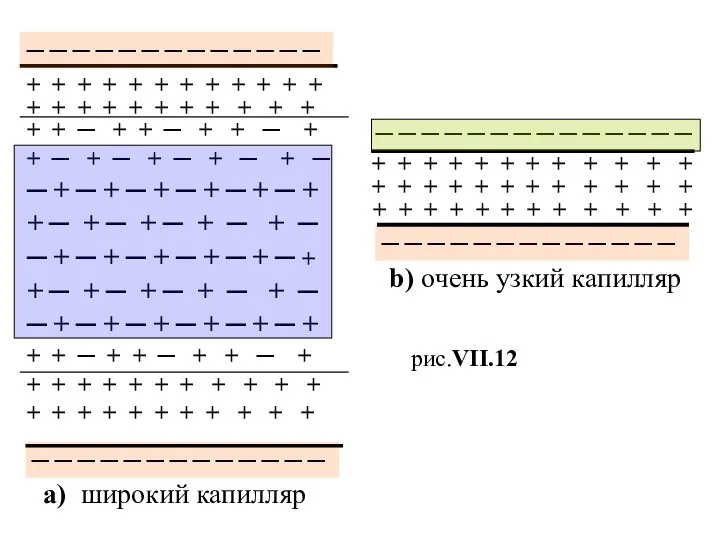
- 50. На рис.VII.12 представлен продольный разрез капилляра с отрицательным зарядом поверхности, заполненного электролитом с ДЭС. Из этого
- 51. ─ ─ ─ ─ ─ ─ ─ ─ ─ ─ ─ ─ ─ ─ + +
- 52. Однако с уменьшением радиуса капилляра доля катионов в общем объеме будет увеличиваться, значит число переноса катиона
- 53. 1) электрохимически неактивные мембраны – не изменяют числа переноса ионов по сравнению с их значениями в
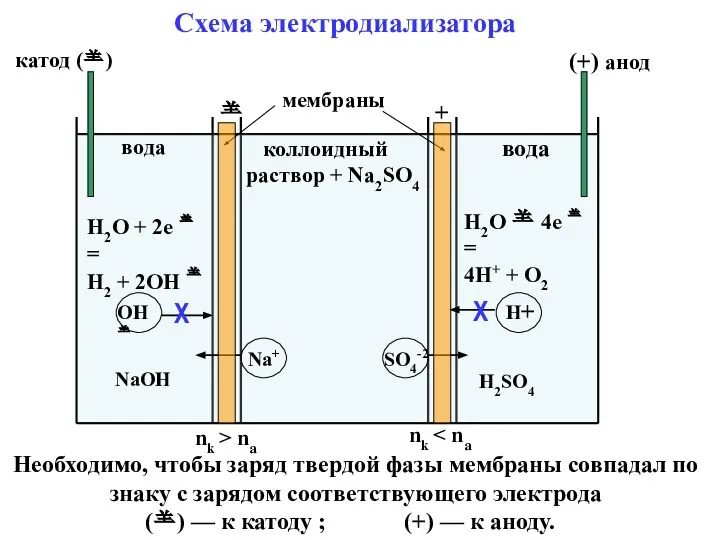
- 54. вода коллоидный раствор + Na2SO4 вода + катод () (+) анод мембраны nk > na
- 55. Электродиализ находит широкое применение прежде всего для очистки воды . При получении дистиллированной воды методом перегонки
- 56. Широкое применение находит электродиализ в медицине и биологии как препаративный метод удаления электролитов из различных коллоидных
- 57. Практическое применение электрокинетических явлений . Электрофорез широко используется : a) в медицине и биологии для: выявления
- 59. Скачать презентацию





































 Химические свойства предельных одноатомных спиртов
Химические свойства предельных одноатомных спиртов Химия – наука о веществах, их свойствах и превращениях Урок №1
Химия – наука о веществах, их свойствах и превращениях Урок №1 Химическая связь
Химическая связь Углерод и кремний
Углерод и кремний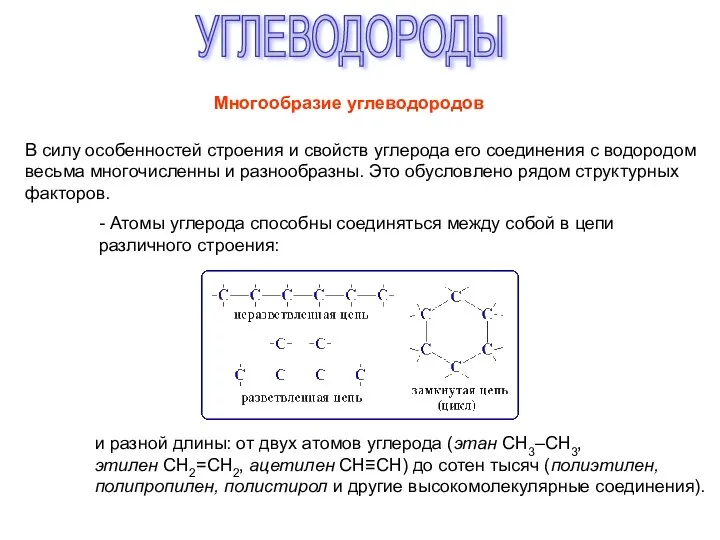 Углеводороды. Многообразие углеводородов
Углеводороды. Многообразие углеводородов Гетерофункциональные соединения
Гетерофункциональные соединения Магматические формации
Магматические формации Полисахариды. Крахмал
Полисахариды. Крахмал Нефть Михеева Анастасия 11-П
Нефть Михеева Анастасия 11-П  Вуглеводні. Підсумковий урок 9 клас
Вуглеводні. Підсумковий урок 9 клас Презентация по Химии "Химическая посуда и оборудование" - скачать смотреть
Презентация по Химии "Химическая посуда и оборудование" - скачать смотреть  Липиды
Липиды Кинетика сложных реакций
Кинетика сложных реакций Положение металлов в Периодической системе Д.И. Менделеева. Особенности строения атомов, свойства
Положение металлов в Периодической системе Д.И. Менделеева. Особенности строения атомов, свойства Chemistry
Chemistry Строение кристаллов
Строение кристаллов Углерод, аллотропные модификации
Углерод, аллотропные модификации Регуляция активности ферментов. Множественные формы ферментов. Введение в клиническую энзимологию. (Лекция 7)
Регуляция активности ферментов. Множественные формы ферментов. Введение в клиническую энзимологию. (Лекция 7) Көміртекті материалдар
Көміртекті материалдар Атомы. Нахождение в природе
Атомы. Нахождение в природе Количества вещества
Количества вещества Презентация Электрохимический ряд напряжений металлов
Презентация Электрохимический ряд напряжений металлов Биосинтез триацилглицеролов и глицерофосфолипидов. Обмен холестерола
Биосинтез триацилглицеролов и глицерофосфолипидов. Обмен холестерола Раздел: «Гетероциклические соединения» Раздел: «Гетероциклические соединения» Лекция №32-33 Тема: «6-ти членные ГЦС» План: 1. О
Раздел: «Гетероциклические соединения» Раздел: «Гетероциклические соединения» Лекция №32-33 Тема: «6-ти членные ГЦС» План: 1. О Оружие массового поражения. Биологическое оружие
Оружие массового поражения. Биологическое оружие  Консистентные смазки для легковых автомобилей
Консистентные смазки для легковых автомобилей Нуклеиновые кислоты
Нуклеиновые кислоты Классификация химических реакций
Классификация химических реакций