Содержание
- 2. Полифункциональные соединения содержат несколько одинаковых функциональных групп. Гетерофункциональные соединения содержат несколько различных функциональных групп. Гетерополифункциональные соединения
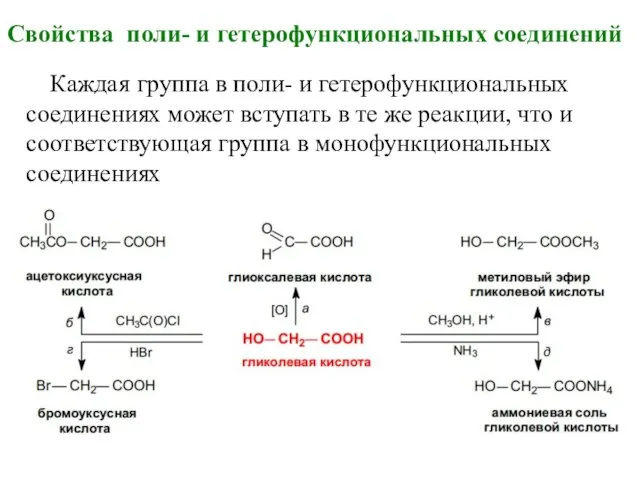
- 3. Свойства поли- и гетерофункциональных соединений Каждая группа в поли- и гетерофункциональных соединениях может вступать в те
- 4. Специфические свойства поли- и гетерофункциональных соединений Реакции циклизации Образование хелатных комплексов
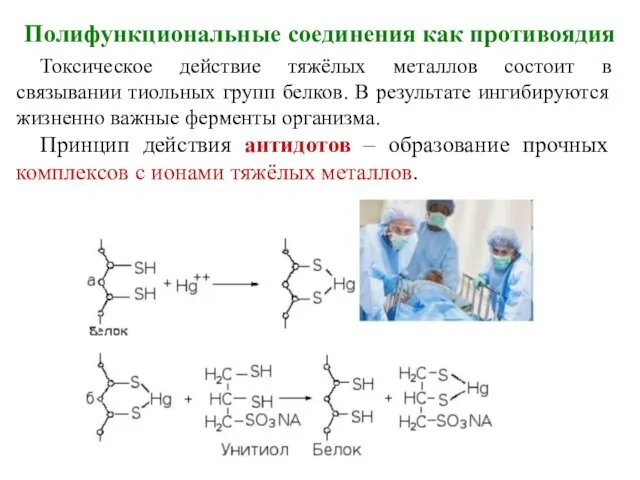
- 5. Полифункциональные соединения как противоядия Токсическое действие тяжёлых металлов состоит в связывании тиольных групп белков. В результате
- 6. Аминокислоты и белки: строение, стереохимия, биологически важные реакции
- 7. Аминокислоты В состав природных полипептидов и белков входят α-аминокислоты, в молекулах которых амино- и карбоксильная группы
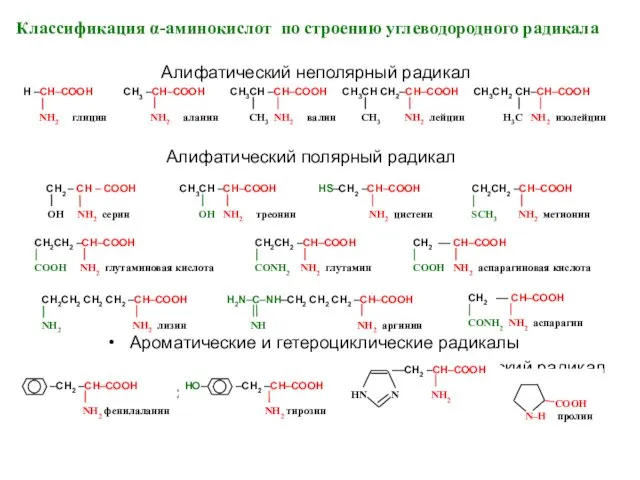
- 8. Классификация α-аминокислот по строению углеводородного радикала Алифатический неполярный радикал Алифатический полярный радикал Ароматические и гетероциклические радикалы
- 9. Заменимые и незаменимые α-аминокислоты Незаменимые α-аминокислоты поступают в организм только из внешней среды, синтез заменимых α-аминокислот
- 10. Относительные конфигурации α-аминокислот В молекулах α-аминокислот (кроме глицина), второй атом углерода является асимметрическим, Молекулы этих кислот
- 11. Конфигурация аминокислот определяет пространственную структуру и биологические свойства как самих аминокислот, биополимеров – белков, которые построены
- 12. Кислотно-основные свойства α-аминокислот В водных растворах и твердом состоянии аминокислоты существуют только в виде внутренних солей
- 13. Значения pI важнейших α-аминокислот Цистеин (Cys) 5,0 Аспарагин (Asp) 5,4 Фенилаланин (Phe) 5,5 Аспарагиновая Треонин (Thr)
- 14. Химические свойства α-аминокислот Реакции с участием карбоксильной группы Реакции с участием аминогруппы Реакции с участием углеводородного
- 15. Реакции с участием карбоксильной группы α-аминокислот Аминокислоты могут вступать в те же химические реакции и давать
- 16. Реакции с участием аминогруппы α-аминокислот Как и другие алифатические амины, аминокислоты могут реагировать с кислотами, ангидридами
- 17. Реакции с участием аминогруппы α-аминокислот Реакции дезаминирования. - окислительное дезаминирование - восстановительное дезаминирование - гидролитическое дезаминирование
- 18. Образование пептидной связи Амино- и карбоксильные группы аминокислот могут реагировать друг с другом. Возникающая при этом
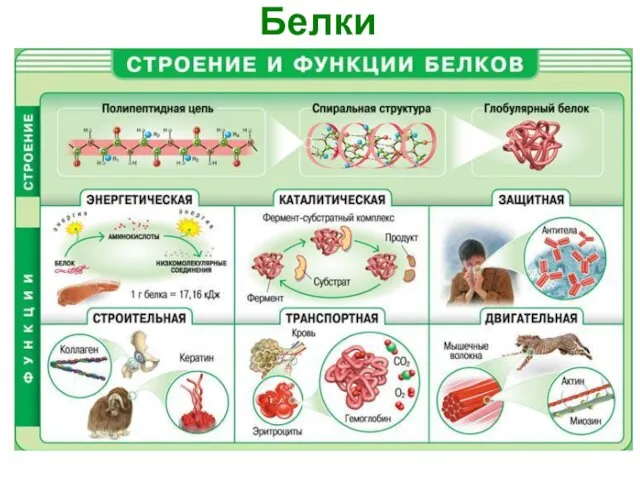
- 19. Белки
- 20. Классификация белков Белки можно классифицировать: – по форме молекул (глобулярные и фибриллярные); – по молекулярной массе
- 21. Функции белков
- 22. Классификация простых белков Альбумины. Примерно 75-80% осмотического давления белков сыворотки крови приходится на альбумины; еще одна
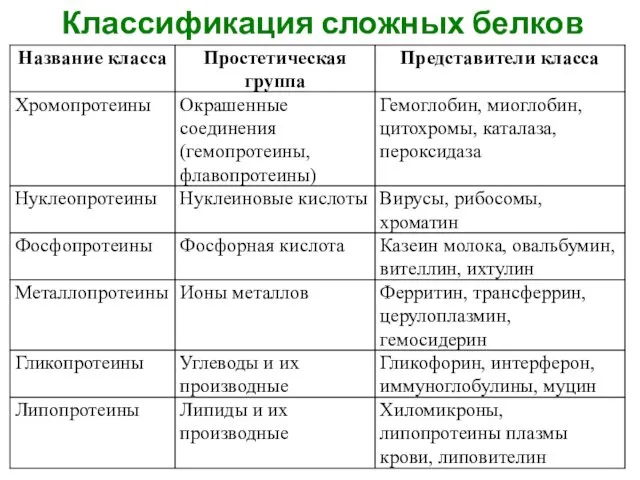
- 23. Классификация сложных белков
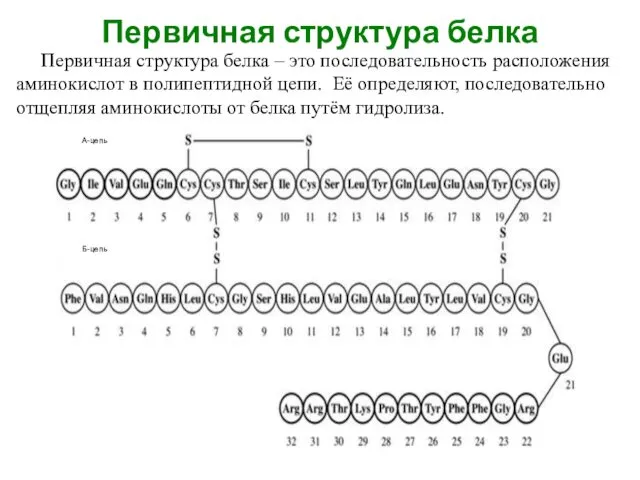
- 24. Первичная структура белка Первичная структура белка – это последовательность расположения аминокислот в полипептидной цепи. Её определяют,
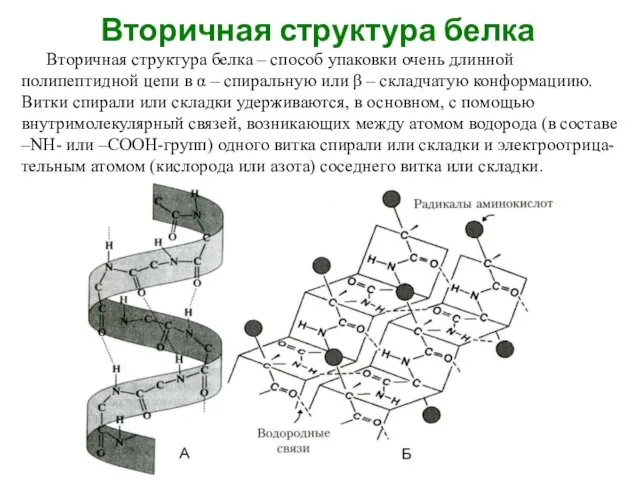
- 25. Вторичная структура белка Вторичная структура белка – способ упаковки очень длинной полипептидной цепи в α –
- 26. Третичная структура белка Третичная структура белка – трёхмерная пространственная ориентация полипептидной спирали или складчатой структуры в
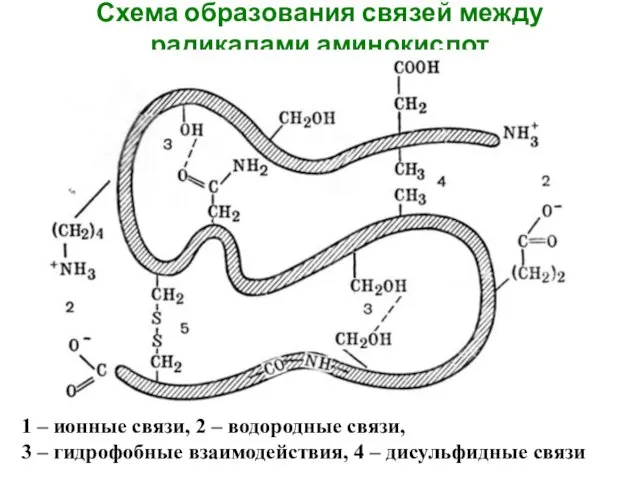
- 27. Схема образования связей между радикалами аминокислот 1 – ионные связи, 2 – водородные связи, 3 –
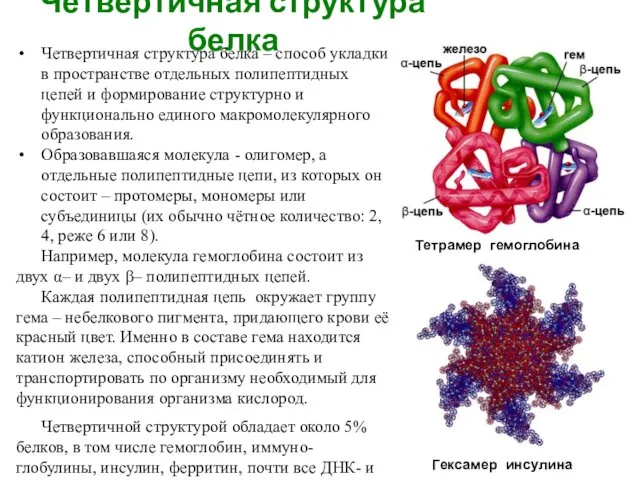
- 28. Четвертичная структура белка Четвертичная структура белка – способ укладки в пространстве отдельных полипептидных цепей и формирование
- 30. Скачать презентацию


















 Коррозия металлов
Коррозия металлов Свойства растворов высокомолекулярных соединений
Свойства растворов высокомолекулярных соединений Керамические материалы
Керамические материалы Периодический закон и периодическая система Д. И. Менделеева
Периодический закон и периодическая система Д. И. Менделеева ИСКУССТВЕННЫЕ ПОЛИМЕРЫ
ИСКУССТВЕННЫЕ ПОЛИМЕРЫ Органикалық қосылыстардың молекуласындағы
Органикалық қосылыстардың молекуласындағы Строение и функции отдельных коферментов
Строение и функции отдельных коферментов Классификация минералов по химическому принципу. Кварц, магнетит
Классификация минералов по химическому принципу. Кварц, магнетит Презентация по Химии "Сетевые образовательные ресурсы по материаловедению" - скачать смотреть
Презентация по Химии "Сетевые образовательные ресурсы по материаловедению" - скачать смотреть  Курсовая работа на тему: «Пьезокварцевое микровзвешивание солей в воде»
Курсовая работа на тему: «Пьезокварцевое микровзвешивание солей в воде» Тест для подготовки к ГИА-9 по химии по теме «Строение атома» А1 Работу выполнил ученик 10-а класса МБОУ «Куженерская средняя общ
Тест для подготовки к ГИА-9 по химии по теме «Строение атома» А1 Работу выполнил ученик 10-а класса МБОУ «Куженерская средняя общ Предмет органической химии.
Предмет органической химии. Гибридизация орбиталей и строение молекул этана, этилена и ацетилена
Гибридизация орбиталей и строение молекул этана, этилена и ацетилена Презентація на тему: “Життя та творчість Д.І.Менделєєва”
Презентація на тему: “Життя та творчість Д.І.Менделєєва”  Элемент цинк
Элемент цинк Харчові добавки. e-числа Підготувала учениця 7(11)-Б класу Луцької гімназії №4 Імені Модеста Левицького Цибульська Вікторія
Харчові добавки. e-числа Підготувала учениця 7(11)-Б класу Луцької гімназії №4 Імені Модеста Левицького Цибульська Вікторія  Материалы, используемые в конструкциях космических аппаратов
Материалы, используемые в конструкциях космических аппаратов Амінокислоти. Класифікація та номенклатура
Амінокислоти. Класифікація та номенклатура Карбоновые кислоты
Карбоновые кислоты Термодинамика химического равновесия. Уравнения изотермы, изобары, изохоры Вант-Гоффа
Термодинамика химического равновесия. Уравнения изотермы, изобары, изохоры Вант-Гоффа Аскорбиновая кислота. Глютаминовая кислота. Кислота аминокапроновая
Аскорбиновая кислота. Глютаминовая кислота. Кислота аминокапроновая Лекция 3. Протолитические равновесия и процессы
Лекция 3. Протолитические равновесия и процессы Презентация по Химии "Жиры животных" - скачать смотреть
Презентация по Химии "Жиры животных" - скачать смотреть  Вычисление массовой доли элемента в молекуле
Вычисление массовой доли элемента в молекуле “TERRA” программасы бойынша ферросиликоалюминийдің балқуының фазалық күйіндегі термодинамикалық есептеуі
“TERRA” программасы бойынша ферросиликоалюминийдің балқуының фазалық күйіндегі термодинамикалық есептеуі Электролиз. Расчетные задачи
Электролиз. Расчетные задачи Алмастырылмайтын аминқышқылды алу биотехнологиясы
Алмастырылмайтын аминқышқылды алу биотехнологиясы Наглядное пособие «Динамические модели». Химическое равновесие в растворах
Наглядное пособие «Динамические модели». Химическое равновесие в растворах