Содержание
- 2. Теория электролитической диссоциации Аррениуса пригодна лишь для водных растворов, в неводных растворителях она несостоятельна. Например, NH4Cl,
- 3. Протолитическая теория кислот и оснований (Теория Бренстеда-Лоури) Кислота – молекула или ион, способные отдавать Н+ (протон).
- 4. Протонная теория объясняет кислотные и оснoвные свойства веществ происходящими между ними процессами протолиза - обмена протонами.
- 5. Амфолитами являются: вода; гидроксиды (Zn, Al, Pb, Sn, Cr); гидроанионы многоосновных кислот (НСО3-, НРО42-, Н2РО4-); аминокислоты
- 6. Жидкие протонсодержащие растворители вступают в обратимую реакцию автопротолиза. Например, для воды: 2Н2О = Н3О+ + ОН-
- 7. Водородный показатель рН – это отрицательный десятичный логарифм активности водородных ионов: рН = - lg cн+.
- 8. Растворенные в воде вещества выполняющие по отношению к ней функции кислоты или основания, называют протолитами в
- 9. Если протолит A- (молекула или ион) - основание, то обратимая реакция протолиза имеет вид: A- +
- 10. Для каждой сопряженной пары кислота/основание значения Kа и Kb связаны соотношением: Ka х Kb = Kw
- 11. Расчет рН кислот и оснований Кислоты сильные слабые рН = - lgСк-та рН = - lg(α
- 13. Буферными называют растворы, способные сохранять значение рН при разбавлении или добавлении небольших количеств кислоты или щелочи.
- 14. Механизм поддержания рН Рассмотрим ацетатный буферный раствор: СН3СООН ↔ СН3СОО- + Н+; СН3СООNa → СН3СОО- +
- 15. рН буферных растворов рассчитывается по формулам Гендерсона – Гассельбаха: Для кислого буфера: Для основного буфера:
- 16. Буферная емкость Величину, характеризующую способность буферного раствора противодействовать смещению реакции среды при добавлении кислот и щелочи,
- 17. Буферная ёмкость зависит от: природы добавляемых веществ и компонентов буферного раствора. исходной концентрации компонентов буферной системы.
- 18. Максимальная буферная емкость, т.е. наибольшая способность этой системы противостоять изменению рН, соответствует значению рН = рК.
- 19. Буферные системы крови Нормальное значение рН плазмы крови 7,40 ± 0,05. Механизм действия разбирается на практическом
- 20. Кислотно-основное состояние организма (КОС) Для оценки состояния буферных систем и выяснения причин сдвигов КОС предложены следующие
- 24. Скачать презентацию





















 1_Bazovye_raschetnye_formuly
1_Bazovye_raschetnye_formuly Гетерофункциональные органические соединения
Гетерофункциональные органические соединения Свойства катализатора. Влияние массы катализатора на скорость реакции
Свойства катализатора. Влияние массы катализатора на скорость реакции Отбор проб товаров для анализа. Химико-аналитический контроль
Отбор проб товаров для анализа. Химико-аналитический контроль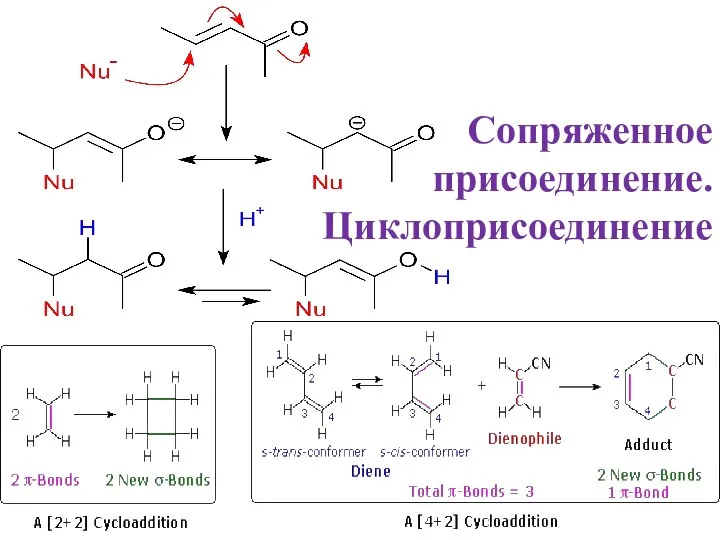 Сопряженное присоединение. Циклоприсоединениеie
Сопряженное присоединение. Циклоприсоединениеie Масс-спектрометрия (МС)
Масс-спектрометрия (МС) Классификации, номенклатура, строение и свойства органических соединений
Классификации, номенклатура, строение и свойства органических соединений Великие ученые XIX-XX веков
Великие ученые XIX-XX веков Презентация Электролиты
Презентация Электролиты Атоми і хімічні елементи. Молекули, їх рух. Дифузія
Атоми і хімічні елементи. Молекули, їх рух. Дифузія Производство шампуня. Технология
Производство шампуня. Технология 140 лет дому, который построил Д.И. Менделеев
140 лет дому, который построил Д.И. Менделеев 160198375
160198375 Презентация Лекарства дома
Презентация Лекарства дома Биохимия. Введение
Биохимия. Введение Углеводы (моносахариды, олигосахариды, полисахариды)
Углеводы (моносахариды, олигосахариды, полисахариды) Автомобильные бензины
Автомобильные бензины Силикатная промышленность
Силикатная промышленность Кислоты
Кислоты Виробництво біогазу Виконав: студент IV курсу групи БЛБ-43з Вила Віктор
Виробництво біогазу Виконав: студент IV курсу групи БЛБ-43з Вила Віктор  Хроматографические методы анализа
Хроматографические методы анализа Электролиз
Электролиз Оксиды. Химические свойства
Оксиды. Химические свойства Основные законы химии. Законы и формулировки
Основные законы химии. Законы и формулировки Метод крутого восхождения или метод Бокса-Уилсона. Симплексный метод оптимизации
Метод крутого восхождения или метод Бокса-Уилсона. Симплексный метод оптимизации Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Кислород. Свойства кислорода
Кислород. Свойства кислорода Валентность химических элементов (8 класс)
Валентность химических элементов (8 класс)