Содержание
- 2. В этом можно легко убедиться посмотрев на следующие слайды. На них изображены : 1) Насекомое –
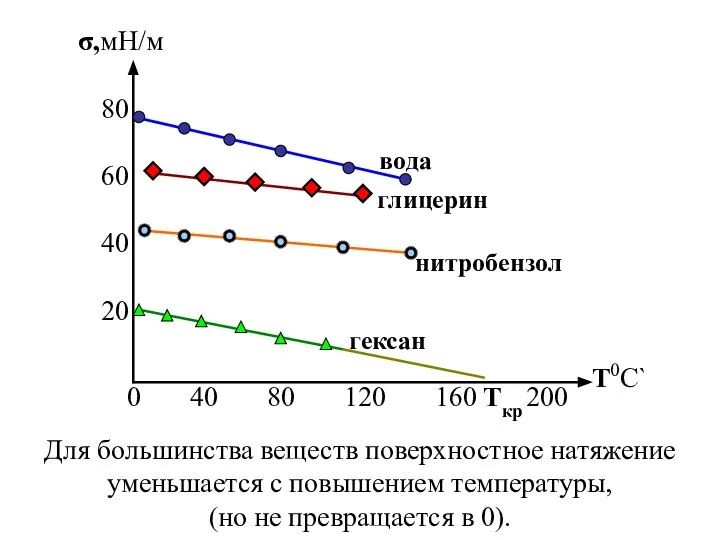
- 6. Величина σ - это энергия, необходимая для выполнения работы по созданию 1 см2 новой поверхности раздела
- 7. Величина свободной поверхностной энергии (Гельмгольца) F( s) = σ * s , где s - площадь
- 8. Для однокомпонентной системы возможен только первый способ уменьшения свободной энергии – т.е. уменьшение поверхности раздела фаз.
- 9. Тогда в поверхностном слое могут находиться молекулы двух типов. Если при этом молекулы первого типа имеют
- 10. газ Жидкость σ1 σ2 ›
- 11. В результате такого перераспределения молекул происходит изменение концентрации вещества в поверхностном слое по сравнению с объемом
- 13. Можно пользоваться производной от свободной энергии Гельмгольца, тогда : (IV.4a) σ = (dF / ds )T,V,ni
- 14. σ,мН/м T0C` 0 40 80 120 160 200 80 60 40 20 Tкр вода глицерин нитробензол
- 16. Существует два основных подхода к термодинамике поверхностных явлений : a) метод избыточных величин Гиббса b) метод
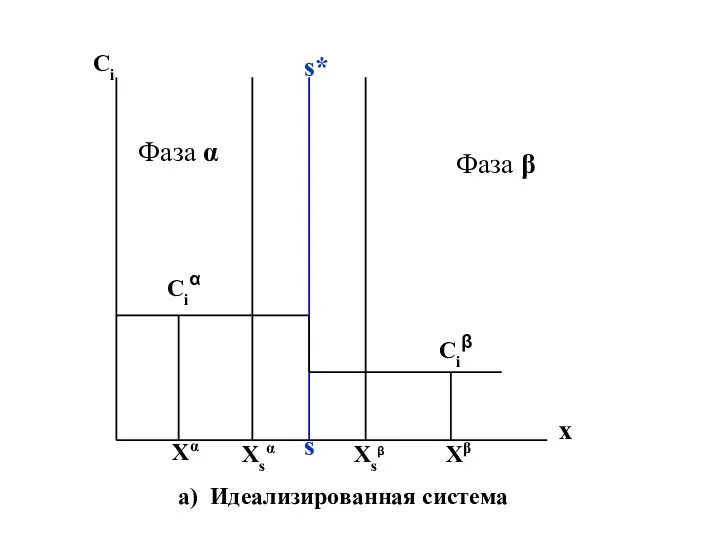
- 17. Ci Ciα Ciβ Фаза α Фаза β s* s Xsα Xsβ Xα Xβ a) Идеализированная система
- 18. Ci Ciα Ciβ Фаза α Фаза β s* s Xsα Xsβ Xα Xβ b) Реальная система,
- 19. Ci Ciα Ciβ Фаза α Фаза β s* s Xsα Xsβ Xα Xβ c) Реальная система,
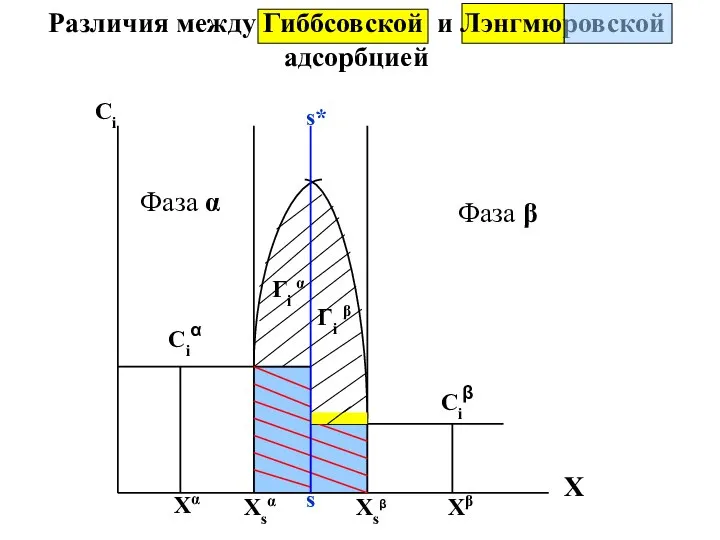
- 20. Ci Ciα Ciβ Фаза α Фаза β s* s Xsα Xsβ Xα Xβ Гi α Гi
- 24. Чтобы сделать переход к развернутой форме уравнения Гиббса, запишем уравнение (IV.13) для бинарной системы, состоящей из
- 25. Ci Ciα Ciβ Фаза α Фаза β s* s Xsα Xsβ Xα Xβ Положение разделяющей поверхности,
- 26. Величина Г2(1) в уравнении (IV.15) называется уже «относительной Гиббсовской адсорбцией» и её физический смысл определяется как
- 28. Рассмотрим границу раздела между жидкостью и газом , например , между водой и воздухом : ясно
- 29. Такие вещества реально существуют и называются они дифильными веществами , молекулы которых содержат одновременно как полярную
- 30. Такое строение указанных молекул приводит к тому , что они накапливаются в поверхностном слое , причем
- 31. газ Жидкость σ1 σ2 ›
- 32. Поверхностная активность – это не свойство вещества самого по себе, как например, плотность , показатель преломления
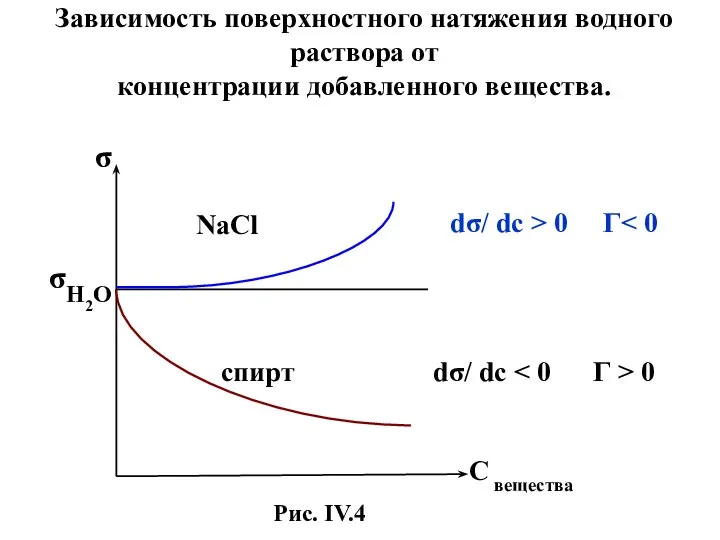
- 33. σ H2O σ NaCl спирт dσ/ dc > 0 Г dσ/ dc 0 Рис. IV.4 Зависимость
- 34. σ С Г с dσ Г = ─ * RT dс Уравнение Гиббса kл Гл =
- 35. Ирвинг Лэнгмюр ( 1881 - 1957)
- 36. первый сформулировал « Принцип независимости поверхностного действия», суть которого состоит в том , что каждая часть
- 38. И, наконец, именно Лэнгмюр ещё в начале ХХ века создал классическую теорию адсорбции, которая не утратила
- 40. Обозначив одной константой kл отношение констант адсорбции и десорбции, α / β = kл и выполнив
- 41. Различия между Гиббсовской и Лэнгмюровской адсорбцией X
- 42. Однако для разбавленных растворов , где концентрация поверхностно-активного компонента в объеме фазы сравнительно невелика по сравнению
- 43. Адсорбция газов на твердой поверхности – это процесс не статический , а динамический , т.е. она
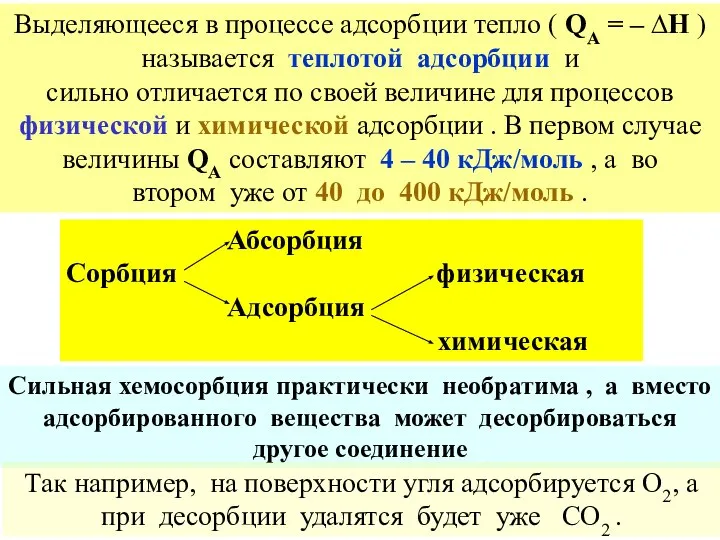
- 44. Что же касается теплоты адсорбции QA , то это реальная и вполне понятная величина, особенно учитывая,
- 45. Выделяющееся в процессе адсорбции тепло ( QA = – ∆H ) называется теплотой адсорбции и сильно
- 46. a) При низких концентрациях с→ 0, тогда kлc « 1 и Гл= Г∞* kлc т.е. зависимость
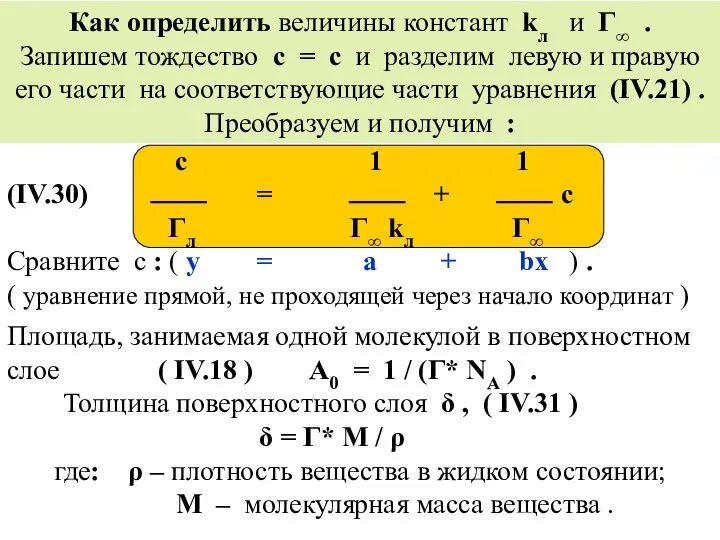
- 47. Как определить величины констант kл и Г∞ . Запишем тождество с = с и разделим левую
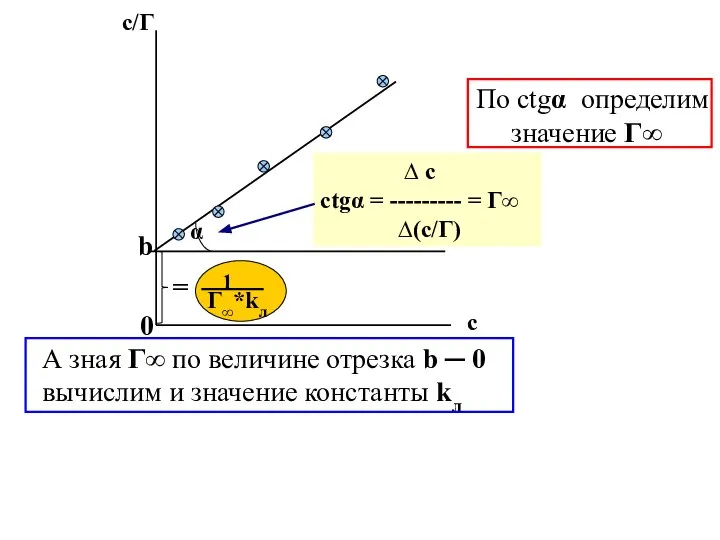
- 48. 1 Г∞*kл ∆ c ctgα = --------- = Г∞ ∆(c/Г) α с/Г с По ctgα определим
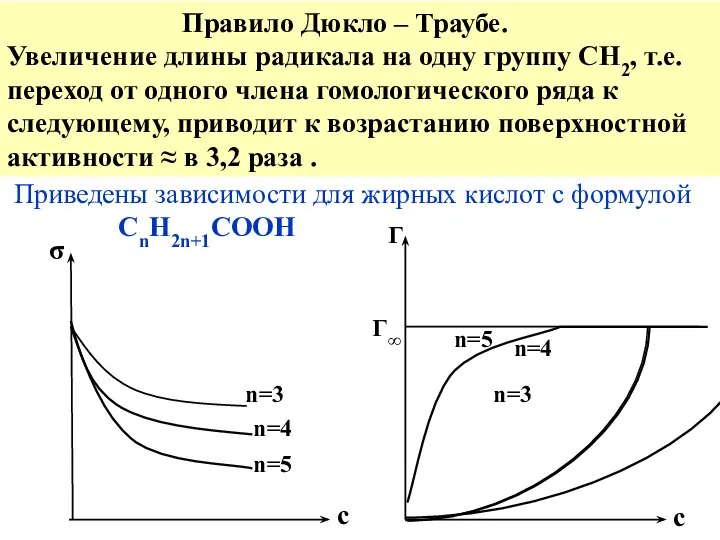
- 49. σ c c Г Г∞ n=3 n=4 n=5 n=3 n=4 n=5 Правило Дюкло – Траубе. Увеличение
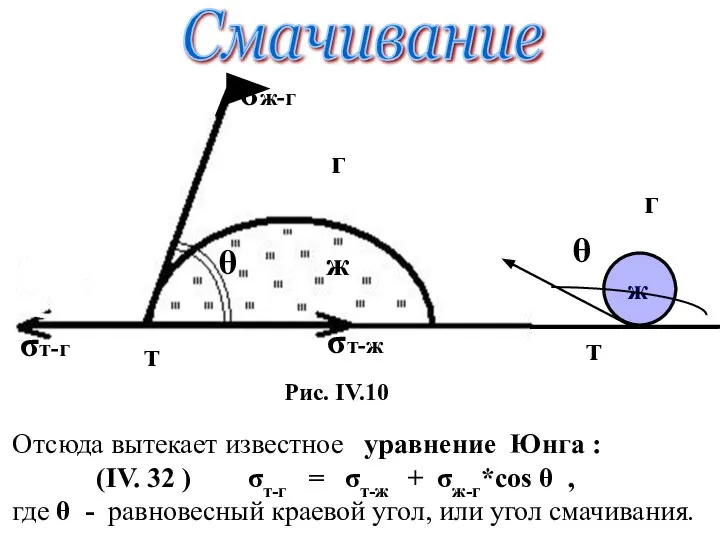
- 50. ж Отсюда вытекает известное уравнение Юнга : (IV. 32 ) σт-г = σт-ж + σж-г*cos θ
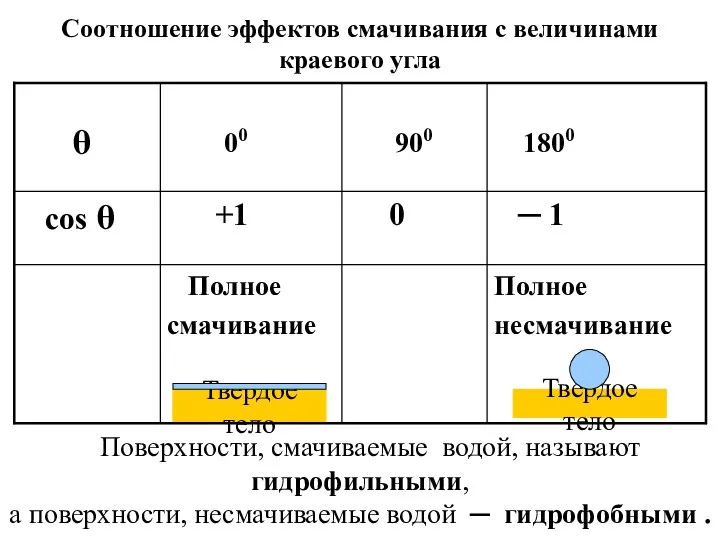
- 51. Твердое тело Соотношение эффектов смачивания с величинами краевого угла Поверхности, смачиваемые водой, называют гидрофильными, а поверхности,
- 52. Поэтому работу, необходимую для разрыва однородной фазы, сечением 1 см2, называют работой когезии Wк , а
- 53. Решая совместно уравнения (IV.32) и (IV.34) , получим для работы адгезии формулу уравнения Дюпре : (IV.35)
- 54. А вот еще частные случаи уравнения Дюпре : работа смачивания Wсм = A т * ∆σ
- 55. (IV.37) Pα - Pβ = PC = 2 σ / R , Дополнительное давление PС ,
- 56. Если жидкость смачивает капилляр, то она в нем поднимается, а если не смачивает ─ то опускается.
- 57. (в момент равновесия соблюдается равенство сил) σ * 2π r * cos θ = π r2*
- 58. Для воды (σ = 72,75 мн/м ; ρ = 1г/см ; g = 981см/с2 ), если
- 59. Уравнения Лапласа (IV.37) и Жюрена (IV.39) лежат в основе двух наиболее распространенных методов измерения поверхностного натяжения
- 60. Это условие наиболее трудно выполнимо, т.к. требует тщательной очистки внутренней поверхности капилляра, причем без применения современных
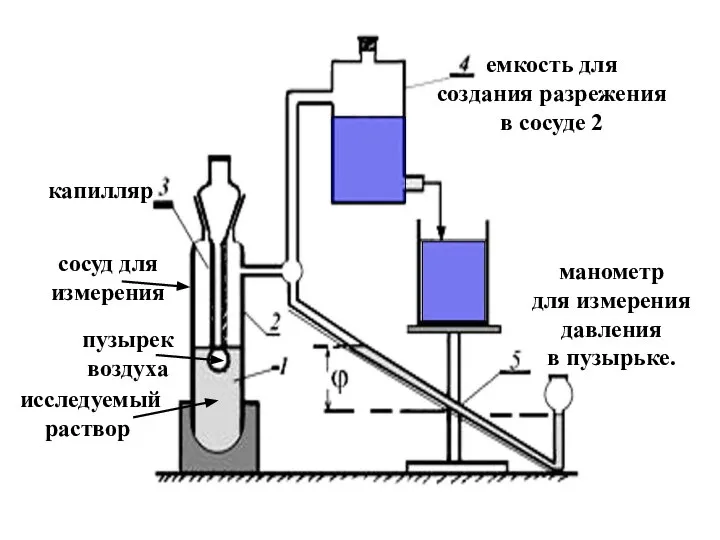
- 61. исследуемый раствор пузырек воздуха сосуд для измерения капилляр емкость для создания разрежения в сосуде 2 манометр
- 62. В этом методе происходит выдувание пузырька воздуха из капилляра в смачивающую его жидкость, при этом давление,
- 63. Определив константу капилляра Кк , проводят серию измерений растворов с неизвестными значениями σх , определяют ΔPmx
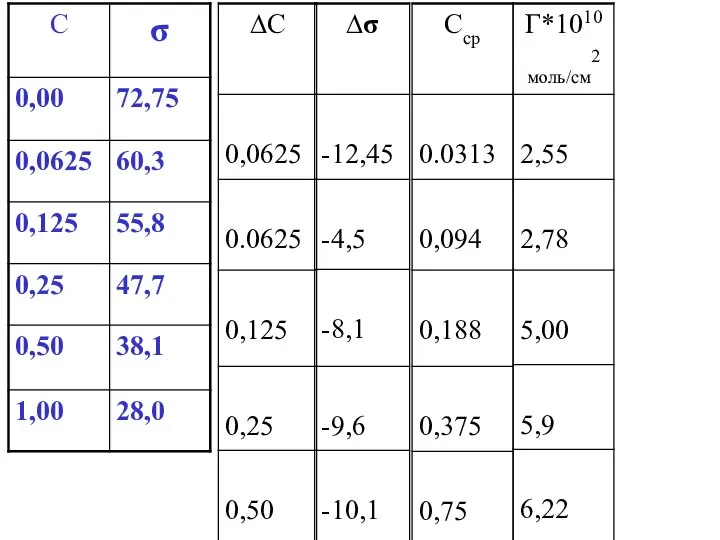
- 64. Пример расчета лабораторной работы по измерению поверхностного натяжения и адсорбции: Первые две колонки таблицы ─ это
- 65. 2. После этого можно заполнить остальные колонки в таблице: ∆С, ∆σ, Сср и Г.
- 67. 3. Расчет величин Г проводят по уравнению Гиббса (IV.17): 0,0325моль/л *(- 12,45эрг/см2) 8,31*10─7эрг/моль*0К * 2930К *
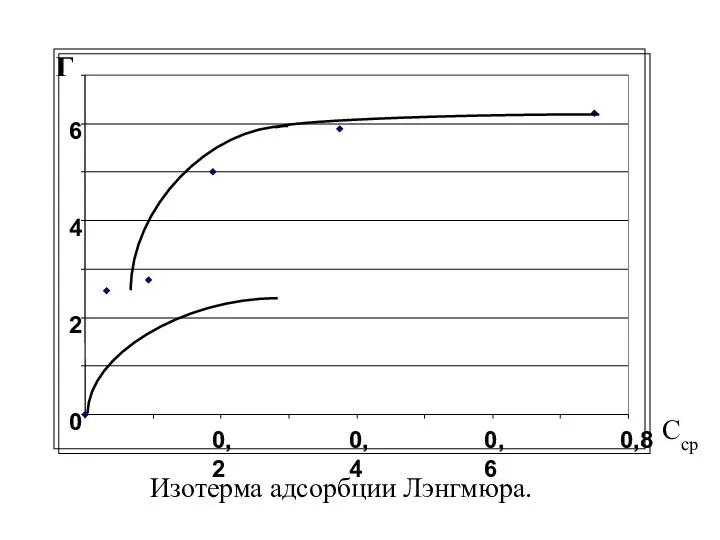
- 68. Г Сср Изотерма адсорбции Лэнгмюра.
- 69. 5. Для определения величин констант Г∞ и kл в этом уравнении нам необходимо построить ещё один
- 71. Сср 6. В нашем случае величина ctgα = Г∞ составляет 6,63*10─ 10 моль/см2 ( если провести
- 72. Значение площади поперечного сечения молекулы ПАВ A0= 1/(NA* Г∞) составит 1/(6,02*1023*6,63*10─10) = 25*10─16см2 = 0,25нм2. Зная
- 73. Адсорбцию из растворов можно разделить на два вида : адсорбцию нейтральных молекул (неэлектролитов) b) избирательную адсорбцию
- 74. Если применяется высокодисперсный адсорбент с очень узкими порами , то с ростом длины молекулы адсорбата выше
- 75. вода вода уголь бензол силикагель силикагель бензойная кислота 1) из водного раствора – это неполярный уголь;
- 76. Когда мы делали анализ уравнения изотермы Лэнгмюра ( IV.21), то показали , что она состоит из
- 77. В отличие от уравнения Лэнгмюра уравнение Фрейндлиха не описывает всего процесса адсорбции : при малых концентрациях
- 78. Для этого готовят серию из 6 – ти растворов исследуемого ПАВ (уксусной кислоты) с разведением каждой
- 79. Константы уравнения Фрейндлиха обычно находят графически по изотерме , построенной в логарифмических координатах . Прологарифмировав уравнение
- 81. Скачать презентацию

































































 Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды Теория химического строения Бутлерова. Второе положение теории Бутлерова. Изомерия. Структурная изомерия
Теория химического строения Бутлерова. Второе положение теории Бутлерова. Изомерия. Структурная изомерия КРУГОВОРОТ ВЕЩЕСТВ В ПРИРОДЕ Маслова А.Л. ГОУ № 483
КРУГОВОРОТ ВЕЩЕСТВ В ПРИРОДЕ Маслова А.Л. ГОУ № 483 Свойства спирта и воды
Свойства спирта и воды Виробництво біогазу
Виробництво біогазу Порядок в жидкостях
Порядок в жидкостях Сплавы
Сплавы Презентация по Химии "d — элементы" - скачать смотреть
Презентация по Химии "d — элементы" - скачать смотреть  Магматические породы и постмагматические процессы
Магматические породы и постмагматические процессы Теория строения химических соединений А. М. Бутлерова
Теория строения химических соединений А. М. Бутлерова Acids and alkalis
Acids and alkalis Биологиялық белсенді қосылыстардың иондалу және липофильділік мәселелері
Биологиялық белсенді қосылыстардың иондалу және липофильділік мәселелері Определение массы и объёма по плотности вещества
Определение массы и объёма по плотности вещества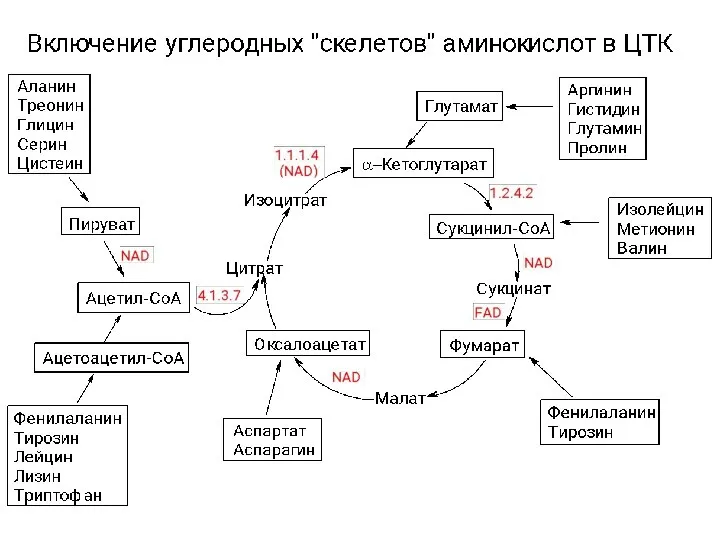 Катаболизм аминокислот
Катаболизм аминокислот Медь и ее сплавы
Медь и ее сплавы Алканы. Пропан
Алканы. Пропан Презентация по Химии "Инертные газы" - скачать смотреть
Презентация по Химии "Инертные газы" - скачать смотреть  Кислородные соединения углерода
Кислородные соединения углерода Подготовка нефти и газового конденсата к переработке. Атмосферная и вакуумная перегонка
Подготовка нефти и газового конденсата к переработке. Атмосферная и вакуумная перегонка Дифференциация магмы
Дифференциация магмы Органические загрязнители вод
Органические загрязнители вод Презентація на тему: Корозія. Шляхи захисту від неї.
Презентація на тему: Корозія. Шляхи захисту від неї.  Budowa pasmowa ciał stałych
Budowa pasmowa ciał stałych Тест по теме: Алкины
Тест по теме: Алкины Дека́н (н-декан) — органическое соединение класса алканов
Дека́н (н-декан) — органическое соединение класса алканов Кислородосодержащие органические соединения Cпирты (алканолы)
Кислородосодержащие органические соединения Cпирты (алканолы) Кислородные соединения углерода
Кислородные соединения углерода Биологическая роль макро и микроэлементов. (Лекция 17)
Биологическая роль макро и микроэлементов. (Лекция 17)