Содержание
- 2. Проэкт Фосфор Выполнили ученики 10 класса Бурдюк ,Власенко ,Черненко
- 3. Фосфор (P) – довольно распространённый химический элемент на нашей планете, но несмотря на это в природе
- 4. Фосфор открыт гамбургским алхимиком Хеннигом Брандом в 1669 году. Подобно другим алхимикам, Бранд пытался отыскать философский
- 5. Свойство простого вещества и промышленное получение фосфора. Вопрос аллотропии фосфора сложен и до конца не решен.
- 6. Белый фосфор (P4), наиболее активная, летучая, форма простого вещества. В чистом виде это бесцветное стекловидное вещество,
- 7. Черный фосфор –Впервые получен в 1914 в виде кристаллической модификации высокой плотности (2690 кг/м3) американским физиком
- 8. Жёлтый фосфор – это тот же самый белый фосфор, но только не подвергшийся очистке. Сильно ядовит,
- 9. Аморфный красный фосфор был открыт в 1847 в Швеции профессором химии Антоном Риттером фон Кристелли Шреттером
- 10. Химические Свойства Фосфора (Р) В жидком и растворенном состоянии, а также в парах до 800 °С
- 11. Фосфор в природе .Его промышленная добыча Содержание фосфора в земной коре оценивается в 8 10-2% по
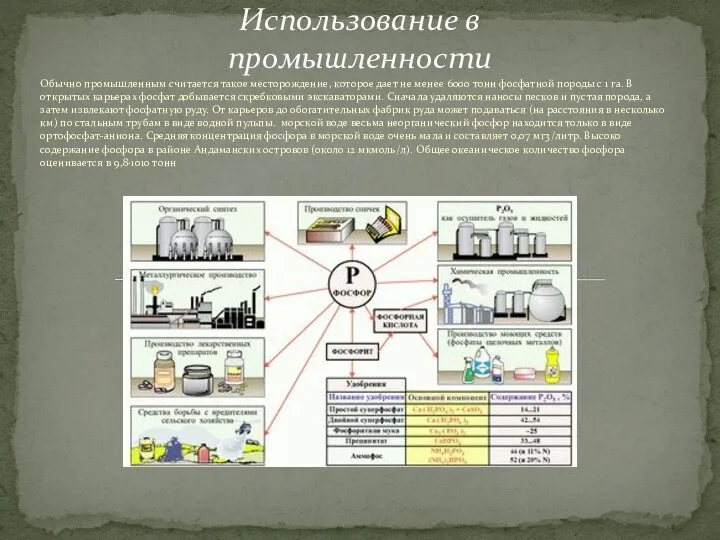
- 12. Обычно промышленным считается такое месторождение, которое дает не менее 6000 тонн фосфатной породы с 1 га.
- 14. Скачать презентацию
Проэкт
Фосфор
Выполнили ученики 10 класса
Бурдюк ,Власенко ,Черненко
Проэкт
Фосфор
Выполнили ученики 10 класса
Бурдюк ,Власенко ,Черненко
Фосфор (P) – довольно распространённый химический элемент на нашей планете, но
Фосфор (P) – довольно распространённый химический элемент на нашей планете, но
Что такое «Фосфор»
Фосфор открыт гамбургским алхимиком Хеннигом Брандом в 1669 году. Подобно другим
Фосфор открыт гамбургским алхимиком Хеннигом Брандом в 1669 году. Подобно другим
История происхождения
Свойство простого вещества и промышленное получение фосфора. Вопрос
аллотропии фосфора сложен
Свойство простого вещества и промышленное получение фосфора. Вопрос
аллотропии фосфора сложен
модификации простого вещества – белую, красную и черную. Иногда их ещё
называют главными аллотропными модификациями, Существует
аморфный фосфор различных цветов и оттенков – от ярко-красного до
фиолетового и коричневого.
Свойства
Белый фосфор (P4), наиболее активная, летучая, форма простого вещества. В чистом
Белый фосфор (P4), наиболее активная, летучая, форма простого вещества. В чистом
Обладает специфическим чесночным запахом.
Жирный на ощупь.
Мягкий ,легко режется ножом.
Температура плавления чистого вещества 44,1°С.
Температура кипения 280°С .
Плотность 1823 кг/м3 (293К).
Промышленный продукт может быть от соломенно- желтого до коричнево-красного или коричневого.
Практически нерастворим в воде(но растворим при комнатной температуре в неполярных органических растворителях:бензоле 3,7 г на 100 г C6H6), тетрахлорметане (1,27 г на 100 г CCl4), диэтиловом эфире (1,39 г на 100 г Et2O).Хорошими растворителями для него считаются жидкие аммиак и диоксид серы, а наилучшими – сероуглерод.)
Фосфор загорается в атмосфере хлора с образованием смеси хлоридов:
P4 +10Cl2 =4PCl3
P4 +10Cl2 =4PCl5
Белый фосфор довольно сильный восстановитель – вытесняет медь, свинец, ртуть и серебро из растворов солей(P4 +10CuSO4 +16H2O=4H3PO4 +10Cu+10H2SO4)Именно поэтому при отравлении белым фосфором рекомендуется выпить сильно разбавленный раствор медного купороса.
При слабом нагревании фосфор окисляется серой, а взаимодействие его с твердыми KClO3 , KMnO4 , KlO3 может приобретать взрывной характер.
В темноте можно наблюдать холодное зеленоватое свечение белого фосфора,
обусловленное протекающей разветвленной цепной реакцией окисления паров
фосфора.
Белый фосфор чрезвычайно ядовит, доза в 0,05-0,1 г смертельна для
человека. Он способен аккумулироваться в организме и вызывать некроз
костных тканей (особенно челюстей).
Белый фосфор
Черный фосфор –Впервые получен в 1914 в виде кристаллической модификации высокой
Черный фосфор –Впервые получен в 1914 в виде кристаллической модификации высокой
Чёрный фосфор
Жёлтый фосфор – это тот же самый белый фосфор, но только
Жёлтый фосфор – это тот же самый белый фосфор, но только
Жёлтый фосфор
Аморфный красный фосфор был открыт в 1847 в Швеции профессором химии
Аморфный красный фосфор был открыт в 1847 в Швеции профессором химии
Красный фосфор
Химические Свойства Фосфора (Р)
В жидком и растворенном состоянии, а также в
Химические Свойства Фосфора (Р)
В жидком и растворенном состоянии, а также в
Взаимодействие с простыми веществами :
Фосфор легко окисляется кислородом: 4P + 5O2 → 2P2O5 (с избытком кислорода), 4P + 3O2 → 2P2O3 (при медленном окислении или при недостатке кислорода)
Взаимодействует со многими простыми веществами — галогенами, серой, некоторыми металлами, проявляя окислительные и восстановительные свойства:
с металлами — окислитель, образует фосфиды: 2P + 3Ca → Ca3P2, 2P + 3Mg → Mg3P2.
с неметаллами — восстановитель: 2P + 3S → P2S3, 2P + 3Cl2 → 2PCl3.
Не взаимодействует с водородом.
Взаимодействие с водой :
Взаимодействует с водой, при этом диспропорционирует: 4Р + 6Н2О → РН3 + 3Н3РО2 (фосфатная кислота).
Взаимодействие со щелочами :
В растворах щелочей диспропорционирование происходит в большей степени: 4Р + 3KOH + 3Н2О → РН3 + 3KН2РО2. Восстановительные свойства :
Сильные окислители превращают фосфор в фосфорную кислоту: 3P + 5HNO3 + 2H2O → 3H3PO4 + 5NO; 2P + 5H2SO4 → 2H3PO4 + 5SO2 + 2H2O.
Реакция окисления также происходит при поджигании спичек, в качестве окислителя выступает бертолетова соль: 6P + 5KClO3 → 5KCl + 3P2O5
Фосфор в природе .Его промышленная добыча
Содержание фосфора в земной коре оценивается
Фосфор в природе .Его промышленная добыча
Содержание фосфора в земной коре оценивается
Апатит (с др.-греч. ἀπατάω «обманываю») – минерал из группы фосфатов: фосфат кальция.
Химическая формула: Ca5[PO4]3(OH, F, Cl).
Блеск стеклянный, иногда жирноватый.
Очень хрупкий.
Удельный вес 3,2-3,4 г/см3
Цвет зеленый, голубовато-зеленый, синевато-зеленый, также бурый, голубой, фиолетовый, редко бесцветный, белый, иногда зеленый с серыми пятнами .
Растворяется в соляной и азотной кислотах. Солянокислый раствор при прибавлении аммиака дает белый студневидный осадок.
Гуано
Сильно разложившееся гуано состоит преимущественно из мометита CaHPO4 и витлокита b - Ca3(PO4)2
Обычно промышленным считается такое месторождение, которое дает не менее 6000 тонн
Обычно промышленным считается такое месторождение, которое дает не менее 6000 тонн
Использование в промышленности










 АЗОТ Дегтярева Марина Олеговна учитель химии Автономное общеобразовательное учреждение Лицей научно-инженерного профи
АЗОТ Дегтярева Марина Олеговна учитель химии Автономное общеобразовательное учреждение Лицей научно-инженерного профи Теоретические основы неорганического синтеза
Теоретические основы неорганического синтеза ТЕМА УРОКА:
ТЕМА УРОКА: Фуллерен С60 и его аналоги
Фуллерен С60 и его аналоги Фосге́н (дихлорангидрид угольной кислоты)
Фосге́н (дихлорангидрид угольной кислоты) Презентация по Химии "Волшебный сад" - скачать смотреть
Презентация по Химии "Волшебный сад" - скачать смотреть  Капсаицин Немного информации
Капсаицин Немного информации Работу выполнил: ученик 11 класса Палкин Денис
Работу выполнил: ученик 11 класса Палкин Денис Классификация неорганических веществ
Классификация неорганических веществ Обзор основных методов исследования супрамолекулярных объектов
Обзор основных методов исследования супрамолекулярных объектов Периодическая система Д.И. Менделеева и строение атома
Периодическая система Д.И. Менделеева и строение атома Материаловедение. Текстильные волокна, пряжа и ткань
Материаловедение. Текстильные волокна, пряжа и ткань Одноатомные спирты
Одноатомные спирты Зат алмасу
Зат алмасу Катализаторы на носителях, получаемые методом пропитки
Катализаторы на носителях, получаемые методом пропитки Көміртекті материалдар
Көміртекті материалдар Культуральные свойства микроорганизмов. Антибиотики. Методы определения антибиотикорезистентности бактерий
Культуральные свойства микроорганизмов. Антибиотики. Методы определения антибиотикорезистентности бактерий Презентация по химии Роль Химии в жизни общества
Презентация по химии Роль Химии в жизни общества Разбор заданий
Разбор заданий Презентация по Химии "Химия вокруг нас" - скачать смотреть
Презентация по Химии "Химия вокруг нас" - скачать смотреть  Презентация по Химии "Оксиды. Состав. Классификация. Номенклатура. Свойства. Получение. Применение" - скачать смотреть бесплат
Презентация по Химии "Оксиды. Состав. Классификация. Номенклатура. Свойства. Получение. Применение" - скачать смотреть бесплат Ароматические углеводороды (арены). Бензол
Ароматические углеводороды (арены). Бензол Горные породы
Горные породы Презентация по Химии "История семи великих камней Алмазного фонда России" - скачать смотреть
Презентация по Химии "История семи великих камней Алмазного фонда России" - скачать смотреть  Генетическая связь между классами веществ
Генетическая связь между классами веществ Кремний
Кремний Химические реакции. по фазовому составу
Химические реакции. по фазовому составу Презентация Производство стекла
Презентация Производство стекла