Содержание
- 2. Сульфатна кислота і сульфати.
- 3. Сульфур (VI) оксид (сірчаний ангідрид, триоксид сірки) SO3 — вищий оксид сірки. У звичайних умовах легколетка
- 4. При взаємодії з водою утворює сульфатну кислоту: SO3 + H2O → H2SO4. Взаємодіє з розчинними основами,
- 5. Історична довідка Сірчану кислоту отримують вже більше 1000 років. Спочатку її отримували алхіміки з «зеленого каменю»
- 6. Перша згадка про кислі гази, що отримуються при прожарюванні квасців або залізного купоросу «зеленого каменя», зустрічається
- 7. Але перші детальні описи добування сірчаної кислоти («Купорового масла») дали італійський вчений В.Берінгучо та німецький алхімік
- 8. Сульфатна кислота являє собою безбарвну маслянисту рідину, що перетворюється при 10, 4 ° С в тверду
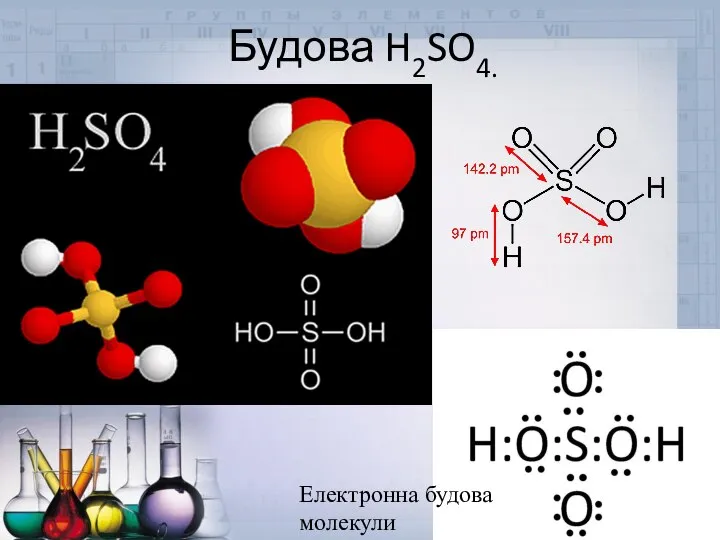
- 9. Будова H2SO4. Електронна будова молекули
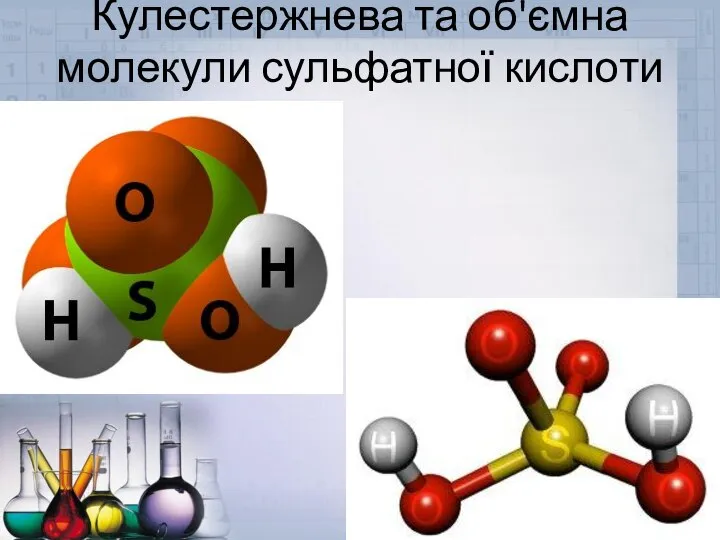
- 10. Кулестержнева та об'ємна молекули сульфатної кислоти
- 11. Одержання сульфатної кислоти. Найбільше значення має контактний спосіб одержання сульфатної кислоти. Процес складається з трьох стадій.
- 12. Фізичні властивості. За звичайних умов чиста сульфатна кислота — безбарвна оліїста рідина без запаху, ρ =
- 13. При розчиненні сірчаної кислоти у воді виділяється велика кількість тепла (19 ккал на моль кислоти) унаслідок
- 15. Здатністю поглинати воду пояснюється і обвуглювання багатьох органічних речовин, вуглеводів (целюлоза, цукор і ін.). Сірчана кислота
- 16. При попаданні сірчаної кислоти на шкіру її необхідно швидко змити сильним струменем води та обробити 5%-им
- 17. Хімічні властивості H2SO4 Дисоціація у водному розчині. Змінює колір індикатора Н2SO4 ↔ Н+ + НSO4- НSO4-
- 18. Продукти взаємодії концентрованої сульфатної кислоти з металами
- 20. Сульфатна кислота при взаємодії з оксидом міді утворює сульфат міді з характерним блакитним забарвленням H2SO4 +
- 21. Основною умовою проходження реакцій з солями є утворення осаду або газу. Якісною реакцією на сульфат-іон є
- 22. Спорідненість сірчаної кислоти до води настільки велика,що вона може служити дегідратуючим агентом; під дією концентрованої сірчаної
- 23. Сульфатну кислоту застосовують: у виробництві мінеральних добрив; як електроліт в свинцевих акумуляторах; для добування різних мінеральних
- 24. На 1 т фосфорних добрив витрачається 2,2-3,4 т сірчаної кислоти, а на 1 т амонійних —
- 25. Охорона праці та навколишнього середовища у виробництві сульфатної кислоти. У виробництві сульфатної кислоти можуть бути втрати
- 27. Найдрібніші крапельки сірчаної кислоти можуть утворюватися в середніх і верхніх шарах атмосфери в результаті реакції водяної
- 28. Восьме чудо світу - так називають індонезійці озера на острові Флорес. Для того що б побачити
- 29. Озеро смерті, що знаходиться на острові Сицілія, — саме "мертве" на Землі. Береги озера позбавлені рослинності,
- 30. Найбільшим родовищем сульфату натрію є затока Кара-Богаз-гол. Вона розташований на східному березі Каспійського моря.
- 31. Сульфати Солі сульфатної кислоти називаються сульфати
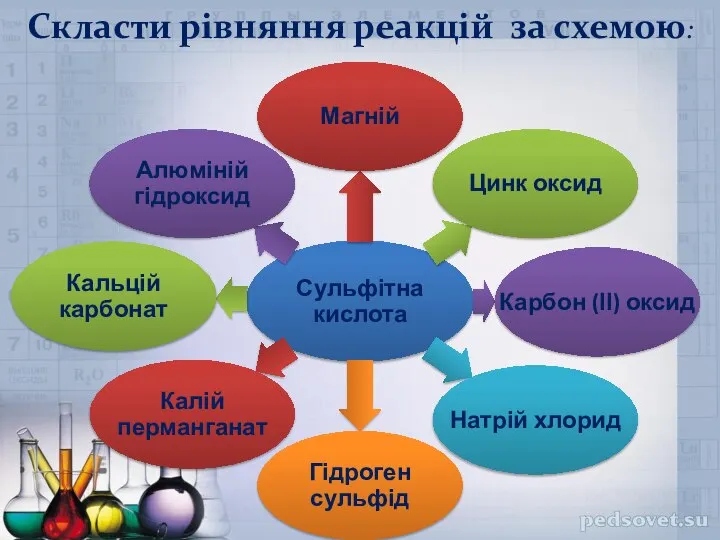
- 33. Скласти рівняння реакцій за схемою:
- 36. Скачать презентацию




























 Физико-химия поверхностных явлений в функционировании живых систем
Физико-химия поверхностных явлений в функционировании живых систем Моделирование процесса приготовления раствора уксусной кислоты различной концентрации
Моделирование процесса приготовления раствора уксусной кислоты различной концентрации Оксигенвмісні органічні сполуки. Лекція 12
Оксигенвмісні органічні сполуки. Лекція 12 Термодинамика. Химическое равновесие. Кинетика
Термодинамика. Химическое равновесие. Кинетика Уральские самоцветы
Уральские самоцветы Презентация по Химии "Миючі засоби в побуті. Мило. Првальні порошки" - скачать смотреть бесплатно
Презентация по Химии "Миючі засоби в побуті. Мило. Првальні порошки" - скачать смотреть бесплатно Электрохимия. Электропроводность растворов. Электродные потенциалы. Гальванические элементы
Электрохимия. Электропроводность растворов. Электродные потенциалы. Гальванические элементы Ферменты как биологические катализаторы
Ферменты как биологические катализаторы принцип работы, применение в технике и быту
принцип работы, применение в технике и быту Ископаемое топливо
Ископаемое топливо 9 класс (обязательный минимум по химии) ПОЛИМЕРЫ
9 класс (обязательный минимум по химии) ПОЛИМЕРЫ  Химическая кинетика. Молекулярность и порядок реакции. Факторы, влияющие на скорость. (Лекция 06)
Химическая кинетика. Молекулярность и порядок реакции. Факторы, влияющие на скорость. (Лекция 06) Степень окисления. Бинарные соединения металлов и не металлов: оксиды, хлориды, сульфиды и др.
Степень окисления. Бинарные соединения металлов и не металлов: оксиды, хлориды, сульфиды и др.  Окислительно-восстановительные реакции (ОВР). Часть 2
Окислительно-восстановительные реакции (ОВР). Часть 2 Презентация Сульфатредуцирующие бактерии
Презентация Сульфатредуцирующие бактерии Презентация по Химии "Окислительно - восстановленные реакции" - скачать смотреть
Презентация по Химии "Окислительно - восстановленные реакции" - скачать смотреть  Презентация по Химии "Презентация Дисперсия света" - скачать смотреть
Презентация по Химии "Презентация Дисперсия света" - скачать смотреть  Перекисное окисление липидов. Характеристика, продукты, биологическая и патофизиологическая роль
Перекисное окисление липидов. Характеристика, продукты, биологическая и патофизиологическая роль Пищевые кислоты
Пищевые кислоты Комплексные соединения.
Комплексные соединения. Lektsia_1_Osnovnye_ponyatia_i_zakony_khimii
Lektsia_1_Osnovnye_ponyatia_i_zakony_khimii ОДНОАТОМНЫЕ СПИРТЫ !! МОУ СПИРТЫ Учитель химии Галимова Э.И.
ОДНОАТОМНЫЕ СПИРТЫ !! МОУ СПИРТЫ Учитель химии Галимова Э.И. Ферменты в пищевой промышленности
Ферменты в пищевой промышленности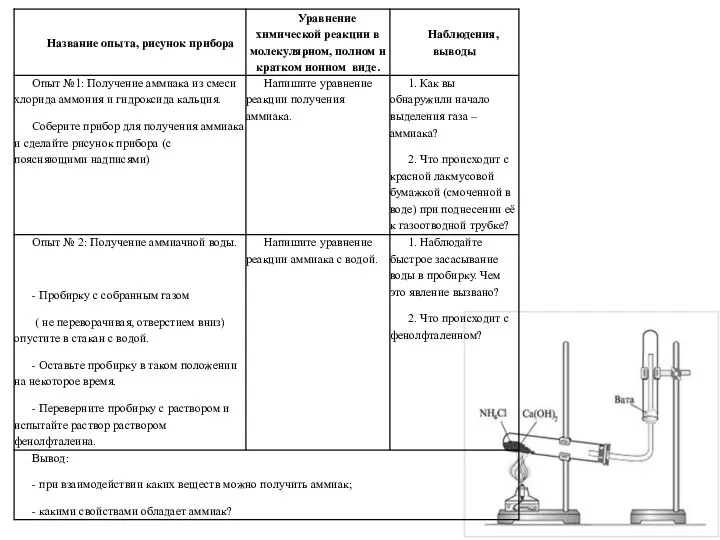 Получение аммиака и изучение его свойств
Получение аммиака и изучение его свойств Беттік активті заттарды өндіру
Беттік активті заттарды өндіру Химическое сопротивление пластмасс
Химическое сопротивление пластмасс Классификация химических реакций по тепловому эффекту
Классификация химических реакций по тепловому эффекту Xимия. Cr, Cu, Fe, Zn
Xимия. Cr, Cu, Fe, Zn