Содержание
- 2. Координационная теория А.Вернера В 1893 г. швейцарским химиком-неоргаником Альфредом Вернером (1866–1919) была сформулирована теория, позволившая понять
- 3. Состав. Согласно теории Вернера центральное положение в комплексных соединениях занимает, как правило, ион металла, который называют
- 4. Комплексообразователь – частица (атом, ион или молекула), координирующая (располагающая) вокруг себя другие ионы или молекулы.
- 5. Комплексообразователь обычно имеет положительный заряд, является d-элементом, проявляет амфотерные свойства, имеет координационное число 4 или 6.
- 6. Лиганды – частицы (молекулы и ионы), координируемые комплексообразователем и имеющие с ним непосредственно химические связи (например,
- 7. Лиганды не связаны друг с другом, так как между ними действуют силы отталкивания. Когда лигандами являются
- 9. Классификация Большое многообразие комплексных соединений и их свойств не позволяет создать единую классификацию. Однако можно группировать
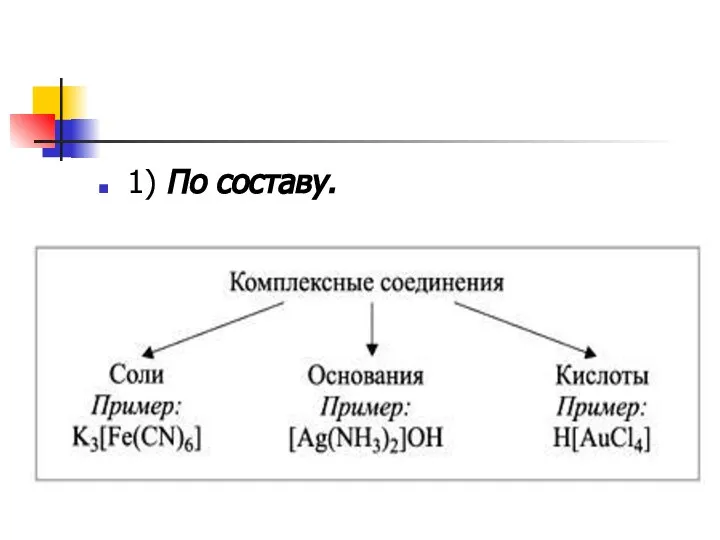
- 10. 1) По составу.
- 11. 2) По типу координируемых лигандов. а) Аквакомплексы – это комплексные катионы, в которых лигандами являются молекулы
- 12. б)Гидроксокомплексы – это комплексные анионы, в которых лигандами являются гидроксид-ионы OH–. Комплексообразователями являются металлы, склонные к
- 13. г) Ацидокомплексы – это комплексные анионы, в которых лигандами являются анионы неорганических и органических кислот. Например:
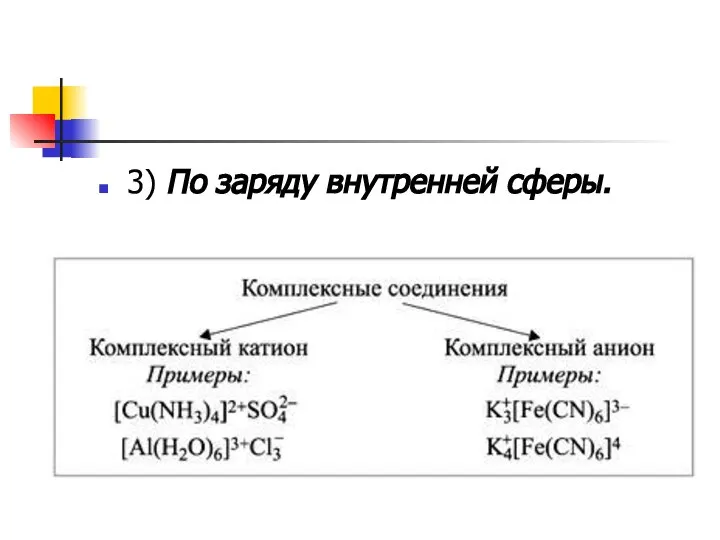
- 14. 3) По заряду внутренней сферы.
- 15. Номенклатура комплексных соединений Наибольшее распространение имеет номенклатура, рекомендованная IUPAC. Название комплексного аниона начинается с обозначения состава
- 16. Если у комплексообразователя переменная степень окисления, то в скобках римскими цифрами указывают его степень окисления, а
- 17. Примеры: K3[Fe(CN)6] – гексацианоферрат(III) калия, K4[Fe(CN)6] – гексацианоферрат(II) калия, K2[Zn(OH)4] – тетрагидроксоцинкат калия.
- 18. Например: [Cu(NH3)4]SO4 – сульфат тетраамминмеди(II), [Al(H2O)6]Cl3 – хлорид гексаакваалюминия.
- 19. Химические свойства комплексных соединений 1. В растворе комплексные соединения ведут себя как сильные электролиты, т.е. полностью
- 20. 2. При действии сильных кислот происходит разрушение гидроксокомплексов а) при недостатке кислоты Na3[Al(OH)6] + 3HCl =
- 21. 3. Нагревание (термолиз) всех аммиакатов приводит к их разложению, например: [Cu(NH3)4]SO4 = CuSO4 + 4NH3 .
- 22. Значение комплексных соединений Координационные соединения имеют исключительно большое значение в природе. Достаточно сказать, что почти все
- 23. Значительную часть природных минералов, в том числе полиметаллических руд и силикатов, также составляют координационные соединения. Более
- 24. Современная химическая отрасль промышленности широко использует координационные соединения как катализаторы при синтезе высокомолекулярных соединений, при химической
- 25. Задания. Письменно дать характеристику следующим комплексным соединениям по строению и классифицировать по признакам: K3[Cr(OH)6], [Cr(H2O)6](NO3)3, Na2[Zn(CN)4],
- 27. Скачать презентацию













![Примеры: K3[Fe(CN)6] – гексацианоферрат(III) калия, K4[Fe(CN)6] – гексацианоферрат(II) калия, K2[Zn(OH)4] – тетрагидроксоцинкат калия.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1196398/slide-16.jpg)
![Например: [Cu(NH3)4]SO4 – сульфат тетраамминмеди(II), [Al(H2O)6]Cl3 – хлорид гексаакваалюминия.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1196398/slide-17.jpg)


![3. Нагревание (термолиз) всех аммиакатов приводит к их разложению, например: [Cu(NH3)4]SO4 = CuSO4 + 4NH3 .](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1196398/slide-20.jpg)




 Iodine. Physical properties. Application of iodine
Iodine. Physical properties. Application of iodine Аттестационная работа. Исследовательская деятельность на уроках химии (8 -9 классы). Исследование речки Беленькой
Аттестационная работа. Исследовательская деятельность на уроках химии (8 -9 классы). Исследование речки Беленькой Презентация по Химии "Химические реакции. Уравнения химических реакций" - скачать смотреть
Презентация по Химии "Химические реакции. Уравнения химических реакций" - скачать смотреть  Алканы и алкены
Алканы и алкены Химические явления. Химические реакции
Химические явления. Химические реакции Химические методы анализа продуктов органического синтеза
Химические методы анализа продуктов органического синтеза Аттестационная работа. Программа элективного курса химия и военное дело. (8-9 класс)
Аттестационная работа. Программа элективного курса химия и военное дело. (8-9 класс) Электролиз.
Электролиз.  Общая характеристика элементов IVA-группы. Углерод и кремний
Общая характеристика элементов IVA-группы. Углерод и кремний Презентация по Химии "АЛЬТЕРНАТИВНЫЕ ИСТОЧНИКИ ЭЛЕКТРОЭНЕРГИИ" - скачать смотреть бесплатно
Презентация по Химии "АЛЬТЕРНАТИВНЫЕ ИСТОЧНИКИ ЭЛЕКТРОЭНЕРГИИ" - скачать смотреть бесплатно Laboratorní sklo a nářadí
Laboratorní sklo a nářadí Стани води
Стани води Фосфор
Фосфор Неорганические вещества в структуре питания
Неорганические вещества в структуре питания Оксид серы(IV). Сернистая кислота. Учитель химии МБОУ «Елховская СОШ» Альметьевского муниципального района Республики Татарстан Г
Оксид серы(IV). Сернистая кислота. Учитель химии МБОУ «Елховская СОШ» Альметьевского муниципального района Республики Татарстан Г Предмет и объекты исследования коллоидной химии. Лекция 01
Предмет и объекты исследования коллоидной химии. Лекция 01 Электролитическая диссоциация
Электролитическая диссоциация Витаминология. История
Витаминология. История Химические элементы. Знаки химических элементов
Химические элементы. Знаки химических элементов Показатель концентрации водородных ионов (лекция 6)
Показатель концентрации водородных ионов (лекция 6) Методы снижения уровня учебного стресса у обучающихся 9-х классов на уроках химии
Методы снижения уровня учебного стресса у обучающихся 9-х классов на уроках химии Оксиды углерода (II) и (IV). Качественная реакция на углекислый газ.
Оксиды углерода (II) и (IV). Качественная реакция на углекислый газ. Лекарственные средства, влияющие на афферентную иннервацию
Лекарственные средства, влияющие на афферентную иннервацию Медь и сплавы
Медь и сплавы Тіндер-тірі организмнің иерархиялық деңгейінің ұйымдастырудың бір түрі. Олардың құрылымдық принциптері
Тіндер-тірі организмнің иерархиялық деңгейінің ұйымдастырудың бір түрі. Олардың құрылымдық принциптері Хлор. Способы получения хлора
Хлор. Способы получения хлора Физическая и коллоидная химия
Физическая и коллоидная химия Скорость химической реакции
Скорость химической реакции