Содержание
- 2. Актуализация знаний Оксиды — это простые или сложные вещества? Свой ответ объясните. Дайте определение оксидов. В
- 4. Знакомы с детства мы с водою, Она есть всюду на Земле - И в облаках над
- 5. Актуализация знаний Оксиды — это простые или сложные вещества? Свой ответ объясните. Дайте определение оксидов. В
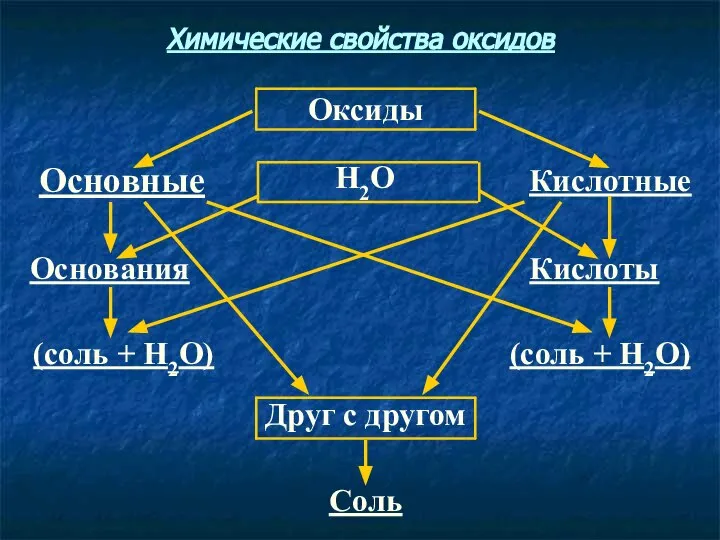
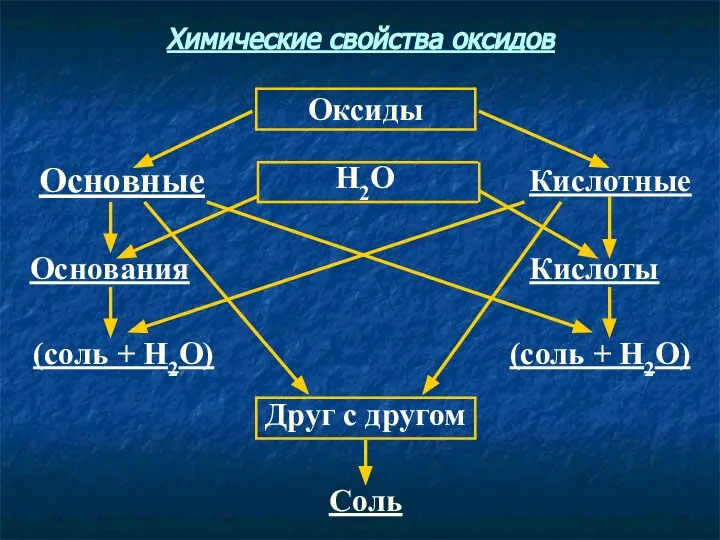
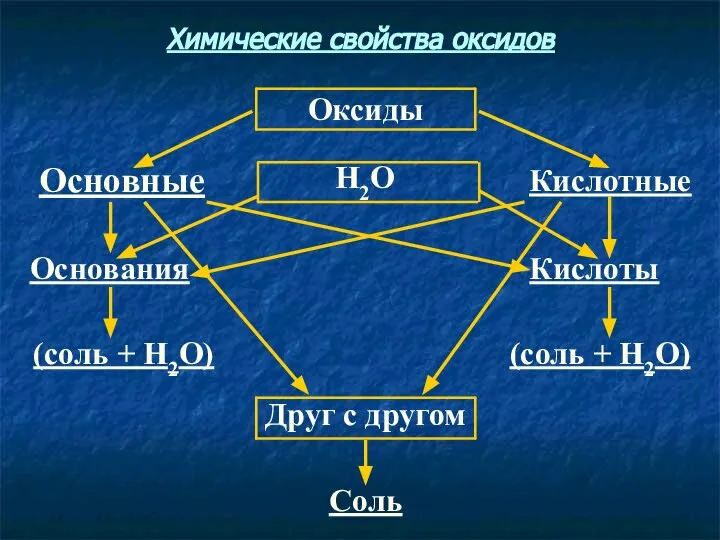
- 6. Соль Друг с другом (соль + Н2О) (соль + Н2О) Кислоты Основания Кислотные Н2О Основные Оксиды
- 7. Найдите лишнее
- 8. Соль Друг с другом (соль + Н2О) (соль + Н2О) Кислоты Основания Кислотные Н2О Основные Оксиды
- 10. Соль Друг с другом (соль + Н2О) (соль + Н2О) Кислоты Основания Кислотные Н2О Основные Оксиды
- 11. Запомните! Каждому кислотному оксиду соответствует определенная кислота. Например: СО2 → Н2СО3 SО2 → H2SО3 SО3 →
- 12. Запомните! Каждому основному оксиду соответствует определенное основание. Например: Na2O → NaOH CaO → Ca(OH)2 Al2O3 →
- 13. СаО + Н2O → Ca(OH)2 (Осн. оксид + вода = основание) СаО + H2SO4 → CaSO4
- 14. Самостоятельная работа Напишите уравнения реакций химических свойств следующих оксидов:
- 15. Домашнее задание: Выучить схему. Составить уравнения реакций химических свойств следующих оксидов: N2O5 и Al2O3.
- 16. Узнай "загадочный "оксид
- 17. Чтоб появиться я сумел, Прокаливают белый мел. Меня дает огонь в печи И пламя маленькой свечи.
- 18. Применение оксидов В литосфере содержится оксид кремния - песок, оксид алюминия - глина. Они незаменимы в
- 19. Применение оксидов Оксид кальция необходим для получения гашеной извести, которая используется для побелки. Драгоценные камни
- 21. Скачать презентацию















 Лаборатория мирового уровня в области термического анализа и физико-химии процессов тепловых методов добычи
Лаборатория мирового уровня в области термического анализа и физико-химии процессов тепловых методов добычи Темір және оның маңызды қосылыстары
Темір және оның маңызды қосылыстары Биосинтез белка
Биосинтез белка Геолого-промышленные типы месторождений полезных ископаемых
Геолого-промышленные типы месторождений полезных ископаемых Своя игра «Знаешь ли ты химические элементы?»
Своя игра «Знаешь ли ты химические элементы?» Поверхностное натяжение
Поверхностное натяжение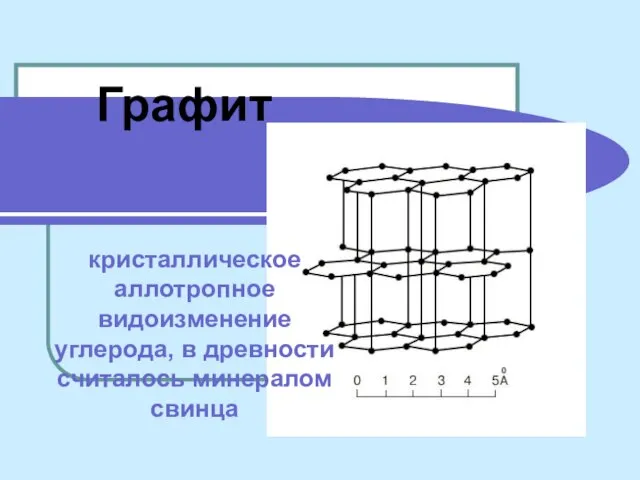 Графит кристаллическое аллотропное видоизменение углерода, в древности считалось минералом свинца
Графит кристаллическое аллотропное видоизменение углерода, в древности считалось минералом свинца Норми радіаційної безпеки (НРБУ-97)
Норми радіаційної безпеки (НРБУ-97) Основания. Гидроксид лития
Основания. Гидроксид лития Тема урока: «Генетическая связь между классами неорганических соединений » ГОУ СОШ №149 Учитель химии: Иванова Г.М.
Тема урока: «Генетическая связь между классами неорганических соединений » ГОУ СОШ №149 Учитель химии: Иванова Г.М. Нефть. Лекция 5
Нефть. Лекция 5 Оксиды. Классы неорганических соединений
Оксиды. Классы неорганических соединений Тема урока Железо Цель урока: Рассмотреть электронное строение атома железа, дать общую характеристику его. Изучить основные
Тема урока Железо Цель урока: Рассмотреть электронное строение атома железа, дать общую характеристику его. Изучить основные  Отношение масс элементов в веществе. Массовые доли элементов в веществе
Отношение масс элементов в веществе. Массовые доли элементов в веществе Тема урока: Состав, переработка нефти и экологические проблемы связанные с ней.
Тема урока: Состав, переработка нефти и экологические проблемы связанные с ней. Тканые армирующие наполнители
Тканые армирующие наполнители Презентация по химии Строение атома
Презентация по химии Строение атома  Предмет химии
Предмет химии Обмен веществ и энергии, основа существования клетки
Обмен веществ и энергии, основа существования клетки Взаимосвязь обмена веществ
Взаимосвязь обмена веществ Общая химия. Химическая термодинамика. Первый закон термодинамики. Термохимия
Общая химия. Химическая термодинамика. Первый закон термодинамики. Термохимия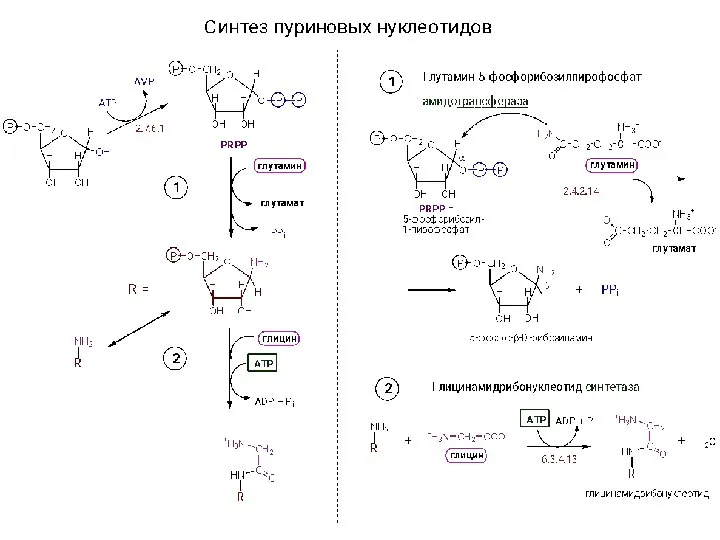 Синтез нуклеотидов
Синтез нуклеотидов Классификация и номенклатура органических соединений. (Лекция 1)
Классификация и номенклатура органических соединений. (Лекция 1) Сполуки неметалічних елементів з гідрогеном. Амоніак та хлороводень
Сполуки неметалічних елементів з гідрогеном. Амоніак та хлороводень Технологические методы производства деталей машин из ПКМ, содержащих дисперсные наполнители
Технологические методы производства деталей машин из ПКМ, содержащих дисперсные наполнители Металлические сплавы
Металлические сплавы Спирты
Спирты Атомы, молекулы, химические элементы. Формы существования элементов в природе
Атомы, молекулы, химические элементы. Формы существования элементов в природе