Содержание
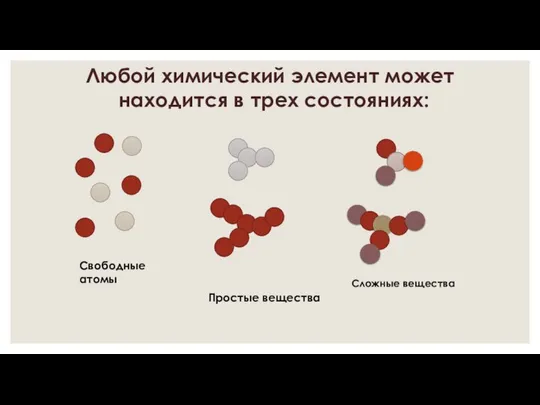
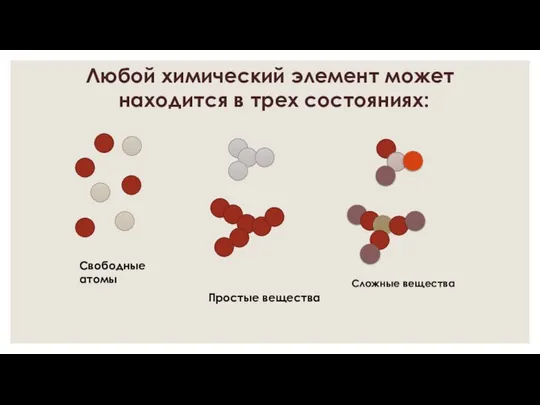
- 2. Любой химический элемент может находится в трех состояниях: Свободные атомы Простые вещества Сложные вещества
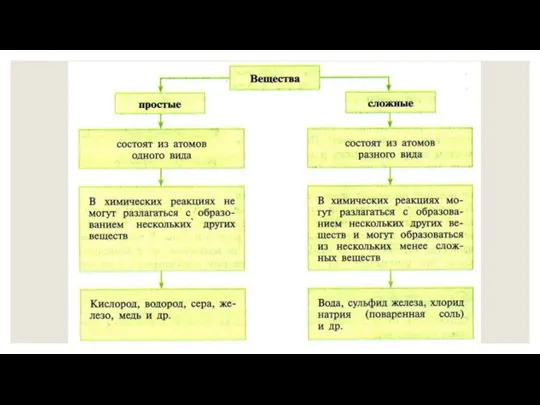
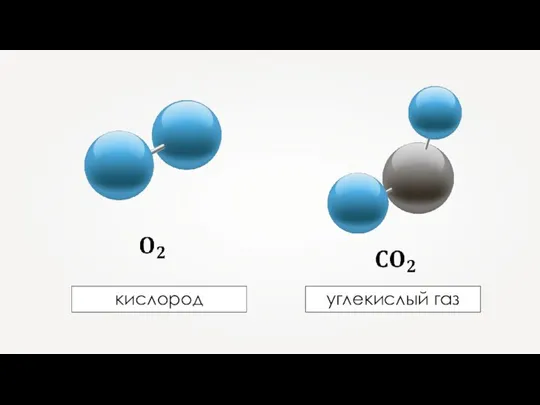
- 3. Вещество – это то, из чего состоят физические тела.
- 6. Потренируемся Задание: распределите объекты по группам: Свободные атомы Атомы, входящие в состав простого вещества Атомы, входящие
- 7. Любой химический элемент может находится в трех состояниях: Свободные атомы Простые вещества Сложные вещества
- 8. Строение атома Атом- это наименьшая, химически неделимая часть химического элемента, являющаяся носителем его свойств
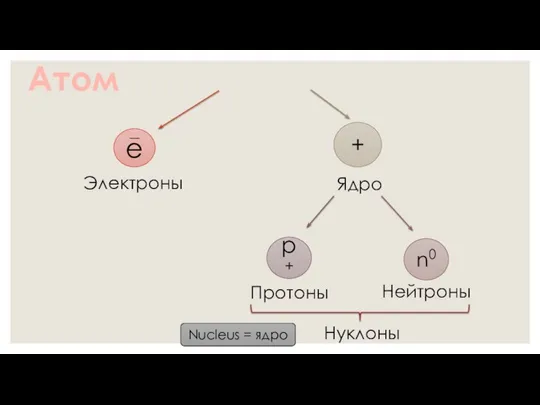
- 9. Атом e Электроны + Ядро p+ n0 Протоны Нейтроны Нуклоны Nucleus = ядро
- 10. Z – протонное число (показывает количество протонов в ядре и их суммарную массу (относительную)) N –
- 11. Be 9 4 - Нуклонное число (равно относительной атомной массе) - Протонное число (равно порядковому номеру
- 12. АТОМНАЯ ЭЛЕКТРОННАЯ ОРБИТАЛЬ Атомная электронная орбиталь – область околоядерного пространства, в которой наиболее вероятно (> 90%)
- 13. Распределение электронов по энергетическим уровням Энергетические уровни= электронные слои Число энергетических уровней в атоме равно номеру
- 14. ЭЛЕКТРОННАЯ СХЕМА Символ элемента Заряд ядра Распределение электронов по слоям (энергетическим уровням) Заряд ядра = порядковый
- 15. ЧИСЛО ЭНЕРГЕТИЧЕСКИХ УРОВНЕЙ = НОМЕРУ ПЕРИОДА Число электронов на слоях неоднородно. 1 уровень – 2 электрона
- 16. Задания
- 17. Задания
- 18. Задания Рассчитайте количество протонов, нейтронов и электронов у следующих атомов: кислород, мышьяк и скандий
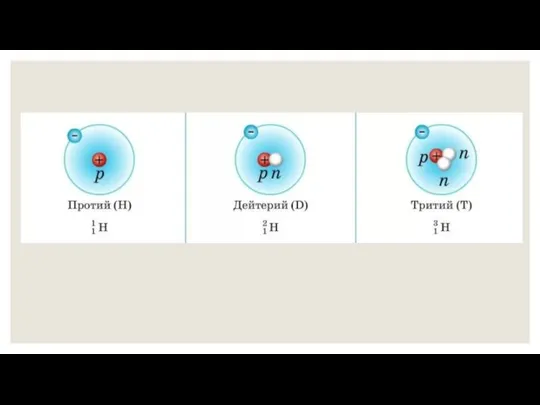
- 20. Изотопы Изотопы- это разновидности атомов одного и того же химического элемента, имеющие одинаковое число протонов, но
- 21. Задания Изобразите схемы строения атомов: натрия, азота, кальция и фосфора
- 22. Задания
- 24. Скачать презентацию















 Історія створення і виробництво мила
Історія створення і виробництво мила  Аттестаионная работа. Сахар. Изучаем и исследуем
Аттестаионная работа. Сахар. Изучаем и исследуем 1. Молекулярная кристаллическая решетка Характеристика У веществ с молекулярным строением в узлах кристаллической решетки
1. Молекулярная кристаллическая решетка Характеристика У веществ с молекулярным строением в узлах кристаллической решетки  Углеводы (сахариды)
Углеводы (сахариды) Окисно-відновні процеси
Окисно-відновні процеси Щелочные металлы IА группы. Литий
Щелочные металлы IА группы. Литий Cинтетичні миючі засоби і їхній вплив на людину
Cинтетичні миючі засоби і їхній вплив на людину  Спирти. Класифікація спиртів
Спирти. Класифікація спиртів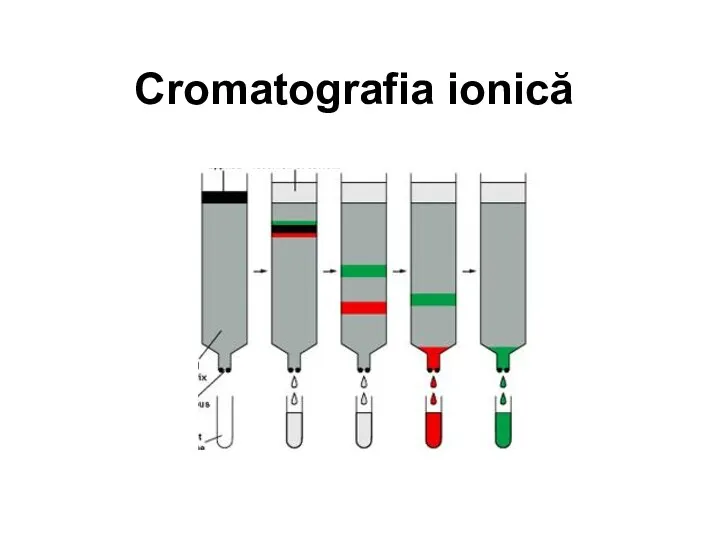 Cromatografia ionică
Cromatografia ionică Лекарственные формы для глаз в условиях аптечного производства
Лекарственные формы для глаз в условиях аптечного производства Сложные реакции
Сложные реакции Эмульсия. Основные типы эмульсий
Эмульсия. Основные типы эмульсий Нефть. Образование нефти
Нефть. Образование нефти Рекомендации по подготовке учащихся к выполнению заданий различного уровня сложности ЕГЭ по химии
Рекомендации по подготовке учащихся к выполнению заданий различного уровня сложности ЕГЭ по химии Аттестационная работа. Образовательная программа элективного курса «Химия вокруг нас»
Аттестационная работа. Образовательная программа элективного курса «Химия вокруг нас» Стеклянные товары. Основные сырьевые материалы для производства стекла
Стеклянные товары. Основные сырьевые материалы для производства стекла Общие свойства металлов
Общие свойства металлов Пространственное строение. Стереоизомерия. Структура и функции биолекул
Пространственное строение. Стереоизомерия. Структура и функции биолекул Метод изолирования Васильевой
Метод изолирования Васильевой Эмульсии и эмульгаторы
Эмульсии и эмульгаторы ТВОРЦІ ХІМІЇ
ТВОРЦІ ХІМІЇ  Окислительное фосфорилирование
Окислительное фосфорилирование Класифікація розчинів. Осмос. Осмотичний тиск
Класифікація розчинів. Осмос. Осмотичний тиск Органічна хімія Виробництво лугів та кислот
Органічна хімія Виробництво лугів та кислот  Қалдық мөлшерлер. Бромды метил буының концентрациясын анықтау тәсілдемесі
Қалдық мөлшерлер. Бромды метил буының концентрациясын анықтау тәсілдемесі Сульфокислоты ароматического ряда и их производные применяемые в медицине и косметологии
Сульфокислоты ароматического ряда и их производные применяемые в медицине и косметологии Динамическая биохимия. Введение в обмен веществ и энергии. (Лекция 7)
Динамическая биохимия. Введение в обмен веществ и энергии. (Лекция 7) Материаловедение как наука
Материаловедение как наука