Содержание
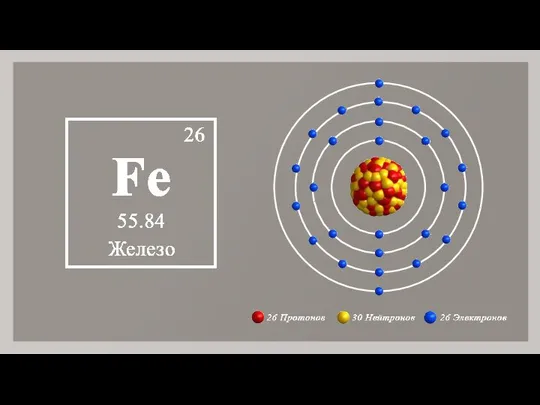
- 2. Ге́нри Гвин Дже́фрис Мо́зли (1887 – 1915 гг) Протоны Электроны Нейтроны
- 3. Порядковый номер элемента Заряд ядра атома Число протонов в ядре Число электронов в атоме = =
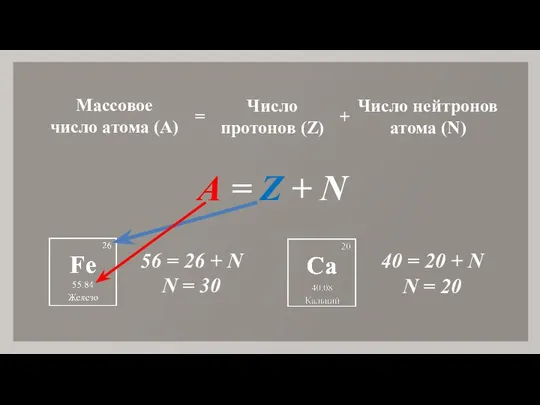
- 6. Массовое число атома (А) Число протонов (Z) = + А = Z + N Число нейтронов
- 7. Атомы одного элемента, которые имеют разные массовые числа, называются изотопами С О 12 6 18 8
- 8. Элемент водород имеет 3 изотопа, каждый имеет свое название: H 1 1 протий 1 протон, 0
- 9. Относительная атомная масса (Ar) – это средняя величина массовых чисел природных изотопов этого элемента w( Сl)
- 11. Скачать презентацию






 Презентация по Химии "Презентація про мене" - скачать смотреть
Презентация по Химии "Презентація про мене" - скачать смотреть  Фосфор
Фосфор Хімія у створенні нових матеріалів та побуті
Хімія у створенні нових матеріалів та побуті ОГЭ, вопрос 16 1-4
ОГЭ, вопрос 16 1-4 Начальные этапы обмена липидов
Начальные этапы обмена липидов Полимеры. Пластмассы. Волокна. Цели: - узнать что такое пластмассы, волокна их отличие от полимеров; - изучить классификацию пл
Полимеры. Пластмассы. Волокна. Цели: - узнать что такое пластмассы, волокна их отличие от полимеров; - изучить классификацию пл Презентация по Химии "«Сахароза»" - скачать смотреть бесплатно
Презентация по Химии "«Сахароза»" - скачать смотреть бесплатно Щавелевая кислота
Щавелевая кислота Хімічний елемент Літій
Хімічний елемент Літій Кислородные соединения азота. Азотная кислота
Кислородные соединения азота. Азотная кислота Предельные одноатомные спирты
Предельные одноатомные спирты Серебра нитрат и другие препараты серебра. Ртути окись желтая
Серебра нитрат и другие препараты серебра. Ртути окись желтая Посвящение в химики!
Посвящение в химики! Гормоны, как лекарственные вещества. Анализ, применение и хранение. (Тема 4)
Гормоны, как лекарственные вещества. Анализ, применение и хранение. (Тема 4) Узинская ООШ исслед.работа Лобановой Елизаветы
Узинская ООШ исслед.работа Лобановой Елизаветы ТБ в школе и в быту
ТБ в школе и в быту Твердые тела и их свойства
Твердые тела и их свойства  Геология и геохимия нефти и газа
Геология и геохимия нефти и газа Азотсодержащие органические соединения
Азотсодержащие органические соединения Lekcii_ - 2017-lech_ped 11
Lekcii_ - 2017-lech_ped 11 Юные химики
Юные химики Курсовая работа. Влияние микроэлементов на физиологические процессы
Курсовая работа. Влияние микроэлементов на физиологические процессы Материаловедение. Текстильные волокна, пряжа и ткань
Материаловедение. Текстильные волокна, пряжа и ткань Electrochemistry. Oxidation-reduction equilibrium in water solutions
Electrochemistry. Oxidation-reduction equilibrium in water solutions Презентация по Химии "Углерод" - скачать смотреть
Презентация по Химии "Углерод" - скачать смотреть  Химически опасные объекты (ХОО)
Химически опасные объекты (ХОО) Теория химического строения А. М. Бутлерова. Часть III
Теория химического строения А. М. Бутлерова. Часть III Платина. Свойства
Платина. Свойства