Химические и физические свойства
Физические свойства: Серная кислота – бесцветная вязкая жидкость, имеющая
температуру плавления 10 °C, температура кипения 296 °C (с разложением на H2O и SO3). Серная кислота – сильная кислота. Концентрированная серная кислота в большом количестве поглощает пары воды, поэтому ее используют для осушения газов.
Химические свойства.
1. Концентрированная серная кислота является сильным окислителем. Окислительно-восстановительные реакции требуют нагревания, а продуктом реакции в основном является SO2.
2. С металлами вступает в реакцию по-разному в зависимости от концентрации. Разбавленная серная кислота взаимодействует со всеми металлами, стоящими в ряду напряжений до водорода. Концентрированная серная кислота окисляет все металлы, стоящие в ряду напряжений, и серебро в том числе.
3. Разбавленная серная кислота взаимодействует с основаниями, основными и амфотерными оксидами, солями.











 Йод. Положение в периодической системе
Йод. Положение в периодической системе Композиты. Полимерные композиционные материалы
Композиты. Полимерные композиционные материалы Углерод. Металлы. 9 класс
Углерод. Металлы. 9 класс Термодинамические возможности получения меди с применением программного комплекса АСТРА-4
Термодинамические возможности получения меди с применением программного комплекса АСТРА-4 Презентация по Химии "мінеральні добрива." - скачать смотреть бесплатно_
Презентация по Химии "мінеральні добрива." - скачать смотреть бесплатно_ Етанол (етиловий спирт, винний спирт)
Етанол (етиловий спирт, винний спирт) Органічні сполуки в побуті Виконав Учень 11-Т класу ЗОШ №1 Новак Сергій
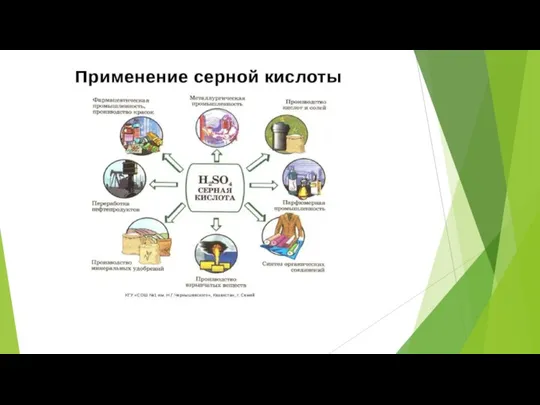
Органічні сполуки в побуті Виконав Учень 11-Т класу ЗОШ №1 Новак Сергій  Производство серной кислоты
Производство серной кислоты Изучение адсорбции аминокислот на поверхности гидроксилапатита при варьировании рН
Изучение адсорбции аминокислот на поверхности гидроксилапатита при варьировании рН Radiation dosimetry
Radiation dosimetry Строение атома
Строение атома Общенаучные методы исследований
Общенаучные методы исследований Закономерности адсорбции ионов и адагуляции коллоидных частиц. Самосборка на поверхности. (Лекция 9)
Закономерности адсорбции ионов и адагуляции коллоидных частиц. Самосборка на поверхности. (Лекция 9) Строение атома. Движение электрона в атоме
Строение атома. Движение электрона в атоме КИСЛОРОД
КИСЛОРОД  Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Робота учениці 11 – А класу Каплун Ірини
Пластмаси, синтетичні каучуки, гума, штучні й синтетичні волокна Робота учениці 11 – А класу Каплун Ірини  Кислотность и основность рганических соединений. Инфракрасная спектроскопия
Кислотность и основность рганических соединений. Инфракрасная спектроскопия Изомерия. Типы изомерии
Изомерия. Типы изомерии Презентация по Химии "Органическая химия" - скачать смотреть бесплатно
Презентация по Химии "Органическая химия" - скачать смотреть бесплатно Алкины. Способы получения
Алкины. Способы получения Уголь. Виды угля
Уголь. Виды угля Щелочные металлы
Щелочные металлы Обмен липидов
Обмен липидов Композиционные материалы – материалы будущего
Композиционные материалы – материалы будущего Методы экстрагирования ЛРС и оборудование
Методы экстрагирования ЛРС и оборудование Alkanes. A “family” of hydrocarbons
Alkanes. A “family” of hydrocarbons Презентация тест по химии
Презентация тест по химии Презентация по Химии "Медь." - скачать смотреть бесплатно
Презентация по Химии "Медь." - скачать смотреть бесплатно