Содержание
- 2. C-ацилирование аренов по Фриделю-Крафтсу (синтез ароматических кетонов) Ацилирующие агенты: в основном, карбоновые кислоты, их ангидриды и
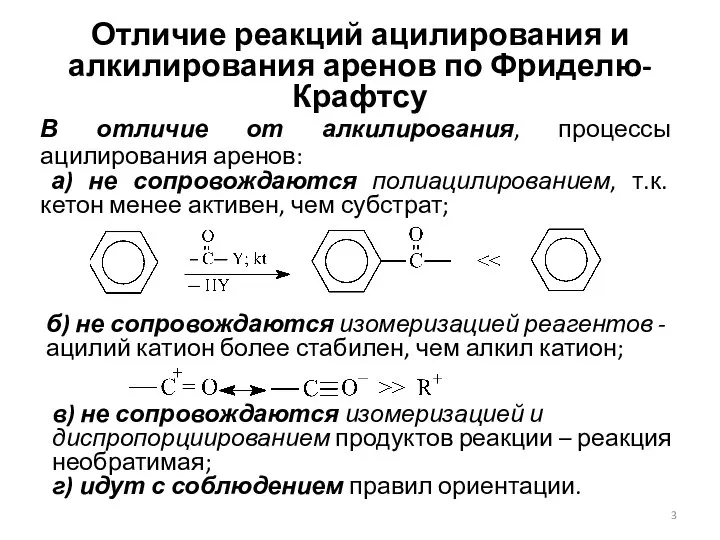
- 3. Отличие реакций ацилирования и алкилирования аренов по Фриделю-Крафтсу В отличие от алкилирования, процессы ацилирования аренов: а)
- 4. Механизм образования электрофильных частиц В результате взаимодействия ацилирующих агентов с катализатором образуются электрофильные частицы: - во-первых,
- 5. Количество кислоты Льюиса должно быть не менее 1 моль на моль субстрата, так как катализатор взаимодействует
- 6. С-ацилирование аренов хлорангидридами кислот Хлорангидриды кислот — самые активные ацилирующие агенты, но малодоступные, нестабильные, дорогие (легко
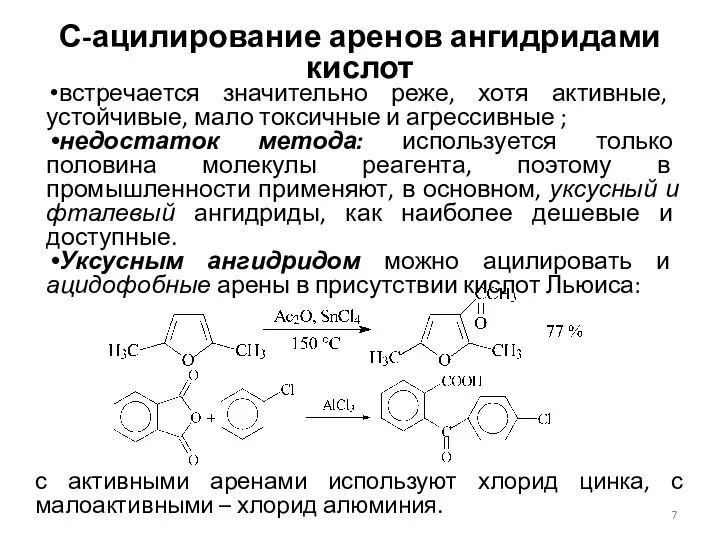
- 7. С-ацилирование аренов ангидридами кислот встречается значительно реже, хотя активные, устойчивые, мало токсичные и агрессивные ; недостаток
- 8. С-ацилирование карбоновыми кислотами встречается редко из-за малой активности реагента, который наиболее доступен, стабилен, дешев, наименее токсичный
- 9. Ацилирование аренов по Гаттерману-Коху (синтез альдегидов) Хлорангидрид муравьиной кислоты нестабильное соединение и в реакциях Фриделя-Крафтса не
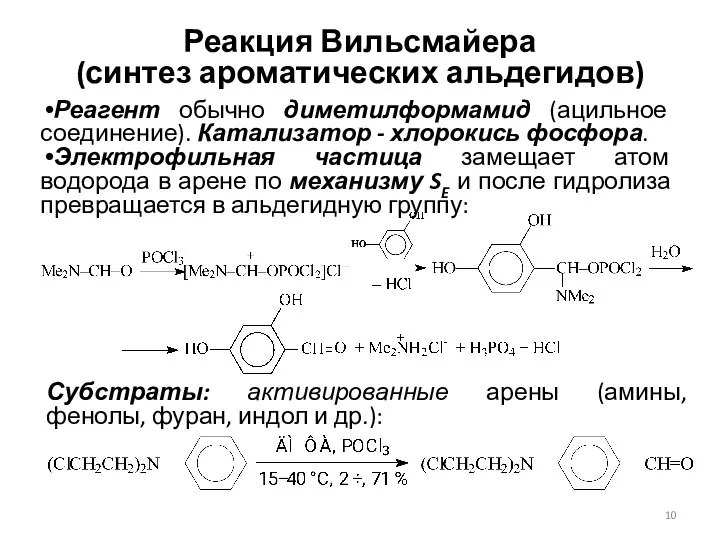
- 10. Реакция Вильсмайера (синтез ароматических альдегидов) Реагент обычно диметилформамид (ацильное соединение). Катализатор - хлорокись фосфора. Электрофильная частица
- 11. Реакция Реймера-Тимана (синтез ароматических гидроксиальдегидов) Субстратом являются фенолы с заместителями первого рода, нафтолы и другие активные
- 12. Реакция Кольбе-Шмидта (синтез ароматических гидроксикислот) Субстратом являются фенолы и аминофенолы. Ацилирующий агент – ангидрид угольной кислоты.
- 13. N-ацилирование (синтез амидов кислот) применяется как для получения нового соединения, так и для защиты аминогруппы; ацилирующие
- 14. Реакционная способность ацильных соединений Определяется величиной положительного заряда на атоме углерода карбонильной группы и способностью уходящей
- 15. Влияние уходящей группы на δ+ ацильной группы В ацильных соединениях одной и той же кислоты, величина
- 16. Способность группы Y уходить чем более сильным основанием является Y , тем хуже уходит. При определении
- 17. Хлорангидриды карбоновых кислот (+) самые активные ацилирующие агенты; реакции необратимые; реагенты можно брать в стехиометрических соотношениях.
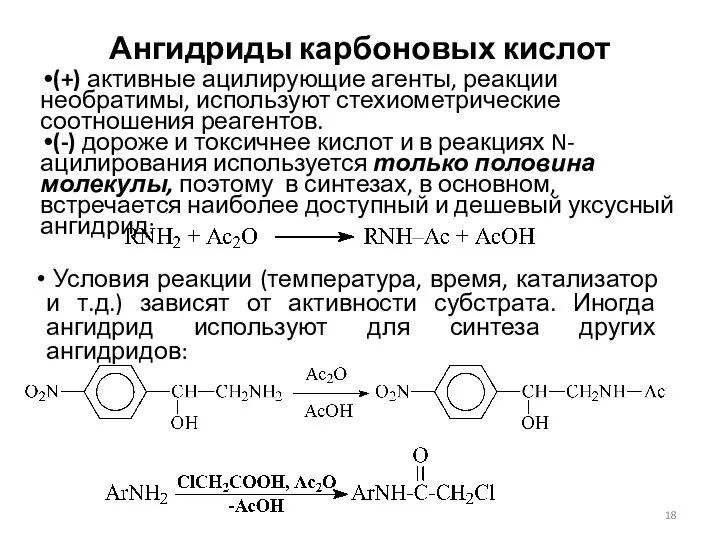
- 18. Ангидриды карбоновых кислот (+) активные ацилирующие агенты, реакции необратимы, используют стехиометрические соотношения реагентов. (-) дороже и
- 19. Карбоновые кислоты (+) наиболее дешевые и доступные; (-) значительно менее активные реагенты, чем их ангидриды, образуют
- 20. Формилирование и ацетилирование аминов проводят в избытке кислоты (с муравьиной кислотой при 150 °С, с уксусной
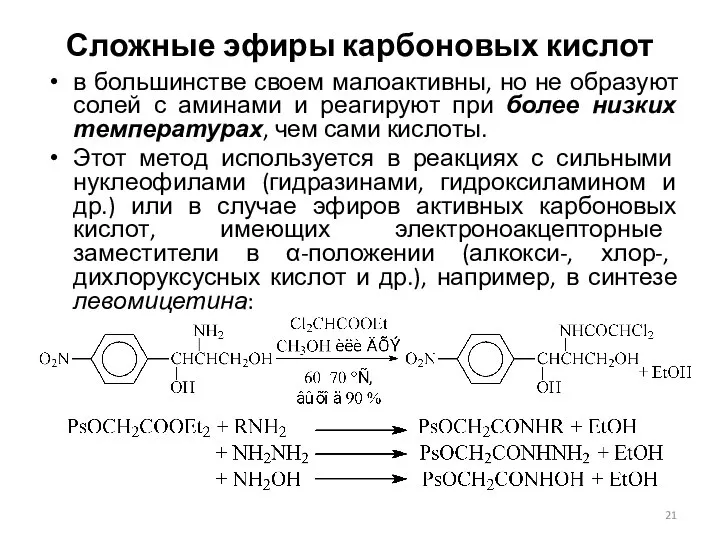
- 21. Сложные эфиры карбоновых кислот в большинстве своем малоактивны, но не образуют солей с аминами и реагируют
- 22. N-ацилирование амидами карбоновых кислот применяют очень редко из-за малой активности реагента. Тем не менее, известны реакции,
- 23. О-Ацилирование (синтез сложных эфиров) проводится реже, чем аминогрупп и идет менее энергично. Механизмы О- и N-ацилирования,
- 24. О-Ацилирование хлорангидридами кислот Для связывания выделяющегося хлористого водорода применяют основания или ведут реакцию в таких условиях
- 25. О-Ацилирование ангидридами кислот используется только половина молекулы, поэтому в промышленности применяют, в основном, уксусный и фталевый
- 26. О-Ацилирование карбоновыми кислотами наиболее дешевый и доступный реагент но значительно менее активный, чем ангидриды, не взаимодействует
- 27. Механизм реакции этерификации SNAE Схема включает: активацию СООН, AN, создания хорошо уходящей группы и E уходящей
- 29. Скачать презентацию





















 Презентация по Химии "Ярмарок професій" - скачать смотреть
Презентация по Химии "Ярмарок професій" - скачать смотреть  Требования, предъявляемые к дизельным топливам
Требования, предъявляемые к дизельным топливам Работу выполнила ученица 9 А класса ГОУ СОШ №546 г. Москвы Коломиец Екатерина Руководитель: учитель химии ГОУ СОШ №546 Симонова Т
Работу выполнила ученица 9 А класса ГОУ СОШ №546 г. Москвы Коломиец Екатерина Руководитель: учитель химии ГОУ СОШ №546 Симонова Т Тесты для самопроверки
Тесты для самопроверки Позднемеловая трубка взрыва щелочных базальтов Красноозерная
Позднемеловая трубка взрыва щелочных базальтов Красноозерная Растворы. Первичные понятия
Растворы. Первичные понятия Как сделать духи для любимой мамочки? Выполнил: Причина Алексей Учащийся 3 класса Б МОУ СОШ № 64
Как сделать духи для любимой мамочки? Выполнил: Причина Алексей Учащийся 3 класса Б МОУ СОШ № 64 Acizi, baze, oxizi, săruri. Caracteristica generală, proprietă ți fizice și chimice
Acizi, baze, oxizi, săruri. Caracteristica generală, proprietă ți fizice și chimice Карбоновые кислоты Учитель химии МОУ лицея № 6 Дробот Светлана Сергеевна
Карбоновые кислоты Учитель химии МОУ лицея № 6 Дробот Светлана Сергеевна  Тест по теме: «Алканы» Автор: учитель химии МОУСОШ № 6 Ким Н. В.
Тест по теме: «Алканы» Автор: учитель химии МОУСОШ № 6 Ким Н. В. Выполнила: Ученица 11 «Б» класса Урывкова Анастасия Кон
Выполнила: Ученица 11 «Б» класса Урывкова Анастасия Кон Отдельные классы дисперсных систем
Отдельные классы дисперсных систем Воздушные и тепловые свойства почв
Воздушные и тепловые свойства почв Нуклеофильное замещение галогена и других функциональных групп
Нуклеофильное замещение галогена и других функциональных групп Своя игра по химии
Своя игра по химии Алкены
Алкены Курс биохимии. Биохимия крови
Курс биохимии. Биохимия крови Открытие периодического закона Д.И. Менделеева
Открытие периодического закона Д.И. Менделеева Органическая химия 10 класс А.А.Карцовой и А.Н.Лёвкина
Органическая химия 10 класс А.А.Карцовой и А.Н.Лёвкина Применение циклической вольтамперометрии для определения истинной Sпов платины и оценки стабильности
Применение циклической вольтамперометрии для определения истинной Sпов платины и оценки стабильности Коррозия металлов
Коррозия металлов Агрохимия для восьмиклассников. Учебно-исследовательский проект учащейся 8 «В» класса МОУЛ «ВУВК им. А. П. Киселёва» Желтовой Анн
Агрохимия для восьмиклассников. Учебно-исследовательский проект учащейся 8 «В» класса МОУЛ «ВУВК им. А. П. Киселёва» Желтовой Анн Особенности строения, реакционной способности и методы синтеза аренов
Особенности строения, реакционной способности и методы синтеза аренов Презентация по Химии "Классификация углеводородов" - скачать смотреть
Презентация по Химии "Классификация углеводородов" - скачать смотреть  Силикаты. Пироксены. Амфиболы. Полевые шпаты
Силикаты. Пироксены. Амфиболы. Полевые шпаты Мыс айналымы
Мыс айналымы Хроматографический анализ
Хроматографический анализ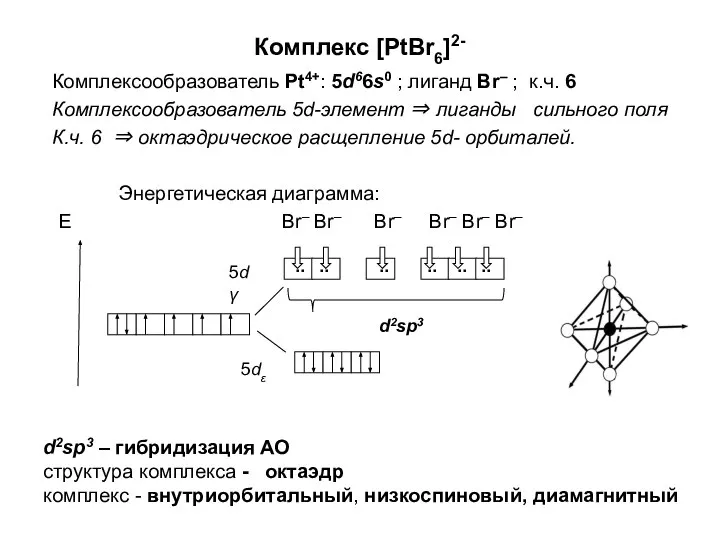 Комплексообразователь. (Лекция 5)
Комплексообразователь. (Лекция 5)