Содержание
- 2. Теория электролитической диссоциации Аррениуса пригодна лишь для водных растворов, в неводных растворителях она несостоятельна. Например, NH4Cl,
- 3. Протолитическая теория кислот и оснований (Теория Бренстеда-Лоури) Основные положения: 1. Кислота – молекула или ион, отдающие
- 4. 2. Кислоты и основания существуют только как сопряженные пары. Их свойства обусловлены процессом протолиза - обмена
- 5. Амфолитами являются: гидроксиды (Zn, Al, Pb, Sn, Cr); гидроанионы многоосновных кислот (НСО3- , НРО42- , Н2РО4-
- 6. Жидкие протонсодержащие растворители вступают в обратимую реакцию автопротолиза. Например, для воды: 2Н2О = Н3О+ + ОН-
- 7. Водородный показатель (рН) Гидроксильный показатель (рОН) Логарифмируя уравнение КW =[Н+][ОН-]=10-14, получаем: Шкала кислотности воды составляет 14
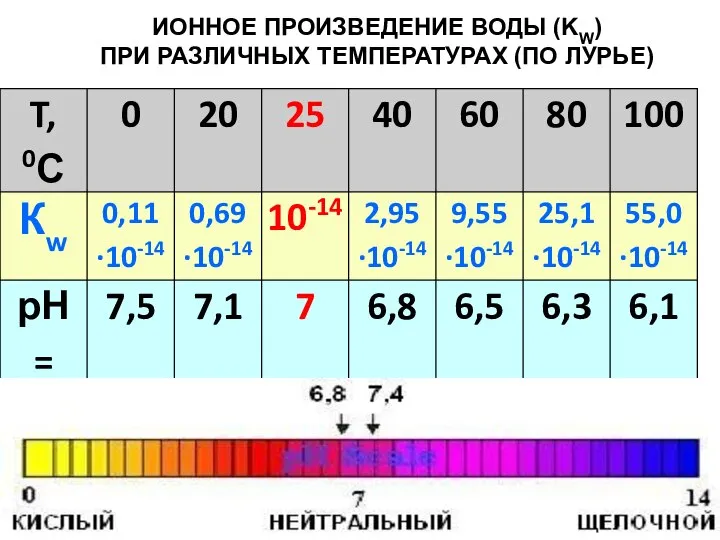
- 8. ИОННОЕ ПРОИЗВЕДЕНИЕ ВОДЫ (KW) ПРИ РАЗЛИЧНЫХ ТЕМПЕРАТУРАХ (ПО ЛУРЬЕ)
- 9. Расчет рН кислот и оснований Кислоты сильные слабые или Основания сильные слабые или Подробно с расчетом
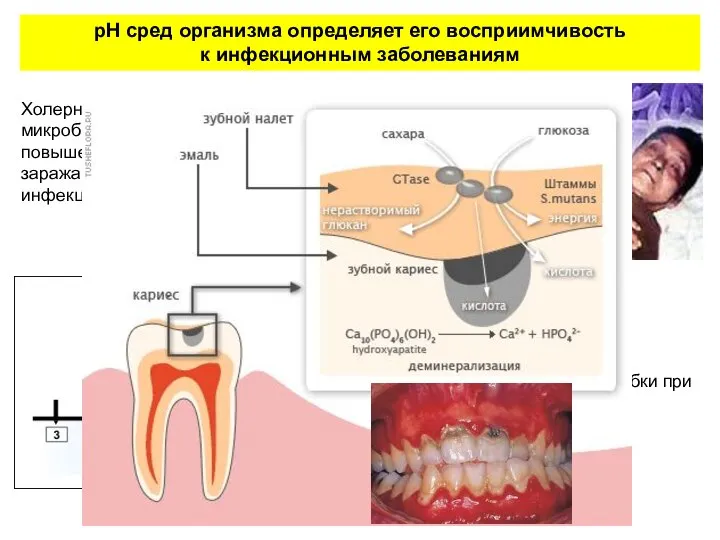
- 11. рН сред организма определяет его восприимчивость к инфекционным заболеваниям
- 12. Растворы, способные сохранять значение рН при разбавлении или добавлении небольших количеств кислоты или щелочи. Классификация БС
- 13. Механизм поддержания рН Рассмотрим ацетатный буферный раствор: СН3СООН ↔ СН3СОО- + Н+; СН3СООNa → СН3СОО- +
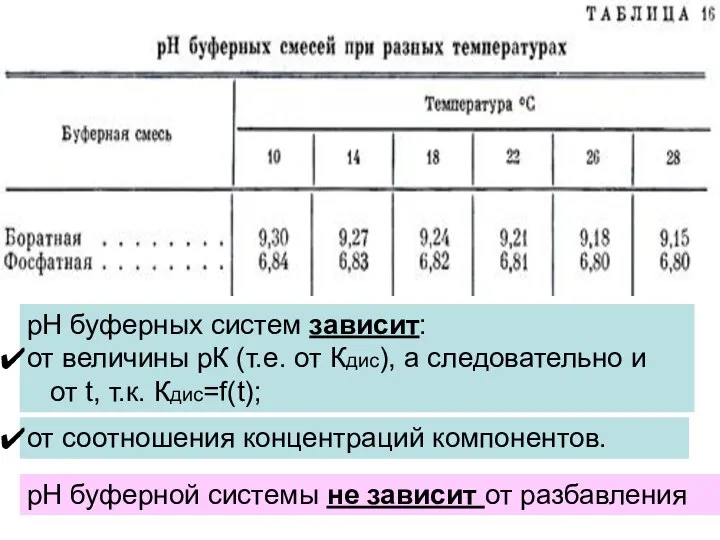
- 14. рН буферных растворов рассчитывается по формулам Гендерсона – Гассельбаха: Для кислого буфера: Для основного буфера: рН
- 15. Буферная емкость Буферная ёмкость (В) – количество моль эквивалентов сильной кислоты или щелочи, добавление которой к
- 16. Буферная ёмкость зависит от: природы добавляемых веществ и компонентов буферного раствора. исходной концентрации компонентов буферной системы.
- 17. Максимальная буферная емкость, т.е. наибольшая способность этой системы противостоять изменению рН, соответствует значению рН = рК.
- 18. Буферные системы крови рН плазмы крови 7,40 ± 0,05 Норма Механизм действия разбирается на лабораторном занятии
- 19. Кислотно-основное состояние организма (КОС) Показатели КОС (метод микро – Аструп) Ва - буферная емкость по кислоте:
- 20. SB — стандартный бикарбонат, содержание НСОз- в крови — в норме 24,4±3 ммоль/л BE — избыток
- 21. АЦИДОЗ уменьшение буферной Ва МЕТАБОЛИЧЕСКИЙ РЕСПИРАТОРНЫЙ НАКОПЛЕНИЕ НЕЛЕТУЧИХ КИСЛОТ с(НСО3-) р(СО2) ВЕ Причины: кислородное голодание тканей;
- 22. АЦИДОЗ уменьшение буферной Ва МЕТАБОЛИЧЕСКИЙ РЕСПИРАТОРНЫЙ НАКОПЛЕНИЕ ЛЕТУЧЕЙ КИСЛОТЫ (СО2) с(НСО3-) > норма р(СО2) > норма
- 23. АЛКАЛОЗ увеличение буферной Ва > норма емкости по кислоте КОМПЕНСИРОВАННЫЙ рН ≈ норма ДЕКОМПЕНСИРОВАННЫЙ рН >
- 24. АЛКАЛОЗ увеличение буферной Ва > норма емкости по кислоте КОМПЕНСИРОВАННЫЙ рН ≈ норма ДЕКОМПЕНСИРОВАННЫЙ рН >
- 25. Примечание*: значения ВЕ ± (4 – 5) – стресс-нормальное состояние ± (6 - 9) – тревожное
- 27. Скачать презентацию





![Водородный показатель (рН) Гидроксильный показатель (рОН) Логарифмируя уравнение КW =[Н+][ОН-]=10-14, получаем:](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397043/slide-6.jpg)















 Твердые тела и их физические свойства
Твердые тела и их физические свойства Сполуки фосфору
Сполуки фосфору Методы выделения, очистки, идентификации и изучения мембранных структур
Методы выделения, очистки, идентификации и изучения мембранных структур Молекулярно-кінетичні явища в дисперсних системах
Молекулярно-кінетичні явища в дисперсних системах Расчёты по уравнению реакции
Расчёты по уравнению реакции Комбинированные задачи. Задание 34
Комбинированные задачи. Задание 34 Биологическая роль липидов. Транспортные формы липидов
Биологическая роль липидов. Транспортные формы липидов Спирты и их влияние на здоровье человека
Спирты и их влияние на здоровье человека Галогенидные и полигалогенидные комплексы висмута и теллура: синтез и физико-химические свойства
Галогенидные и полигалогенидные комплексы висмута и теллура: синтез и физико-химические свойства Вода. Растворимость, растворы
Вода. Растворимость, растворы Стан електронів у атомі
Стан електронів у атомі Сера
Сера Нефть. Образование нефти
Нефть. Образование нефти Thermal Energy, Chemical Energy
Thermal Energy, Chemical Energy Агрегирование ПАВ в воде и неполярных растворителях
Агрегирование ПАВ в воде и неполярных растворителях Презентация по Химии "Адсорбционная хроматография. Жидкостная хроматография" - скачать смотреть
Презентация по Химии "Адсорбционная хроматография. Жидкостная хроматография" - скачать смотреть  Органические соединения в быту
Органические соединения в быту Девиз урока: «Зажечь, увлечь и подвести»
Девиз урока: «Зажечь, увлечь и подвести»  Химические реакции. Тепловой эффект
Химические реакции. Тепловой эффект Структура периодической системы химических элементов
Структура периодической системы химических элементов Жиры в природе
Жиры в природе Слоистые силикаты
Слоистые силикаты В глубине кристалла (11 класс)
В глубине кристалла (11 класс) Личный опыт сортировки мусора
Личный опыт сортировки мусора Спирты. Органическая химия
Спирты. Органическая химия Викторина «Своя игра» в рамках декады по биологии, географии и химии
Викторина «Своя игра» в рамках декады по биологии, географии и химии  Природные каменные материалы
Природные каменные материалы Химическая связь
Химическая связь