Содержание
- 2. План: Теории кислот и оснований Автопротолиз воды Расчет кислотности в растворах кислот и оснований Кислотно-основное равновесие
- 3. Гомеостаз – состояние относительного постоянства внутренней среды организма. Изогидрия – один из важнейших факторов гомеостаза живых
- 4. Теория С.Аррениуса (классическая) НС1 = Н+ + С1-, кислота – донор протона NaOH = OН- +
- 5. Теория Бренстеда-Лоури (протонная) НА = Н+ + А-, кислота – донор протона В + Н+ =
- 6. Электронная теория Льюиса Ограниченность протонной теории – не объясняет кислотно-основные свойства ряда веществ (BCl3, SiCl4 и
- 7. Вода слабый электролит 2Н2О ↔ Н3О+ + ОН- или Н2О + Н2О ↔ Н3О+ + ОН-
- 10. Виды кислотности Активная кислотность – концентрация свободных ионов Н+. Потенциальная (резервная) кислотность – концентрация ионов Н+,
- 11. Биохимические процессы протекают при определенном значении рН. рН биологических жидкостей: Сдвиг рН от нормы – наличие
- 12. Ацидоз – устойчивое нарушение рН ниже нормы (передозировка снотворного). Алкалоз – устойчивое нарушение рН выше нормы
- 13. Диссоциация кислот и оснований НА → Н+ + А- или НА + Н2О → Н3О+ +
- 18. Для 2-х кислотных оснований k1>>k2, тогда рН = 14 – 0,5рК1 + 0,5lgСосн kкисл и kосн
- 19. РЕЗЮМЕ: рН = -lgCK – для сильных кислот рН = 14 + lgCосн – для сильных
- 21. Скачать презентацию


















 Презентация по Химии "Ярмарок професій" - скачать смотреть
Презентация по Химии "Ярмарок професій" - скачать смотреть  Требования, предъявляемые к дизельным топливам
Требования, предъявляемые к дизельным топливам Работу выполнила ученица 9 А класса ГОУ СОШ №546 г. Москвы Коломиец Екатерина Руководитель: учитель химии ГОУ СОШ №546 Симонова Т
Работу выполнила ученица 9 А класса ГОУ СОШ №546 г. Москвы Коломиец Екатерина Руководитель: учитель химии ГОУ СОШ №546 Симонова Т Тесты для самопроверки
Тесты для самопроверки Позднемеловая трубка взрыва щелочных базальтов Красноозерная
Позднемеловая трубка взрыва щелочных базальтов Красноозерная Растворы. Первичные понятия
Растворы. Первичные понятия Как сделать духи для любимой мамочки? Выполнил: Причина Алексей Учащийся 3 класса Б МОУ СОШ № 64
Как сделать духи для любимой мамочки? Выполнил: Причина Алексей Учащийся 3 класса Б МОУ СОШ № 64 Acizi, baze, oxizi, săruri. Caracteristica generală, proprietă ți fizice și chimice
Acizi, baze, oxizi, săruri. Caracteristica generală, proprietă ți fizice și chimice Карбоновые кислоты Учитель химии МОУ лицея № 6 Дробот Светлана Сергеевна
Карбоновые кислоты Учитель химии МОУ лицея № 6 Дробот Светлана Сергеевна  Тест по теме: «Алканы» Автор: учитель химии МОУСОШ № 6 Ким Н. В.
Тест по теме: «Алканы» Автор: учитель химии МОУСОШ № 6 Ким Н. В. Выполнила: Ученица 11 «Б» класса Урывкова Анастасия Кон
Выполнила: Ученица 11 «Б» класса Урывкова Анастасия Кон Отдельные классы дисперсных систем
Отдельные классы дисперсных систем Воздушные и тепловые свойства почв
Воздушные и тепловые свойства почв Нуклеофильное замещение галогена и других функциональных групп
Нуклеофильное замещение галогена и других функциональных групп Своя игра по химии
Своя игра по химии Алкены
Алкены Курс биохимии. Биохимия крови
Курс биохимии. Биохимия крови Открытие периодического закона Д.И. Менделеева
Открытие периодического закона Д.И. Менделеева Органическая химия 10 класс А.А.Карцовой и А.Н.Лёвкина
Органическая химия 10 класс А.А.Карцовой и А.Н.Лёвкина Применение циклической вольтамперометрии для определения истинной Sпов платины и оценки стабильности
Применение циклической вольтамперометрии для определения истинной Sпов платины и оценки стабильности Коррозия металлов
Коррозия металлов Агрохимия для восьмиклассников. Учебно-исследовательский проект учащейся 8 «В» класса МОУЛ «ВУВК им. А. П. Киселёва» Желтовой Анн
Агрохимия для восьмиклассников. Учебно-исследовательский проект учащейся 8 «В» класса МОУЛ «ВУВК им. А. П. Киселёва» Желтовой Анн Особенности строения, реакционной способности и методы синтеза аренов
Особенности строения, реакционной способности и методы синтеза аренов Презентация по Химии "Классификация углеводородов" - скачать смотреть
Презентация по Химии "Классификация углеводородов" - скачать смотреть  Силикаты. Пироксены. Амфиболы. Полевые шпаты
Силикаты. Пироксены. Амфиболы. Полевые шпаты Мыс айналымы
Мыс айналымы Хроматографический анализ
Хроматографический анализ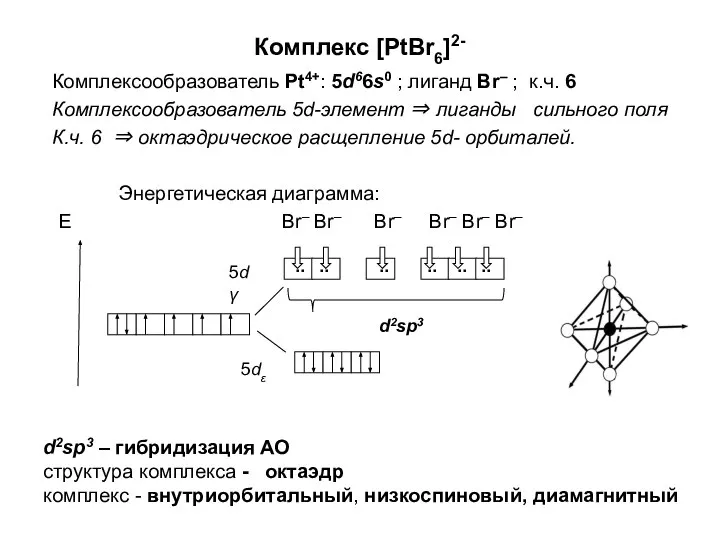 Комплексообразователь. (Лекция 5)
Комплексообразователь. (Лекция 5)