Содержание
- 2. Теоретическими продуктами полного сгорания топлива являются CO2,SO2,H2O и азот воздуха N2 (окислением азота обычно пренебрегают). Пользуясь
- 3. Балансы элементарных реакций позволяют рассчитать массовые расходы кислорода и продуктов реакции, приходящиеся на единицу массы данного
- 4. Массовый баланс реакции полного горения углерода C+O2=CO2 12 кг С + 32 кг О2 = 44
- 5. Молярная и атомная массы реагентов и продуктов горения Лекция 4
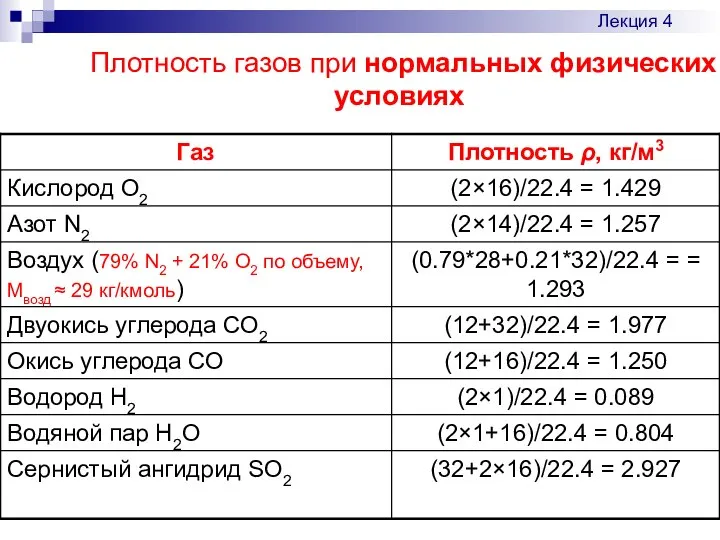
- 6. Плотность газов при нормальных физических условиях Лекция 4
- 7. Лекция 3 1 кг С + 2.66 кг (1.86 м3) О2 = 3.66 кг (1.86 м3)
- 8. Лекция 4 Теоретический объем (расход) воздуха – это объем воздуха (при нормальных условиях), необходимый для полного
- 9. Лекция 3 Теоретический объем воздуха (0,21О2+0.79N2), м3/кг Здесь предполагается, что имеющийся в топливе водород частично уже
- 10. Лекция 3 Теоретический объем воздуха для полного сгорания сухого газообразного топлива, м3/м3
- 11. Условно принимается, что азот в составе как топлива, так и воздуха, участвующего в горении, переходит в
- 12. Лекция 3 Теоретическое количество водяного пара Кроме сухих газов в состав продуктов сгорания входит водяной пар,
- 13. 0.0161 – объём водяного пара в 1 м3 атмосферного воздуха; Лекция 3 Gф – масса пара,
- 14. Лекция 3 складывается из объемов трёхатомных газов* теоретического количества азота и теоретического количества водяного пара *
- 15. Скорость горения в топочной камере определяется концентрациями топлива и окислителя, а также интенсивностью их перемешивания друг
- 16. Коэффициент избытка воздуха на входе в топку – это отношение количества воздухаVв , действительно подаваемого в
- 17. Для пылеугольных топок α т = 1.2-1.25, при этом нижний предел относится к бурым и каменным
- 18. Лекция 3 С другой стороны, действительный объем продуктов сгорания складывается из сухих газов и водяных паров
- 19. Действительный объем водяных паров Лекция 3 Действительный объём сухих газов
- 20. Лекция 3 Масса продуктов сгорания Gг (кг/кг) Согласно закону сохранение вещества масса газообразных продуктов сгорания складывается
- 21. Для горючих сланцев объём трёхатомных газов К – коэффициент разложения карбонатов: при слоевом сжигании К =
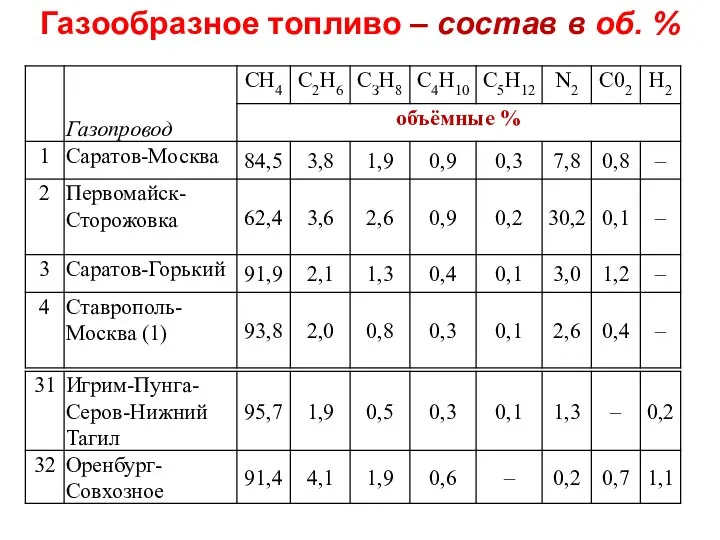
- 22. Газообразное топливо – состав в об. %
- 23. Объём трёхатомных газов: Объем сухих газов: Лекция 3 Теоретический объем азота: Теоретический объем продуктов сгорания (α
- 24. Лекция 3 Теоретический объём водяных паров в продуктах сгорания газообразного топлива (пар-продукт + влага топлива +
- 25. Часто в топочных камерах с помощью дымососа поддерживается небольшое разрежение для предотвращения выбросов газов в помещение
- 26. В балансовых испытаниях котла коэффициент избытка воздуха определяется с помощью газового анализа проб продуктов сгорания, отбираемых
- 27. При сжигании чистого углерода в теоретическом количестве воздуха (α = 1) концентрация СО2 в сухих продуктах:
- 28. Лекция 4 При сжигании природных топлив, в которых кроме С присутствуют другие горючие элементы (Н и
- 30. Лекция 3 По-существу, это уравнение представляет собой баланс массы кислорода: исходный кислород в воздухе-окислителе (21%) расходуется
- 31. Лекция 3 После подстановки значений концентраций О2 и N2 в азотную формулу получаем общее выражение для
- 32. Физический смысл: при полном сгорании топлива объем подаваемого для горения воздуха приближенно равен объему сухих продуктов,
- 33. Лекция 3
- 34. Лекция 4 Коэффициент Бунте для газообразных топлив
- 35. Лекция 3 где вместо измеренной концентрации О2 в сухих газах используется избыточная концентрация кислорода, из которой
- 36. Лекция 3 Отсюда Концентрация азота в сухих продуктах неполного сгорания в пренебрежении небольшим количеством топливного азота
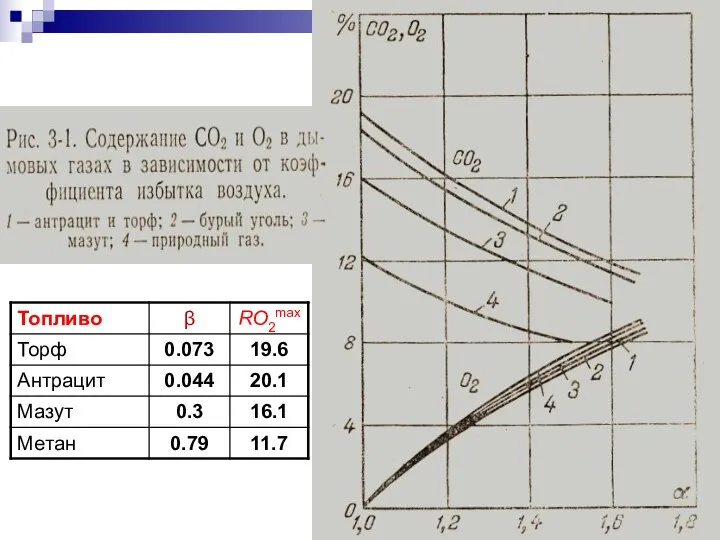
- 37. Так как концентрация свободного кислорода в продуктах сгорания О2 в основном зависит от избытка воздуха, то
- 38. Тesto 325 М/XL Измеряет в дымовых газах концентрации О2 и СО (СО с компенсацией по Н2
- 39. Тesto 330-1/2 Измеряет концентрацию в дымовых газах О2 , СО, NO. Имеет встроенный дифманометр. Два канала
- 40. Тesto 300 М/XL Измеряет концентрацию в дымовых газах О2, СО, NO. Имеет встроенный дифманометр. Два канала
- 42. Скачать презентацию




































 Викторина по теме «Искусственные и синтетические полимеры Выполнила Немцева Т.А. учитель биологии и химии
Викторина по теме «Искусственные и синтетические полимеры Выполнила Немцева Т.А. учитель биологии и химии Химический состав костей
Химический состав костей Стеклоткани. Виды стеклотканей
Стеклоткани. Виды стеклотканей МОУ «Масловская средняя общеобразовател
МОУ «Масловская средняя общеобразовател История нефтедобычи в России
История нефтедобычи в России Атомы и молекулы. Простые и сложные вещества. 8 класс
Атомы и молекулы. Простые и сложные вещества. 8 класс Физические и химические свойства меди
Физические и химические свойства меди Степень окисления
Степень окисления Физико-химия поверхностных явлений в функционировании живых систем
Физико-химия поверхностных явлений в функционировании живых систем Агрохімія Розмаїтого Дмитра, 10-А клас
Агрохімія Розмаїтого Дмитра, 10-А клас  Физические и химические явления Учитель химии «Чажемтовской СОШ» Косова Е.М.
Физические и химические явления Учитель химии «Чажемтовской СОШ» Косова Е.М. Основные понятия и законы химии
Основные понятия и законы химии Чистые вещества и смеси. Уголь и вода
Чистые вещества и смеси. Уголь и вода Формы существования химических элементов. Химические и физические явления
Формы существования химических элементов. Химические и физические явления Фотохимический смог
Фотохимический смог Процессы растворения твёрдых веществ
Процессы растворения твёрдых веществ Органическая химия. Этапы развития органической химии
Органическая химия. Этапы развития органической химии Кривые титрования
Кривые титрования Цеоліти як адсорбенти та основа сучасних каталізаторів. Структура, здатність до модифікування
Цеоліти як адсорбенти та основа сучасних каталізаторів. Структура, здатність до модифікування Открытие водорода
Открытие водорода Спирты в жизни человека
Спирты в жизни человека Простые вещества – металлы
Простые вещества – металлы Галогены. Физические свойства
Галогены. Физические свойства Процессы и операции формообразования. Металлургия цветных металлов
Процессы и операции формообразования. Металлургия цветных металлов Кальцій
Кальцій Алкалоидтар. Алкалоидтар туралы түсінік. Жіктелуі
Алкалоидтар. Алкалоидтар туралы түсінік. Жіктелуі Фармацевтические суспензии и эмульсии
Фармацевтические суспензии и эмульсии Решение задач по теме Концентрация раствора
Решение задач по теме Концентрация раствора