Содержание
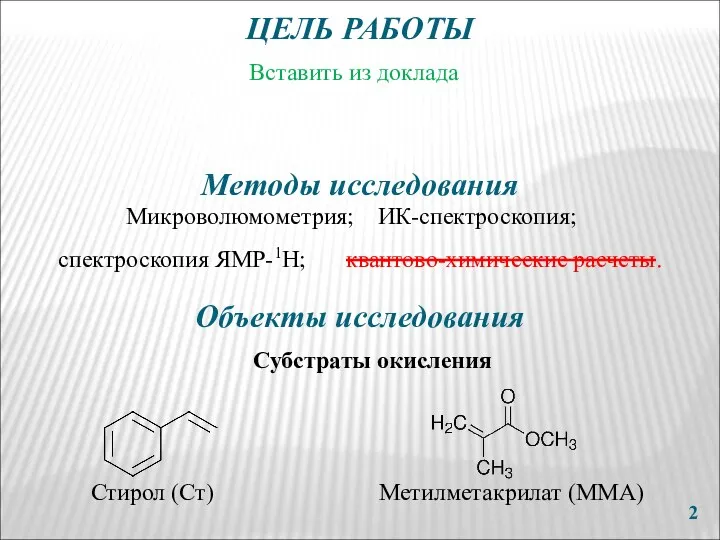
- 2. Вставить из доклада ЦЕЛЬ РАБОТЫ Объекты исследования Стирол (Ст) Метилметакрилат (ММА) Субстраты окисления Методы исследования Микроволюмометрия;
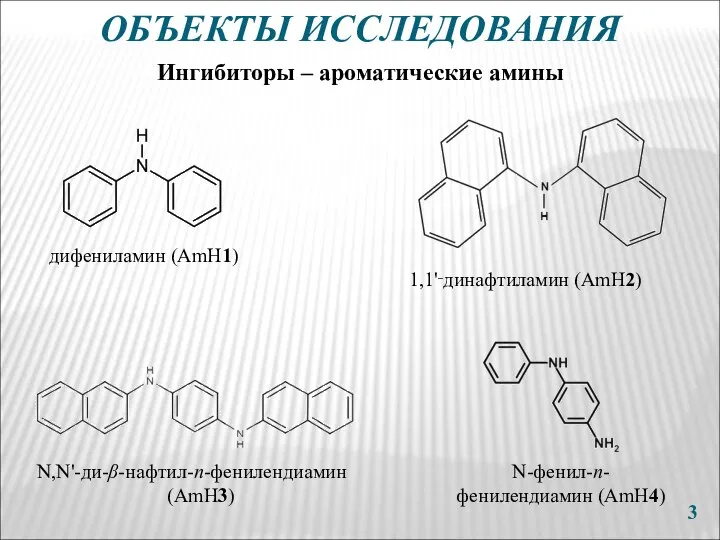
- 3. ОБЪЕКТЫ ИССЛЕДОВАНИЯ Ингибиторы – ароматические амины 1,1'‑динафтиламин (AmH2) дифениламин (AmH1) N,N'-ди-β-нафтил-п-фенилендиамин (AmH3) N-фенил-п- фенилендиaмин (AmH4)
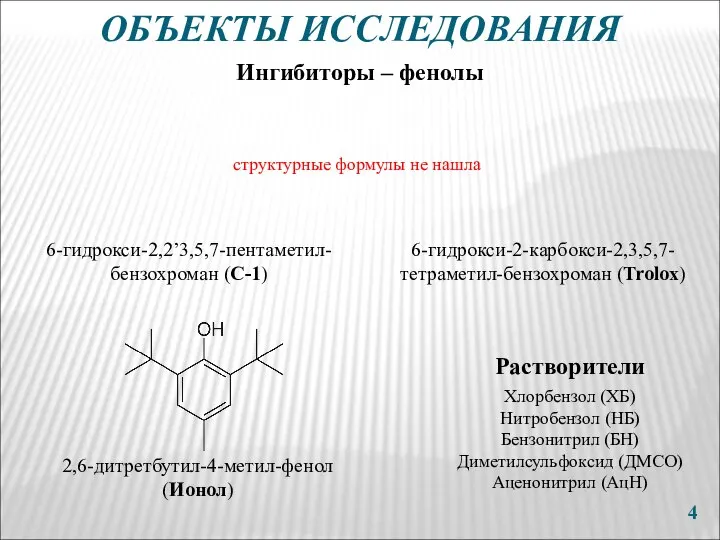
- 4. ОБЪЕКТЫ ИССЛЕДОВАНИЯ 6-гидрокси-2-карбокси-2,3,5,7-тетраметил-бензохроман (Trolox) 6-гидрокси-2,2’3,5,7-пентаметил-бензохроман (С-1) 2,6-дитретбутил-4-метил-фенол (Ионол) Ингибиторы – фенолы Растворители Хлорбензол (ХБ) Нитробензол (НБ)
- 5. МЕХАНИЗМ ОКИСЛЕНИЯ НЕПРЕДЕЛЬНЫХ СОЕДИНЕНИЙ В ЖИДКОЙ ФАЗЕ Е.М. Плисс, Р.Б. Сафиуллин, С.С. Злотский. Ингибированное окисление непредельных
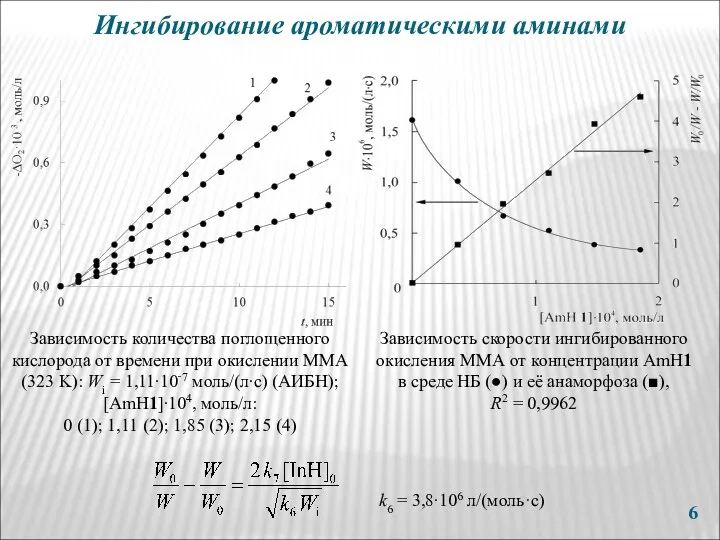
- 6. Ингибирование ароматическими аминами Зависимость количества поглощенного кислорода от времени при окислении ММА (323 K): Wi =
- 7. Экспериментальные значения констант k7⋅10–3 ± 10% [л/(моль·с)] при окислении ММА, ингибированном ароматическими аминами, в различных растворителях,
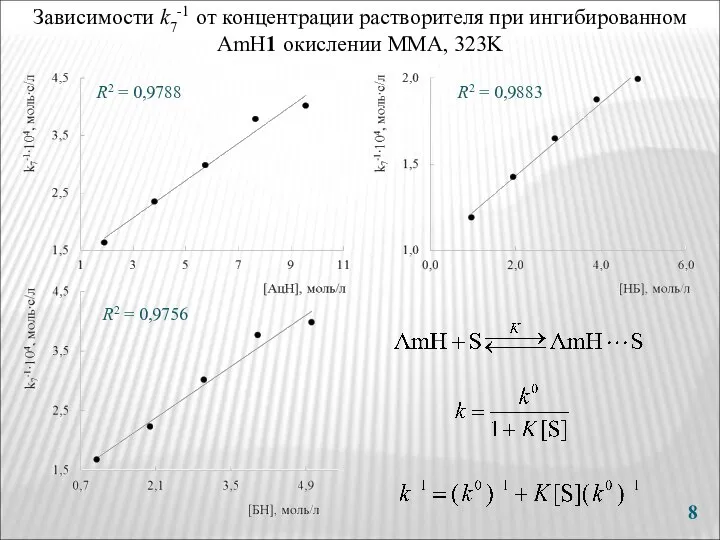
- 8. Зависимости k7-1 от концентрации растворителя при ингибированном AmH1 окислении ММА, 323K R2 = 0,9788 R2 =
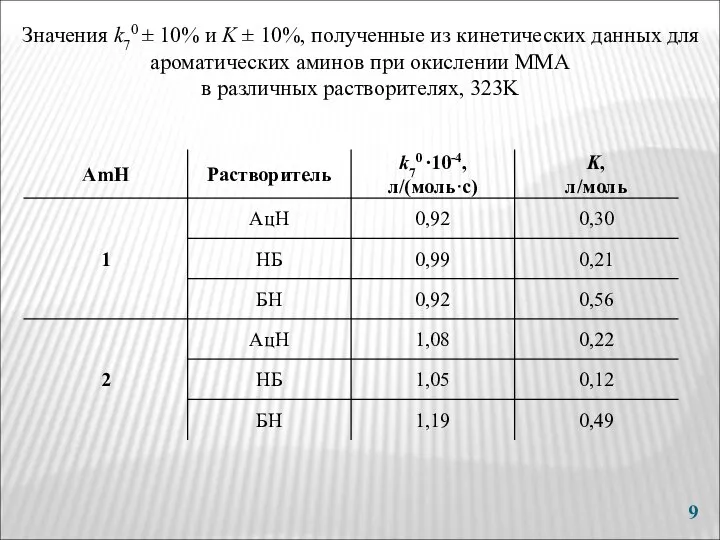
- 9. Значения k70 ± 10% и K ± 10%, полученные из кинетических данных для ароматических аминов при
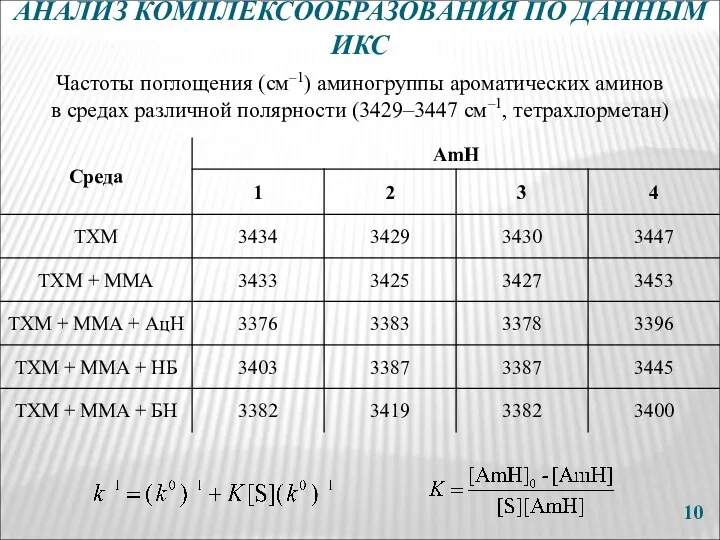
- 10. Частоты поглощения (см–1) аминогруппы ароматических аминов в средах различной полярности (3429–3447 см–1, тетрахлорметан) АНАЛИЗ КОМПЛЕКСООБРАЗОВАНИЯ ПО
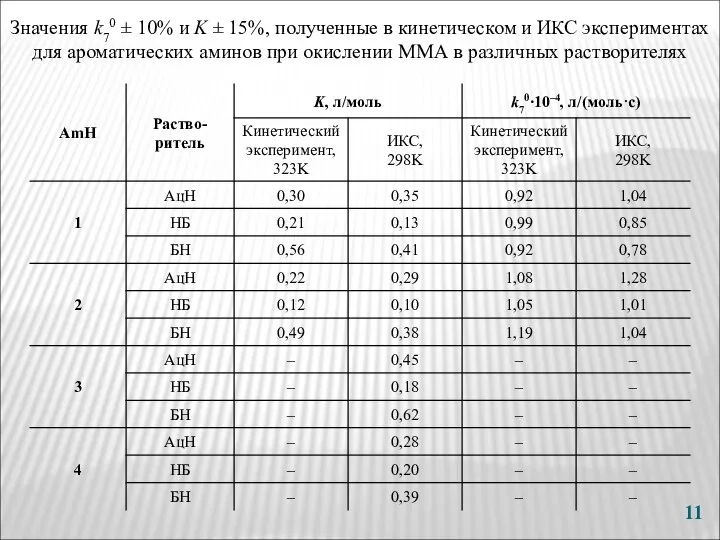
- 11. Значения k70 ± 10% и K ± 15%, полученные в кинетическом и ИКС экспериментах для ароматических
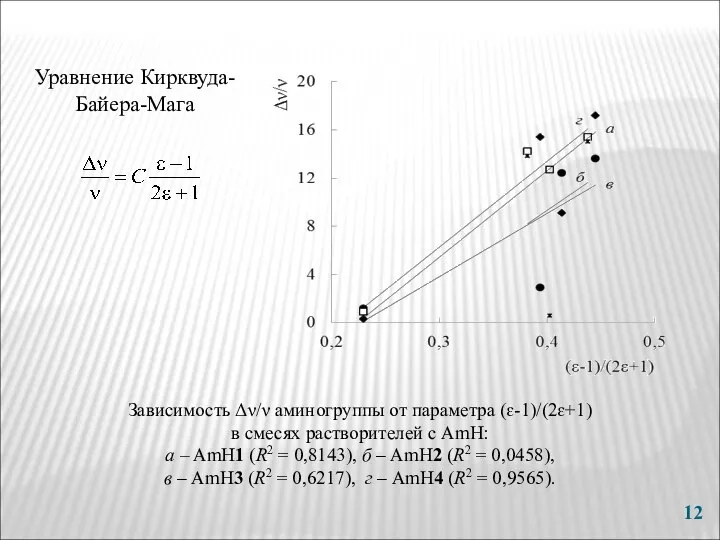
- 12. Зависимость Δν/ν аминогруппы от параметра (ɛ-1)/(2ɛ+1) в смесях растворителей с AmH: а – AmH1 (R2 =
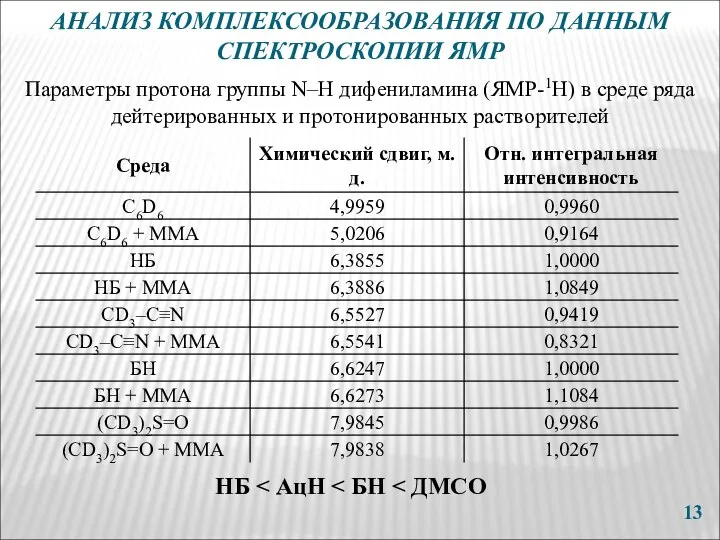
- 13. АНАЛИЗ КОМПЛЕКСООБРАЗОВАНИЯ ПО ДАННЫМ СПЕКТРОСКОПИИ ЯМР НБ Параметры протона группы N–H дифениламина (ЯМР-1H) в среде ряда
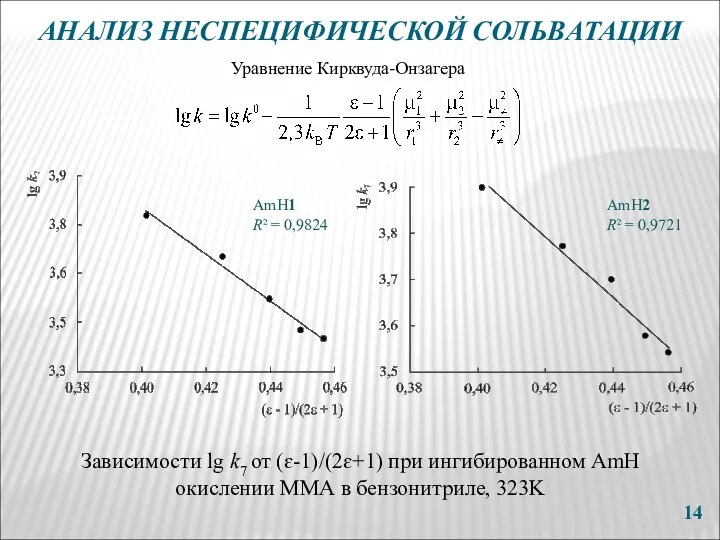
- 14. АНАЛИЗ НЕСПЕЦИФИЧЕСКОЙ СОЛЬВАТАЦИИ Зависимости lg k7 от (ɛ-1)/(2ɛ+1) при ингибированном AmH окислении ММА в бензонитриле, 323K
- 15. Е.М. Плисс, Р.Б. Сафиуллин, С.С. Злотский. Ингибированное окисление непредельных соединений. Кинетика, механизм, связь структуры с реакционной
- 16. Кинетика поглощения кислорода при окислении ММА [ММА] = 8 моль/л; [C-1], моль/л: 1 – 0; 2
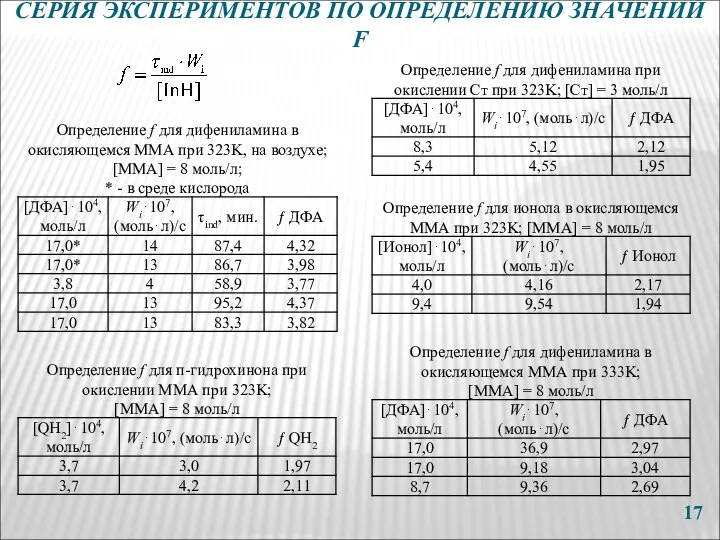
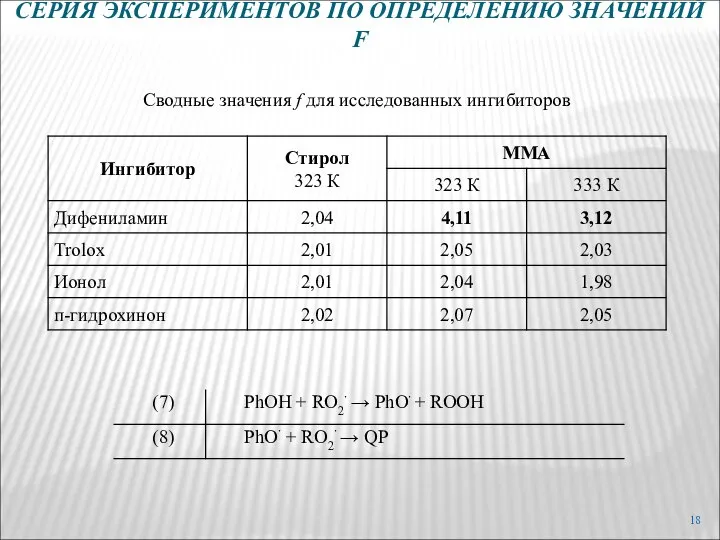
- 17. СЕРИЯ ЭКСПЕРИМЕНТОВ ПО ОПРЕДЕЛЕНИЮ ЗНАЧЕНИЙ F
- 18. СЕРИЯ ЭКСПЕРИМЕНТОВ ПО ОПРЕДЕЛЕНИЮ ЗНАЧЕНИЙ F
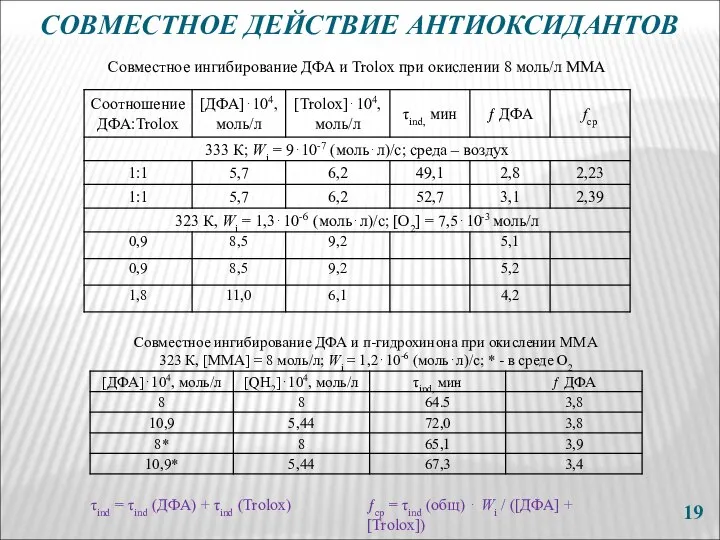
- 19. СОВМЕСТНОЕ ДЕЙСТВИЕ АНТИОКСИДАНТОВ τind = τind (ДФА) + τind (Trolox) ƒср = τind (общ) ⋅ Wi
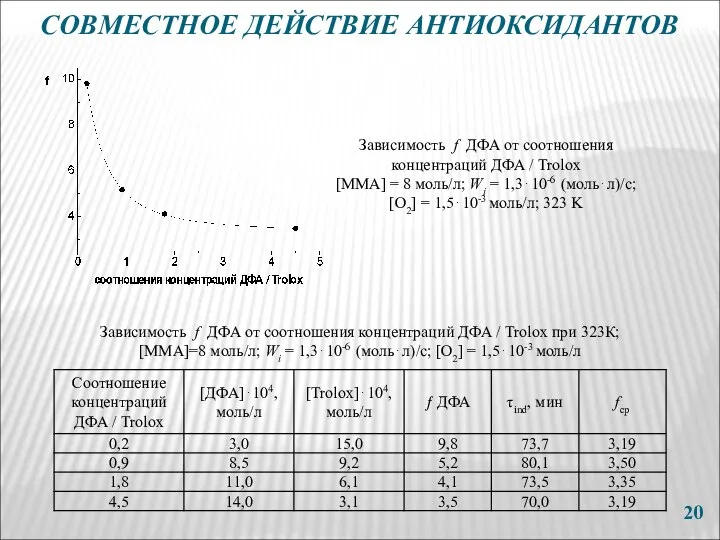
- 20. СОВМЕСТНОЕ ДЕЙСТВИЕ АНТИОКСИДАНТОВ Зависимость f ДФА от соотношения концентраций ДФА / Trolox [ММА] = 8 моль/л;
- 22. Скачать презентацию

![Экспериментальные значения констант k7⋅10–3 ± 10% [л/(моль·с)] при окислении ММА, ингибированном](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1319606/slide-6.jpg)

![Кинетика поглощения кислорода при окислении ММА [ММА] = 8 моль/л; [C-1],](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1319606/slide-15.jpg)
 Коллигативные свойства растворов. Осмос. Осмотическое давление
Коллигативные свойства растворов. Осмос. Осмотическое давление Как «архангельский мужик … стал разумен и велик». О Михаиле Васильевиче Ломоносове
Как «архангельский мужик … стал разумен и велик». О Михаиле Васильевиче Ломоносове  Теория химико-технологических процессов органического синтеза. Введение. (Лекция 1)
Теория химико-технологических процессов органического синтеза. Введение. (Лекция 1) Мыло и мыловарение
Мыло и мыловарение Харчові добавки
Харчові добавки  Органическая химия
Органическая химия Химический состав клетки
Химический состав клетки Целлюлоза Выполнила студентка 11 группы Сыровацкая Лилия
Целлюлоза Выполнила студентка 11 группы Сыровацкая Лилия  Угольная кислота и ее соли
Угольная кислота и ее соли Важнейшие классы неорганических соединений
Важнейшие классы неорганических соединений Презентация по Химии "Галогени" - скачать смотреть бесплатно
Презентация по Химии "Галогени" - скачать смотреть бесплатно Таблица «Периодическая система Д.И.Менделеева»
Таблица «Периодическая система Д.И.Менделеева» Строение и свойства белков
Строение и свойства белков Водородная связь
Водородная связь Этот удивительный Мир симметрии - презентация_
Этот удивительный Мир симметрии - презентация_ Розроблення моделі легування квантової точки InAs в матриці GaAs в хлоридній системі
Розроблення моделі легування квантової точки InAs в матриці GaAs в хлоридній системі Фазовые равновесия «раствор-пар» в двухкомпонентных системах из двух летучих жидкостей
Фазовые равновесия «раствор-пар» в двухкомпонентных системах из двух летучих жидкостей Кислород. Историческая справка
Кислород. Историческая справка Презентация Изомерия алкенов.
Презентация Изомерия алкенов.  Биологически активные добавки
Биологически активные добавки Жесткость воды и способы ее устранения
Жесткость воды и способы ее устранения Другого ничего в природе нет Другого ничего в природе нет Ни здесь, ни там, в космических глубинах: Все – от песчинок малых до план
Другого ничего в природе нет Другого ничего в природе нет Ни здесь, ни там, в космических глубинах: Все – от песчинок малых до план Функциональная биохимия. Биохимия крови. (Раздел 11. Лекции 22-23)
Функциональная биохимия. Биохимия крови. (Раздел 11. Лекции 22-23) Эластомеры (резины)
Эластомеры (резины) Оксиды углерода
Оксиды углерода Як захистити себе від нітратів
Як захистити себе від нітратів  Катализ. Влияние катализатора на скорость химической реакции
Катализ. Влияние катализатора на скорость химической реакции Горение. Подводный факел
Горение. Подводный факел