Содержание
- 3. Щёлочноземе́льные мета́ллы —химические элементы 2-й группы периодической таблицы элементов: бериллий, магний, кальций, стронций,барий, радий и унбинилий.
- 5. Физические свойства К щёлочноземельным металлам относят только кальций, стронций, барий и радий, реже магний. Первый элемент
- 7. Химические свойства Щёлочноземельные металлы имеют электронную конфигурацию внешнего энергетического уровня ns², и являются s-элементами, наряду с
- 9. Скачать презентацию
Слайд 2
Слайд 3
Щёлочноземе́льные мета́ллы —химические элементы 2-й группы периодической таблицы элементов: бериллий, магний, кальций, стронций,барий, радий и унбинилий.
Щёлочноземе́льные мета́ллы —химические элементы 2-й группы периодической таблицы элементов: бериллий, магний, кальций, стронций,барий, радий и унбинилий.
Слайд 4
Слайд 5
Физические свойства
К щёлочноземельным металлам относят только кальций, стронций, барий и
Физические свойства
К щёлочноземельным металлам относят только кальций, стронций, барий и
радий, реже магний. Первый элемент этой подгруппы, бериллий, по большинству свойств гораздо ближе к алюминию, чем к высшим аналогами группы, в которую он входит. Второй элемент этой группы, магний, в некоторых отношениях значительно отличается от щелочноземельных металлов по ряду химических свойств. Все щёлочноземельные металлы серые, твёрдые при комнатной температуре вещества. В отличие от щелочных металлов, они существенно более твёрдые, и ножом преимущественно не режутся (исключение — стронций. Рост плотности щёлочноземельных металлов наблюдается только начиная с кальция. Самый тяжёлый — радий, по плотности сравнимый с германием (ρ= 5,5 г/см3).
Слайд 6
Слайд 7
Химические свойства
Щёлочноземельные металлы имеют электронную конфигурацию внешнего энергетического уровня ns², и
Химические свойства
Щёлочноземельные металлы имеют электронную конфигурацию внешнего энергетического уровня ns², и
являются s-элементами, наряду с щелочными металлами. Имея два валентных электрона, щёлочноземельные металлы легко их отдают, и во всех соединениях имеют степень окисления +2 (очень редко +1).
Химическая активность щёлочноземельных металлов растёт с ростом порядкового номера. Бериллий в компактном виде не реагирует ни с кислородом, ни с галогенами даже при температуре красного каления (до 600 °C, для реакции с кислородом и другими халькогенами нужна ещё более высокая температура, фтор — исключение). Магний защищён оксидной плёнкой при комнатной температуре и более высоких (до 650 °C) температурах и не окисляется дальше. Кальций медленно окисляется и при комнатной температуре вглубь (в присутствии водяных паров), и сгорает при небольшом нагревании в кислороде, но устойчив в сухом воздухе при комнатной температуре. Стронций, барий и радий быстро окисляются на воздухе, давая смесь оксидов и нитридов, поэтому их, подобно щелочным металлам и кальцию, хранят под слоем керосина.
Также, в отличие от щелочных металлов, щелочноземельные металлы не образуют надпероксиды и озониды.
Оксиды и гидроксиды щёлочноземельных металлов имеют тенденцию к усилению основных свойств с ростом порядкового номера.
Химическая активность щёлочноземельных металлов растёт с ростом порядкового номера. Бериллий в компактном виде не реагирует ни с кислородом, ни с галогенами даже при температуре красного каления (до 600 °C, для реакции с кислородом и другими халькогенами нужна ещё более высокая температура, фтор — исключение). Магний защищён оксидной плёнкой при комнатной температуре и более высоких (до 650 °C) температурах и не окисляется дальше. Кальций медленно окисляется и при комнатной температуре вглубь (в присутствии водяных паров), и сгорает при небольшом нагревании в кислороде, но устойчив в сухом воздухе при комнатной температуре. Стронций, барий и радий быстро окисляются на воздухе, давая смесь оксидов и нитридов, поэтому их, подобно щелочным металлам и кальцию, хранят под слоем керосина.
Также, в отличие от щелочных металлов, щелочноземельные металлы не образуют надпероксиды и озониды.
Оксиды и гидроксиды щёлочноземельных металлов имеют тенденцию к усилению основных свойств с ростом порядкового номера.






 Підготувала Бендюк Вікторія,10-Б
Підготувала Бендюк Вікторія,10-Б  Карбоновые кислоты
Карбоновые кислоты Электрохимические цепи
Электрохимические цепи Системы эвтектического типа
Системы эвтектического типа Липиды. Тема 10
Липиды. Тема 10 Хімічні добавки. Е-числа Підготували учні 7-В(г) класу Лучечко Анна Ванівська Галина Вчитель: Глуховецька Оксана Вікторівна
Хімічні добавки. Е-числа Підготували учні 7-В(г) класу Лучечко Анна Ванівська Галина Вчитель: Глуховецька Оксана Вікторівна  Природные источники углеводородов и их переработка
Природные источники углеводородов и их переработка  Кейс № 4.1 одежда для металла
Кейс № 4.1 одежда для металла Статья двумя способами. Приготовление катализатора
Статья двумя способами. Приготовление катализатора Неорганические вяжущие вещества. (Лекция 6)
Неорганические вяжущие вещества. (Лекция 6) Положение металлов в ПСХЭ Д.И. Менделеева. Общие физические свойства металлов
Положение металлов в ПСХЭ Д.И. Менделеева. Общие физические свойства металлов Оксокислоти. Номенклатура
Оксокислоти. Номенклатура Алкадиены. Строение, изомерия, номенклатура, физические и химические свойства
Алкадиены. Строение, изомерия, номенклатура, физические и химические свойства Чи шкідливі пральні порошки для здоров’я?
Чи шкідливі пральні порошки для здоров’я?  Гидроксилпроизводные углеводородов
Гидроксилпроизводные углеводородов Відходи хімічного синтезу: утворення та попередження
Відходи хімічного синтезу: утворення та попередження Коллоидно-химические свойства и методы определения дисперсности НДС. Лекция 3
Коллоидно-химические свойства и методы определения дисперсности НДС. Лекция 3 Группа рассеянных химических элементов
Группа рассеянных химических элементов Свойства неметаллов и их соединений
Свойства неметаллов и их соединений Презентация по химии Строение электронных оболочек атомов.
Презентация по химии Строение электронных оболочек атомов.  Устойчивость дисперсных систем
Устойчивость дисперсных систем Азотсодержащие и гетероциклические соединения. Низкомолекулярные биологическиактивные соединения
Азотсодержащие и гетероциклические соединения. Низкомолекулярные биологическиактивные соединения Презентація на тему «Вологість повітря» Солоділової Катерини 10-Б
Презентація на тему «Вологість повітря» Солоділової Катерини 10-Б Химические реакции с участием макромолекул
Химические реакции с участием макромолекул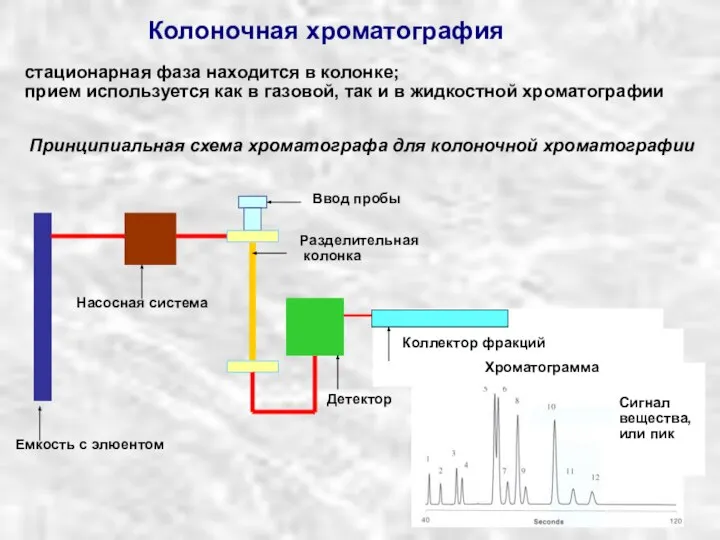 Колоночная хроматография
Колоночная хроматография Аттестационная работа. Химия в нашей жизни
Аттестационная работа. Химия в нашей жизни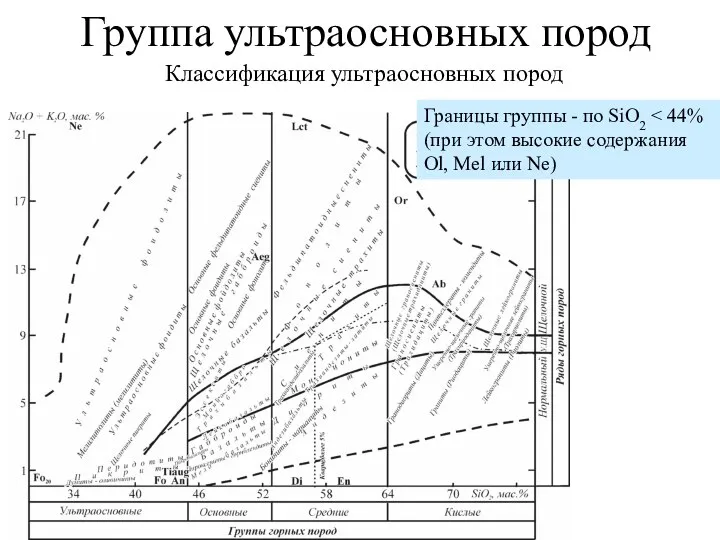 Группа ультраосновных пород
Группа ультраосновных пород Коррозия, как источник загрязнения окружающей среды
Коррозия, как источник загрязнения окружающей среды