Содержание
- 2. Историческая справка Открыта 1 марта 1969г. Д. И. Менделеевым Является графическим отображением периодического закона Известны более
- 3. Длинный вариант периодической системы
- 4. Короткий вариант периодической системы
- 5. Периодический закон Периодический закон (1869 г.): «Свойства химических элементов, а также характер и свойства их соединений
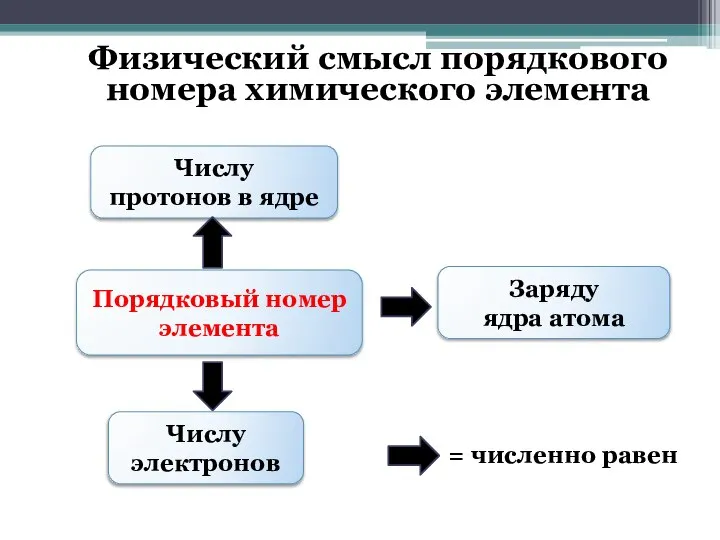
- 6. Числу протонов в ядре Порядковый номер элемента Заряду ядра атома Числу электронов Физический смысл порядкового номера
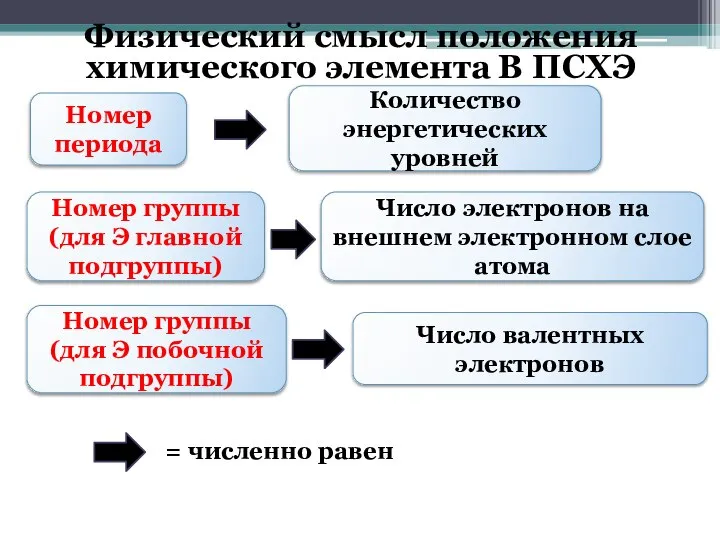
- 7. Физический смысл положения химического элемента В ПСХЭ Номер периода Количество энергетических уровней Номер группы (для Э
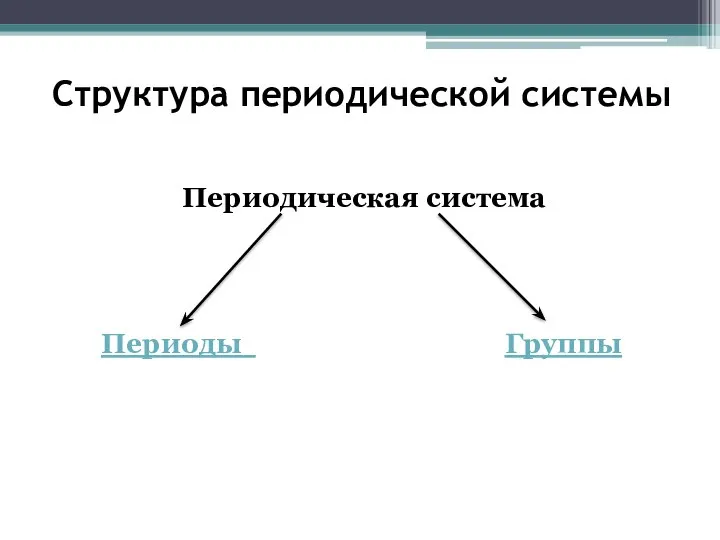
- 8. Структура периодической системы Периодическая система Периоды Группы
- 9. Периоды Горизонтальные ряды, сходных по свойствам элементов Всего 7 Обозначаются римскими цифрами Делятся на малые (I,II,III)
- 10. Группы Горизонтальные ряды сходных по свойствам элементов. Всего 8 Делятся на главные (A) и побочные (B)
- 11. Изменение свойств элементов в периодах При увеличении заряда ядра атома (при движении слева направо): число электронных
- 12. Изменение свойств элементов в группах При увеличении заряда ядра атома (при движении сверху вниз): число электронных
- 13. Домашнее задание 1. § 5,6,7 проработать 2. стр. 27, упр. 1-5 (устно) 3. стр. 32-33, упр.
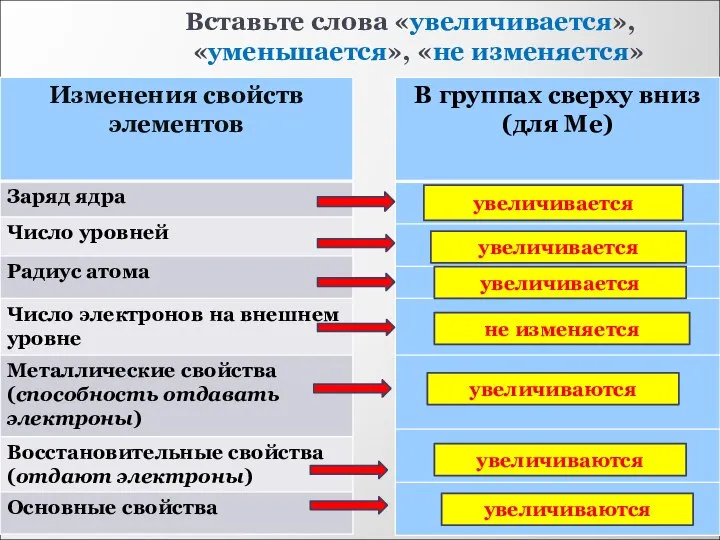
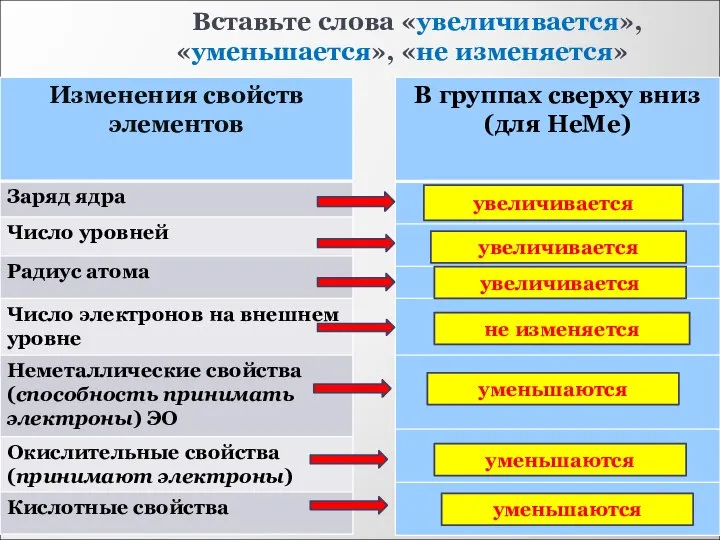
- 14. Вставьте слова «увеличивается», «уменьшается», «не изменяется» увеличивается не изменяется уменьшается увеличивается уменьшаются увеличиваются увеличиваются увеличиваются
- 15. Вставьте слова «увеличивается», «уменьшается», «не изменяется» увеличивается увеличивается увеличивается не изменяется увеличиваются увеличиваются увеличиваются
- 16. Вставьте слова «увеличивается», «уменьшается», «не изменяется» увеличивается увеличивается увеличивается не изменяется уменьшаются уменьшаются уменьшаются
- 17. 1. В ряду химических элементов C → Si → Ge → Sn 1) увеличивается число электронных
- 18. 2. В ряду химических элементов бор - углерод - азот возрастает: 1) способность атома отдавать электроны
- 19. 3. С увеличением порядкового номера элемента в периоде радиус атома: 1) увеличивается 2) уменьшается 3) не
- 20. 4. В главных подгруппах периодической системы с увеличением заряда ядра атомов: 1) усиливаются металлические свойства элементов
- 21. 5. В периоде: 2) идет последовательное заполнение электронами одного энергетического подуровня 3) идет последовательное заполнение электронами
- 22. 6.В периодах с увеличением заряда ядра атомов: 1) усиливаются металлические свойства элементов 4) ослабевают неметаллические свойства
- 23. 7.Металлические свойства элементов в периоде: 1) увеличиваются слева направо 3) не изменяются 8.Радиус атома в группе:
- 25. Скачать презентацию

















 Можно ли выкрасить кристаллы в домашних условиях
Можно ли выкрасить кристаллы в домашних условиях Качественные реакции
Качественные реакции Аммиак
Аммиак Комплексные соединения
Комплексные соединения Введение. Основные понятия химии
Введение. Основные понятия химии Ксенобиотики. Микросомальное окисление
Ксенобиотики. Микросомальное окисление Молекулярно-кінетичні явища в дисперсних системах
Молекулярно-кінетичні явища в дисперсних системах Имидазол. Получение, свойства, анализ, применение, условия хранения лекарственных препаратов производных имидазола
Имидазол. Получение, свойства, анализ, применение, условия хранения лекарственных препаратов производных имидазола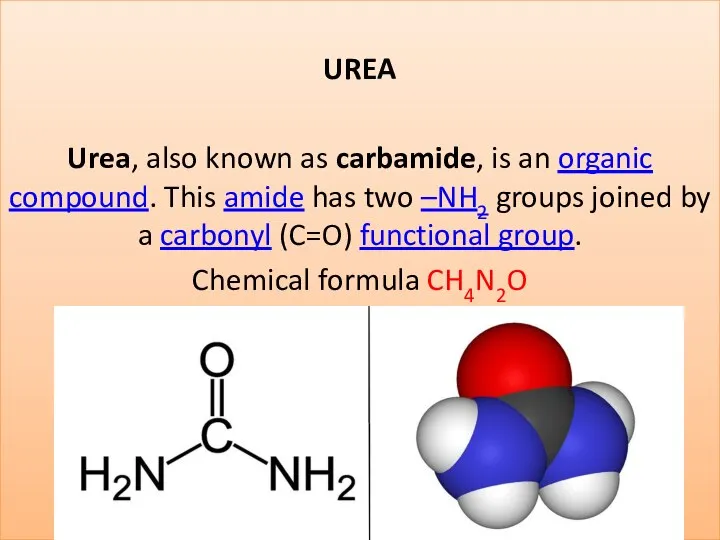 Urea (carbamide)
Urea (carbamide) Презентация по Химии "Силікатні матеріали: скло, кераміка, цемент" - скачать смотреть бесплатно
Презентация по Химии "Силікатні матеріали: скло, кераміка, цемент" - скачать смотреть бесплатно МОЛЯРНЫЙ ОБЪЕМ Химия 8 класс
МОЛЯРНЫЙ ОБЪЕМ Химия 8 класс Хімічний склад і використання мінералів
Хімічний склад і використання мінералів Реакционная способность карбоновых кислот
Реакционная способность карбоновых кислот Современное состояние и пути совершенствования стандартизации лекарственных средств
Современное состояние и пути совершенствования стандартизации лекарственных средств Номенклатура органических соединений
Номенклатура органических соединений Электрохимическая коррозии. Катодные процессы электрохимической коррозии
Электрохимическая коррозии. Катодные процессы электрохимической коррозии Экспериментальное исследование кипения сверхтекучего гелия на цилиндрическом нагревателе внутри пористой оболочки
Экспериментальное исследование кипения сверхтекучего гелия на цилиндрическом нагревателе внутри пористой оболочки Альдегиды. Строение молекул
Альдегиды. Строение молекул Фосфор. Соединения фосфора
Фосфор. Соединения фосфора Углеводороды. Алканы
Углеводороды. Алканы Биотит и тальк
Биотит и тальк Органикалық қосылыстар
Органикалық қосылыстар Практическая работа № 3. Получение, собирание и распознавание газов
Практическая работа № 3. Получение, собирание и распознавание газов Презентация по Химии "Вода" - скачать смотреть
Презентация по Химии "Вода" - скачать смотреть  Качественный и количественный методы исследования растворов
Качественный и количественный методы исследования растворов ГСМ - горюче-смазочные материалы
ГСМ - горюче-смазочные материалы Сероводород
Сероводород Пищевые добавки
Пищевые добавки