Содержание
- 2. Цель урока Изучить химические свойства и стадии получения серной кислоты
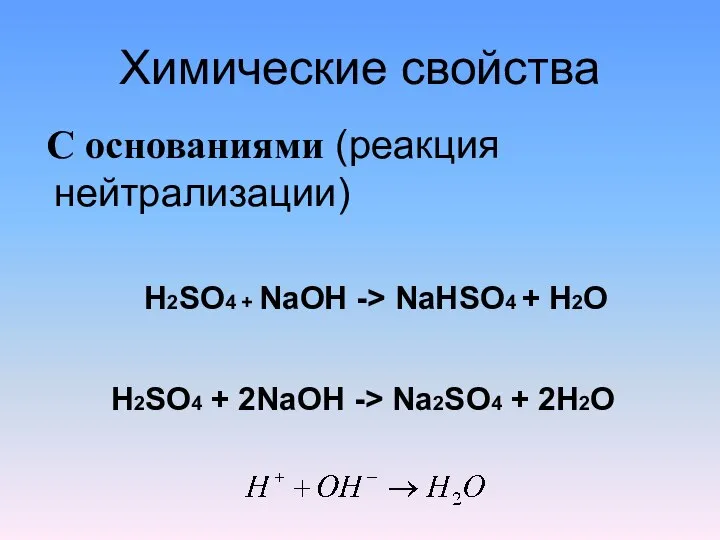
- 3. Химические свойства С основаниями (реакция нейтрализации) H2SO4 + NaOH -> NaHSO4 + H2O H2SO4 + 2NaOH
- 4. Химические свойства С металлами (стоящие в ряду напряжения до водорода) Zn + H2SO4 -> ZnSO4 +
- 5. Химические свойства С солями BaCl2 + H2SO4 -> BaSO4 + 2HCl Хлорид бария является качественным реактивом
- 6. Концентрированная серная кислота Cu + 2H2SO4 -> CuSO4 + SO2 + 2H2O
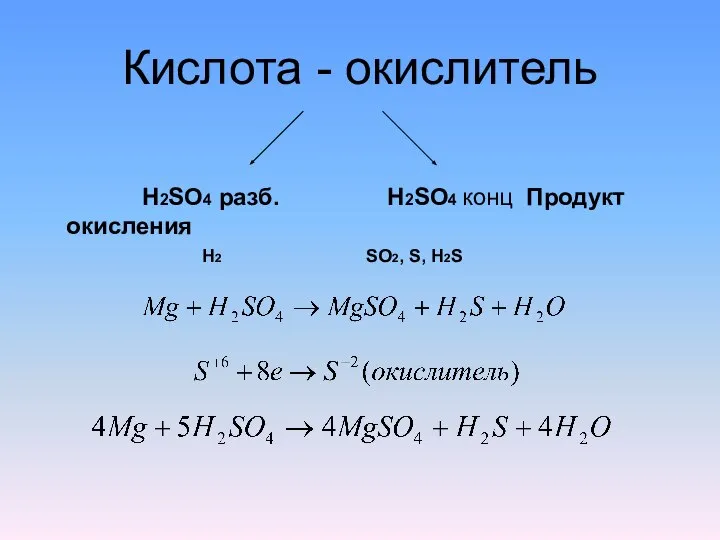
- 7. Кислота - окислитель H2SO4 разб. H2SO4 конц Продукт окисления H2 SO2, S, H2S
- 8. Производство серной кислоты I стадия – получение сернистого газа SO2 Получение из пирита
- 9. Производство серной кислоты II стадия – получение SO3 2-я стадия
- 10. Производство серной кислоты III стадия – получение H2SO4 3-я стадия
- 11. Выводы Серная кислота может являться реагентом для получения водорода Серная кислота является сильным окислителем Серная кислота
- 12. Проверь себя Вариант I Вариант II В 1. А Б 2. Г А 3. А А
- 14. Скачать презентацию









 Презентация по Химии "Загальні способи добування металів" - скачать смотреть бесплатно
Презентация по Химии "Загальні способи добування металів" - скачать смотреть бесплатно Химия өнеркәсібі
Химия өнеркәсібі Относительная атомная масса
Относительная атомная масса Коллоидные растворы поверхностно-активных веществ (ПАВ)
Коллоидные растворы поверхностно-активных веществ (ПАВ) Основания. Гидроксид натрия
Основания. Гидроксид натрия Закономерности протекания химических реакций. Основы химической термодинамики. Лекция 6
Закономерности протекания химических реакций. Основы химической термодинамики. Лекция 6 АТФ Аденозинтрифосфат
АТФ Аденозинтрифосфат Поверхностные явления
Поверхностные явления Алканы. Предельные углеводороды. Парафины. Насыщенные углеводороды
Алканы. Предельные углеводороды. Парафины. Насыщенные углеводороды Производство минеральных удобрений
Производство минеральных удобрений Аттестационная работа. Рабочая программа внеурочной деятельности «Мир под микроскопом». (5 класс)
Аттестационная работа. Рабочая программа внеурочной деятельности «Мир под микроскопом». (5 класс) Отчет по ПП.03.01 «Лаборант химического анализа»
Отчет по ПП.03.01 «Лаборант химического анализа» Минералы. Свойства минералов
Минералы. Свойства минералов Периодический закон и периодическая система Д. И. Менделеева
Периодический закон и периодическая система Д. И. Менделеева обратимые и необратимые реакции, электролитическая диссоциация, сильные и слабые электролиты, определение кислот, солей, основан
обратимые и необратимые реакции, электролитическая диссоциация, сильные и слабые электролиты, определение кислот, солей, основан Маса та розміри атомів і молекул. Кількість речовини
Маса та розміри атомів і молекул. Кількість речовини Дисперсные
Дисперсные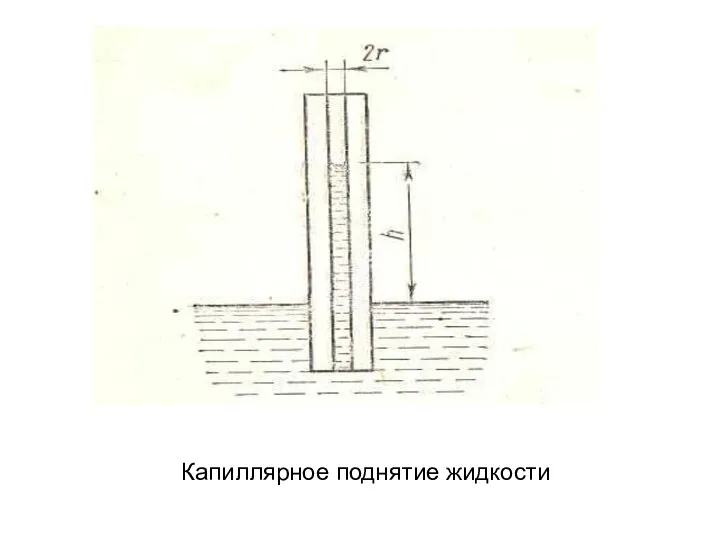 Капиллярное поднятие жидкости
Капиллярное поднятие жидкости Полезные свойства камней
Полезные свойства камней Гетерогенді химиялық реакциялар
Гетерогенді химиялық реакциялар Йод
Йод Презентация по Химии "Металлы. Общая характеристика металлов (нахождение в природе и физические свойства)" - скачать смотреть
Презентация по Химии "Металлы. Общая характеристика металлов (нахождение в природе и физические свойства)" - скачать смотреть  Кислоты. Химические свойства кислот
Кислоты. Химические свойства кислот Презентация на тему: Хром
Презентация на тему: Хром Биохимия ферментов и кинетика
Биохимия ферментов и кинетика Презентация по Химии "Оцтова кислота" - скачать смотреть бесплатно
Презентация по Химии "Оцтова кислота" - скачать смотреть бесплатно Презентация по Химии "Мило,та миючі засоби." - скачать смотреть бесплатно
Презентация по Химии "Мило,та миючі засоби." - скачать смотреть бесплатно Геохимия редкоземельных элементов
Геохимия редкоземельных элементов