Фенолы: понятие, классификация, номенклатура, изомерия, получение, физические свойства, химические свойства, применение
Содержание
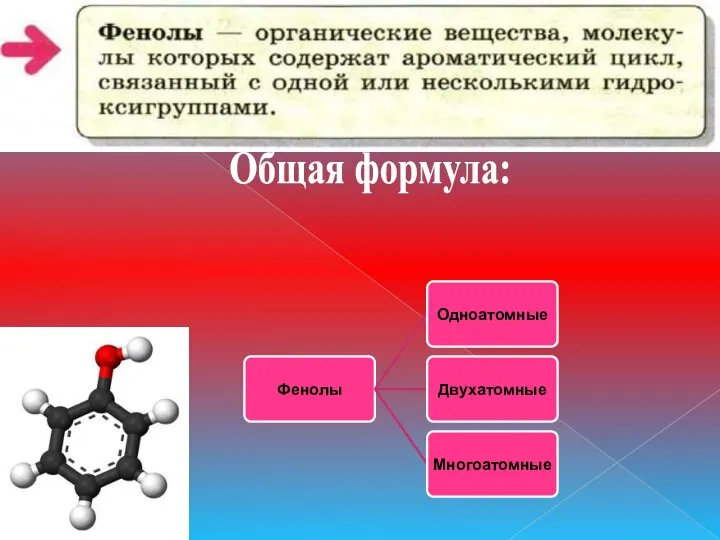
- 2. Общая формула:
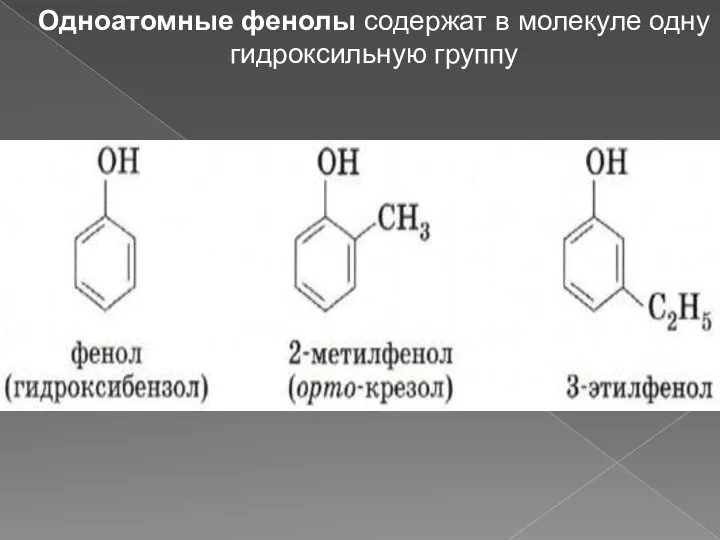
- 3. Одноатомные фенолы содержат в молекуле одну гидроксильную группу
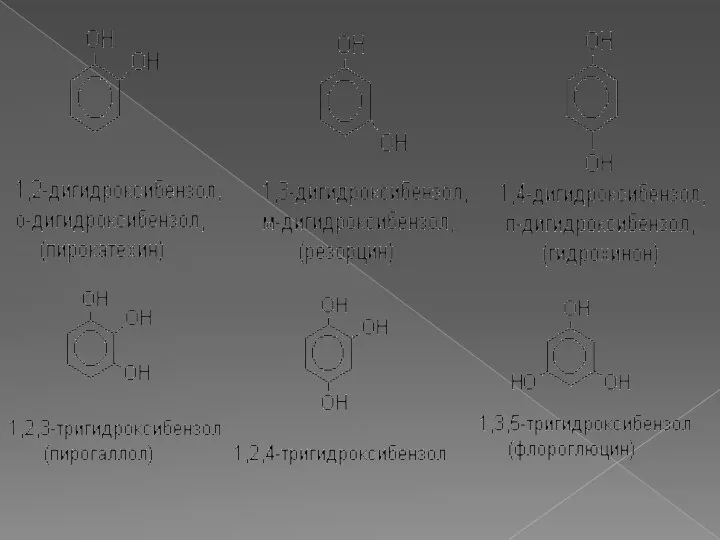
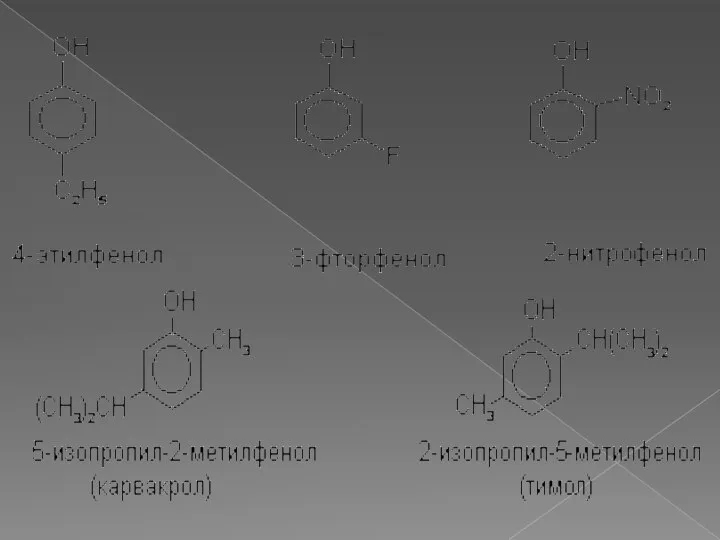
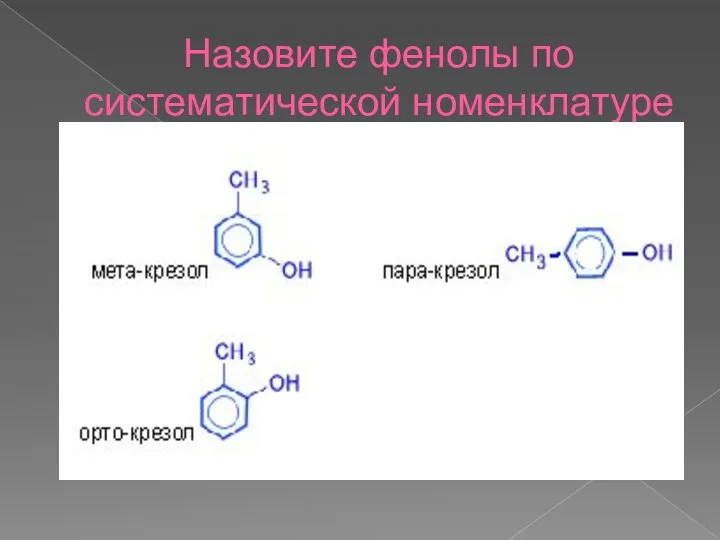
- 6. Назовите фенолы по систематической номенклатуре
- 7. Изомерия фенолов Изомерия положения гидроксигруппы Изомерия углеродного скелета
- 8. Напишите и назовите изомеры фенолов с общей формулой С8Н10О С9Н12О
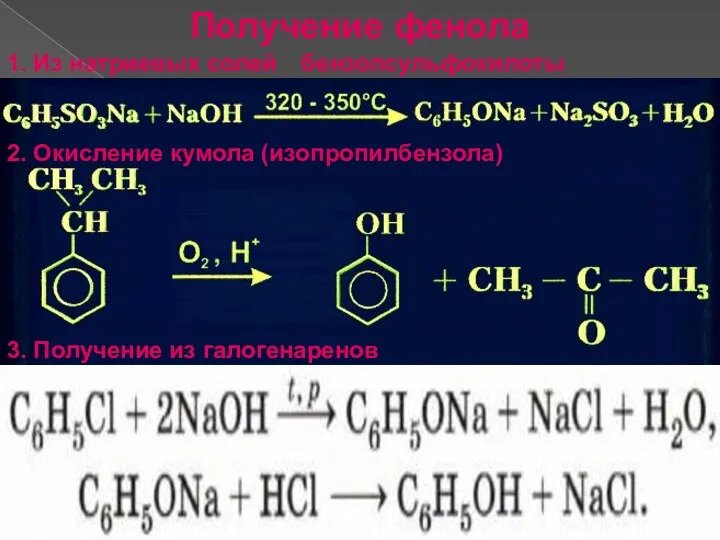
- 9. Получение фенола 1. Из натриевых солей бензолсульфокилоты 2. Окисление кумола (изопропилбензола) 3. Получение из галогенаренов
- 10. Фенол - бесцветные, розовеющие при хранении на воздухе, кристаллы с характерным запахом. Хорошо растворим в ацетоне,
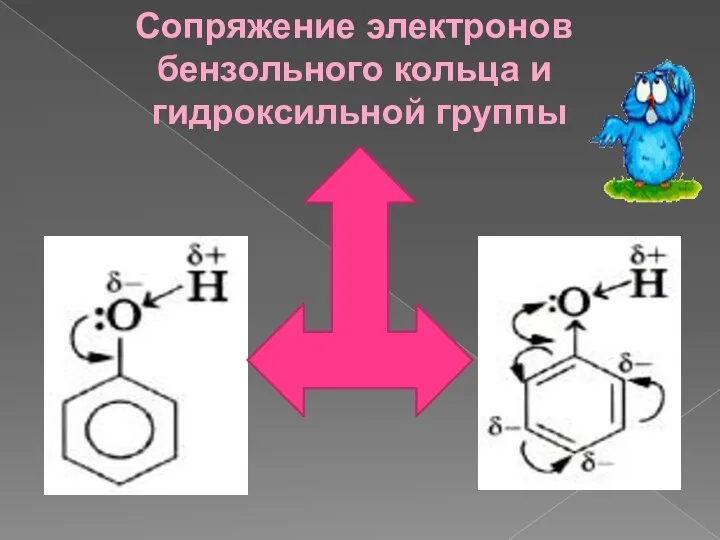
- 11. Сопряжение электронов бензольного кольца и гидроксильной группы
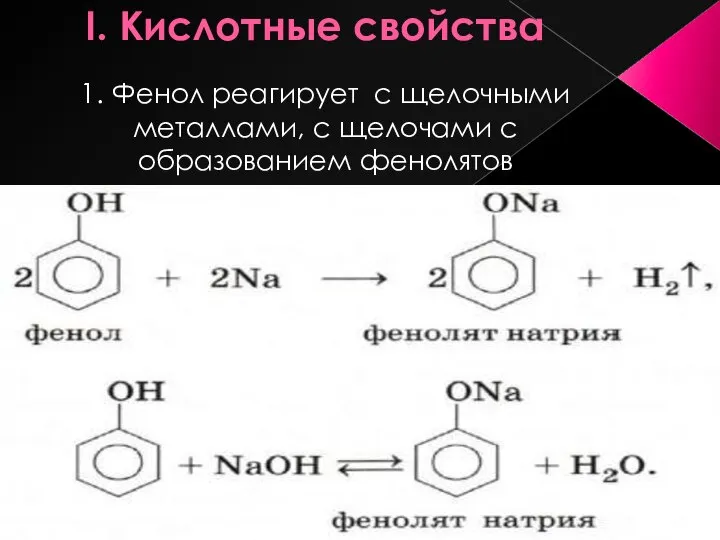
- 12. I. Кислотные свойства 1. Фенол реагирует с щелочными металлами, с щелочами с образованием фенолятов
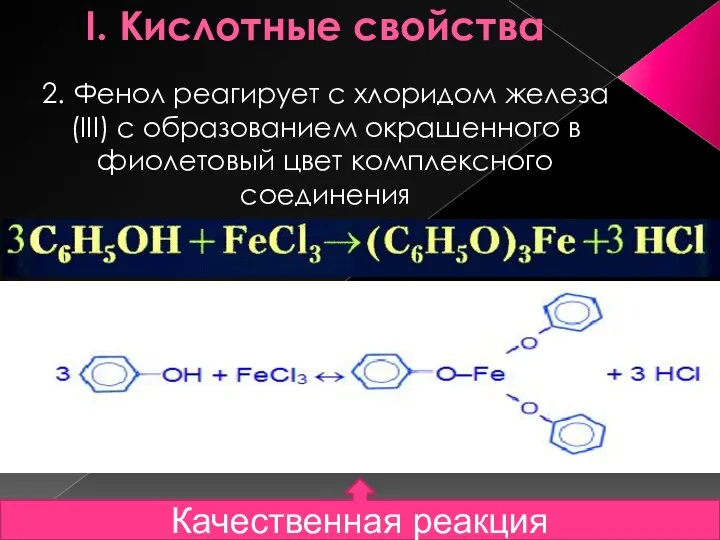
- 13. I. Кислотные свойства 2. Фенол реагирует с хлоридом железа (III) с образованием окрашенного в фиолетовый цвет
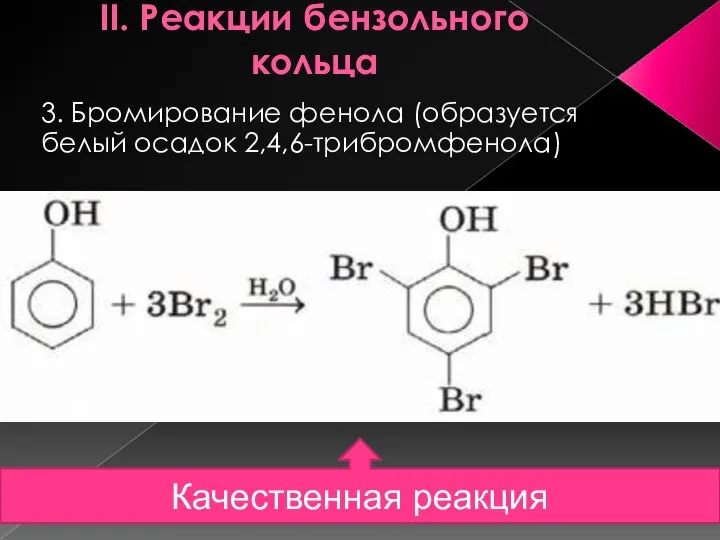
- 14. II. Реакции бензольного кольца 3. Бромирование фенола (образуется белый осадок 2,4,6-трибромфенола) Качественная реакция
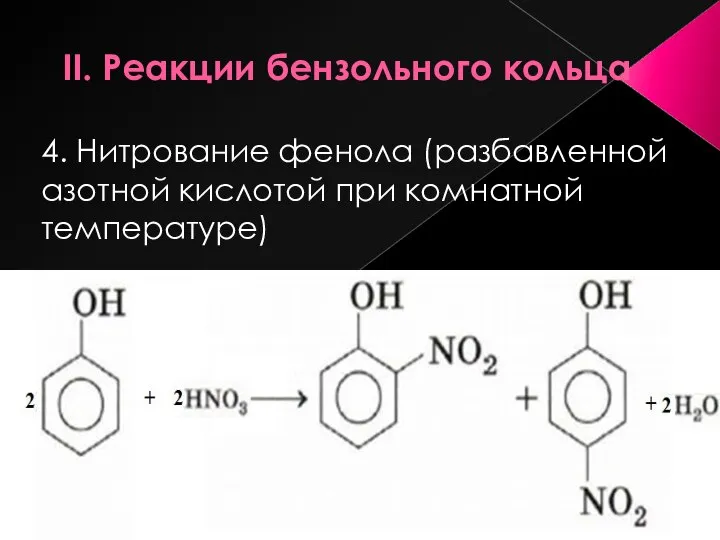
- 15. II. Реакции бензольного кольца 4. Нитрование фенола (разбавленной азотной кислотой при комнатной температуре)
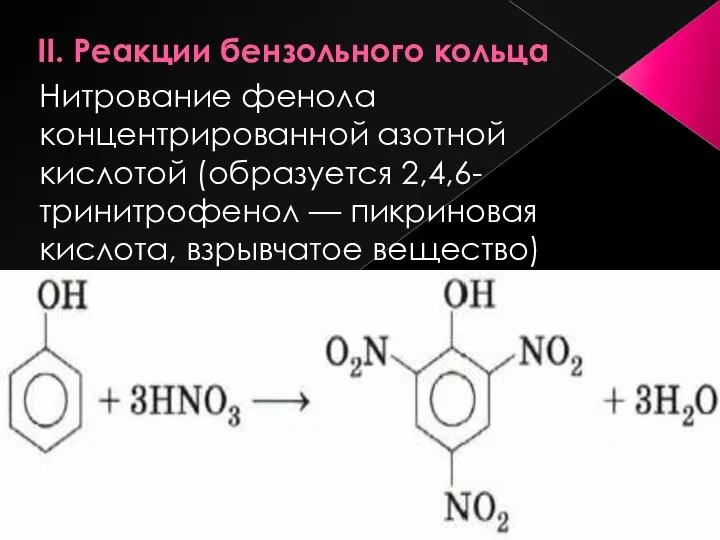
- 16. II. Реакции бензольного кольца Нитрование фенола концентрированной азотной кислотой (образуется 2,4,6-тринитрофенол — пикриновая кислота, взрывчатое вещество)
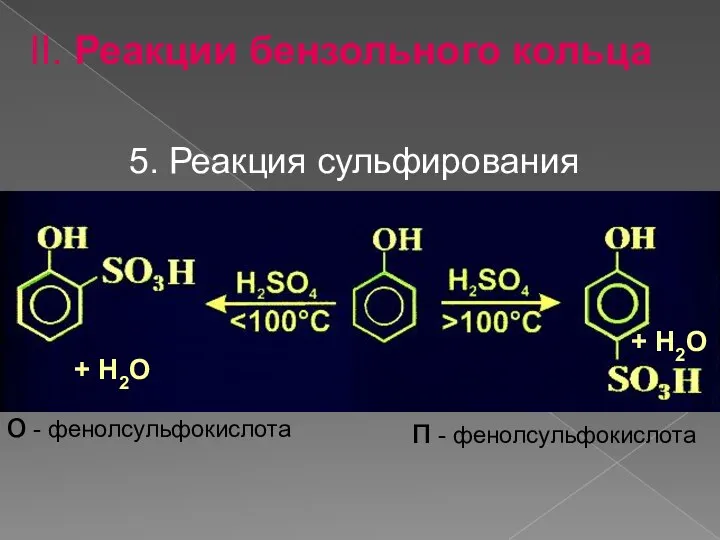
- 17. + H2O + H2O 5. Реакция сульфирования о - фенолсульфокислота п - фенолсульфокислота II. Реакции бензольного
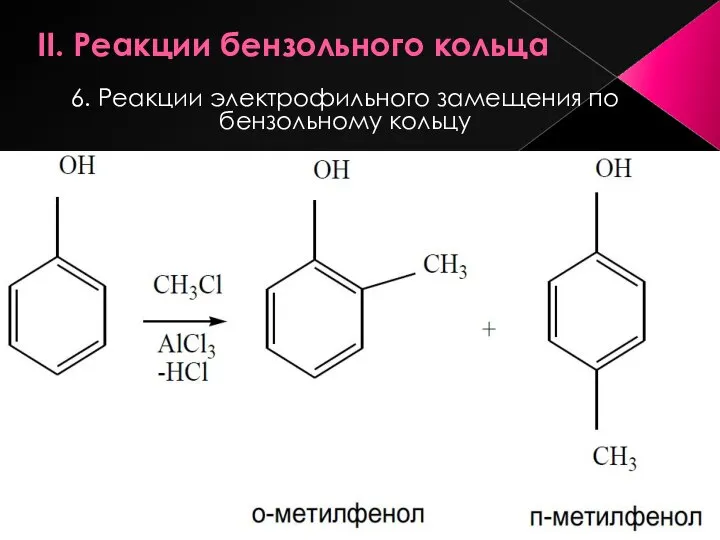
- 18. II. Реакции бензольного кольца 6. Реакции электрофильного замещения по бензольному кольцу
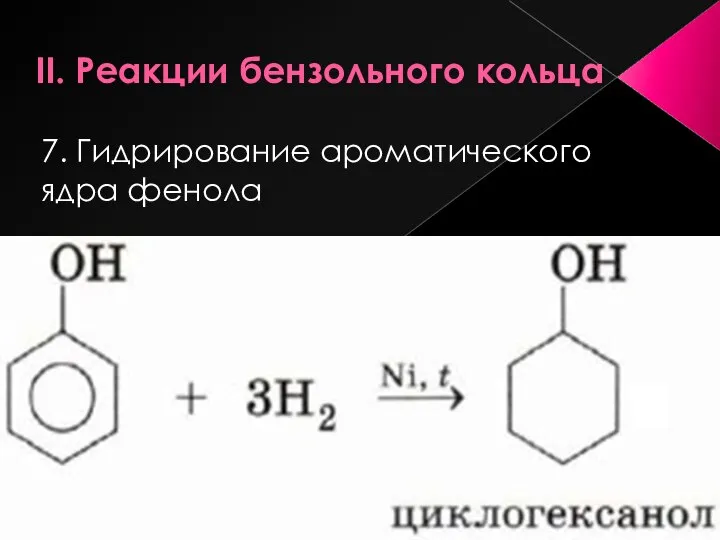
- 19. II. Реакции бензольного кольца 7. Гидрирование ароматического ядра фенола
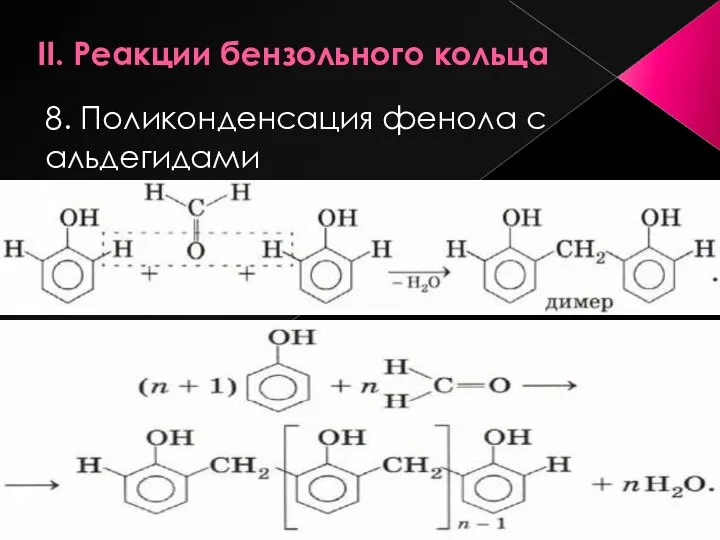
- 20. II. Реакции бензольного кольца 8. Поликонденсация фенола с альдегидами
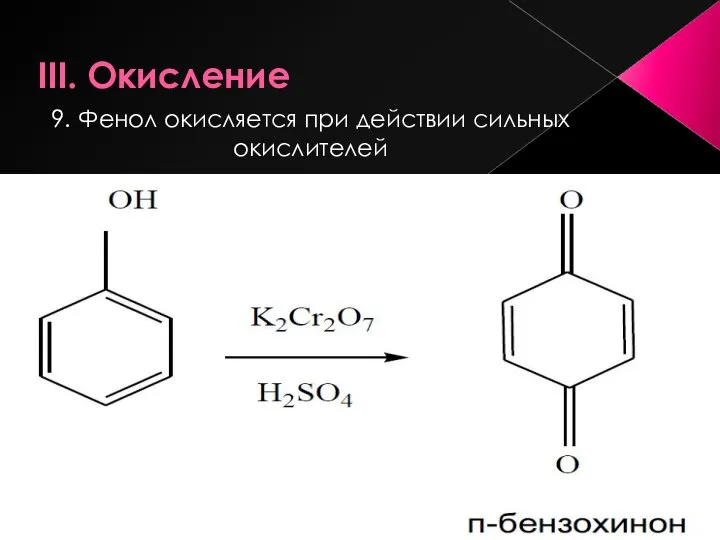
- 21. III. Окисление 9. Фенол окисляется при действии сильных окислителей
- 22. III. Окисление 10. Фенол горит С6Н5ОН+ 7О2 =6СО2 + 3Н2О
- 24. В трёх пробирках без подписи находятся водные растворы пропанола-1, глицерина и фенола. С помощью каких реагентов
- 25. Массовые доли углерода и водорода в гомологе фенола равны соответственно 77,78 и 7,41%. Определите формулу вещества.
- 26. Расположите указанные вещества в порядке усиления кислотных свойств: а) фенол; б) 2-метилфенол; в) 2,4,6-триметилфенол; г) 2,4,6-тринитрофенол;
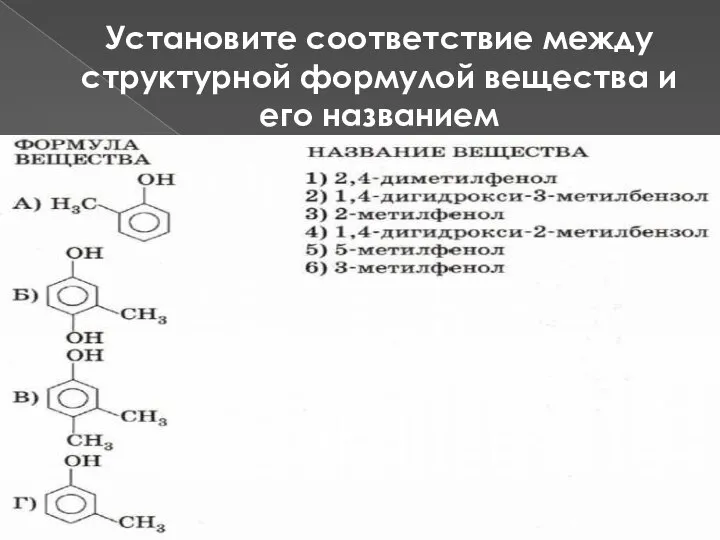
- 27. Установите соответствие между структурной формулой вещества и его названием
- 29. Скачать презентацию








 Установка гидрокрекинга
Установка гидрокрекинга Строение органических молекул. (Лекция 2)
Строение органических молекул. (Лекция 2) Репликация ДНК. Элонгация репликации ДНК. (Лекция 4)
Репликация ДНК. Элонгация репликации ДНК. (Лекция 4) Хлор 11 класс - Презентация
Хлор 11 класс - Презентация Основы строения органических соединений. Теория строения органических соединений
Основы строения органических соединений. Теория строения органических соединений Нанодисперсный политетрафторэтилен. Инертные, антифрикционные, противоизносные покрытия
Нанодисперсный политетрафторэтилен. Инертные, антифрикционные, противоизносные покрытия Биологически активные низкомолекулярные вещества
Биологически активные низкомолекулярные вещества Проект. Создание производства гранулированных биоорганических удобрений
Проект. Создание производства гранулированных биоорганических удобрений Химиялык кару
Химиялык кару Образование раствора
Образование раствора Амфотерность. Амфотерные соединения
Амфотерность. Амфотерные соединения Образование иммунологического синапса
Образование иммунологического синапса Свойства жидкостей
Свойства жидкостей Полимеры. Полимерные материалы
Полимеры. Полимерные материалы Титан. Нахождение в природе
Титан. Нахождение в природе Ароматические соединения (арены)
Ароматические соединения (арены) Кинетика сложных реакций
Кинетика сложных реакций Презентация подготовлена учителем химии ош № 33 г. Симферополя Филиной Лесей Игоревной. Каменный уголь.
Презентация подготовлена учителем химии ош № 33 г. Симферополя Филиной Лесей Игоревной. Каменный уголь.  Геохимия природных процессов. Мономинеральный баланс рубидия в гранодиорите. (Лекция 4)
Геохимия природных процессов. Мономинеральный баланс рубидия в гранодиорите. (Лекция 4) Бейорганикалық заттар технологиясындағы жүйелерді термодинамикалық талдау
Бейорганикалық заттар технологиясындағы жүйелерді термодинамикалық талдау БХиМБ. Катаболизм пищевых и тканевых липидов. Лекция 6
БХиМБ. Катаболизм пищевых и тканевых липидов. Лекция 6 Презентация по Химии "Возникновение органической химии как науки" - скачать смотреть бесплатно
Презентация по Химии "Возникновение органической химии как науки" - скачать смотреть бесплатно Безпечна для довкілля хімія «green chemistry». Основні напрямки та перспективи розвитку
Безпечна для довкілля хімія «green chemistry». Основні напрямки та перспективи розвитку Биохимия старения. (Лекция 24)
Биохимия старения. (Лекция 24) Фосфор. Открытие фосфора
Фосфор. Открытие фосфора Опал
Опал Сорбіт C6H14O6
Сорбіт C6H14O6 Сырьевая база промышленной органической химии. Области применения органических веществ. (Лекция 1)
Сырьевая база промышленной органической химии. Области применения органических веществ. (Лекция 1)