Содержание
- 2. Углерод и его соединения
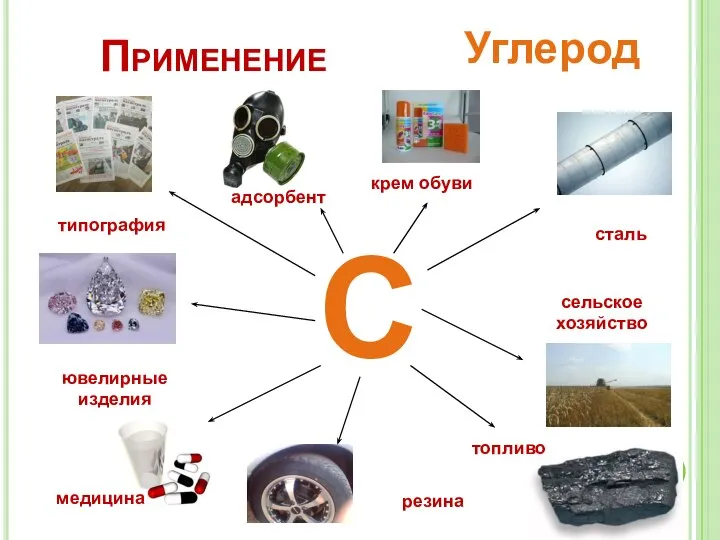
- 3. Углерод С сталь сельское хозяйство топливо медицина типография ювелирные изделия адсорбент резина крем обуви Применение
- 4. ЦЕЛИ УРОКА: – установить строение атома углерода по его положению в ПС; – изучить аллотропные модификации
- 5. Учитывая положение углерода в Периодической системе, ответьте на вопросы: Каков химический знак углерода? Каков атомный номер
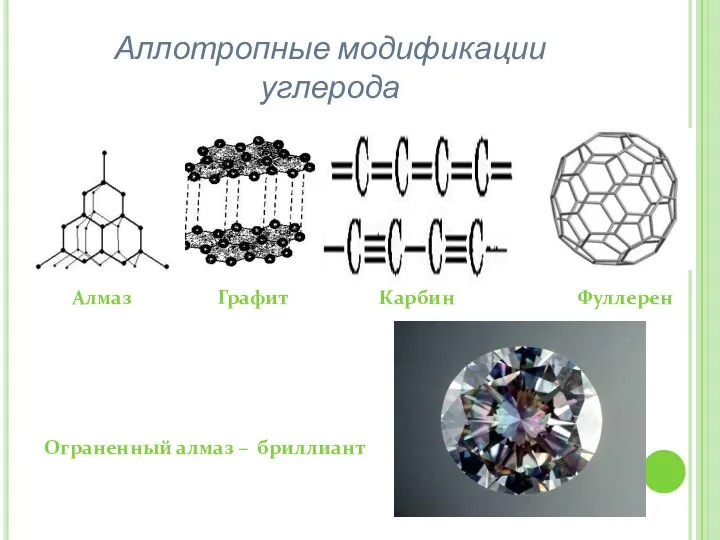
- 6. Аллотропные модификации углерода Алмаз Графит Карбин Фуллерен Ограненный алмаз – бриллиант
- 7. Алмаз Бесцветный Прозрачный Не проводит электрический ток Прочный Твердый Алмаз имеет кубическую элементарную ячейку. В структуре
- 8. Графит Темно-серый Непрозрачный Проводит электрический ток Мягкий Металлический блеск Оставляет след на бумаге Жирный на ощупь
- 9. Карбин представляет собой мелкокристаллический порошок чёрного цвета, обладает полупроводниковыми свойствами. Получен в искусственных условиях из длинных
- 10. Фуллере́ны— молекулярные соединения,представляющие собой выпуклые замкнутые многогранники, составленные из чётного числа трёхкоординированных атомов углерода. Используют для
- 11. окислительные свойства – атомы С принимают четыре электрона, приобретают при этом степень окисления -4 восстановительные свойства
- 12. Окислительные свойства 1.При нагревании углерод соединяется с кислородом, образуя оксид углерода (IV), или углекислый газ: С
- 13. Восстановительные свойства 1. При нагревании с водяным паром он вытесняет из воды водород: Н2O + С
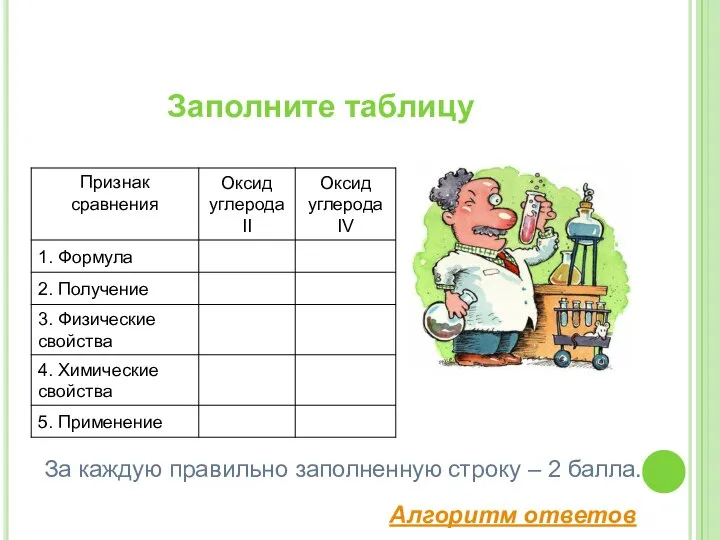
- 14. Заполните таблицу За каждую правильно заполненную строку – 2 балла. Алгоритм ответов
- 15. 2CO + O2 = 2CO2 + Q Fe2O3 + 3CO = 2Fe + 3CO2 CO +
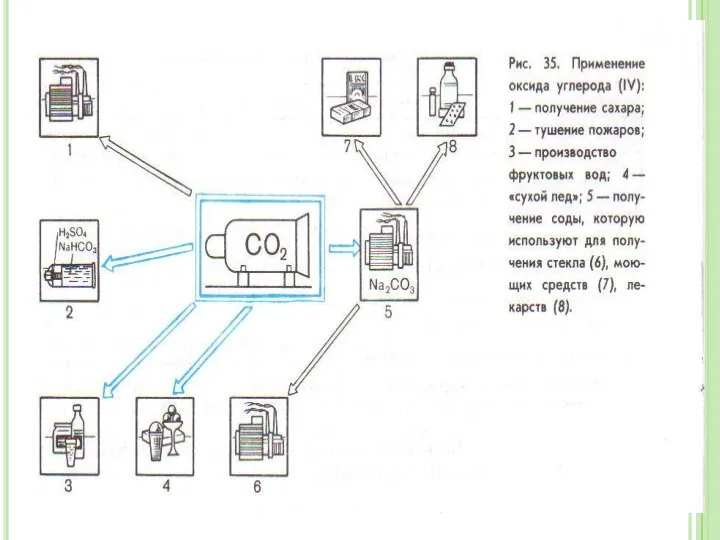
- 16. Углекислый газ – СО2 СО2 - оксид углерода (+4) , углекислый газ– бесцветный газ, слегка кисловатый
- 19. Угольная кислота H2CO3 Угольная кислота́ — слабая двухосновная кислота. В чистом виде не выделена. Образуется в
- 22. Скачать презентацию















 Эколого-геохимическая оценка состояния компонентов природной среды особо охраняемых территорий. Парк Смоленское Поозерье
Эколого-геохимическая оценка состояния компонентов природной среды особо охраняемых территорий. Парк Смоленское Поозерье Аттестационная работа. Мини-проекты на уроках химии. 8 класс
Аттестационная работа. Мини-проекты на уроках химии. 8 класс Химическая кинетика, химическое равновесие и катализ
Химическая кинетика, химическое равновесие и катализ Простой борный суперфосфат
Простой борный суперфосфат Майкл Фарадей и его открытия в электрохимии
Майкл Фарадей и его открытия в электрохимии Презентация по Химии "МЕТАЛЛИЧЕСКАЯ СВЯЗЬ" - скачать смотреть бесплатно
Презентация по Химии "МЕТАЛЛИЧЕСКАЯ СВЯЗЬ" - скачать смотреть бесплатно Презентация по Химии "Химический КВН" - скачать смотреть
Презентация по Химии "Химический КВН" - скачать смотреть  Current Condition(Revision C)
Current Condition(Revision C) Качество питьевой воды
Качество питьевой воды Галогены. Химические свойства галогенов
Галогены. Химические свойства галогенов Классификация и свойства природных энергоносителей
Классификация и свойства природных энергоносителей Материаловедение. Свойства материалов. (Тема 2)
Материаловедение. Свойства материалов. (Тема 2) Медико-биологическое значение неметаллов. Йод
Медико-биологическое значение неметаллов. Йод Титан. Технология титана
Титан. Технология титана Қышқылды-сілтілі тепетеңдік бұзылысының клиникалық биохимиясы
Қышқылды-сілтілі тепетеңдік бұзылысының клиникалық биохимиясы Алюминий и бор
Алюминий и бор Галогены
Галогены Внеурочная работа по химии. Краеведение
Внеурочная работа по химии. Краеведение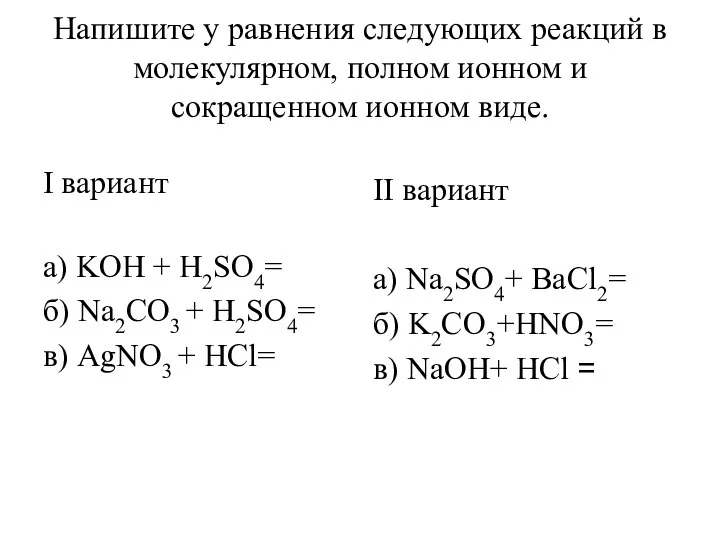 Уравнения реакций в молекулярном, полном ионном и сокращенном ионном виде
Уравнения реакций в молекулярном, полном ионном и сокращенном ионном виде Отчет по элективному курсу по химии Тема: «Окислительные свойства концентрированной серной и азотной кислот». Выполнила ученица
Отчет по элективному курсу по химии Тема: «Окислительные свойства концентрированной серной и азотной кислот». Выполнила ученица  Термопластичні Термореактивні
Термопластичні Термореактивні  Гидрогеохимия урана и тория
Гидрогеохимия урана и тория Непредельные углеводороды. Алкины. Уроки 25-26
Непредельные углеводороды. Алкины. Уроки 25-26 Химическая связь
Химическая связь Спирты. Классификация спиртов
Спирты. Классификация спиртов Комплексные соединения
Комплексные соединения Теоретические основы металлургии. Благородные металлы
Теоретические основы металлургии. Благородные металлы Цепная сополимеризация
Цепная сополимеризация