Содержание
- 2. КИСЛОТЫ– ЭТО СЛОЖНЫЕ ВЕЩЕСТВА, молекулы которых состоят из атомов водорода, способных замещаться на атомы металла, и
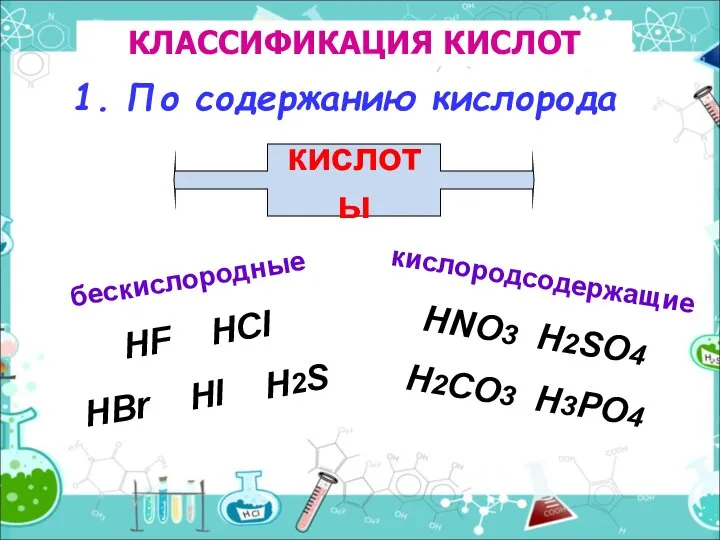
- 3. КЛАССИФИКАЦИЯ КИСЛОТ бескислородные HF HCl HBr HI H2S 1. По содержанию кислорода кислородсодержащие HNO3 H2SO4 H2CO3
- 4. 2. По количеству атомов водорода КИСЛОТЫ одноосновные HCl HNO3 двухосновные H2S H2SO4 трехосновные H3PO4
- 5. Химические свойства кислот 2NaOH + H2SO4 → Na2SO4 + 2H2O основание + кислота = соль +
- 6. Химические свойства кислот 3. Взаимодействие с оксидами: H2SO4 + CаO→ CаSO4 + H2O 2HCl + ZnO→
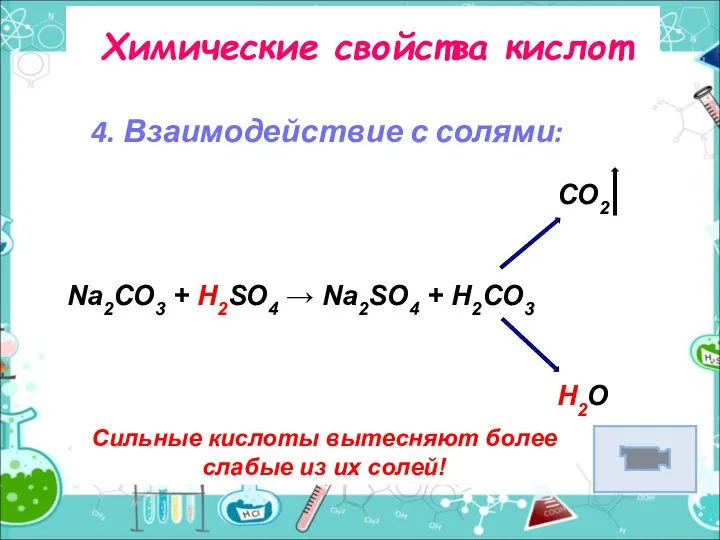
- 7. Химические свойства кислот 4. Взаимодействие с солями: Сильные кислоты вытесняют более слабые из их солей! CO2
- 8. Химические свойства кислот 5. Взаимодействие с металлами: Zn + 2HCl → ZnCl2 + H2 Cu
- 9. Способы получения кислот БЕСКИСЛОРОДНЫХ КИСЛОРОДСОДЕРЖАЩИХ Взаимодействие водорода с неметаллом Н2+Сl2=2НСl общий способ получения кислот К2SiO3+ 2НСl
- 10. Соляная кислота, находящаяся в желудке, помогает переваривать пищу Молочная кислота образуется в мышцах при физической нагрузке
- 11. КИСЛОТЫ ПРИМЕНЯЮТСЯ В МЕДИЦИНЕ Аскорбиновая, фолиевая, липоевая, ацетил- салициловая и другие
- 13. Скачать презентацию








 Белки, гормоны, антитела, ферменты
Белки, гормоны, антитела, ферменты Аммиак. Урок 58
Аммиак. Урок 58 Алкены – непредельные углеводороды
Алкены – непредельные углеводороды Презентация по Химии "Чипсы - вред или польза?" - скачать смотреть
Презентация по Химии "Чипсы - вред или польза?" - скачать смотреть  Кислород- история открытия, роль в природе
Кислород- история открытия, роль в природе Фракциялық айдау
Фракциялық айдау Аммиак. Физические и химические свойства. Получение и применение
Аммиак. Физические и химические свойства. Получение и применение Виды химической связи
Виды химической связи Бытовая химия в нашей жизни
Бытовая химия в нашей жизни Основные положения теории электролитической диссоциации
Основные положения теории электролитической диссоциации Колообіг нітрогену в природі
Колообіг нітрогену в природі Фенолы. Физические свойства
Фенолы. Физические свойства Презентация по Химии "СТРУКТУРНАЯ ФОРМУЛА КРАХМАЛА" - скачать смотреть
Презентация по Химии "СТРУКТУРНАЯ ФОРМУЛА КРАХМАЛА" - скачать смотреть  Періодична система Менделєєва. Елементи 6 групи
Періодична система Менделєєва. Елементи 6 групи Химия соединения железа
Химия соединения железа ПОЛЕЗНЫЕ ИЛИ ОПАСНЫЕ
ПОЛЕЗНЫЕ ИЛИ ОПАСНЫЕ Изотопы. Химические и физические свойства
Изотопы. Химические и физические свойства Общая геология. Породообразующие минералы
Общая геология. Породообразующие минералы Биологическая химия
Биологическая химия Полиазометины (полишиффовы основания)
Полиазометины (полишиффовы основания) Количество вещества (8 класс)
Количество вещества (8 класс) Тему «Соли». Нитрат серебра(I) AgNO3
Тему «Соли». Нитрат серебра(I) AgNO3 Будова електронних оболонок і властивості хіиічних елементів. (8 клас)
Будова електронних оболонок і властивості хіиічних елементів. (8 клас) Химия в сельском хозяйстве
Химия в сельском хозяйстве Биохимия, как наука
Биохимия, как наука Альдегиды и кетоны
Альдегиды и кетоны Химия
Химия Общая геохимия. Периодический закон Менделеева. Строение электронных оболочек. Геохимические классификации элементов
Общая геохимия. Периодический закон Менделеева. Строение электронных оболочек. Геохимические классификации элементов