Содержание
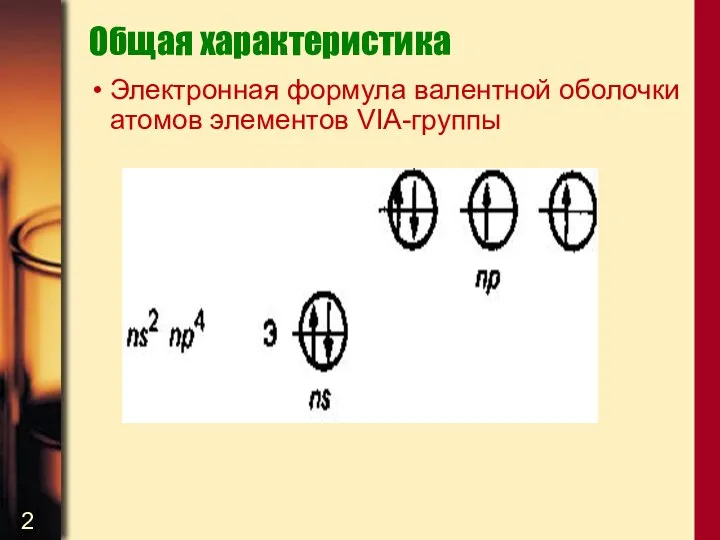
- 2. Общая характеристика Электронная формула валентной оболочки атомов элементов VIA-группы
- 3. В зависимости от состояния электронной оболочки проявляются разные степени окисления (СО). В соединениях с металлами и
- 4. Кислород (ОЭО = 3,5) Во фтороксиде F2O СО кислорода положительна и равна 4-2. С остальными элементами
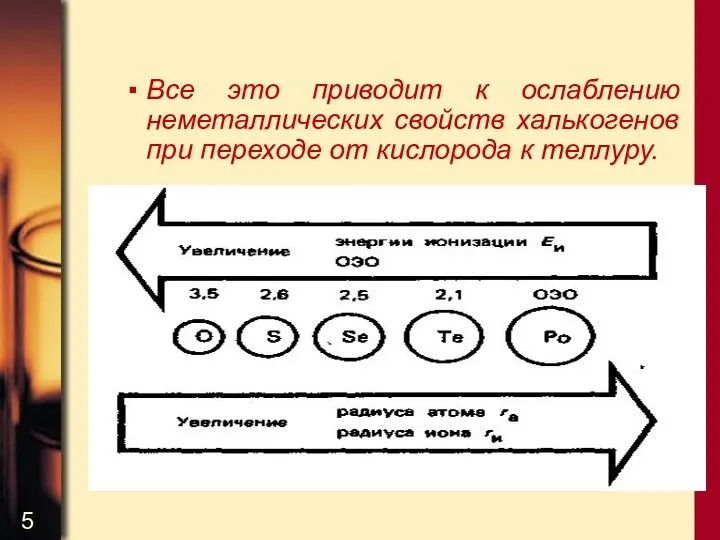
- 5. Все это приводит к ослаблению неметаллических свойств халькогенов при переходе от кислорода к теллуру.
- 6. В нормальных условиях водородные соединения Н2Э элементов VIA-группы, за исключением воды, — газы с очень неприятным
- 7. Сера, селен, теллур образуют два ряда кислотных оксидов: ЭО2 и ЭО3. Им соответствуют кислотные гидроксиды состава
- 8. Химические свойства кислорода. Кислород — самый распространенный элемент в земной коре (49,4 %) Элемент кислород существует
- 9. Озон — сильнейший окислитель. Окисляет металлы, бурно реагирует с органическими веществами, при низкой температуре окисляет соединения,
- 10. Кислород – один из самых активных неметаллов. Он образует соединения со всеми химическими элементами, кроме гелия,
- 11. Главная химическая функция кислорода в организме – окисление веществ, которое сопровождается выделением энергии. Для клетки очень
- 12. Сера и ее соединения. Сера входит в состав белков, липидов, также в состав некоторых витаминов и
- 13. Сероводород Очень ядовит, т.к. за счет связывания атомов меди в цитохромоксидазе блокирует перенос электронов с этого
- 14. Для оксида SO2, кислоты H2SO3 и ее солей характерна окислительно-восстановительная двойственность: 2SO2(восстановитель)+O2→2SO3 SO2(окислитель)+2H2S→3S+2H2O H2SO3(восстановитель)+Cl2+H2O→H2SO4+2HCl 2Na2SO3(восстановитель)+O2→2Na2SO4 H2SO3(окислитель)+2H2S→3S+H2O
- 15. Na2S2O3. – соль тиосерной кислоты H2S2O3. Тиосерная кислота неустойчива и при получении распадается: Na2S2O3+2HCl→H2S2O3+2NaCl H2S2O3→H2O+SO2+S. Тиосульфат-ион
- 16. Диоксид серы может присоединять кислород, переходя в триоксид серы: 2SO2+O2 ( Pt,t) → 2SO3. Растворение его
- 17. В разбавленных растворах серная кислота – окислитель за счет катионов водорода, которые восстанавливаются до элементарного водорода:
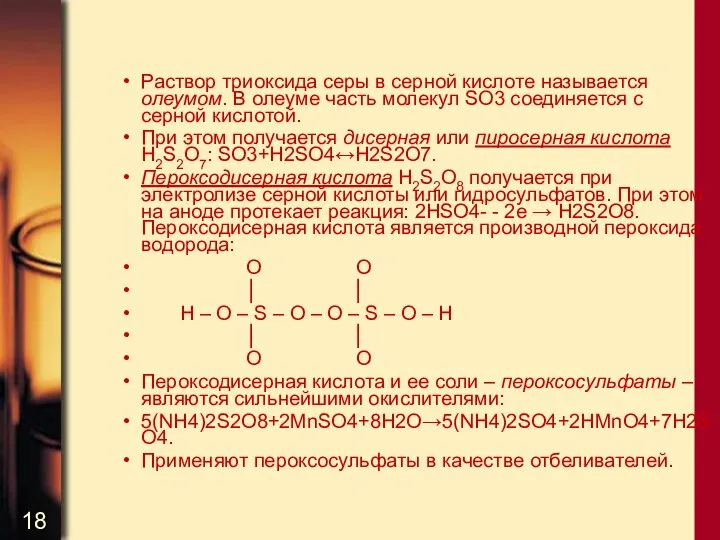
- 18. Раствор триоксида серы в серной кислоте называется олеумом. В олеуме часть молекул SO3 соединяется с серной
- 19. . Селен и теллур. По химическим свойствам селен и теллур похожи на серу. С водородом они
- 20. Соединения Se+4 и Те+4 проявляют преимущественно окислительные свойства, легко восстанавливаясь до свободных селена и теллура. Например:
- 21. SeO3 и ТеО3 – кислотные оксиды. Кислородные кислоты – селеновая H2SeO4 и теллуровая Н2ТеО4 – кристаллические
- 22. S -Макроэлемент [0,16%],. Суточная потребность 4-5 г. Входит в состав +++белков, гормонов, витаминов. +++тиоловых соединений, участвующих
- 23. ++++. Приём серы внутрь способствует рассасыванию нарывов, +++++ сера используется как слабительное средство. +++++В виде мазей
- 25. Кремний Вакантные орбитали способны к образованию дополнительного πp-d связей по донорно-акцепторному механизму, если у партнеров есть
- 26. Кремний В соответствии с правилом 8-N кристаллизуется в структуре алмаза Энергия связей меньше, чем в алмазе,
- 27. Элементы подгруппы Ge Они полные электронные и слоевые аналоги 2 особенности Валентной конфигурации ns2np2 предшествует полностью
- 28. Элементы подгруппы Ge Сверху вниз по группе металличность нарастает, но немонотонно (Ge близок к Si) В
- 29. Простые вещества Ge - структура типа алмаза, известны и фазы высокого давления Sn – тетрагональная решетка,
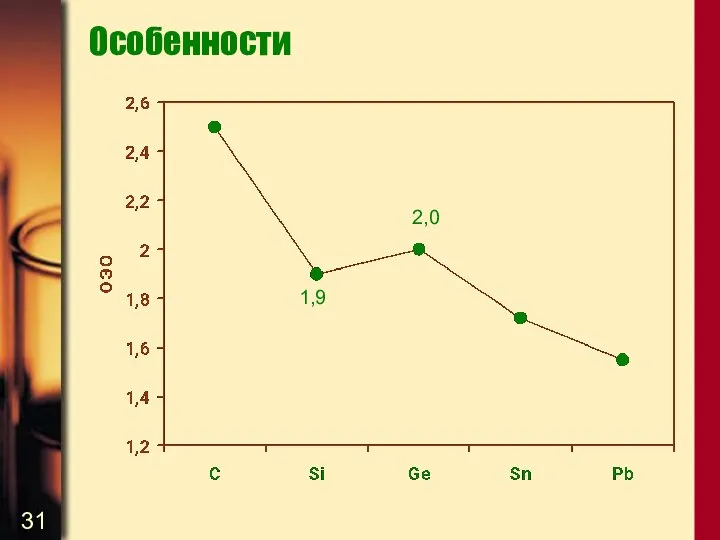
- 30. Особенности Итак, атомные радиусы в ряду C – Si – Ge – Sn – Pb увеличиваются
- 31. Особенности 2,0 1,9
- 32. Особенности В химических соединениях элементы IVA группы проявляют степени окисления –4, 0, +2, +4 Устойчивость соединений
- 33. Особенности При движении сверху вниз по группе происходит последовательный переход от неметаллов к металлам, окислительные свойства
- 34. Нахождение в природе и получение Содержание: С (0,048 %) в живых организмах: в организме человека массой
- 35. Нахождение в природе и получение Si самый распространенный после О элемент: 25,7 масc. %
- 36. Нахождение в природе и получение Ge и Sn (2,1·10–4 и 1,5·10-4 %) соответственно Pb (1,3·10–4 масс.
- 37. Получение Кремний SiCl4 + 2Zn (tºC) → Si + 2ZnCl2 а так же при термическом разложении
- 38. Получение Олово SnO2 + 2C (tºC) = Sn + 2CO↑ Свинец – обжиг галенита 2PbS +
- 39. Химические свойства Углерод взаимодействует из галогенов лишь с F2, не вступает в реакцию с N2 и
- 40. Химические свойства Аморфный уголь – восстановитель: ZnO + C (tºC) = Zn + CO↑ Для фуллеренов
- 41. Химические свойства Реакционная способность простых веществ в ряду Si – Ge – Sn – Pb возрастает
- 42. Химические свойства В ряду стандартных электродных потенциалов – Sn и Pb до водорода, Ge – после,
- 43. Химические свойства С HCl — при нагревании, PbCl2 малорастворим. В H2SO4 и концентрированной HNO3 пассивируется Мелкодисперсный
- 44. Водородные соединения Углеводороды — в курсе органической химии CH4 – карбид водорода: ОЭО (C = 2,6,
- 45. Водородные соединения Водородные соединения Si, Ge, Sn, Pb – силаны, германы, станнаны, плюмбаны Силаны и германы
- 46. Водородные соединения ЭН4 — тетраэдры В ряду СН4 – SiH4 – GeH4 – SnH4 возрастают Tпл.
- 47. Водородные соединения Возрастание атомного радиуса сверху вниз создает возможность повышения к.ч. и образования промежуточных соединений Реакционная
- 48. Водородные соединения Хлорирование SiH4 и SnH4 интенсивно протекает и в темноте, метана – на свету SiH4
- 49. Кислородные соединения Элементы IVА группы проявляют степени окисления +2 и +4 CO и СО2, неустойчивый С3О2
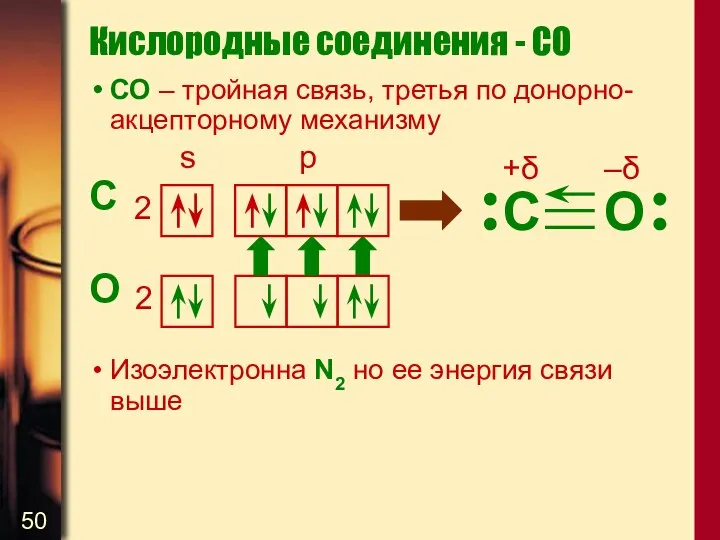
- 50. СО – тройная связь, третья по донорно-акцепторному механизму C O Изоэлектронна N2 но ее энергия связи
- 51. Кислородные соединения - CO Молекула СО диамагнитна. Сочетает свойства донора и акцептора (наличие е- пары на
- 52. Кислородные соединения - CO Это несолеобразующий оксид, формиаты образуются при 100–130ºС, р = 5атм с расплавленными
- 53. Кислородные соединения – CO2 O = C = O - линейная молекула 2σ – связи С
- 54. Кислородные соединения – CO2 Молекула неполярная => мало растворим в H2O Химически инертен, высокая энергия связи
- 55. Кислородные соединения – CO2 Кислотный оксид: CaO + CO2 → CaCO3 Ca(OH)2 + CO2 → CaCO3
- 56. Кислородные соединения – H2CO3 H2CO3 – слабая и неустойчивая кислота, в свободном виде из водных растворов
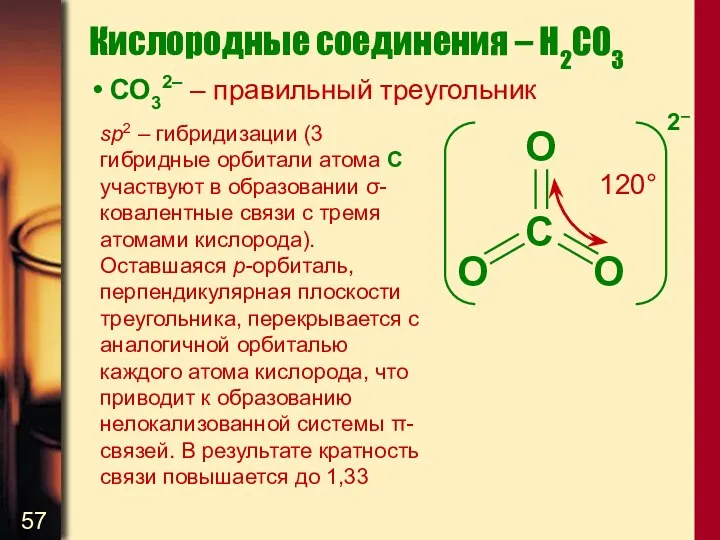
- 57. Кислородные соединения – H2CO3 СО32– – правильный треугольник sp2 – гибридизации (3 гибридные орбитали атома С
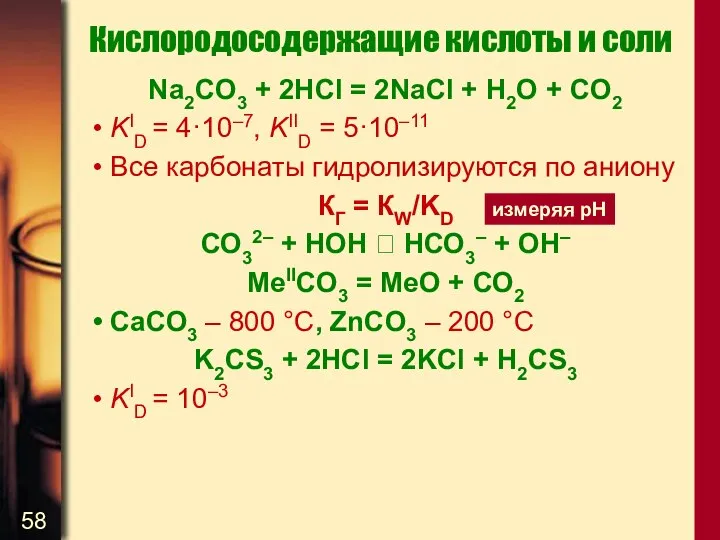
- 58. Кислородосодержащие кислоты и соли Na2CO3 + 2HCl = 2NaCl + H2O + CO2 KID = 4·10–7,
- 59. Кислородосодержащие кислоты и соли Пероксомоноугольная H2CO4 Пероксодиугольная H2C2O6 O = C O – H O –
- 60. Кислородосодержащие кислоты и соли Na2C2O6 + 2H2O = 2NaHCO3 + H2O2 Na2C2O6 + H2SO4 = Na2SO4
- 61. Кислородные соединения – H2CO3 Донорные свойства СО32– – в реакциях образования комплексов с переходными металлами, когда
- 62. Кислородные соединения Si От С к Si уменьшается прочность кратной связи Э – О и увеличивается
- 63. Кислородные соединения Si SiO2 – при обычных температурах и давлениях – кварц, тридимит, кристобалит Все построены
- 64. Кислородные соединения Si
- 65. Кислородные соединения Si Взаимные переходы между различными модификациями SiO2 требуют разрыва связи Si – O –
- 66. Кислородные соединения Si SiO2 проявляет кислотные свойства с растворами и расплавами щелочей, основными оксидами и карбонатами:
- 67. Кислородные соединения Si H4SiO4 – не выделена, т.к. при концентрировании претерпевает поликонденсацию. Слабая кислота Na2SiO3 +
- 68. Кислородные соединения Si В H2O растворимы только силикаты щелочных металлов и аммония, в растворе гидролизируются, формально:
- 69. Кислородные соединения Ge, Sn, Pb Сверху вниз с увеличением размера Э+4 их к.ч. в ряду диоксидов
- 70. Кислородные соединения Ge, Sn, Pb GeO2 – окисление Ge + O2 или обезвоживание гидратов. Много аналогий
- 71. Кислородные соединения Ge, Sn, Pb Диоксиды GeO2, SnO2 обладают слабыми окислительными свойствами ЭO2 + 2C (tºC)
- 72. Кислородные соединения Ge, Sn, Pb В H2O, разбавленных кислотах HCl, HNO3, H2SO4 и щелочах не растворяются.
- 73. Кислородные соединения Ge, Sn, Pb Еще известны смешанные оксиды Sn3O4, Pb3O4 3PbO2 (300-500 °С) = Pb3O4
- 74. Кислородные соединения Ge, Sn, Pb Состав высших гидрооксидов не соответствует H2ЭO3 или Э(OH)4. Это ЭО2∙xH2O Свойства
- 75. Кислородные соединения Ge, Sn, Pb Получают сплавлением Na2CO3 + GeO2 = Na2GeO3 + CO2↑ 2CaO +
- 76. Кислородные соединения Ge, Sn, Pb При гидролизе SnCl4 в присутствии NH3 образуется гидрат SnO2∙nH2O. Свежеполученный осадок
- 77. Соединения Э(II) Все элементы в степени окисления +2 обладают неподеленной электронной парой, которая обуславливает их стереохимию
- 78. Оксиды (II) GeO2 + Ge = 2GeO Склонен к диспропорционированию, на воздухе медленно окисляется до GeO2
- 79. Оксиды (II) SnO имеет несколько кристаллических модификаций. Это типичное амфотерное соединение. В к-тах – соли и
- 80. Оксиды (II) Для PbO – кристаллические формы: красная тетрагональная (глет) и желтая ромбическая (массикот) PbO +
- 81. Оксиды (II) Восстановительные свойства соединений слабеют в рядах Ge(II) – Sn(II) – Pb(II) Ge(II) и Sn(II)
- 82. Галогениды Типа СHal4 – для всех галогенов, неполярные соединения, тетраэдрические молекулы ССl4 – не смешивается с
- 83. Галогениды SiF4 + (n+2)H2O = H2SiF6 + SiO2∙nH2O↓ + 2HF Частично гидролизируется, а частично реагирует с
- 84. Галогениды Дигалогениды диспропорционируют 2GеHal2 Ge + GeHal4 SnCl2 – не диспропорционирует, но является сильным восстановителем
- 85. Галогениды Изменение стабильности 2-х степеней окисления: Si – диспропорционируют и SiO, и SiHal2 Ge – GeO
- 86. Галогениды Э+4 – основные свойства выражены слабо, ЭHal4 склонны к глубокому гидролизу ЭHal4 + 6H2O =
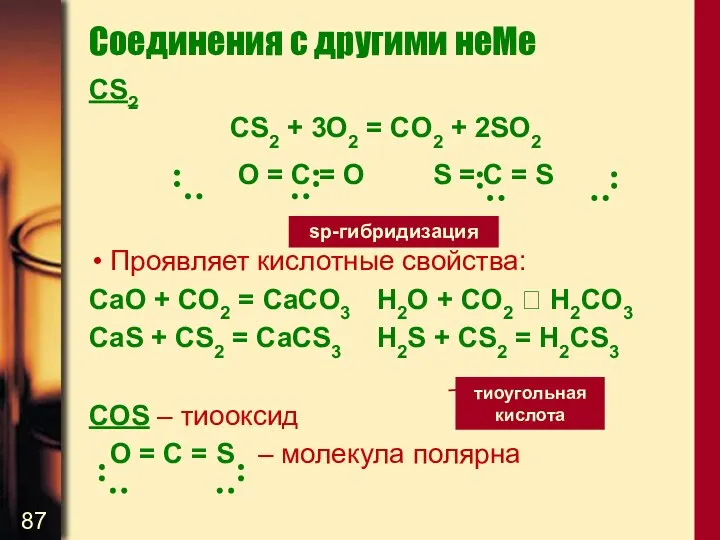
- 87. Соединения с другими неМе CS2 CS2 + 3O2 = CO2 + 2SO2 О = С =
- 88. Соединения с другими неМе SiC – карборунд
- 89. Соединения с азотом электрическая дуга – (CN)2 Здесь нечетное число вал. электронов •C ≡ N мономер
- 90. Соединения с азотом Существуют смешанные галогенцианы ClCN + 2NaOH NaCl + NaCNO + H2O H
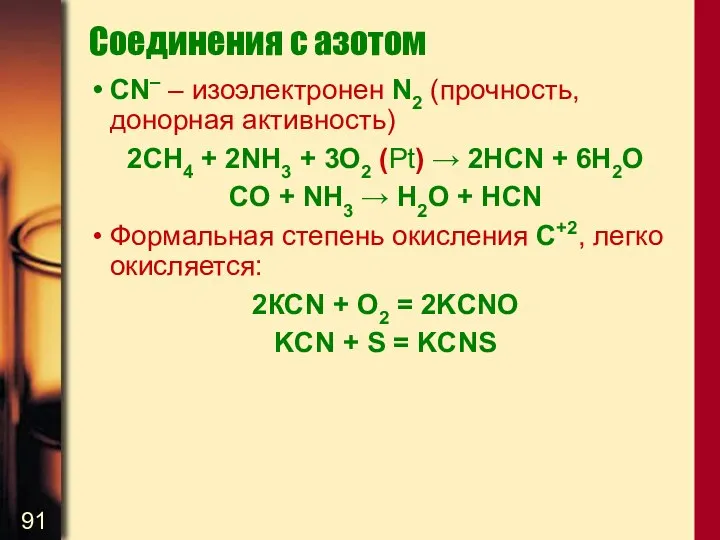
- 91. Соединения с азотом CN– – изоэлектронен N2 (прочность, донорная активность) 2CH4 + 2NH3 + 3O2 (Pt)
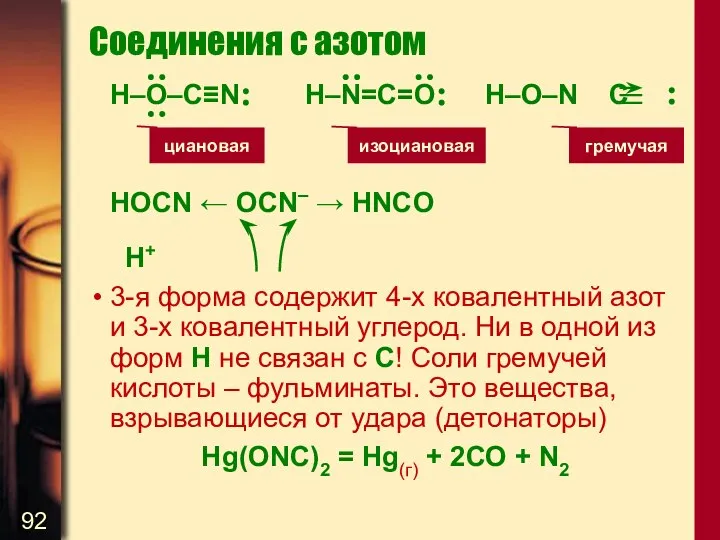
- 92. Соединения с азотом H–O–C≡N H–N=C=O H–O–N C HOCN ← OCN– → HNCO H+ 3-я форма содержит
- 94. Скачать презентацию

















![S -Макроэлемент [0,16%],. Суточная потребность 4-5 г. Входит в состав +++белков,](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396404/slide-21.jpg)































































 Контрольная работа по химическим реакциям
Контрольная работа по химическим реакциям Презентация по Химии "Алотропія карбону" - скачать смотреть
Презентация по Химии "Алотропія карбону" - скачать смотреть  Закономерности процессов тепло- и газообмена на пожаре
Закономерности процессов тепло- и газообмена на пожаре Смещение химического равновесия. Принцип Ле Шателье-Брауна
Смещение химического равновесия. Принцип Ле Шателье-Брауна Алкадиены
Алкадиены Кислотно-основное титрование в неводных средах
Кислотно-основное титрование в неводных средах Азот и фосфор
Азот и фосфор Производство аммиака
Производство аммиака Е-числа в школьном буфете
Е-числа в школьном буфете Спирты. Классификация спиртов
Спирты. Классификация спиртов Строение, реакционные способности и методы синтеза алкадиенов
Строение, реакционные способности и методы синтеза алкадиенов Презентация по Химии "Массовая доля вещества в растворе" - скачать смотреть
Презентация по Химии "Массовая доля вещества в растворе" - скачать смотреть  Абсорбционная осушка газа
Абсорбционная осушка газа Строение атома
Строение атома Презентация по химии Такой разный песок
Презентация по химии Такой разный песок  История одного металла. Медь и её сплавы.
История одного металла. Медь и её сплавы.  Применение центрифугирования
Применение центрифугирования Решение заданий ЕГЭ на составление окислительно-восстановительных реакций
Решение заданий ЕГЭ на составление окислительно-восстановительных реакций Лёгкие металлы
Лёгкие металлы Полімери. Поліетилен.
Полімери. Поліетилен.  Вещества и физические тела
Вещества и физические тела Производные углеводородов с одновалентной функцией
Производные углеводородов с одновалентной функцией Реакцияға қабілетті олигомерлердің мономерлерге қарағанда артықшылығы
Реакцияға қабілетті олигомерлердің мономерлерге қарағанда артықшылығы Азотсодержащие соединения. (Лекция 13)
Азотсодержащие соединения. (Лекция 13) Классификация металлов
Классификация металлов Твердые растворы Zn1,92-2хMg0,08Mn2xSiO4 и Zn1,76-2хMg0,24Mn2xSiO4: синтез и спектроскопические свойства
Твердые растворы Zn1,92-2хMg0,08Mn2xSiO4 и Zn1,76-2хMg0,24Mn2xSiO4: синтез и спектроскопические свойства Исследование орехов мендаля на содержание цианид-ионов
Исследование орехов мендаля на содержание цианид-ионов Модуль Химия на кухне. Углеводы
Модуль Химия на кухне. Углеводы