Содержание
- 2. Атомы благородных газов (инертных) имеют завершённый (устойчивый) внешний энергетический уровень. Атомы других элементов пытаются приобрести конфигурацию
- 3. Химическая связь – это силы взаимодействия, которые соединяют отдельные атомы в молекулы, ионы, кристаллы
- 4. Число общих электронных пар, т.е. число ковалентных химических связей, которые данный атом образует с другими атомами,
- 5. У элементов главных подгрупп это электроны внешнего энергетического уровня. Они расположены дальше от ядра и менее
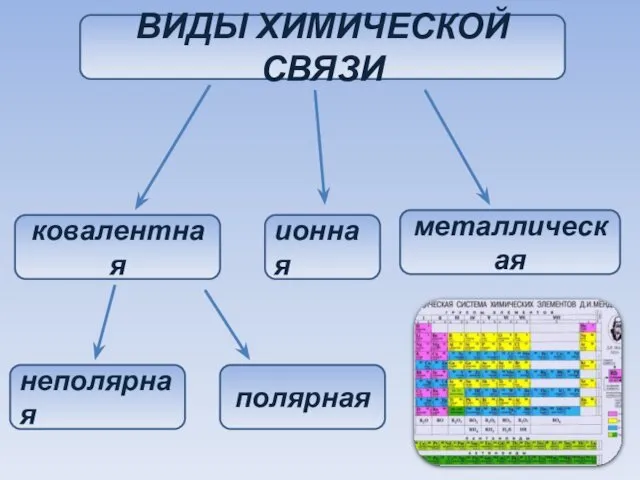
- 6. ВИДЫ ХИМИЧЕСКОЙ СВЯЗИ ковалентная ионная металлическая неполярная полярная
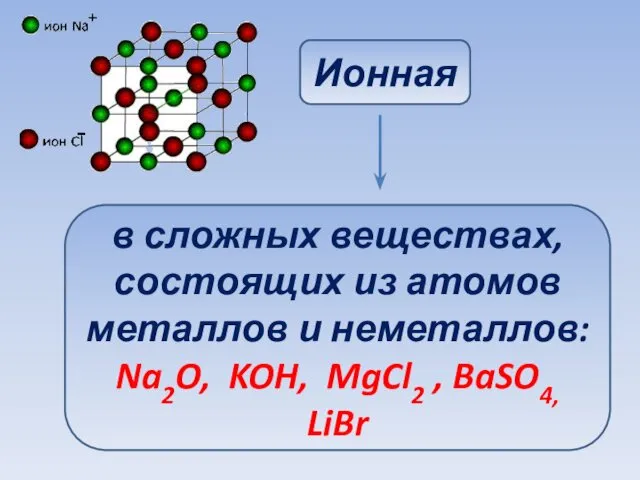
- 7. Ионная в сложных веществах, состоящих из атомов металлов и неметаллов: Na2O, KOH, MgCl2 , BaSO4, LiBr
- 9. 2Na0+O0→Na+2O2- 3K0+N0→K+N3- Al0+3F0→Al3+F-
- 10. Al Na Ba Fe Mg Металлическая – в простых веществах-металлах
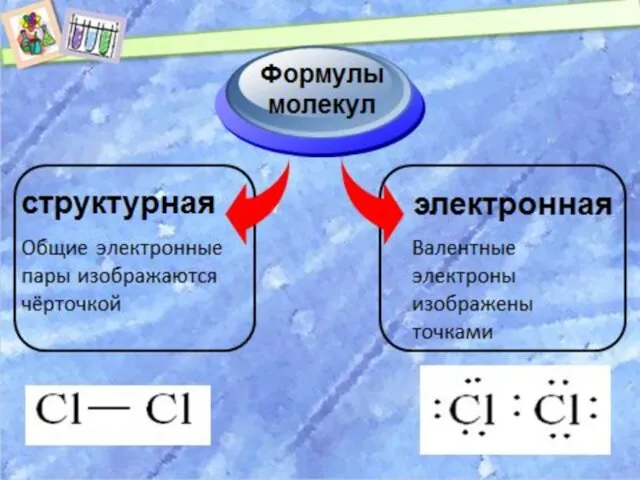
- 12. Химическая связь, возникающая в результате образования общих электронных пар, называют атомной или ковалентной
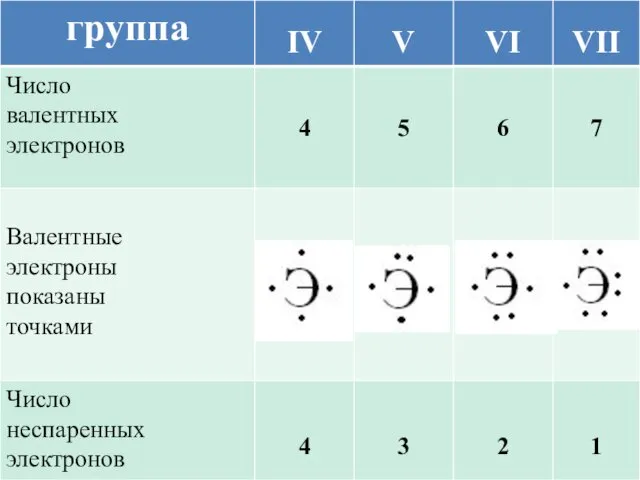
- 13. В образовании ковалентной связи принимают участие неспаренные валентные электроны атома, которые располагаются на внешнем уровне по
- 14. Число неспаренных электронов = 8 – (минус) № группы элемента
- 17. Электроотрицательность – это способность атома химического элемента притягивать к себе общие электронные пары
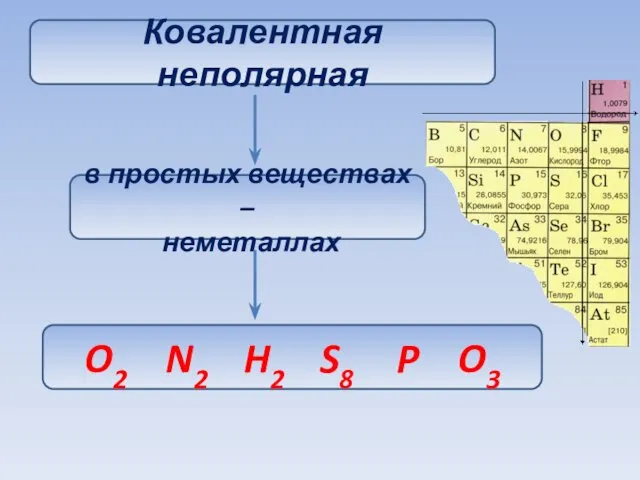
- 18. Ковалентная неполярная связь - – это разновидность ковалентной связи, которая образуется между атомами с одинаковой электроотрицательностью
- 19. Ковалентная неполярная в простых веществах – неметаллах O2 N2 H2 S8 P O3
- 22. Ковалентная полярная связь - – это разновидность ковалентной связи, которая образуется между атомами с одинаковой электроотрицательностью
- 23. Ковалентная полярная в сложных веществах, состоящих из атомов разных неметаллов: НСl N2O5 SF6 H3BO3 Р2О5
- 27. ТРЕНИРОВОЧНЫЙ ТЕСТ (САМОПРОВЕРКА) 1. В каком ряду находятся вещества только с ковалентной связью? Выписать и указать:
- 28. H2S N2 LiCl BaO Ca(NO3)2 Pb F2 Определите вид химической связи в каждом из данных соединений
- 29. В каких соединениях ионный тип связи NaCL CO2 ALBr3 H2O MgO HNO3
- 30. Из перечня веществ выберите формулы с ковалентной неполярной связью Cl2 CO2 Mg H2O O3 N2
- 31. Какие соединения имеют ковалентно - полярный тип связи CaO NH3 CL2 HBr KCL CH4
- 32. При выполнении конспекта, все задания на самопроверку записать в тетрадь!
- 34. Скачать презентацию





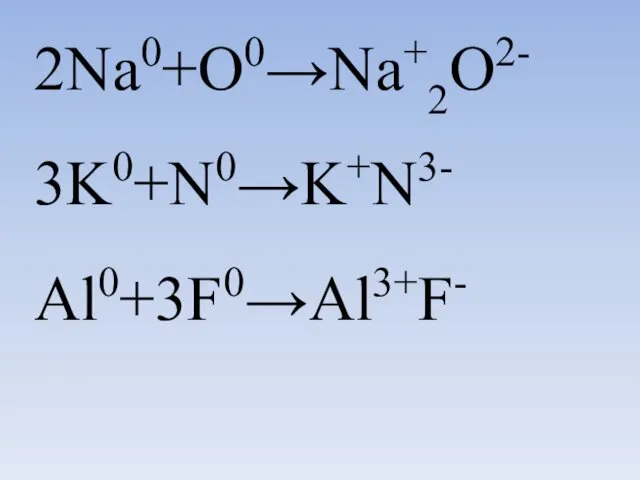




















 Строение алканов. Физические и химические свойства алканов. Получение алканов
Строение алканов. Физические и химические свойства алканов. Получение алканов Основания – сложные вещества. (11 класс)
Основания – сложные вещества. (11 класс) Неметаллы 9 класс
Неметаллы 9 класс Индикаторная бумага
Индикаторная бумага Синтез 2,4-диметил-3,5-ди(этоксикарбонил)пиррола
Синтез 2,4-диметил-3,5-ди(этоксикарбонил)пиррола Биосинтез ДНК
Биосинтез ДНК Комплексиметрическое титрование. (Лекция 12)
Комплексиметрическое титрование. (Лекция 12) Лекция 6. Химическая кинетика
Лекция 6. Химическая кинетика Определение качественного состава минеральных вод
Определение качественного состава минеральных вод Аттестационная работа. Программа внеурочной деятельности по химии “Занимательная химия”. (8 класс)
Аттестационная работа. Программа внеурочной деятельности по химии “Занимательная химия”. (8 класс) Тест по химии
Тест по химии «Системно – деятельностный подход как механизм реализации ФГОС нового поколения» обучающий семинар МБОУ «СОШ №15», п.Аршан – 2015г
«Системно – деятельностный подход как механизм реализации ФГОС нового поколения» обучающий семинар МБОУ «СОШ №15», п.Аршан – 2015г Атомы и молекулы. Простые и сложные вещества. 8 класс
Атомы и молекулы. Простые и сложные вещества. 8 класс Химические элементы и организм человека
Химические элементы и организм человека Занятие по познавательному развитию на тему: «Где спрятался воздух?» в средней группе.
Занятие по познавательному развитию на тему: «Где спрятался воздух?» в средней группе.  Регуляция и патология липидного обмена
Регуляция и патология липидного обмена Stereoselective total syntheses of guanacastepenes N and O
Stereoselective total syntheses of guanacastepenes N and O Биохимические аспекты рационального питания
Биохимические аспекты рационального питания Липиды. Химия липидов. Переваривание липидов в ЖКТ. Нарушение переваривания и всасывания
Липиды. Химия липидов. Переваривание липидов в ЖКТ. Нарушение переваривания и всасывания Химия S - элементов
Химия S - элементов Anti-food. Classification of food additives
Anti-food. Classification of food additives Щелочной металл натрий
Щелочной металл натрий Исследование остаточной концентрации моющих средств на посуде
Исследование остаточной концентрации моющих средств на посуде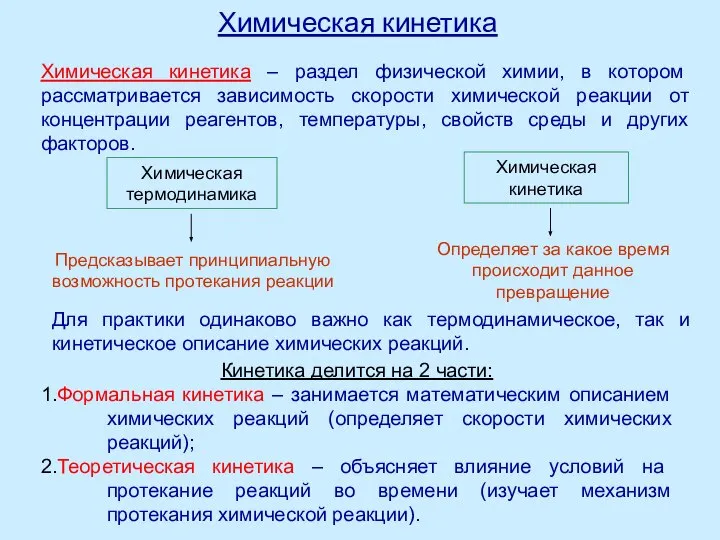 Химическая кинетика
Химическая кинетика Хімічні волокна
Хімічні волокна  Д. И. Менделеев
Д. И. Менделеев Сложные эфиры. Жиры. Мыла. (10 класс)
Сложные эфиры. Жиры. Мыла. (10 класс) Полипропилен. Молекулалық құрылымы
Полипропилен. Молекулалық құрылымы