Содержание
- 2. Основные понятия и определения Химическая кинетика – это раздел химии, изучающий скорости и механизмы хим. р-ций
- 3. Основные понятия и определения Механизм р-ции – Лимитирующая стадия –
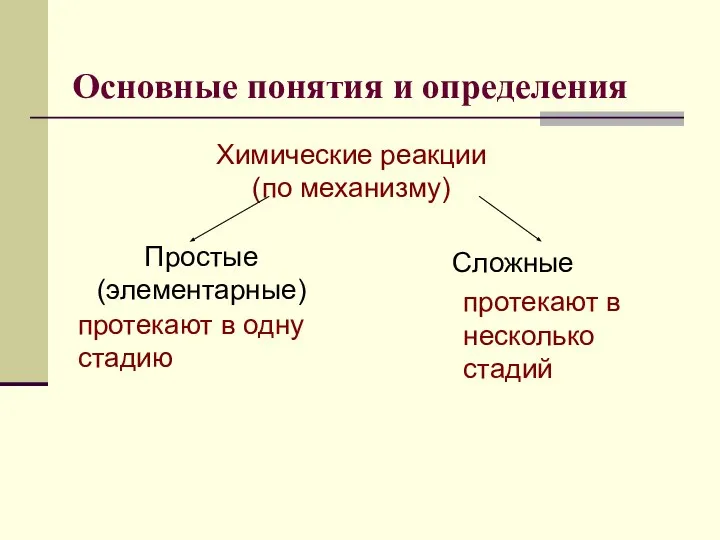
- 4. Основные понятия и определения Химические реакции (по механизму) Простые (элементарные) Сложные протекают в одну стадию протекают
- 5. Основные понятия и определения Молекулярность – Простые реакции мономолекулярные бимолекулярные тримолекулярные
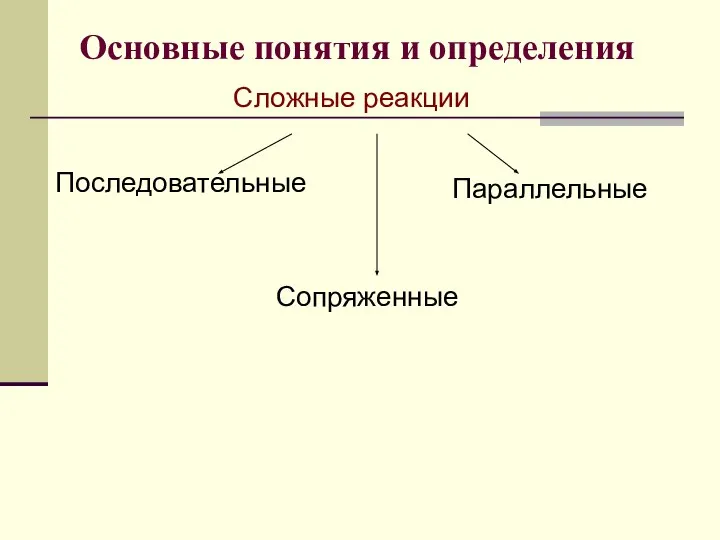
- 6. Основные понятия и определения Сложные реакции Последовательные Параллельные Сопряженные
- 7. Основные понятия и определения Цепные реакции (Н.Н. Семенов) 1 стадия: зарождение цепи 2 стадия: развитие цепи
- 8. Основные понятия и определения Элементарный акт хим. р-ции – СХР – СХР – изменение конц-ций реаг.
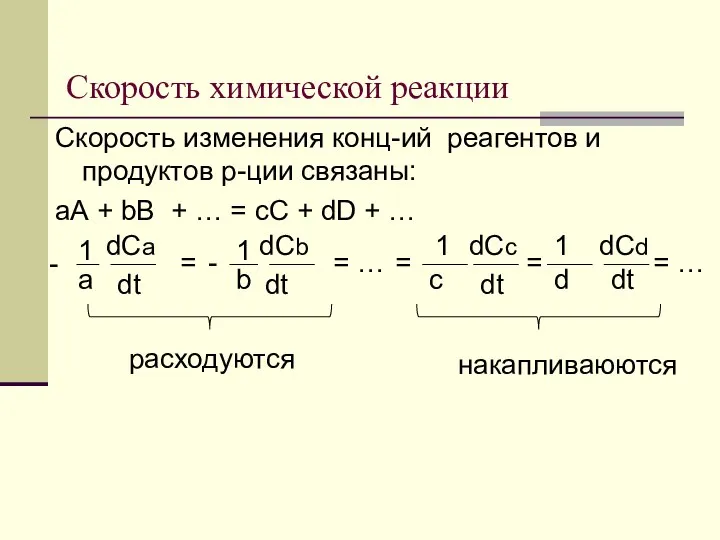
- 9. Скорость химической реакции Скорость изменения конц-ий реагентов и продуктов р-ции связаны: аА + bB + …
- 10. Факторы, влияющие на скорость химической реакции Скорость хим. р-ции зависит от: природы реагирующих в-в конц. реаг.
- 11. Зависимость СХР от концентрации реагентов 1867 г. Гульдберг и Вааге Закон действующих масс СХР прямо пропорциональна
- 12. Зависимость СХР от концентрации aA + bB = cC + dD Применим к р-ции ЗДМ и
- 13. Константа скорости химической реакции k - константа скорости хим. р-ции Физический смысл k то k =
- 14. Зависимость скорости от температуры 1884 г. Вант-Гофф Эмпирическое правило: Повышение температуры на 10о увеличиваетет скорость гомогенной
- 15. Теория активных столкновений Для протекания р-ции необходимо: столкновение молекул наличие у молекул достаточной Е благоприятная ориентация
- 16. Энергия активации Еа – это избыточная Е, кот. должны обладать молекулы, чтобы между ними произошло взаим-ие.
- 17. Энергия активации Уравнение Аррениуса (1889 г.) k = kо∙ е -Еа/RT
- 18. Расчет энергии активации Ea для многих р-ций изм-ся в пределах от 50 до 250 кДж/моль. Если
- 19. Катализ Катализ – это явление измения СХР при участии катализатора. Катализаторы – в-ва, изменяющие СХР, но
- 21. Скачать презентацию















 Цинк. Знаходження в періодичній системі і основні характеристики
Цинк. Знаходження в періодичній системі і основні характеристики Диктант: название алканов
Диктант: название алканов Тіршілік процесіне қатысатын гетерофункционалды қосылыстар
Тіршілік процесіне қатысатын гетерофункционалды қосылыстар Реферат по химии на тему
Реферат по химии на тему Кольорові метали
Кольорові метали  Строение атома
Строение атома Органические вещества в быту
Органические вещества в быту  Типы изомерии
Типы изомерии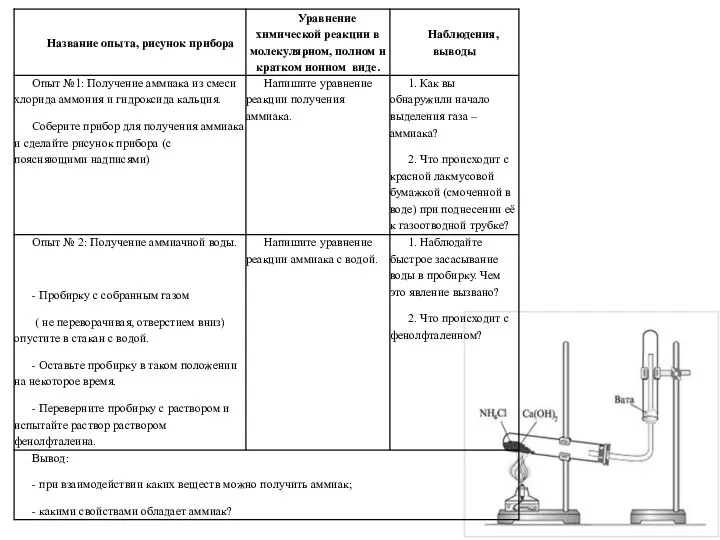 Получение аммиака и изучение его свойств
Получение аммиака и изучение его свойств ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ  Підготував: учень 10-Б класу Федоренко Роман
Підготував: учень 10-Б класу Федоренко Роман  Мило. Мийні засоби
Мило. Мийні засоби Вещества и их свойства
Вещества и их свойства Натрій. Знаходження в періодичній системі і основні характеристики
Натрій. Знаходження в періодичній системі і основні характеристики Гидроксид лития ( LiOH)
Гидроксид лития ( LiOH) Материалы с малой плотностью
Материалы с малой плотностью Формирование понятий химии высокомолекулярных соединений
Формирование понятий химии высокомолекулярных соединений Понятие о простых формах. Номенклатура простых форм высшей категории. Простые формы кристаллов высшей категории
Понятие о простых формах. Номенклатура простых форм высшей категории. Простые формы кристаллов высшей категории Композитные материалы
Композитные материалы Пиридин. Методы получения пиридина. Химические свойства. Биологически активные производные. (Леекция 5)
Пиридин. Методы получения пиридина. Химические свойства. Биологически активные производные. (Леекция 5) Эвапориты. Химические осадки из ионных растворов
Эвапориты. Химические осадки из ионных растворов Витамины
Витамины Буровые технологические жидкости для бурения и крепления горизонтальных скважин
Буровые технологические жидкости для бурения и крепления горизонтальных скважин Фосге́н (дихлорангидрид угольной кислоты)
Фосге́н (дихлорангидрид угольной кислоты) Йододефицит. Выполнила Кириллова Анастасия.
Йододефицит. Выполнила Кириллова Анастасия.  Фосфор
Фосфор Презентация по Химии "Теория нормализации" - скачать смотреть бесплатно
Презентация по Химии "Теория нормализации" - скачать смотреть бесплатно Химические сюжеты в научно-фантастических произведениях
Химические сюжеты в научно-фантастических произведениях