Содержание
- 2. ХИМИЧЕСКАЯ СВЯЗЬ Теория химической связи – центральный вопрос современной химии. Без него нельзя понять причин многообразия
- 3. Рассмотрение химической связи требует ответа на три извечных вопроса: Что? Почему? Как ? Что такое химическая
- 4. 1. ЧТО ТАКОЕ ХИМИЧЕСКАЯ СВЯЗЬ? «Под химической связью следует понимать силу, удерживающую атомы друг около друга
- 5. 2. ПОЧЕМУ ОБРАЗУЕТСЯ ХИМИЧЕСКАЯ СВЯЗЬ? Почему большинство элементов (кроме благородных газов) обычно существуют в природе не
- 6. 2. ПОЧЕМУ ОБРАЗУЕТСЯ ХИМИЧЕСКАЯ СВЯЗЬ? Ответ вытекает из следующего термодина-мического принципа: «минимуму энергии системы соответствует максимум
- 7. 2. ПОЧЕМУ ОБРАЗУЕТСЯ ХИМИЧЕСКАЯ СВЯЗЬ? Таким образом, образование химических соединений происходит потому, что возникает энергетическое состояние
- 8. 3. КАК ОБРАЗУЕТСЯ ХИМИЧЕСКАЯ СВЯЗЬ, ИЛИ КАКОВА ПРИРОДА ХИМИЧЕСКОЙ СВЯЗИ ? Фундаментальная роль в образовании химических
- 9. У s- и p- элементов внешними электро-нами: … ns1-2 или …ns2np1-6 2. У d-элементов внешними ns-
- 10. В зависимости от характера распреде-ления электронной плотности между взаимодействующими атомами различают различные типы химической связи: ТИПЫ
- 11. ТИПЫ ХИМИЧЕСКОЙ СВЯЗИ Ионная Ковалентная Металлическая. ОСНОВНЫЕ ТИПЫ: 1. Водородная химическая связь. 2. Вандерваальсовы взаимодействия. КРОМЕ
- 12. С В О Й С Т В А Х И М И Ч Е С К
- 13. Ионная химическая связь представляет собой электростатическое взаимодействие отрицательно и положительно заряженных ионов в химическом соединении. Такая
- 14. НEНАПРАВЛЕННОСТЬ И НЕНАСЫЩАЕМОСТЬ ИОННОЙ СВЯЗИ. Распределение силовых полей двух разноименных ионов Каждый ион может притягивать к
- 15. Чисто ионной связи не существует. Можно лишь говорить о степени (доле) ионности связи. Для оценки способности
- 16. ВЫВОД. Связи ионными на 100% практически не бывают. РАЗНОСТЬ ЭО АТОМОВ И СТЕПЕНЬ ИОННОСТИ СВЯЗИ Разность
- 17. Li 0,98 Na 0,93 К 0,91 Rb 0,89 Be 1,5 Mg 1,2 Ca 1,04 Sr 0,99
- 18. Ковалентная связь – связь, образуемая парой электронов, распределенной (обобществленной) между двумя или большим числом атомов. Первую
- 19. Стремление атомов к достижению устойчивых электронных конфигураций, как в атомах благородных газов составляет суть положения, известного
- 20. ОБРАЗОВАНИЕ ОКТЕТА Cl· + ·Cl ׃ → ׃Cl ׃ Cl ׃ . . . . Na·
- 21. ТЕОРИИ ХИМИЧЕСКОЙ СВЯЗИ В современной теории химической связи для описания ковалентной связи и строения молекул используют
- 22. КОВАЛЕНТНАЯ СВЯЗЬ. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ Метод ВС основан на следующих идеях: 1. Химическая ковалентная связь возникает
- 23. 3. Согласно методу ВС атомы, вступающие в химическую связь, обмениваются между собой электронами, которые образуют связывающие
- 24. 2. Донорно-акцепторный: КОВАЛЕНТНАЯ СВЯЗЬ. МЕТОД ВАЛЕНТНЫХ СВЯЗЕЙ Существуют два принципиальных механизма образования ковалентной связи: 1. Обменный:
- 25. 1. Обменный механизм образования ковалентной связи В этом способе общая электронная пара образуется в результате перекрывания
- 26. МЕТОД ВС Перекрывание 1s – орбиталей двух атомов водорода схематически изображают так: Н Н Н :
- 27. ПРИМЕР: Рассмотрим образование иона аммония: NH3 + H+ → NH4+ H ׃ N ׃ + □
- 28. N 2S 2P H+ 1S 1S 1S 1S H H H Н+ + :NH3 → NH4+
- 29. СВОЙСТВА КОВАЛЕНТНОЙ СВЯЗИ 1. НАСЫЩАЕМОСТЬ 2. НАПРАВЛЕННОСТЬ 3. ПОЛЯРИЗУЕМОСТЬ НАСЫЩАЕМОСТЬ КОВАЛЕНТНОЙ СВЯЗИ. ВАЛЕНТНОСТЬ Вследствие насыщаемости ковалентной
- 30. Возбужденное состояние атома возникает в результате распаривания электронов и перехода их на свободные орбитали того же
- 31. Валентность определяемая числом имеющихся в атоме неспаренных электронов или образую-щихся при его возбуждении называется СПИНВАЛЕНТНОСТЬЮ. С
- 32. ВАЛЕНТНОСТЬ. Таким образом, суммарная валентность элемента равна числу неспаренных электронов (обменный механизм) плюс число связей, образованных
- 33. Полярность связи количественно оценивается дипольным моментом μ, который является произведением длины диполя l — расстояния между
- 34. Полярность молекулы, как и полярность связи, оценивают величиной дипольного момента μ: μ = q ∙ l
- 35. Дипольные моменты молекул μ, Кл • м
- 36. Кратность связи определяется числом общих электронных пар. Так кратность связи в молекуле хлороводорода (Н-Cl) равна одному,
- 37. КЛАССИФИКАЦИЯ КОВАЛЕНТНЫХ СВЯЗЕЙ ПО СПОСОБУ ПЕРЕКРЫВАНИЯ АО а) Связь, образованная перекрыванием АО по линии, соединяющей ядра
- 38. НАПРАВЛЕННОСТЬ СВЯЗЕЙ. СОСОБЫ ПЕРЕКРЫВАНИЯ АО σ-связь π-связь δ-связь s-s s-p p-p d-d p-p d-p d-d d-d-перекрывание
- 39. σ-связь π-связь Обычно σ-π-связи иллюстрируют на примере p-p-перекрывания Ось связи В связи с меньшим перекрыванием АО
- 40. ϭ- связь π-связи Молекула ацетилена линейна! 180о H − C ≡ C − H Ϭ- и
- 41. Гибридизация – смешение в процессе образования химической связи разных по форме и энергии АО (s-, p-,
- 42. Благодаря гибридизации достигается бо′льшая прочность химических связей! Гибридная sр - орбиталь асимметрична и сильно вытянута, по
- 43. sp2 – гибридизация ТИПЫ ГИБРИДИЗАЦИИ АО sp – гибридизация 120º (s +р)-орбитали две sр -орбитали (s+p+p)
- 44. sp3 – гибридизация CН4 Н2О NН3 О N C 104,50 107,30 Н-C-Н = 109,50 Н-О-Н =
- 45. ПРОСТРАНСТВЕННАЯ КОНФИГУРАЦИЯ МОЛЕКУЛ. Гибридизация АО определяет пространствен-ную конфигурацию молекул. Так, при sp-гибридизации образуются линейные молекулы, при
- 46. Лекция №8. ГИБРИДИЗАЦИЯ ВАЛЕНТНЫХ ОРБИТАЛЕЙ (s + р)-орбитали две sр-орбитали sp – гибридизация sр -гибридизация валентных
- 47. sp2-Гибридизация sр2-Гибридизация валентных орбиталей имеет место, например, в плоских молекулах (s+p+p) –орбитал и три sp2-орбитали ВCl3,
- 48. sp3-гибридизация Структура молекул СН4, Н2О и NН3 CН4 Н2О NН3 О N C 104,50 107,30 Н-C-Н
- 49. ТИПЫ ГИБРИДИЗАЦИИ АО И ФОРМА МОЛЕКУЛ
- 50. МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ. Основные положения метода МО: а) образование химических связей является результа-том перехода электронов с
- 51. г) распределение электронов по новым МО или энергетическим уровням производится в соответствии с принципом наименьшей энергии,
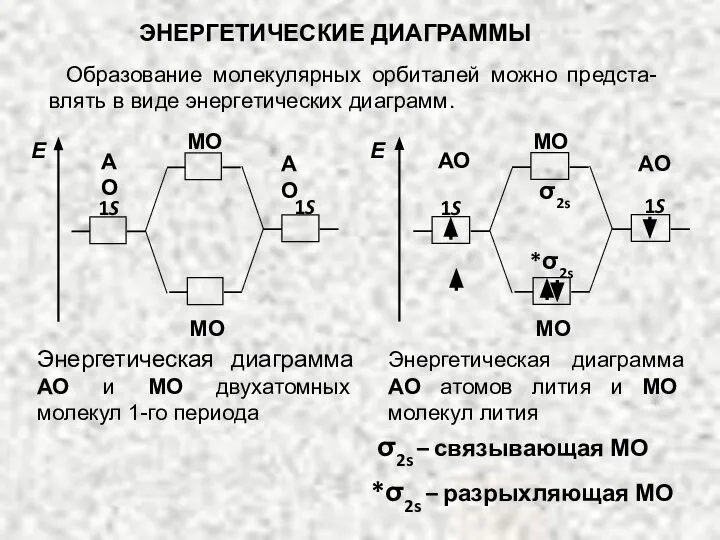
- 52. Энергетическая диаграмма АО и МО двухатомных молекул 1-го периода Энергетическая диаграмма АО атомов лития и МО
- 53. б) АО должны возможно полнее перекрываться; в) АО должны иметь одинаковую симметрию относительно межядерной оси. ЭНЕРГЕТИЧЕСКИЕ
- 54. По возрастанию энергии МО орбитали двухатомных молекул первого периода и начала второго периода (до N2) можно
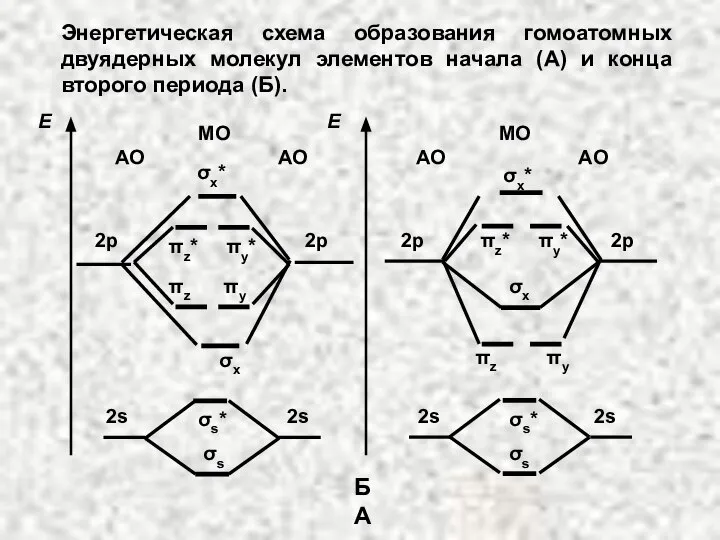
- 55. Энергетическая схема образования гомоатомных двуядерных молекул элементов начала (А) и конца второго периода (Б). МО АО
- 56. ПОРЯДОК СВЯЗИ = число связ. эл-ов – число разр. эл-ов 2 ПОРЯДОК СВЯЗИ N2 O2 σx*
- 57. ХИМИЧЕСКАЯ СВЯЗЬ ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
- 58. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Определить разность относительных электро-отрицательностей атомов для связей Н — О и О —
- 59. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Р е ш е н и е 1. По данным табл. ЭО вычисляем
- 60. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Объяснить механизм образования молекулы SiF4 и иона SiF62 ‾. Может ли существовать ион
- 61. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Р е ш е н и е 2(a). Электронная конфигурация атома кремния 1s22s22p63s23p2.
- 62. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Р е ш е н и е 2(б). Четыре неспаренных электрона возбужденного атома
- 63. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Р е ш е н и е 2(в). Углерод (1s22s22p2 ) может образовать,
- 64. Определите максимальную валентность кислорода и фтора. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Пример 3.
- 65. Кислород и фтор во всех соединениях проявляют постоянную валентность, равную двум для кислорода и единице для
- 66. Какую валентность проявляет хлора ? ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Пример 4.
- 67. Решение 4. Хлор проявляет переменную валентность 1, 3, 5, 7, так как на 3-м энергетическом уровне
- 68. Пример 5. Определите возможные валентности атома кобальта. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
- 69. Решение 5. Отсутствие неспаренных электронов у атома кобальта на внешнем 4-м энергетическом уровне, определяет его валентность
- 70. В возбужденном состоянии происходит рас-спаривание 4s-пары электронов и валентность кобальта может быть 2, 3, 4. ПРИМЕРЫ
- 71. Пример 6. Определите пространственную структуру молекулы H2S. Почему валентный угол чуть больше 90°? ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
- 72. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Н Н S х у z 920 3s Н 1s1 Н 1s1 S
- 73. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Пример 7. Вычислите дипольный момент молекулы HI, если длина диполя равна 0,09 •
- 74. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Пример 8. Одинаковая ли полярность молекул ВН3 и SbH3?
- 75. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Решение. Для оценки полярности молекулы используют величину электрического момента диполя молекулы μм, равную
- 76. Решение 8(а). Молекула ВН3 имеет плоскую треугольную форму (sp2-гибридизация). Гибридные связи направлены под углом 120°. Векторная
- 77. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Решение 8(б). Молекула SbH3 имеет пирамида-льную форму. Связи в молекуле SbH3 направлены от
- 78. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Пример 9. Какая из молекул В2 или С2 характеризуется более высокой энергией диссоциации
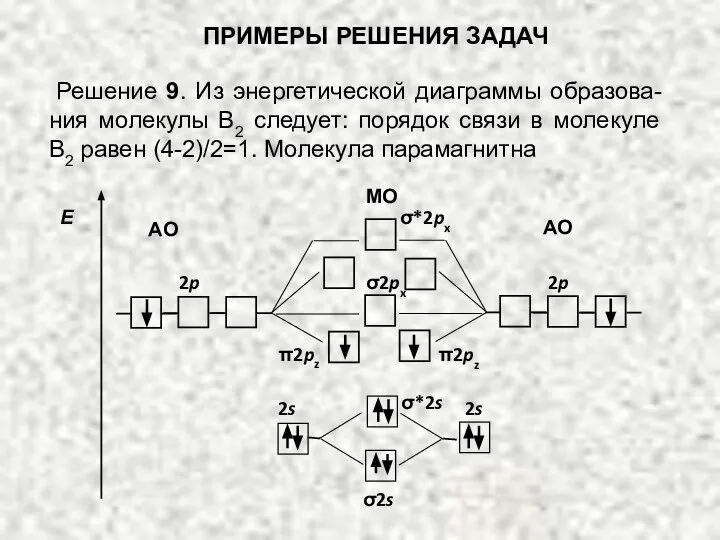
- 79. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ Решение 9. Из энергетической диаграммы образова-ния молекулы В2 следует: порядок связи в молекуле
- 80. ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ 2p АО АО МО Е 2p π2pz σ*2s π2pz σ2s 2s 2s σ2px
- 81. ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ
- 82. 236. Описать с позиций метода ВС электронное строение молекулы BF3 и иона BF4‾. 237. Сравнить способы
- 83. ИНДИВИДУАЛЬНЫЕ ЗАДАЧИ Задача 1: 1) покажите распределение валентных электронов по орбиталям для каждого атома в рассматриваемых
- 84. МНОГОВАРИАНТНЫЕ ЗАДАЧИ Задача 2: 1) напишите электронные формулы атомов, образующих данную молекулу; 2) нарисуйте энергетическую схему
- 85. Таблица исходных данных МНОГОВАРИАНТНЫЕ ЗАДАЧИ
- 86. МНОГОВАРИАНТНЫЕ ЗАДАЧИ Таблица исходных данных
- 88. Скачать презентацию


















































































 Сахароза
Сахароза Стеклообразное состояние полимеров. (Лекция 5)
Стеклообразное состояние полимеров. (Лекция 5) Применение 3D-принтеров для решения химических задач
Применение 3D-принтеров для решения химических задач Коллоидные растворы
Коллоидные растворы Простые вещества, металлы
Простые вещества, металлы Презентация по Химии "Спирты. Польза и вред" - скачать смотреть
Презентация по Химии "Спирты. Польза и вред" - скачать смотреть  Пресс - конференция «Карбоновые кислоты в природе, химические свойства, применение.»
Пресс - конференция «Карбоновые кислоты в природе, химические свойства, применение.» Тема уроку: Електричний струм в металах. Мета: ознайомити учнів із елементами класичної електронної теорії; з’ясувати при
Тема уроку: Електричний струм в металах. Мета: ознайомити учнів із елементами класичної електронної теорії; з’ясувати при Физико-химические методы анализа
Физико-химические методы анализа Ионообменная хроматография: классический и высокоэффективные методы
Ионообменная хроматография: классический и высокоэффективные методы Аттестационная работа. Исследование влияния питательных веществ на качество выгонки древесно-кустарниковых растений
Аттестационная работа. Исследование влияния питательных веществ на качество выгонки древесно-кустарниковых растений Типы изомерии
Типы изомерии Тема урока: Природный каучук.
Тема урока: Природный каучук. Атом құрылысы Сu. Биологиялық маңызы
Атом құрылысы Сu. Биологиялық маңызы Липиды растений и их обмен
Липиды растений и их обмен Органическая химия. История развития
Органическая химия. История развития Основные понятия и законы химии
Основные понятия и законы химии Катализ. Лекция 1
Катализ. Лекция 1 Біохімічний рівень організації
Біохімічний рівень організації Building blocks. Atoms. Elements. Structure of the atom
Building blocks. Atoms. Elements. Structure of the atom Сырьевая база парфюмерно-косметической промышленности
Сырьевая база парфюмерно-косметической промышленности Презентация Химия в криминалистике
Презентация Химия в криминалистике  Аминокислоты, пептиды, белки, нуклеиновые кислоты. Их биологическая роль
Аминокислоты, пептиды, белки, нуклеиновые кислоты. Их биологическая роль Серная кислота H2SO4
Серная кислота H2SO4 Элементы главной подгруппы VII группы Периодической системы Д.И. Менделеева
Элементы главной подгруппы VII группы Периодической системы Д.И. Менделеева Электростатические взаимодействия, как фактор, определяющий структуру и реакционную способность органических соединений
Электростатические взаимодействия, как фактор, определяющий структуру и реакционную способность органических соединений Гидролиз органических и неорганических соединений
Гидролиз органических и неорганических соединений Цікаві досліди з хімії
Цікаві досліди з хімії