Содержание
- 2. Что читать? Карапетьянц М. Х., Дракин С. И. Общая и неорганическая химия. Ахметов Н. С. Общая
- 3. Список сокращений и основных обозначений Выучить! Чупахин А. П. Химический процесс: энергетика и равновесие . Стр.
- 4. Примеры обозначений H - энтальпия A - работа с - теплоемкость ср - изобарная теплоемкость C
- 5. Изучили: Будем изучать: Строение вещества Статистическое состояние Процесс Движение
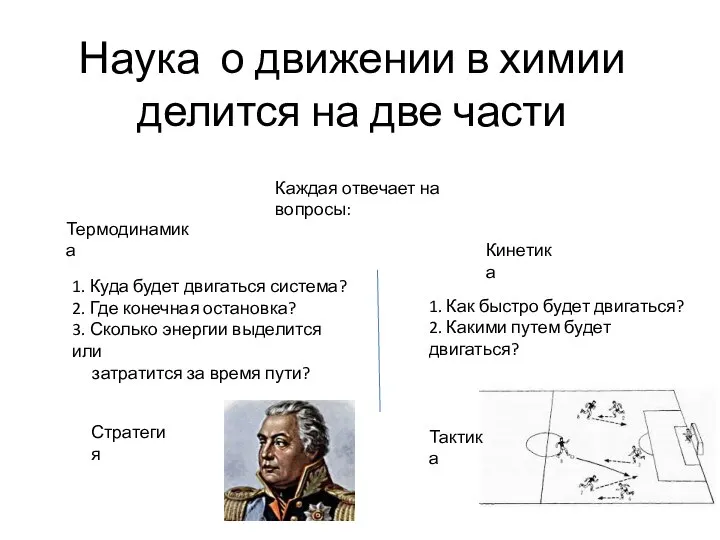
- 6. Наука о движении в химии делится на две части Термодинамика Кинетика 1. Куда будет двигаться система?
- 7. Термодинамика Отдел физики, изучающий теплоту и закономерности теплового движения. Николя́ Леона́р Сади́ Карно́ Nicolas Léonard Sadi
- 8. Химическая термодинамика рассматривает взаимосвязи между работой и энергией применительно к химическим превращениям.
- 9. Очень много определений
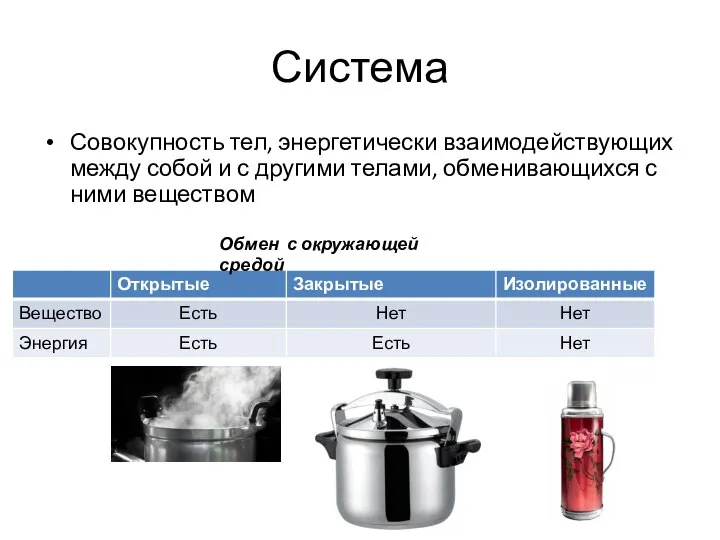
- 10. Система Совокупность тел, энергетически взаимодействующих между собой и с другими телами, обменивающихся с ними веществом Обмен
- 11. Система Гомогенные Гетерогенные Однородные Не однородные
- 12. Процессы Изотермические (T =const) Изохорические (V =const) Изобарические (P =const) Адиабатические (Q =const) Изолированная система
- 13. Процессы Обратимые процессы – процессы, в которых система возвращается в первоначальное состояние. Необратимые – когда система
- 14. Процессы Самопроизвольными называют такие процессы, которые протекают без внешнего воздействия, при постоянстве всех внешних условий. Равновесные
- 15. Функции Функции могут зависеть от пути процесса. Функции, которые зависят от начального и конечного состояний системы
- 16. Экстенсивные и интенсивные функции Экстенсивное свойство системы прямо пропорционально массе системы и обладает аддитивностью (можно складывать):
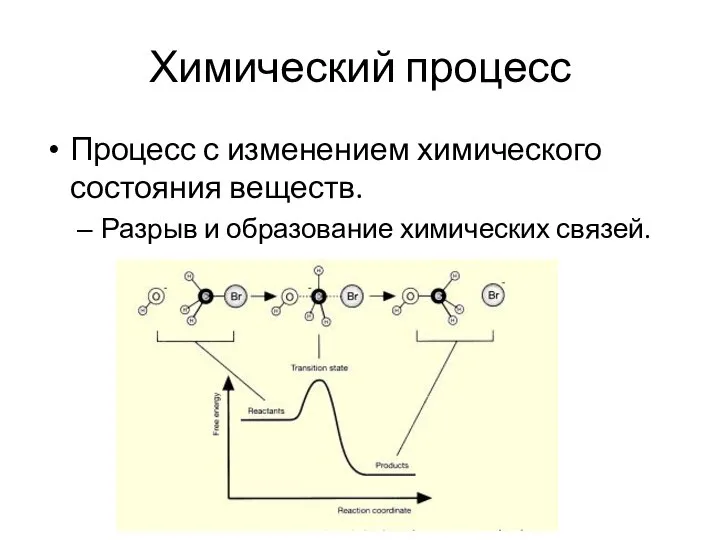
- 17. Химический процесс Процесс с изменением химического состояния веществ. Разрыв и образование химических связей.
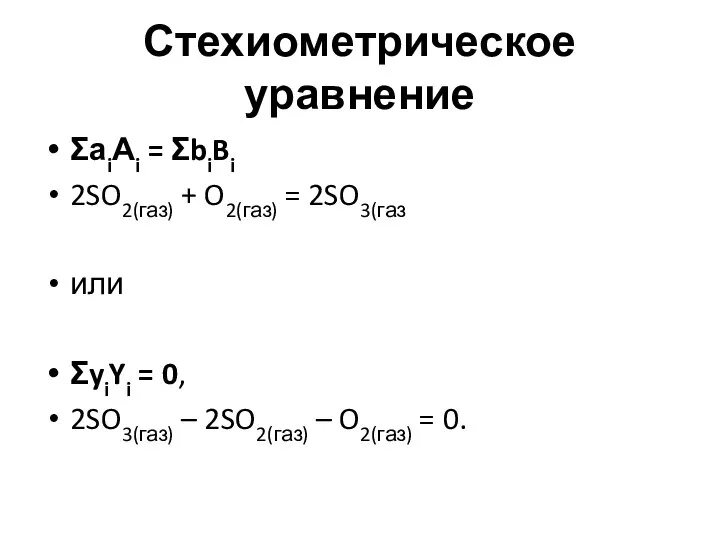
- 18. Стехиометрическое уравнение ΣаiАi = ΣbiBi 2SO2(газ) + O2(газ) = 2SO3(газ или ΣyiYi = 0, 2SO3(газ) –
- 19. Стехиометрическое уравнение ХП отражает фундаментальные законы природы – сохранение массы и заряда. (Закон Ломоносова–Лавуазье) 2SO2(газ) +
- 20. Энергия Энергия – форма существования материи. Мера движения и взаимодействия материи. Кинетическая и потенциальная. Потенциалы: Гравитационный
- 21. Энергия системы Тепловое движение Энергия химических и межмолекулярных связей (электромагнитное взаимодействие) Фактор упорядочения Концентрации частиц
- 22. Тепловая энергия RТ в расчёте на моль – kТ на молекулу R = NA · k
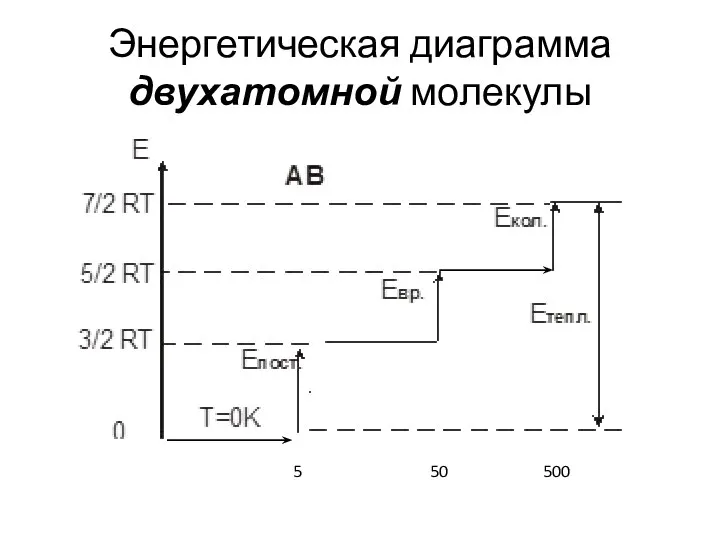
- 23. Энергетическая диаграмма двухатомной молекулы 5 50 500
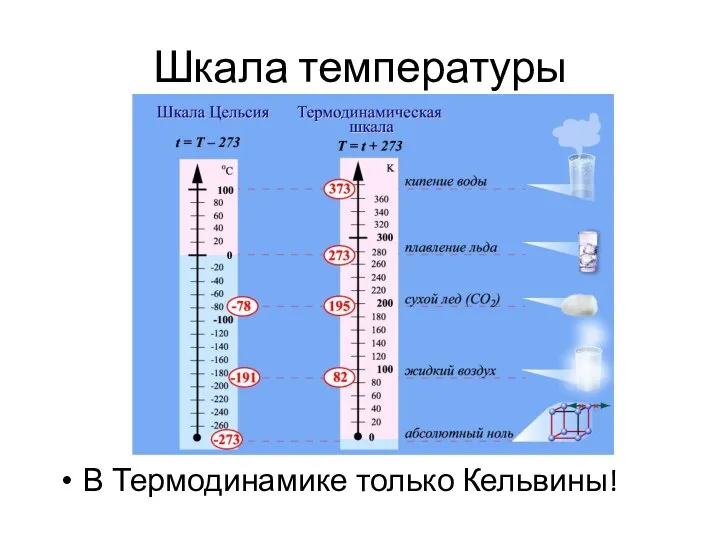
- 24. Шкала температуры В Термодинамике только Кельвины!
- 25. Теплоемкость Теплоёмкость с – это количество теплоты δQ, поглощаемой телом при его нагревании на dТ, т.
- 26. Энергия химических связей Химический процесс – разрыв и образование химических связей. Энергия 1 моля хим. связи
- 27. Диссоциация двухатомной молекулы H2 = H + H 435,9 O2 = O + O 498,7 N2
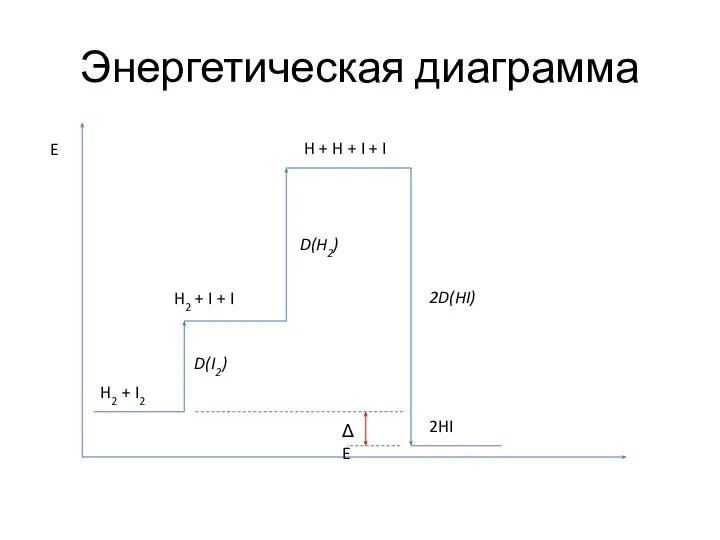
- 28. Образование иодоводорода из простых веществ H2 + I2 = 2HI Нужно разорвать две связи H—H и
- 29. Образование иодоводорода из простых веществ ΔE = -9,9 кДж/моль Отрицательное значение - энергия выделяется. Экзотермичная реакция.
- 30. Энергетическая диаграмма H2 + I2 2HI H2 + I + I H + H + I
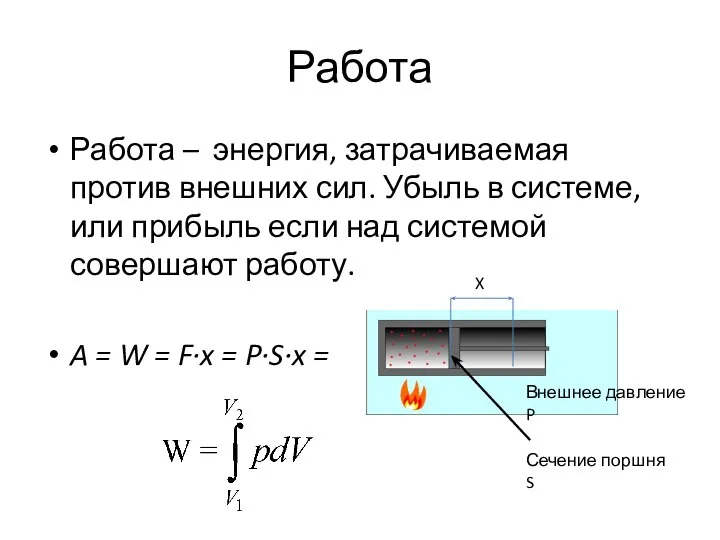
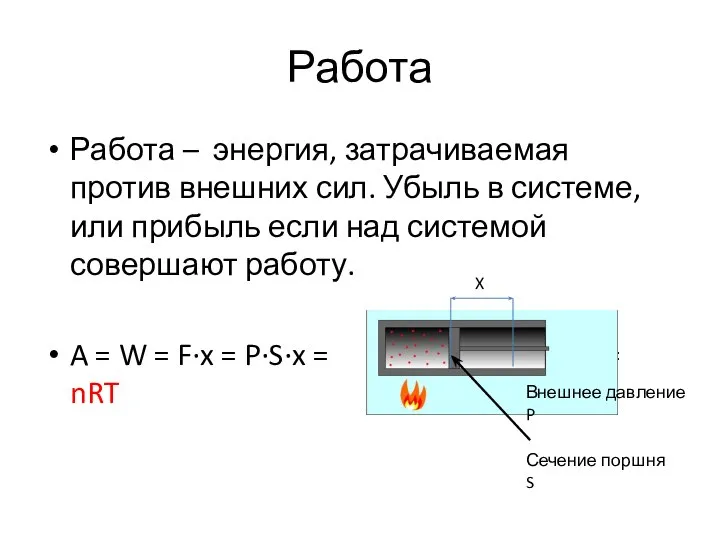
- 31. Работа Работа – энергия, затрачиваемая против внешних сил. Убыль в системе, или прибыль если над системой
- 32. 1 начало термодинамики ΔU = Q – W, dU = δQ – δW Закон сохранения энергии
- 33. Изменение теплоты при изохорном процессе ΔQv = ΔU + W Так как ΔV = 0, P·ΔV
- 34. PV = nRT Закон Ломоносова-Клапейрона Размерность PV и nRT – Джоуль. К этому уравнению вернемся позже.
- 35. Работа Работа – энергия, затрачиваемая против внешних сил. Убыль в системе, или прибыль если над системой
- 36. Изменение теплоты при изохорном процессе ΔQp = ΔU + W W = PΔV = RT ΔQp
- 37. Энтальпия H Энтальпи́я — термодинамический потенциал, характеризующий состояние системы в термодинамическом равновесии при выборе в качестве
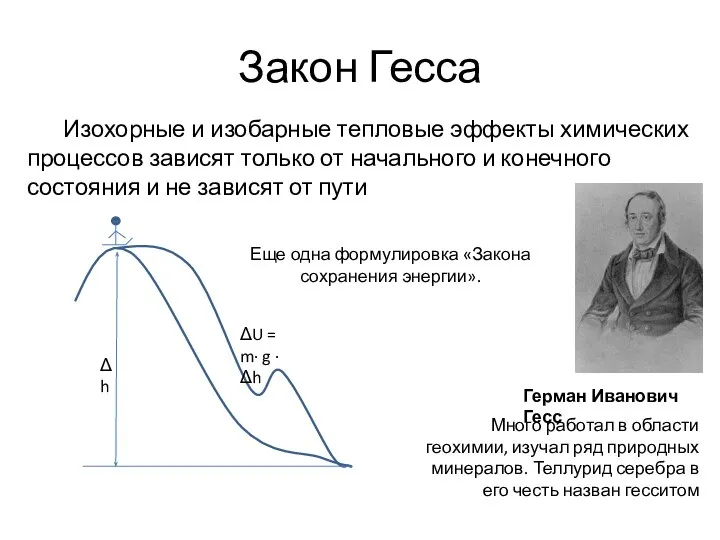
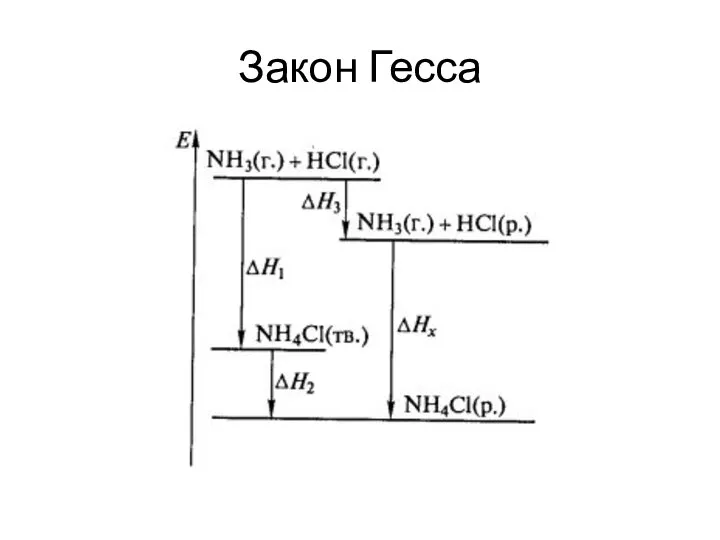
- 38. Закон Гесса Герман Иванович Гесс Много работал в области геохимии, изучал ряд природных минералов. Теллурид серебра
- 39. Закон Гесса
- 41. Скачать презентацию

























 Презентация по химии Строение атома
Презентация по химии Строение атома  Новые наноматериалы. Получение, свойства и применение
Новые наноматериалы. Получение, свойства и применение Функциональные производные с простой связью C-“O”. Часть 4 (продолжение) …окси-производные
Функциональные производные с простой связью C-“O”. Часть 4 (продолжение) …окси-производные Общие сведения о полезных ископаемых. (Лекция 2)
Общие сведения о полезных ископаемых. (Лекция 2) Смесители. Пропеллерная мешалка
Смесители. Пропеллерная мешалка Щелочноземельные металлы
Щелочноземельные металлы Информационно – исследовательский проект Кристаллы вокруг нас.
Информационно – исследовательский проект Кристаллы вокруг нас. Дисперсні системи
Дисперсні системи Полиуретаны. Структура и строение
Полиуретаны. Структура и строение Лекция 10. Химия s-элементов
Лекция 10. Химия s-элементов Фармацевтическая химия
Фармацевтическая химия Натуральный комплекс минералов
Натуральный комплекс минералов Алкалоидтар. Алкалоидтар туралы түсінік
Алкалоидтар. Алкалоидтар туралы түсінік Пищевые добавки
Пищевые добавки Присадки к маслам
Присадки к маслам Буферные системы
Буферные системы Давайте повторим Заключительный урок в 8 классе
Давайте повторим Заключительный урок в 8 классе  Серная кислота. (9 класс)
Серная кислота. (9 класс) Металлы. Общая характеристика
Металлы. Общая характеристика Альдегидтер және кетондар
Альдегидтер және кетондар Н2O Матвієнко А. 10-а
Н2O Матвієнко А. 10-а  Металл золото
Металл золото Кислород. Общая характеристика и нахождение в природе. 8 класс
Кислород. Общая характеристика и нахождение в природе. 8 класс Общая характеристика элементов V-А-группы. Азот
Общая характеристика элементов V-А-группы. Азот Аттестационная работа. Рабочая программа элективного курса по химии для 8 класса
Аттестационная работа. Рабочая программа элективного курса по химии для 8 класса Кислоты. Состав. Классификация
Кислоты. Состав. Классификация НАСЛІДКИ ЧОРНОБИЛЬСЬКОЇ ТРАГЕДІЇ Чорнобиль продемонстрував всемогутність і безсилля людини та застеріг її: не захоплюйся своєю
НАСЛІДКИ ЧОРНОБИЛЬСЬКОЇ ТРАГЕДІЇ Чорнобиль продемонстрував всемогутність і безсилля людини та застеріг її: не захоплюйся своєю  Презентация по Химии "Основания." - скачать смотреть бесплатно
Презентация по Химии "Основания." - скачать смотреть бесплатно