Закономерности изменения свойств химических элементов в Периодической Системе Химических Элементов ( ПСХЭ)
Содержание
- 2. Задание 1) Записать все выводы и выполнить задания из презентации или из документа к уроку 2)
- 3. I. ТЕСТ «ПОВТОРЕНЬЕ –МАТЬ УЧЕНЬЯ» 1) Как определить число энергетических уровней в атоме элемента: а) по
- 4. ПОВТОРЕНЬЕ –МАТЬ УЧЕНЬЯ 2) Как определяется место химического элемента в периодической системе Д.И. Менделеева: а) количеством
- 5. ПОВТОРЕНЬЕ –МАТЬ УЧЕНЬЯ 3)Сколько энергетических уровней в атоме кальция: а) 1 б) 2 в) 3 г)
- 6. ПОВТОРЕНЬЕ –МАТЬ УЧЕНЬЯ 4) Укажите элемент, возглавляющий большой период периодической системы элементов: а) Cu (№29) б)
- 7. ПОВТОРЕНЬЕ –МАТЬ УЧЕНЬЯ 5) Атом, в ядре которого содержится 18 нейтронов и 16 протонов, имеет заряд
- 8. ПОВТОРЕНЬЕ –МАТЬ УЧЕНЬЯ 6) Атомы одного химического элемента содержат: а) одинаковое число нейтронов в ядре б)
- 9. ПОВТОРЕНЬЕ –МАТЬ УЧЕНЬЯ 7) Назовите элемент, расположенный в II периоде , на внешнем слое атома 4
- 10. ПОВТОРЕНЬЕ –МАТЬ УЧЕНЬЯ 8) Оперделите схему строения атома фтора: а) +? ) ) ) 2e 8e
- 11. ПОВТОРЕНЬЕ –МАТЬ УЧЕНЬЯ 9) Определите какой это элемент: + Z ) ) ) ? 4е а)
- 12. ПРОВЕРКА 1) г 2)в 3)г 4)в 5)г 6) в 7)г 8)г 9)б
- 13. II.ИЗУЧАЕМ НОВЫЙ МАТЕРИАЛ «Закономерности изменения свойств химических элементов в ПСХЭ»
- 14. 1.Изменение свойств химических элементов в периодах
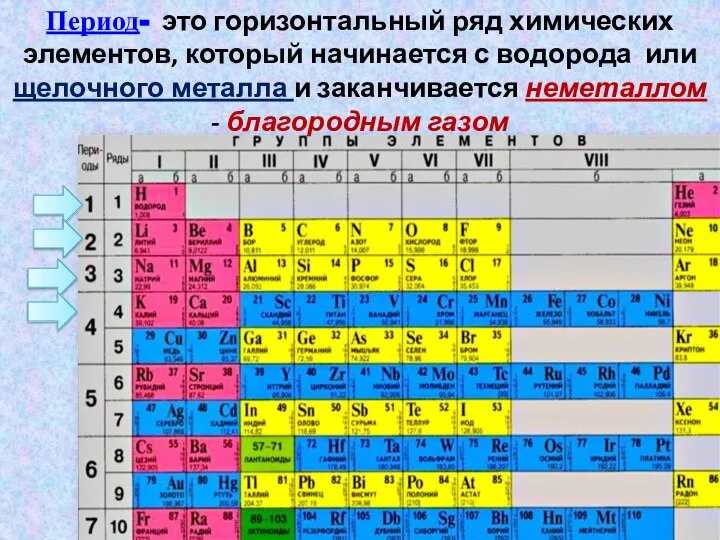
- 15. Период- это горизонтальный ряд химических элементов, который начинается с водорода или щелочного металла и заканчивается неметаллом
- 16. IIпериод: Li……………………………………Ne III период: Na…………………………….....Ar IV период: K………………………………………. ………………………………………………………….Kr Например:
- 17. РАССМОТРИМ СТРОЕНИЕ АТОМОВ Х.Э. 2 ПЕРИОДА
- 18. Рассмотрим строение атомов х.э. на примере х.э. III периода 13Na +13 ) ) ) или 1s2
- 19. Изменение радиуса атома х.э. в периодах слева направо
- 21. Вывод №1.В одном периоде слева направо: 1)заряд ядра атома увеличивается; 2)количество электронов на внешнем слое атомов
- 22. Вывод №2 Период- это горизонтальный ряд химических элементов, в котором слева направо ослабевают металлические и усиливаются
- 23. 2.Изменение свойств химических элементов в группах главных подгруппах
- 24. Вспомним, что ГРУППА Х.Э. – вертикальный ряд химических элементов, сходных по свойствам . стр.183 (2019г) или
- 25. Изменения свойств химических элементов и их соединений в группах главных подгруппах (А) В группах все элементы
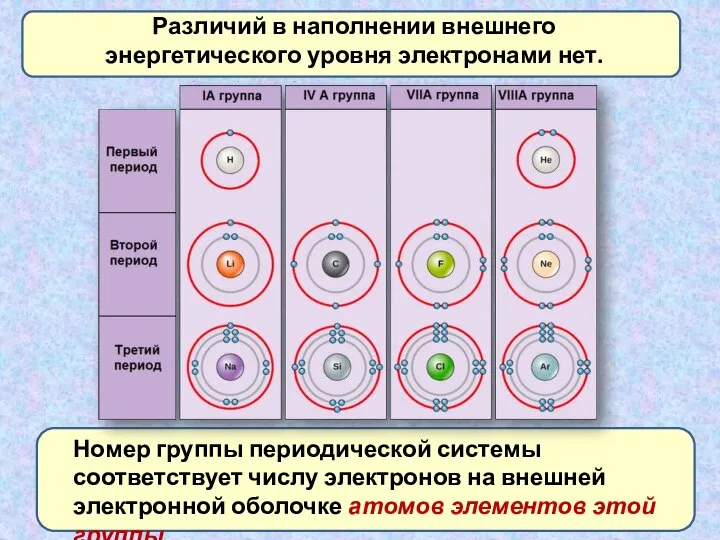
- 26. Различий в наполнении внешнего энергетического уровня электронами нет. Номер группы периодической системы соответствует числу электронов на
- 28. Вывод №3. В одной группе сверху вниз: 1)заряд ядра атома увеличивается; 2)количество электронов на внешнем слое
- 29. Вывод №4. ГРУППА Х.Э. – ЭТО вертикальный ряд химических элементов, в котором сверху вниз усиливаются металлические
- 30. Задание №1. Заполните таблицу «Закономерности изменения свойств химических элементов в ПСХЭ»
- 32. 1) Как изменяются радиусы атомов в периоде: а) увеличиваются б) уменьшаются в) не изменяются Задание №2
- 33. 2)У какого из элементов более выражены металлические свойства а) литий б) калий в) натрий
- 34. 3)Между радиусами атомов поставить знаки больше или меньше а) радиус атома натрия радиус атома магния б)
- 35. 4)Как изменяются радиусы атомов в главных подгруппах сверху вниз: а) увеличиваются б) уменьшаются в) не изменяются
- 36. 5) Чем определяются свойства химических элементов: а) величиной относительной атомной масс б) числом электронов на внешнем
- 37. 6)У какого элемента наиболее выражены неметаллические свойства: а) Кремний б) Углерод г) Кислород
- 38. 7)Металлический характер свойств элементов в ряду Li --> Na --> K --> Rb: 1) уменьшается 2)
- 39. 8) Неметаллические свойства усиливаются в ряду: 1) S, O, F 2) B, C, Si 3) S,
- 40. Задание 1) Записать все выводы и выполнить задания из презентации или из документа к уроку 2)
- 42. Скачать презентацию





































 Когда его называли гением, он морщился: "Какой там гений. Трудился всю жизнь, вот и стал гением". Когда в 26 лет писал курс "
Когда его называли гением, он морщился: "Какой там гений. Трудился всю жизнь, вот и стал гением". Когда в 26 лет писал курс " Энергетический обмен
Энергетический обмен Белки. Классификация белков. (Тема 2)
Белки. Классификация белков. (Тема 2) Железо. Строение атома, физические и химические свойства простого вещества
Железо. Строение атома, физические и химические свойства простого вещества Геохимия природных процессов. Метеориты
Геохимия природных процессов. Метеориты Тема урока «Азот и его свойства». Цель: узнать о строении атома и молекулы азота, о его физических и химических свойствах, круговор
Тема урока «Азот и его свойства». Цель: узнать о строении атома и молекулы азота, о его физических и химических свойствах, круговор Химия. Введение
Химия. Введение Нуклеотиды Нуклеотиды Нуклеиновые кислоты
Нуклеотиды Нуклеотиды Нуклеиновые кислоты  Окислительно-восстановительные реакции (ОВР). Часть 2
Окислительно-восстановительные реакции (ОВР). Часть 2 Коррозия металла
Коррозия металла Теория строения химических веществ
Теория строения химических веществ Коррозия металлов
Коррозия металлов Алкилирование изобутана олефинами
Алкилирование изобутана олефинами Структура и свойства чистого титана
Структура и свойства чистого титана Металловедение. Наука, изучающая состав, внутреннее строение и свойства металлов и сплавов
Металловедение. Наука, изучающая состав, внутреннее строение и свойства металлов и сплавов Химия в медицине
Химия в медицине Изотопная геохимия. Изотопы
Изотопная геохимия. Изотопы №6. Электрофильное замещение в ароматических соединениях.
№6. Электрофильное замещение в ароматических соединениях.  Природні сполуки алюмінію і методи одержання
Природні сполуки алюмінію і методи одержання Аттестационная работа. Программа регионального компонента образовательной области Химия
Аттестационная работа. Программа регионального компонента образовательной области Химия Глицерин
Глицерин Пластмассы и волокна
Пластмассы и волокна Соли. Формула соли
Соли. Формула соли The chemistri of life and the micro universe
The chemistri of life and the micro universe Поливинилацетат
Поливинилацетат Иониты и цеолиты. Цеолитные катализаторы
Иониты и цеолиты. Цеолитные катализаторы Классификация и номенклатура оксидов и кислот
Классификация и номенклатура оксидов и кислот Природні сполуки Силіцію.
Природні сполуки Силіцію.