Содержание
- 2. Вещество (более 70 млн.) Что надо знать о каждом веществе? Формула (из чего состоит) Структура (как
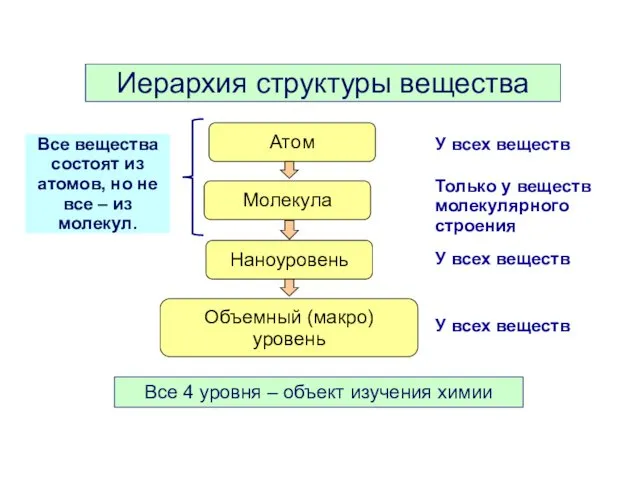
- 3. Иерархия структуры вещества Атом Молекула Наноуровень Объемный (макро) уровень У всех веществ Только у веществ молекулярного
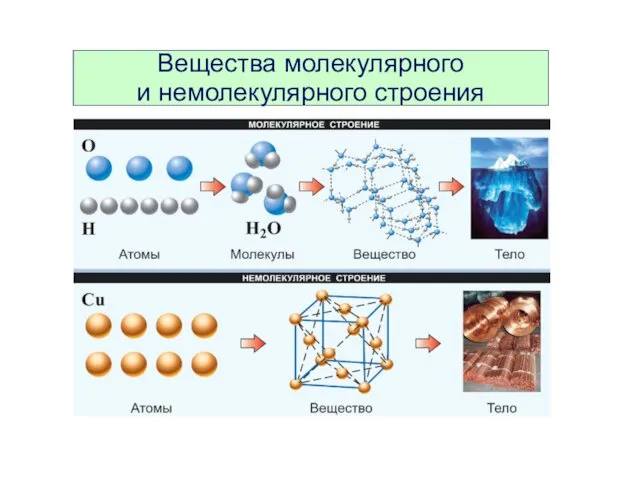
- 4. Вещества молекулярного и немолекулярного строения
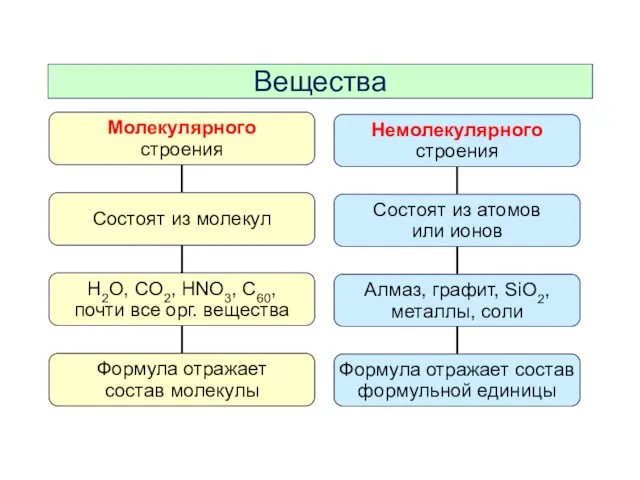
- 5. Вещества
- 6. Вещества Хлорид натрия Формульная единица NaCl
- 7. Вещества Диоксид кремния Формульная единица SiO2 Минералогический музей имени Ферсмана находится возле входа в Нескучный сад.
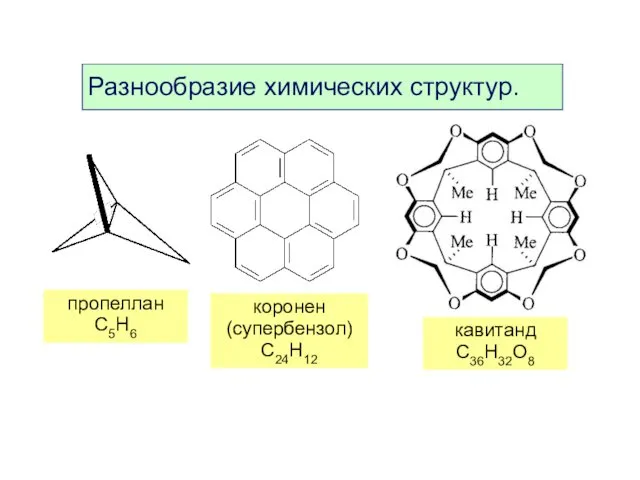
- 8. Разнообразие химических структур. пропеллан C5H6 коронен (супербензол) C24H12 кавитанд C36H32O8
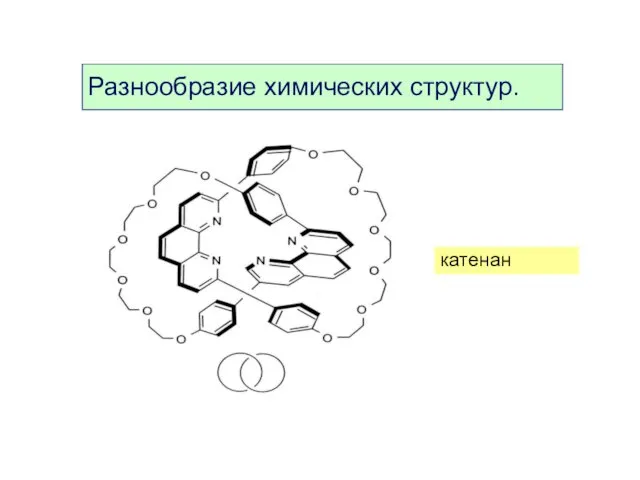
- 9. катенан Разнообразие химических структур.
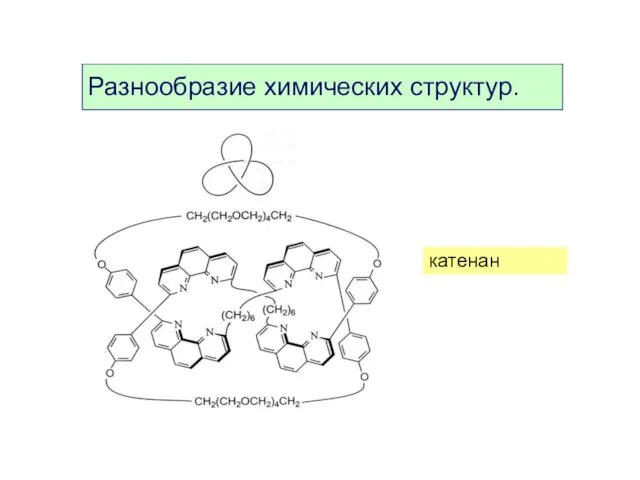
- 10. катенан Разнообразие химических структур.
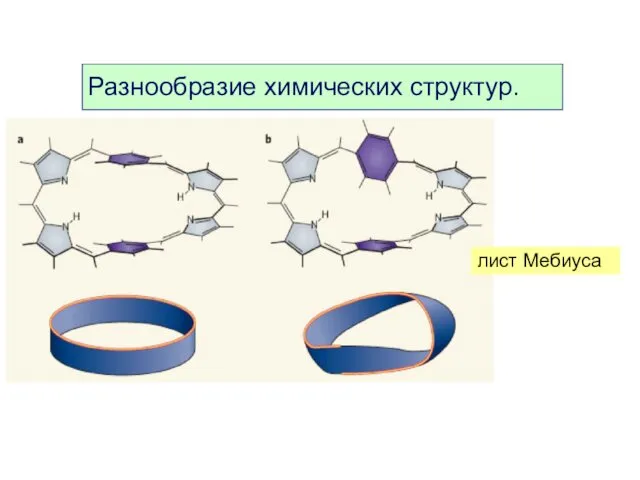
- 11. лист Мебиуса Разнообразие химических структур.
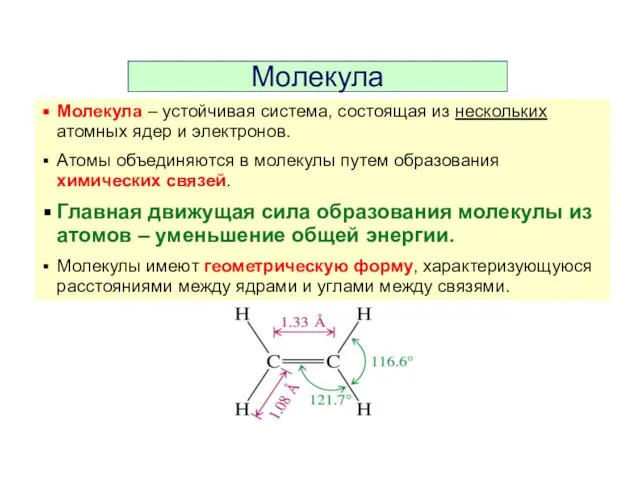
- 12. Молекула Молекула – устойчивая система, состоящая из нескольких атомных ядер и электронов. Атомы объединяются в молекулы
- 13. Главная движущая сила образования химической связи между частицами вещества – уменьшение общей энергии системы.
- 14. Основные типы химической связи: Ионная Ковалентная Металлическая Основные межмолекулярные взаимодействия: Водородные связи Ван-дер-Ваальсовы связи
- 15. Ионная связь Если связь образуют атомы с резко различающимися значениями электроотрицательности (ΔОЭО ≥ 1,7), общая электронная
- 16. Ионная связь Кулоновский потенциал сферически симметричен, направлен во все стороны, поэтому ионная связь ненаправлена. Кулоновский потенциал
- 17. Ионная связь Соединения с ионным типом связи твердые, хорошо растворимые в полярных растворителях, имеют высокие температуры
- 18. Ионная связь Кривая I: притяжение ионов, если бы они представляли собой точечные заряды. Кривая II: отталкивание
- 19. Химическая связь в молекулах Химическую связь в молекулах можно описать с позиций двух методов: - метода
- 20. Метод валентных связей Теория Гейтлера-Лондона Основные положения метода ВС: 1. Связь образуют два электрона с противоположными
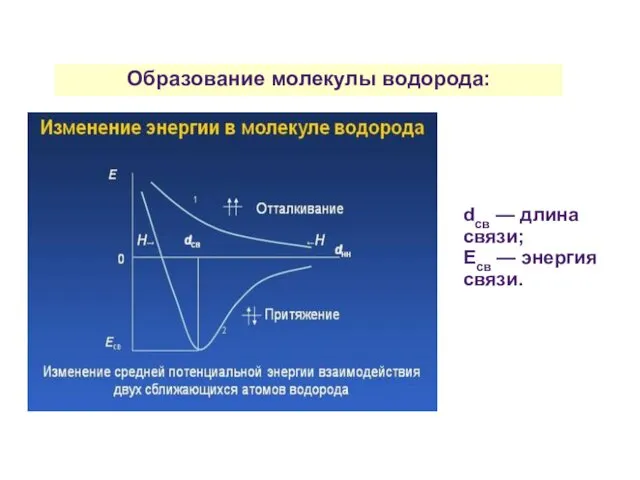
- 21. Образование молекулы водорода: dсв — длина связи; Есв — энергия связи.
- 22. При сближении двух атомов возникают силы притяжения и отталкивания: 1) притяжения: «электрон-ядро» соседних атомов; 2) отталкивания:
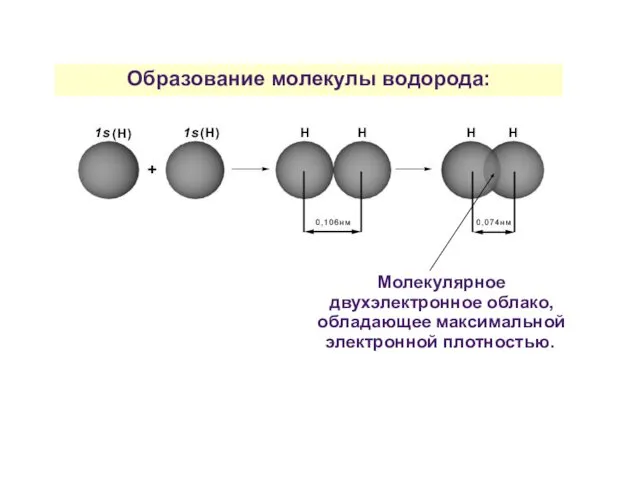
- 23. Образование молекулы водорода: Молекулярное двухэлектронное облако, обладающее максимальной электронной плотностью.
- 24. Химическая связь, осуществляемая общими электронными парами, называется ковалентной. Общая электронная пара может образоваться двумя способами: 1)
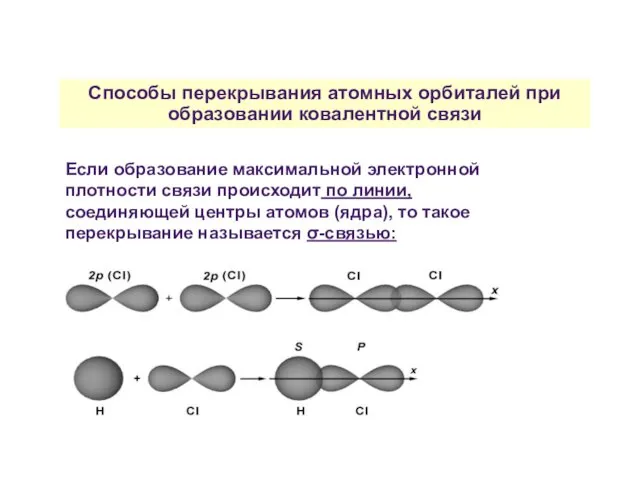
- 25. Способы перекрывания атомных орбиталей при образовании ковалентной связи Если образование максимальной электронной плотности связи происходит по
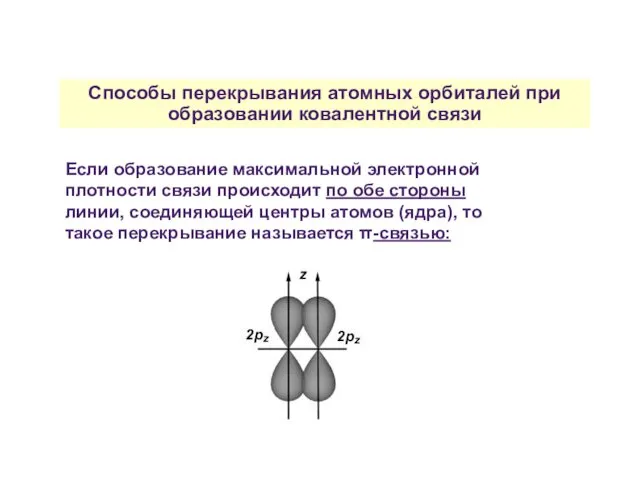
- 26. Способы перекрывания атомных орбиталей при образовании ковалентной связи Если образование максимальной электронной плотности связи происходит по
- 27. Полярная и неполярная ковалентная связь 1) Если связь образуют одинаковые атомы, двухэлектронное облако связи распределяется в
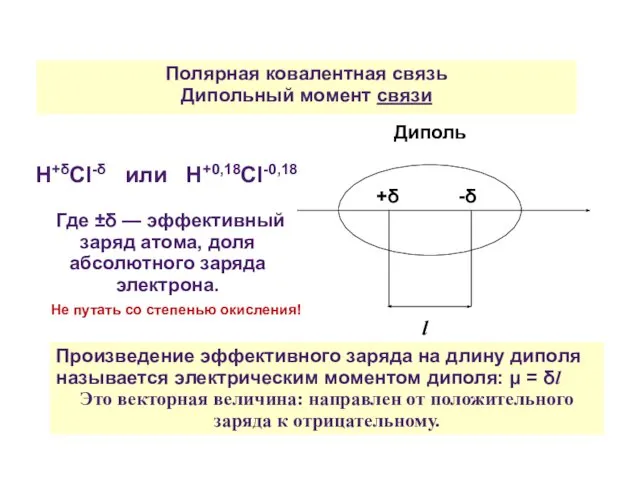
- 28. Полярная ковалентная связь Дипольный момент связи H+δCl-δ или H+0,18Cl-0,18 Где ±δ — эффективный заряд атома, доля
- 29. Полярная ковалентная связь Дипольный момент молекулы Дипольный момент молекулы равен сумме векторов дипольных моментов связей с
- 30. Полярная ковалентная связь Дипольный момент молекулы В произведении μ = δl обе величины разнонаправлены. Поэтому надо
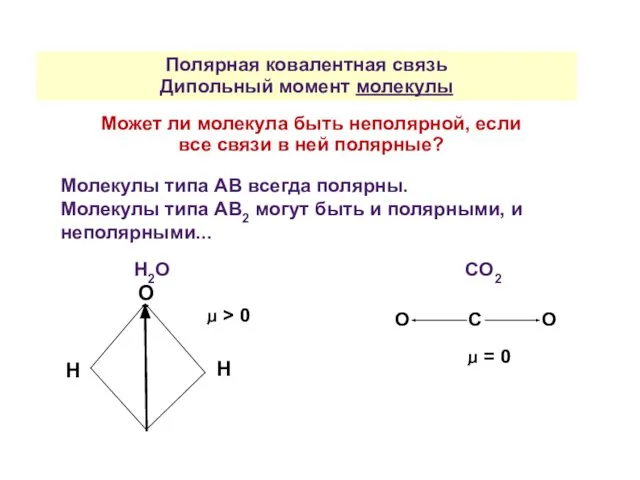
- 31. Полярная ковалентная связь Дипольный момент молекулы Может ли молекула быть неполярной, если все связи в ней
- 32. Полярная ковалентная связь Молекулы, состоящие из трех атомов и более (АВ2, АВ3, АВ4, АВ5, АВ6) ,
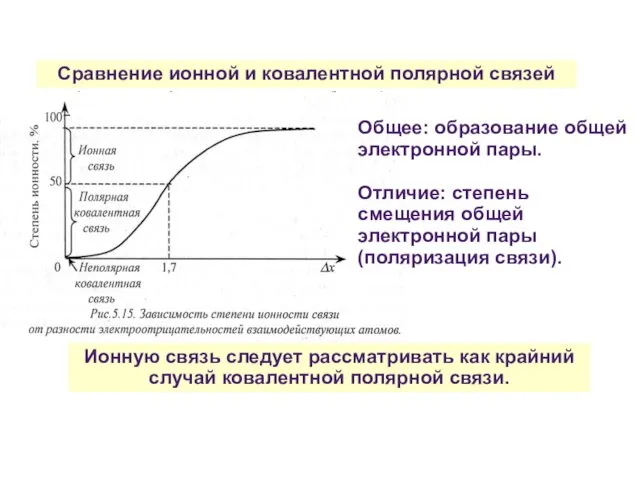
- 33. Сравнение ионной и ковалентной полярной связей Ионную связь следует рассматривать как крайний случай ковалентной полярной связи.
- 34. Сравнение характеристик ионной и ковалентной полярной связей Ковалентная связь: насыщена и направлена Насыщаемость (максимальная валентность) —
- 35. Сравнение характеристик ионной и ковалентной полярной связей Направленность связи задают валентные углы. Валентные углы определяют экспериментально
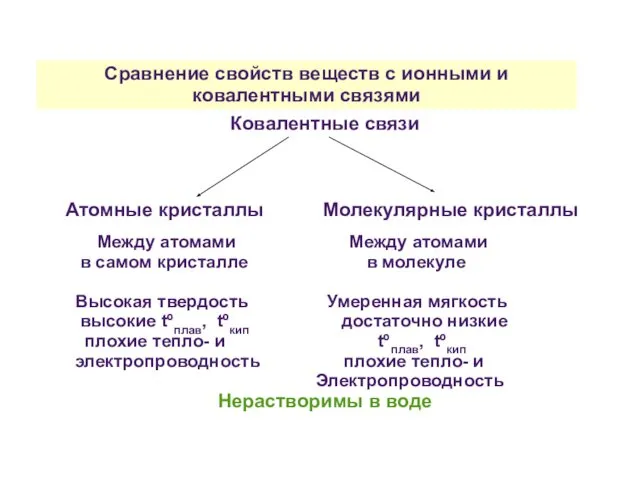
- 36. Сравнение свойств веществ с ионными и ковалентными связями Ковалентные связи Атомные кристаллы Молекулярные кристаллы Между атомами
- 37. Сравнение свойств веществ с ионными и ковалентными связями Молекулярный кристалл Температура плавления 112,85 °С
- 38. Сравнение свойств веществ с ионными и ковалентными связями Атомный ковалентный кристалл Температура плавления ≈ 3700 °С
- 39. Сравнение свойств веществ с ионными и ковалентными связями Ионные связи между ионами в кристалле твердость и
- 40. Сравнение свойств веществ с ионными и ковалентными связями Ионный кристалл Температура плавления ≈ 800 °С
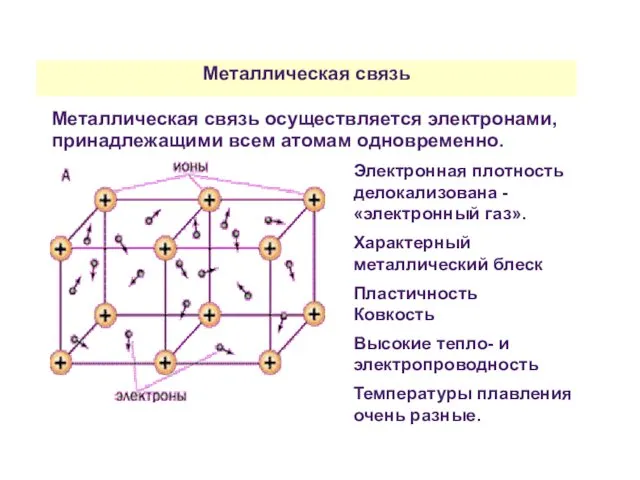
- 41. Металлическая связь Металлическая связь осуществляется электронами, принадлежащими всем атомам одновременно. Электронная плотность делокализована - «электронный газ».
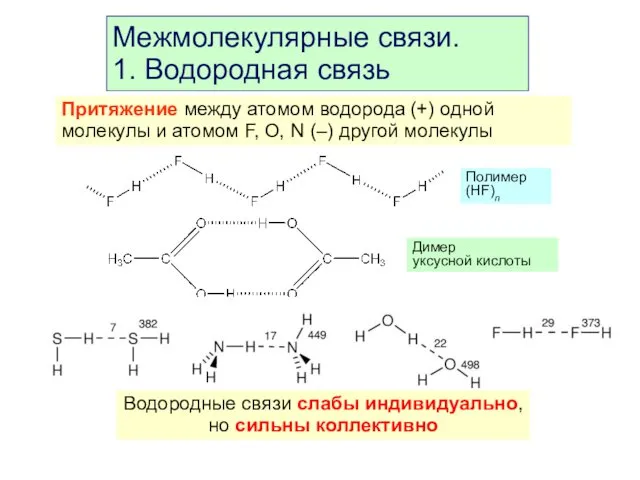
- 42. Межмолекулярные связи. 1. Водородная связь Притяжение между атомом водорода (+) одной молекулы и атомом F, O,
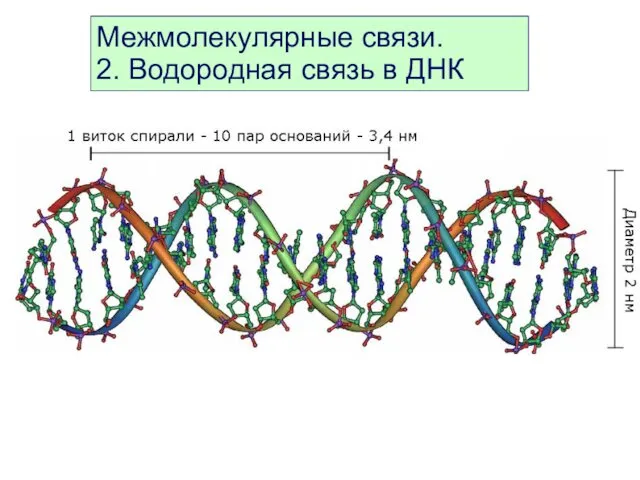
- 43. Межмолекулярные связи. 2. Водородная связь в ДНК
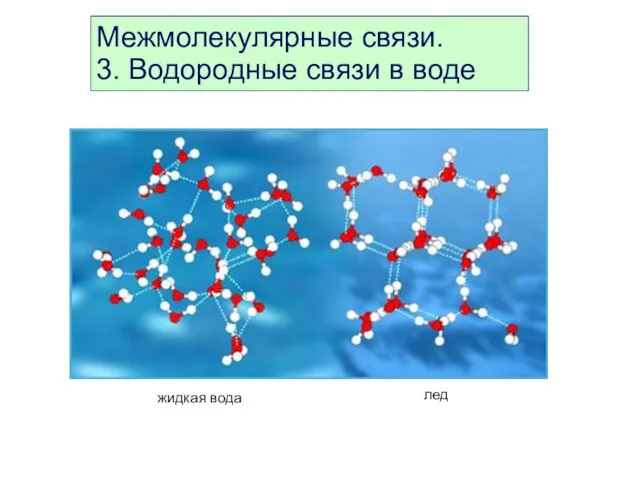
- 44. Межмолекулярные связи. 3. Водородные связи в воде
- 45. Межмолекулярные связи. 4. Образование водородных связей в воде жидкая вода превращение воды в лед
- 46. Межмолекулярные связи. 5. Ван-дер-ваальсовы связи Даже если между молекулами нет водородных связей, молекулы всегда притягиваются друг
- 48. Скачать презентацию

























 Арены и ароматичность
Арены и ароматичность АЛОТРОПНІ ФОРМИ КАРБОНУ АВТОР: НАЗАРЕНКО МАКСИМ ВОЛОДИМИРОВИЧ 9-А КЛАС,ГІМНАЗІЯ №32 ПЕЧЕРСЬКИЙ РАЙОН, М. КИЇВ ПЕДАГОГІЧНИЙ КЕ
АЛОТРОПНІ ФОРМИ КАРБОНУ АВТОР: НАЗАРЕНКО МАКСИМ ВОЛОДИМИРОВИЧ 9-А КЛАС,ГІМНАЗІЯ №32 ПЕЧЕРСЬКИЙ РАЙОН, М. КИЇВ ПЕДАГОГІЧНИЙ КЕ Препараты гормонов стероидной структуры
Препараты гормонов стероидной структуры Закон постоянства углов Стено
Закон постоянства углов Стено Растворы. Общая характеристика растворов
Растворы. Общая характеристика растворов Арены. Бензол
Арены. Бензол Обмен веществ и энергии, основа существования клетки
Обмен веществ и энергии, основа существования клетки КАЛЬЦИЙ И ЕГО СОЕДИНЕНИЯ 9 класс МКОУ «СОШ № 85» г. Тайшет Иркутской обл. Учитель: Никитюк Л.Ф.
КАЛЬЦИЙ И ЕГО СОЕДИНЕНИЯ 9 класс МКОУ «СОШ № 85» г. Тайшет Иркутской обл. Учитель: Никитюк Л.Ф. Пены. Пенообразование
Пены. Пенообразование Введение в титриметрический анализ. Кислотно-основное титрование
Введение в титриметрический анализ. Кислотно-основное титрование Щелочные металлы
Щелочные металлы Ковалентная химическая связь
Ковалентная химическая связь Элементы группы VII B
Элементы группы VII B Мыс айналымы
Мыс айналымы Презентация по Химии "Разнообразие кристаллов и их выращивание" - скачать смотреть
Презентация по Химии "Разнообразие кристаллов и их выращивание" - скачать смотреть  Модифицирование структуры полисахаридов гидрофобными заместителями: твердофазный синтез, исследование структуры и свойств
Модифицирование структуры полисахаридов гидрофобными заместителями: твердофазный синтез, исследование структуры и свойств Макроэлементы и микроэлементы
Макроэлементы и микроэлементы Виды изомерии у моносахаридов
Виды изомерии у моносахаридов Презентация по теме «Металлы» «Уран» Работа Садковского Ивана 9 «В»
Презентация по теме «Металлы» «Уран» Работа Садковского Ивана 9 «В» Хімічний склад і використання мінералів
Хімічний склад і використання мінералів Характеристика элементов VIIA-группы (галогены)
Характеристика элементов VIIA-группы (галогены) Электролиз: опыты к заданиям ЕГЭ
Электролиз: опыты к заданиям ЕГЭ Биосинтез жирных кислот и триацилглицеролов. Обмен липидов. (Лекция 13)
Биосинтез жирных кислот и триацилглицеролов. Обмен липидов. (Лекция 13) Аттестационная работа. Методическая разработка фрагмента урока химии с элементами исследовательской деятельности
Аттестационная работа. Методическая разработка фрагмента урока химии с элементами исследовательской деятельности Электрохимические методы. (Лекция 3)
Электрохимические методы. (Лекция 3) Электролиз. Урок химии 11 класс
Электролиз. Урок химии 11 класс Переработка нефти. (10 класс)
Переработка нефти. (10 класс) Сплавы, растворы и смеси. Задачи на концентрвцию
Сплавы, растворы и смеси. Задачи на концентрвцию