Содержание
- 2. Железо Металл, занимающий четвёртое место по распространённости в земной коре. Входит в состав следующих минералов: Магнитный
- 3. Получение железа Восстановление оксида железа углём, водородом, угарным газом при нагревании. Алюмотермия оксидов железа Электрометаллургический способ
- 4. 1. Восстановление оксида железа FeO + H2 t Fe + H2O FeO + C t Fe
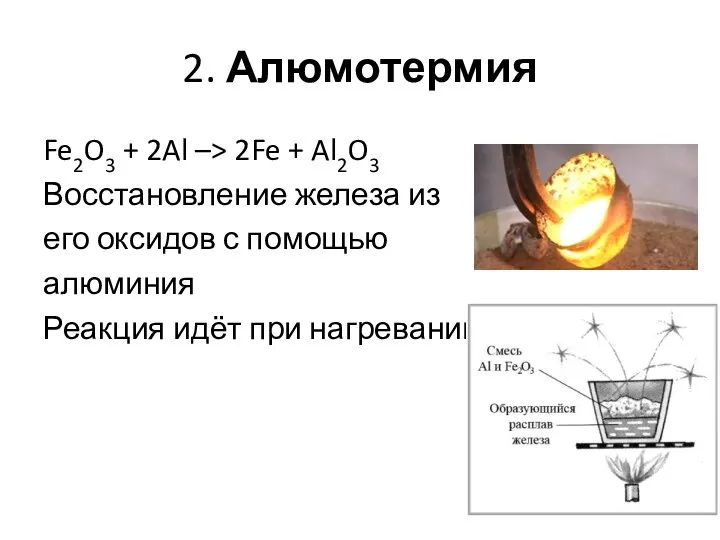
- 5. 2. Алюмотермия Fe2O3 + 2Al –> 2Fe + Al2O3 Восстановление железа из его оксидов с помощью
- 6. Производство чугуна и стали Чугун – железоуглеродистый сплав, содержащий более 2% углерода. Кроме углерода, в нем
- 7. Производство чугуна Для получения чугуна необходимо осуществить процессы восстановления железа из железных руд (минералов, содержащих железо).
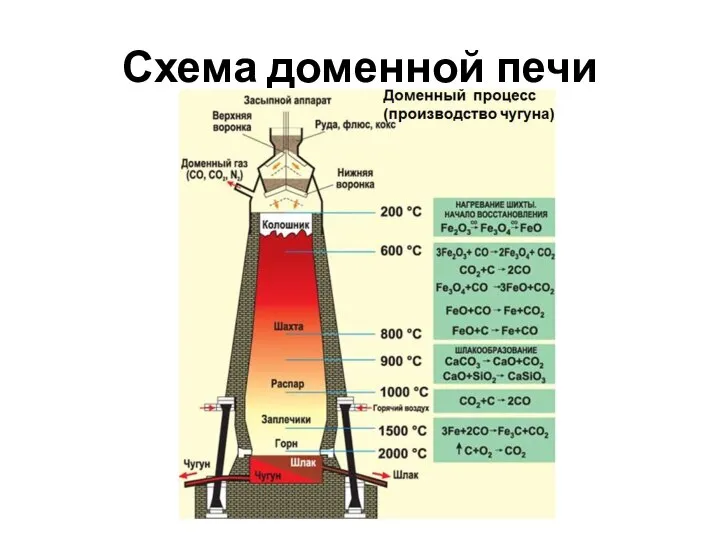
- 8. Схема доменной печи
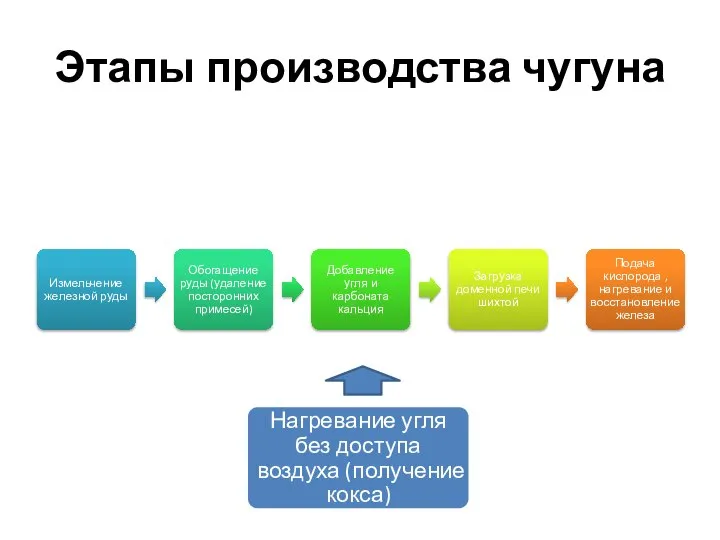
- 9. Этапы производства чугуна
- 10. Минералы железа перед производством размалывают (измельчают) Удаляют из порошка примеси, которые называют «пустой породой». Остаток, содержащий
- 11. 4. Уголь предварительно нагревают без доступа воздуха. В таких условиях уголь не окисляется и превращается в
- 12. В нижней части домны кокс сгорает до углекислого газа. Эта реакция экзотермическая и от большого количества
- 13. Кокс – твёрдое вещество, СО – угарный газ. Газы легче проникают через отверстия между частицами железной
- 14. Восстановленное железо при температуре 1535 плавится и превращается в жидкость. В нём растворяется кокс, и другие
- 15. Силикаты и другие примеси плавятся при более низкой температуре, чем чистое железо и всплывают на поверхность.
- 16. Полученный чугун (около 10%) используется для производства чугунных изделий (сковородки, утюги, моховики). Его называют «литейным». Оставшийся
- 17. В последнее время всё шире в мире распространяется прямое восстановление железа с помощью метана: 3CH4 +
- 18. Химические свойства железа Железо в соединениях проявляет степени окисления +2 и +3. Менее устойчивая +6. Железо
- 19. 1. Взаимодействие с простыми веществами Железо реагирует с простыми веществами неметаллами только при нагревании.
- 20. 2. Взаимодействие со сложными веществами 1. Во лажном воздухе железо подвергается коррозии и покрывается слоем ржавчины.
- 21. 2. Взаимодействие со сложными веществами 2. Раскалённое железо реагирует с водой. Реакция протекает при очень высокой
- 22. 2. Взаимодействие со сложными веществами 3. Железо растворяется в разбавленных кислотах без нагревания
- 23. HNO3 разб. восстанавливается или до NO или до нитрата аммония (зависит от соотношения реагентов и концентрации
- 24. 2. Взаимодействие со сложными веществами 4. Железо пассивируется концентрированной азотной и серной кислотой и не реагирует
- 25. 2. Взаимодействие со сложными веществами 5. Железо вытесняет менее активный металл из раствора его соли:
- 26. Соединения железа Fe+2 Оксид железа (II) FeO Твёрдое вещество чёрного цвета не растворимое в воде. Проявляет
- 27. Соединения железа Fe+2 Оксид железа (II) FeO Растворяясь в азотной кислоте проявляет восстановительные свойства
- 28. Соединения железа Fe+2 Гидроксид железа(II) Fe(OН)2 Твёрдое вещество ,белого с зеленоватым оттенком цвета не растворимое в
- 29. Соединения железа Fe+2 Соединения железа (II) проявляют восстановительные свойства и могут вступать в ОВР с окислителями.
- 30. Соединения железа Fe+2 По этой причине свежеприготовленный гидроксид железа (II) окисляется кислородом воздуха и буреет.
- 31. Соединения железа Fe+2 Восстановительные свойства солей железа +2 проявляются в ОВР:
- 32. Соединения Fe+2
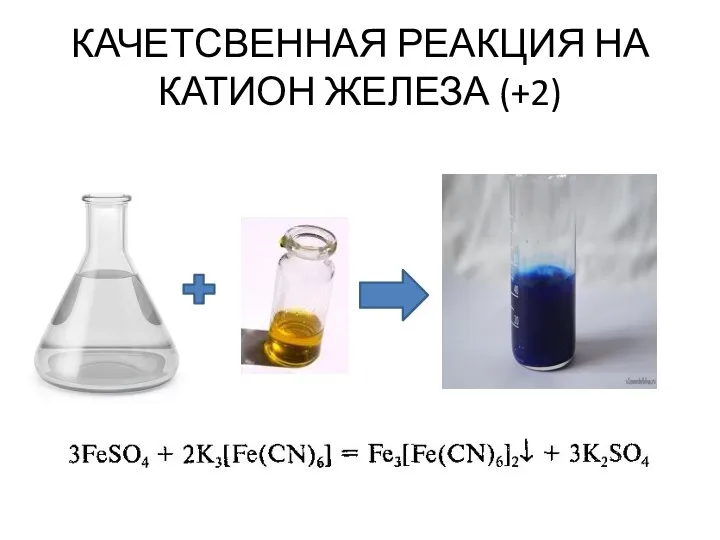
- 33. КАЧЕТСВЕННАЯ РЕАКЦИЯ НА КАТИОН ЖЕЛЕЗА (+2) При взаимодействии бесцветного раствора соли железа (+2) с раствором гексоцианоферрата
- 34. КАЧЕТСВЕННАЯ РЕАКЦИЯ НА КАТИОН ЖЕЛЕЗА (+2) Гексоцианоферрат (III) калия имеет другое название «красная кровяная соль» В
- 35. КАЧЕТСВЕННАЯ РЕАКЦИЯ НА КАТИОН ЖЕЛЕЗА (+2)
- 36. Соединения железа Fe+3 Оксид железа (III) Fe2O3 Нерастворимое в воде вещество бурого цвета В отличие от
- 37. Амфотерные свойства оксида железа (III) Растворяется в кислотах Твёрдый сплавляется со щелочами и карбонатами щелочных металлов
- 38. Магнитный железняк Fe3O4 Двойной оксид железа FeO·Fe2O3 Растворяется в кислотах с образованием двух солей железа: Азотная
- 39. Гидроксид железа (III) Студнеобразное нерастворимое в воде вещество бурого цвета
- 40. Гидроксид железа (III) амфотерен Растворяется в кислотах Сплавляется со щелочами и карбонатами щелочных металлов:
- 41. Гидроксид железа (III) амфотерен 3. В отличие от железа, оксида железа (III) растворяется в концентрированных растворах
- 42. Соединения железа Fe+3 Соединения железа (III) проявляют окислительные свойства и могут вступать в ОВР с восстановителями.
- 43. Соединения Fe+3
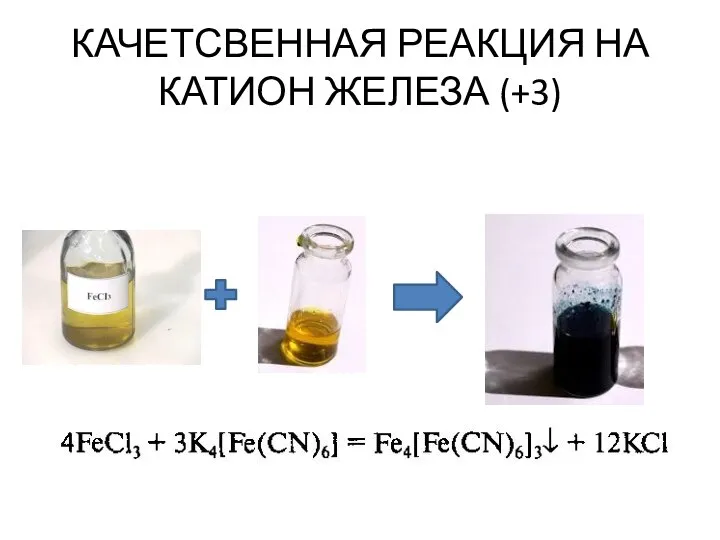
- 44. КАЧЕТСВЕННАЯ РЕАКЦИЯ НА КАТИОН ЖЕЛЕЗА (+3) При взаимодействии желтоватого раствора соли железа (+3) с раствором гексоцианоферрата
- 45. КАЧЕТСВЕННАЯ РЕАКЦИЯ НА КАТИОН ЖЕЛЕЗА (+3) Гексоцианоферрат (II) калия имеет другое название «жёлтая кровяная соль» В
- 46. КАЧЕТСВЕННАЯ РЕАКЦИЯ НА КАТИОН ЖЕЛЕЗА (+3)
- 47. КАЧЕТСВЕННАЯ РЕАКЦИЯ НА КАТИОН ЖЕЛЕЗА (+3) Ещё одна реакция для идентификации катиона железа Fe+3 это взаимодействие
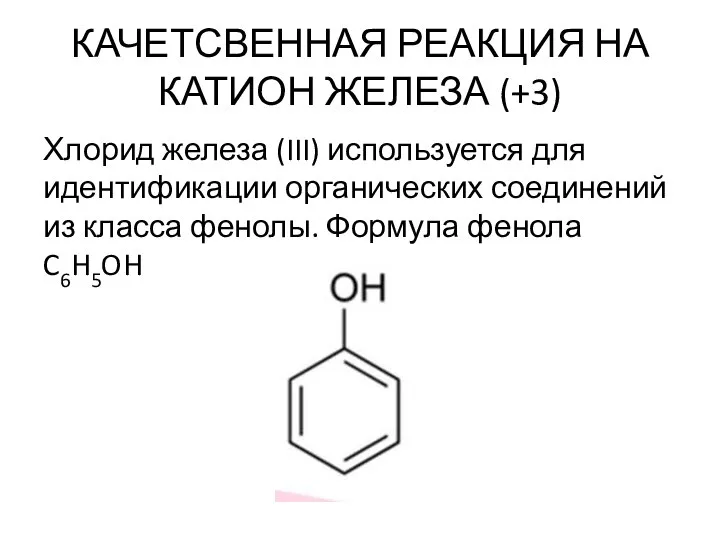
- 48. КАЧЕТСВЕННАЯ РЕАКЦИЯ НА КАТИОН ЖЕЛЕЗА (+3) Хлорид железа (III) используется для идентификации органических соединений из класса
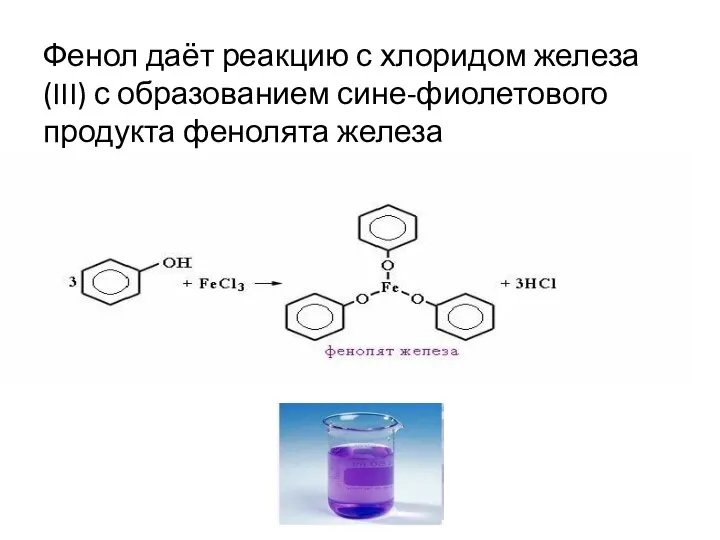
- 49. Фенол даёт реакцию с хлоридом железа (III) с образованием сине-фиолетового продукта фенолята железа
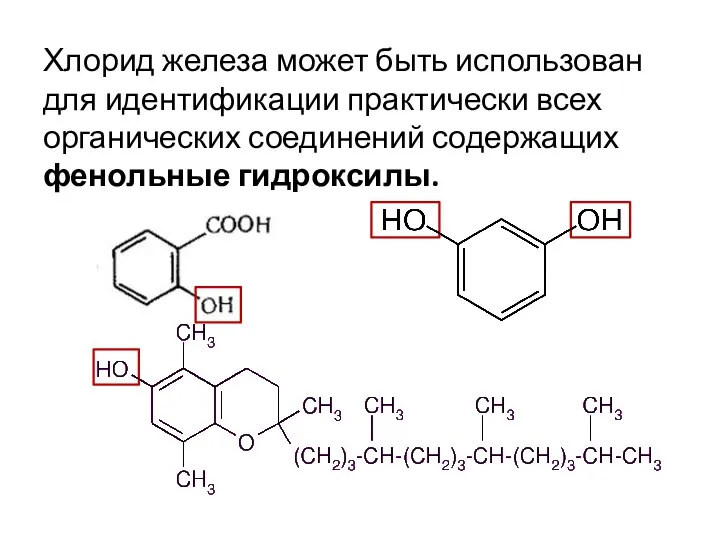
- 50. Хлорид железа может быть использован для идентификации практически всех органических соединений содержащих фенольные гидроксилы.
- 51. Получение оксидов и гидроксидов железа Оксид железа (II) Разложение гидроксида в атмосфере инертного газа без доступа
- 52. Получение оксидов и гидроксидов железа Гидроксид железа (II) Из солей железа +2 БЕЗ ДОСТУПА ВОЗДУХА
- 53. Получение оксидов и гидроксидов железа Оксид железа (III) Обжиг пиприта 2. Разложение гидроксида железа (III)
- 54. Получение оксидов и гидроксидов железа Гидроксид железа (III) Из солей железа +3 ДОСТУП ВОЗДУХА ВОЗМОЖЕН
- 55. Ферраты Соли содержащие феррат ион FeO4-2. Соответствуют железной кислоте H2FeO4 Как правило окрашены в фиолетовый цвет.
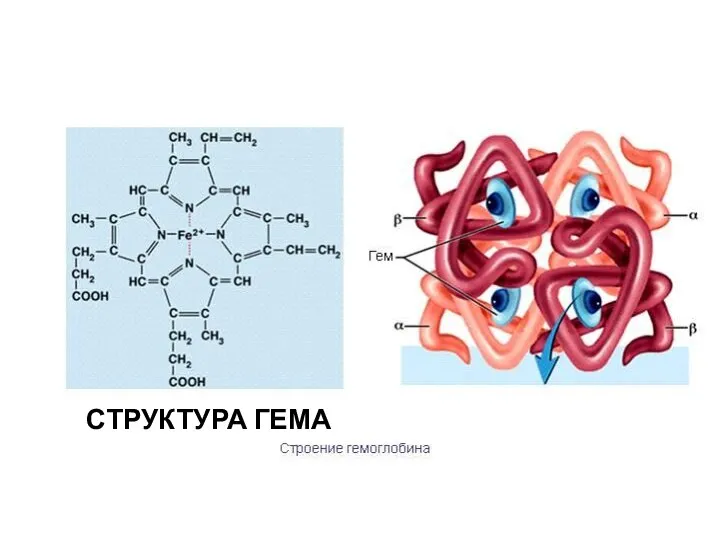
- 56. Биологическое значение железа Железо является макроэлементом, который входит в состав гемоглобина – белка, который транспортирует кислород
- 57. СТРУКТУРА ГЕМА
- 58. Получение марганца Восстановление углеродом или кремнием оксидов марганца Алюмотермия Электролиз раствора MnSO4
- 59. Химические свойства Марганец окрашен в светло-серый цвет, а порошок его в чёрный цвет. На воздухе покрывается
- 60. 1. Взаимодействие с простыми веществами 1. Марганец реагирует с кислородом с образованием различных оксидов, состав которых
- 61. 1. Взаимодействие с простыми веществами 2. Марганец реагирует с другими неметаллами при нагревании С хлором реагирует
- 62. Взаимодействие со сложными веществами С водой реагирует марганец медленно при комнатной температуре, при нагревании быстрее. Растворяется
- 63. Взаимодействие со сложными веществами 3. Растворяется в горячих концентрированных азотной и серной кислотах На холоду марганец
- 64. Взаимодействие со сложными веществами 5. Взаимодействие со щелочными расплавами окислителей 6. Взаимодействие с растворами солей 7.
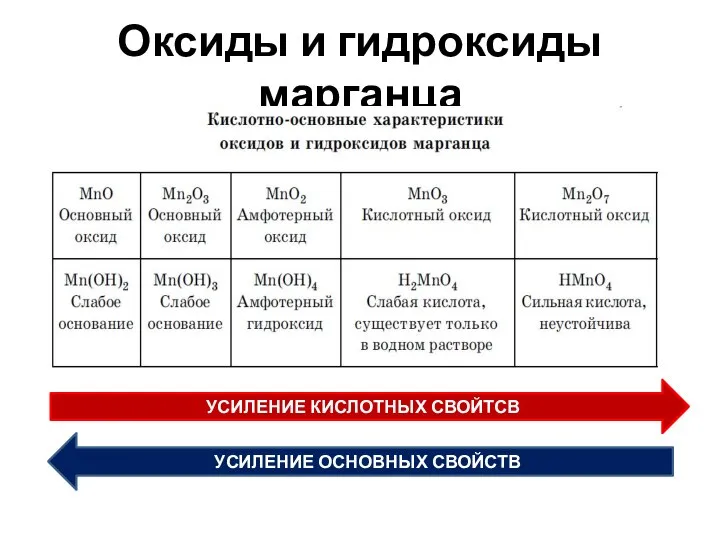
- 65. Оксиды и гидроксиды марганца УСИЛЕНИЕ КИСЛОТНЫХ СВОЙТСВ УСИЛЕНИЕ ОСНОВНЫХ СВОЙСТВ
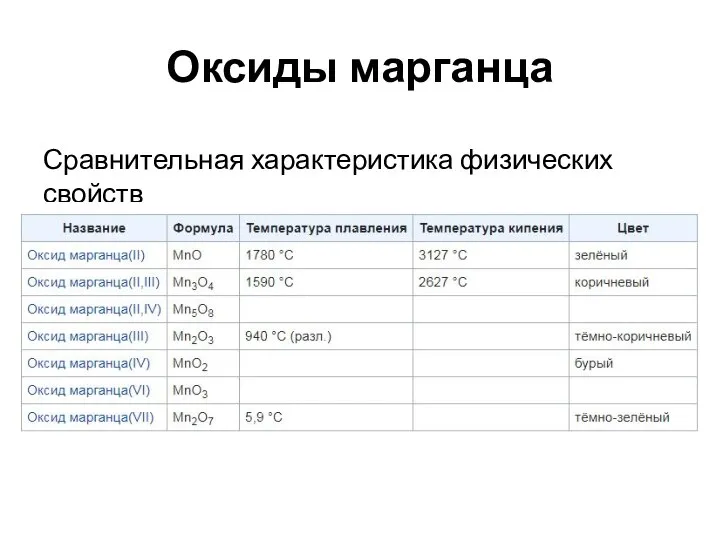
- 66. Оксиды марганца Сравнительная характеристика физических свойств
- 67. Гидроксид марганца (II) Mn(OH)2 Светло-розовые кристаллы нерастворимые в воде. На воздухе окисляясь темнеет. Проявляет основные свойства
- 68. Окислительно-восстановительные свойства
- 72. Хром Основные минералы, содержащие хром: Металлический хром – блестящий серебристо-белый металл. В соединениях хром проявляет степени
- 73. Получение хрома Алюмотермия 2. Кремнетермия 3. Электролиз растворов солей
- 74. Взаимодействие с простыми веществами Хром реагирует с простыми веществами только при нагревании, так как покрывается прочной
- 75. Взаимодействие со сложными веществами Хром вступает в реакцию с парами воды С кислотами неокислителями реагирует по
- 76. Взаимодействие со сложными веществами 3. Хром растворяется в азотной разбавленной кислоте на холоду 4. С концентрированными
- 77. Взаимодействие со сложными веществами 5. Хром взаимодействует со щелочными растворами окислителей, образуя раствор хромата жёлтого цвета
- 78. Оксид хрома (II) Чёрное кристаллическое вещество нерастворимое в воде. Получить его можно окисляя амальгамированный хром на
- 79. Гидроксид хрома (II) Нерастворимый в воде гидроксид жёлтого цвета, проявляющий основные свойства
- 80. Оксид хрома (III) Амфотерный твёрдый оксид зелёного цвета нерастворим в воде.
- 81. Получение Разложение дихромата аммония «химический вулкан»
- 82. Амфотерные свойства Cr2O3 Растворяется в кислотах Сплавляется со шеломами, образуя хромиты Сплавляется с карбонатами щелочных металлов,
- 83. С водным раствором щёлочи образуется комплексная соль – гексагидроксохромат (III) натрия
- 84. Гидроксид хрома (III) Амфотерный гидроксид, нерастворимый в воде серо-зелёного цвета, но растворимый в кислотах и щелочах
- 85. Получение гидроксидов хрома Гидроксиды хрома получаются путём добавления щёлочи в к растворам солей хрома
- 86. Или используют необратимый гидролиз солей хрома:
- 87. CrO3 оксид хрома Кристаллическое вещество красного цвета, кислотного характера. Растворяется в воде и образует две кислоты
- 88. Хроматы и дихроматы Соли хромовой и дихромовой кислот. Хроматы существуют только в щелочной среде (жёлтого цвета
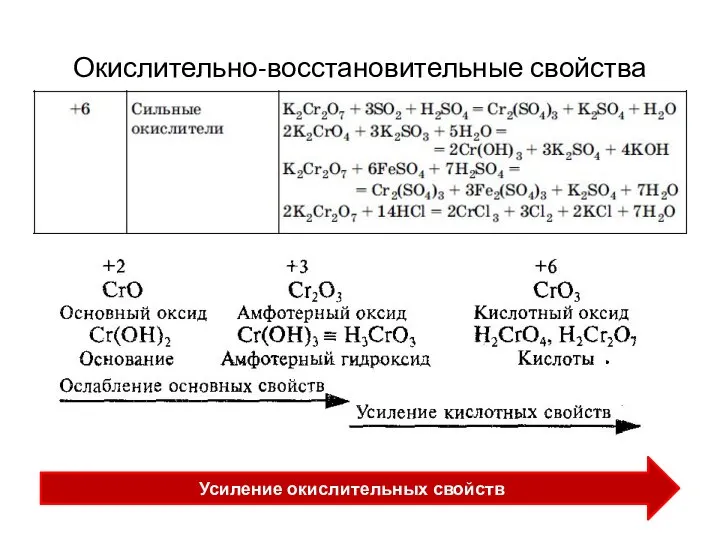
- 89. Окислительно-восстановительные свойства
- 90. Окислительно-восстановительные свойства Усиление окислительных свойств
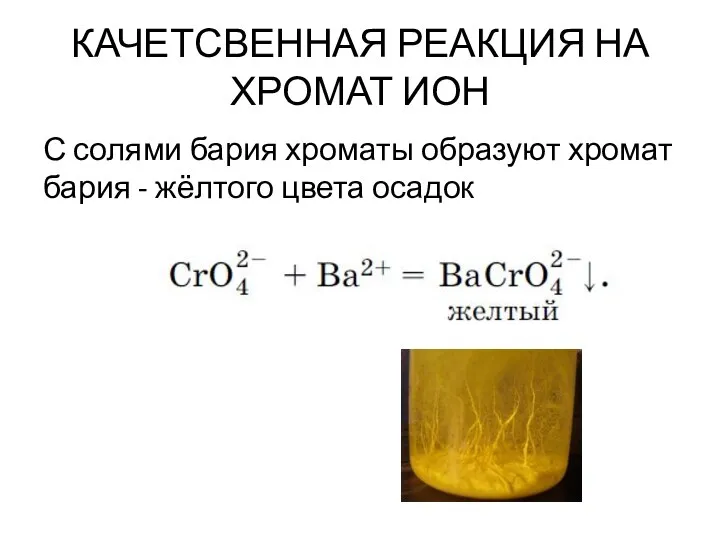
- 91. КАЧЕТСВЕННАЯ РЕАКЦИЯ НА ХРОМАТ ИОН С солями бария хроматы образуют хромат бария - жёлтого цвета осадок
- 93. Скачать презентацию













































































 Гидролиз солей
Гидролиз солей Характеристика ПМ общетехнического, инженерного и констркуционного назначения
Характеристика ПМ общетехнического, инженерного и констркуционного назначения Linear form of polyphenylsilsesquioxanes
Linear form of polyphenylsilsesquioxanes Тиімді қоректенудің биохимиялық негіздері. Қоректік заттар катаболизмінің жалпы жолдары
Тиімді қоректенудің биохимиялық негіздері. Қоректік заттар катаболизмінің жалпы жолдары Химическая связь
Химическая связь Альдегидтер және кетондар
Альдегидтер және кетондар Явление когда один элемент образует несколько простых веществ - аллотропия
Явление когда один элемент образует несколько простых веществ - аллотропия Презентация по Химии "Подгруппа углерода." - скачать смотреть
Презентация по Химии "Подгруппа углерода." - скачать смотреть  Растворы электролитов и неэлектролитов. (Лекция 2)
Растворы электролитов и неэлектролитов. (Лекция 2) Муниципальное образовательное учреждение «Лицей №3» Научно-исследовательская работа по химии «Получение ароматических масел»
Муниципальное образовательное учреждение «Лицей №3» Научно-исследовательская работа по химии «Получение ароматических масел» Презентация по Химии "Круговорот углерода в природе" - скачать смотреть бесплатно_
Презентация по Химии "Круговорот углерода в природе" - скачать смотреть бесплатно_ Химическая кинетика
Химическая кинетика Предпрофильный курс Мир химии
Предпрофильный курс Мир химии Термодинамика фазовых равновесий
Термодинамика фазовых равновесий Карбонові кислоти
Карбонові кислоти Синтетика в нашому житті
Синтетика в нашому житті  Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Свободные радикалы и болезни человека
Свободные радикалы и болезни человека Теория Опарина
Теория Опарина Kлассификация органических соединений. Углеводороды (алканы, алкены, алкины) лекция 1.2
Kлассификация органических соединений. Углеводороды (алканы, алкены, алкины) лекция 1.2 Биологически важные гетероциклы
Биологически важные гетероциклы «Круговорот кислорода в природе»
«Круговорот кислорода в природе»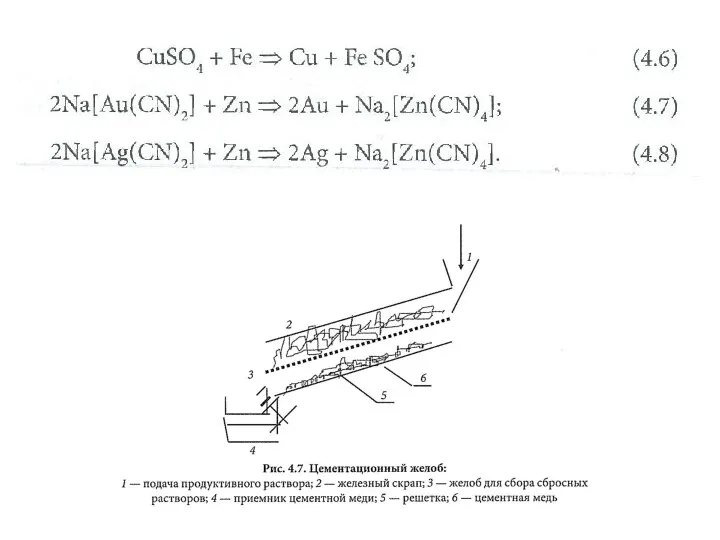 Гальванохимическая очистка. Сорбция
Гальванохимическая очистка. Сорбция Процессы горения. Способы сжигания топлива. Горелочные устройства
Процессы горения. Способы сжигания топлива. Горелочные устройства Металлы VБ–подгруппы
Металлы VБ–подгруппы Атомно – молекулярное учение
Атомно – молекулярное учение Металлы в периодической системе Д. И. Менделеева. железо
Металлы в периодической системе Д. И. Менделеева. железо Интоксикация пестицидами
Интоксикация пестицидами