Содержание
- 2. Основные понятия Кинетика – наука о скоростях и механизмах процессов Химическая кинетика изучает скорости и механизмы
- 3. Скорость химической реакции Под скоростью химической реакции понимается число элементарных актов взаимодействия реагентов в единицу времени
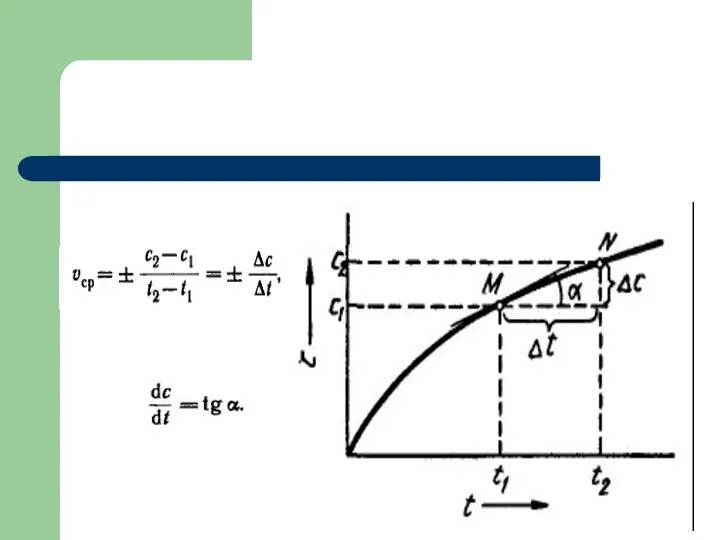
- 4. Скорость химической реакции На практике скорость химической реакции выражается изменением концентрации реагентов или продуктов в единицу
- 8. Классификация химических реакций а) Гомогенные- реакции в которых реагенты находятся в одном агрегатном состоянии б) Гетерогенные-
- 9. ВЛИЯНИЕ КОНЦЕНТРАЦИЙ РЕАГИРУЮЩИХ ВЕЩЕСТВ НА СКОРОСТЬ РЕАКЦИЙ В
- 10. Классификация химических реакций
- 11. Простые химические реакции Простая или элементарная реакция протекает в одну стадию, без образования промежуточных веществ. Простые
- 13. Мономолекулярная реакция – в элементарном акте участвует одна молекула (разложение)
- 14. Бимолекулярная реакция - в элементарном акте участвуют 2 молекулы (столкновение двух молекул)
- 15. Трехмолекулярная реакция в элементарном акте участвуют три молекулы, вероятность их столкновения мала
- 16. Сложные реакции Сложные реакции протекают в несколько стадий с образованием промежуточных продуктов. Сложные реакции бывают: последовательные
- 17. Последовательные реакции
- 18. Параллельные реакции
- 19. Цепные реакции
- 20. Закон действующих масс (Гульдберг и Вааге) Скорость химической реакции пропорциональна концентрации реагирующих веществ.
- 21. Где: СА, СВ – молярные концентрации реагентов в любой момент времени моль/л, k – константа скорости
- 22. ПРИМЕР: по N2O первый порядок, по Н2 первый порядок, суммарный - второй. Для простой реакции общий
- 23. Порядок реакции Если реакция сложная, то происходит ряд промежуточных превращений и порядок реакции равен порядку реакции
- 24. ПРИМЕР: Реакция образования воды, сложная цепная реакция: 2Н2 + О2 = 2Н2О Н2 + О2 =
- 25. ПРИМЕР: порядок по водороду - 0,4 порядок по кислороду – 0,3 сумма равна 0,7 порядок реакции
- 26. Графическое определение порядка реакции в координатах (C; t) Если построить зависимость в координатах концентрация от времени,
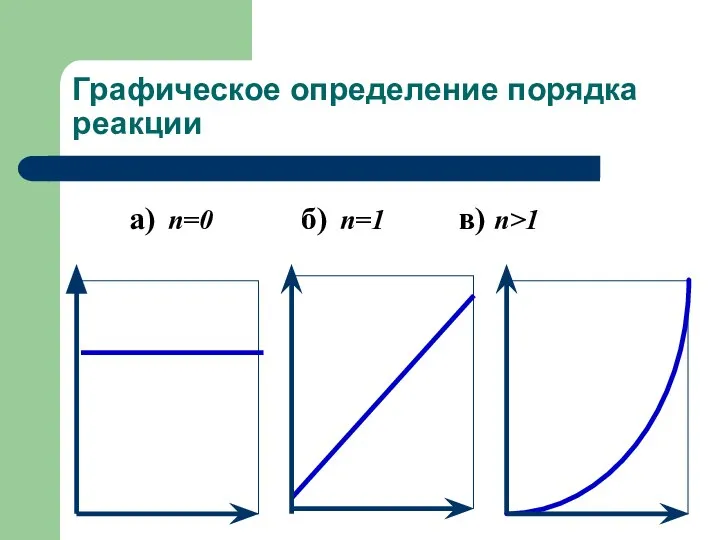
- 27. Графическое определение порядка реакции а) n=0 б) n=1 в) n>1
- 28. Влияние температуры на скорость химической реакции Чем выше температура, тем больше скорость химической реакции. Почему? При
- 29. Влияние температуры на скорость химической реакции Осуществить синтез воды 2Н2 + О2 = 2Н2О, при t
- 30. Влияние температуры на скорость химической реакции Правило Вант-Гоффа: При увеличении температуры на каждые 100 скорость химической
- 31. Температурный коэффициент γ – температурный коэффициент Вант-Гоффа, показывает во сколько раз возросла скорость химической реакции. Где
- 32. Пример: Во сколько раз увеличится скорость химической реакции при повышении Т от 200 до 500 ºС,
- 33. Решение:
- 34. Пример: При 100 ºС реакция идет за 16 минут , сколько времени надо при 140 ºС,
- 35. Решение:
- 36. Теория активации Увеличение скорости реакции с повышением температуры значительно больше, чем увеличение скорости движения молекул. Разъясняет
- 37. Теория активации Во взаимодействие вступают только активные молекулы, энергия которых превышает среднюю энергию молекул данного вещества.
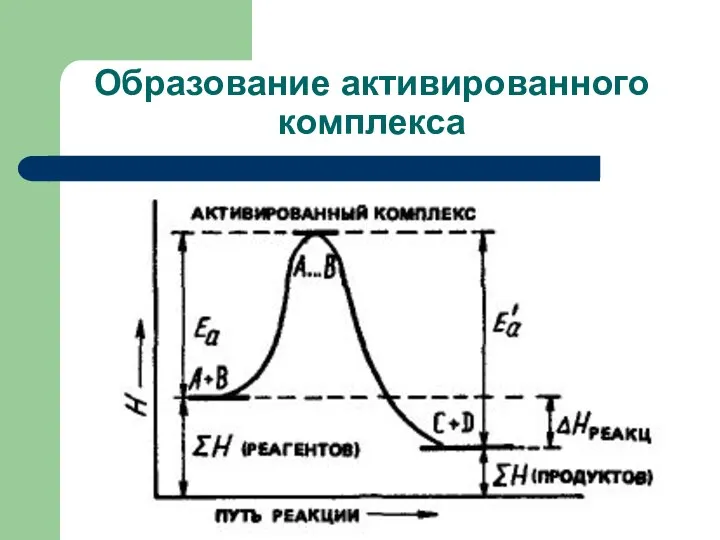
- 38. Энергия активации Энергия, которую надо придать молекулам реагирующих веществ, для того, чтобы сделать их активными, называется
- 39. Важно! Энергия активации характеристика реакции в целом, а не для вещества. Энергия активации - это наименьшая
- 40. Реакция начинается только между теми частицами, которые обладают повышенной энергией. Такие частицы при столкновении сначала образуют
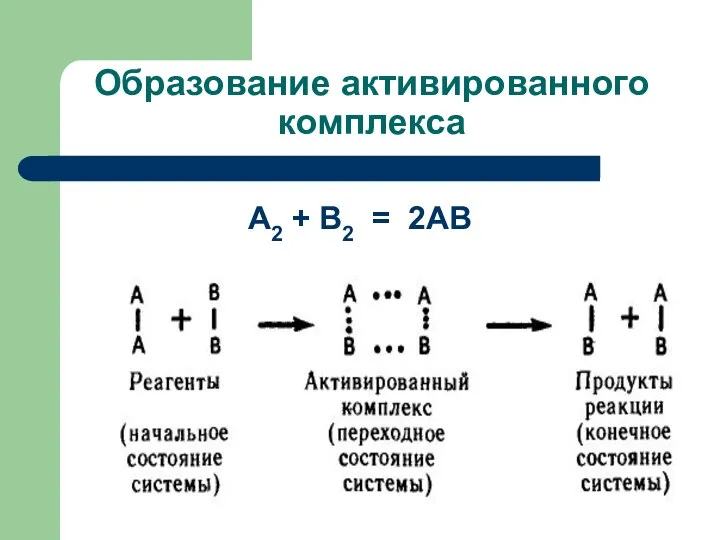
- 41. Образование активированного комплекса А2 + В2 = 2АВ
- 42. Пример: Н2 + J2 = 2HJ Электронные облака не дают взаимодействовать молекулам, избыточная энергия нужна для
- 43. Образование активированного комплекса
- 44. Образование активированного комплекса В активированном комплексе происходит перераспределение электронной плотности между атомами: связи А-В начинают образовываться
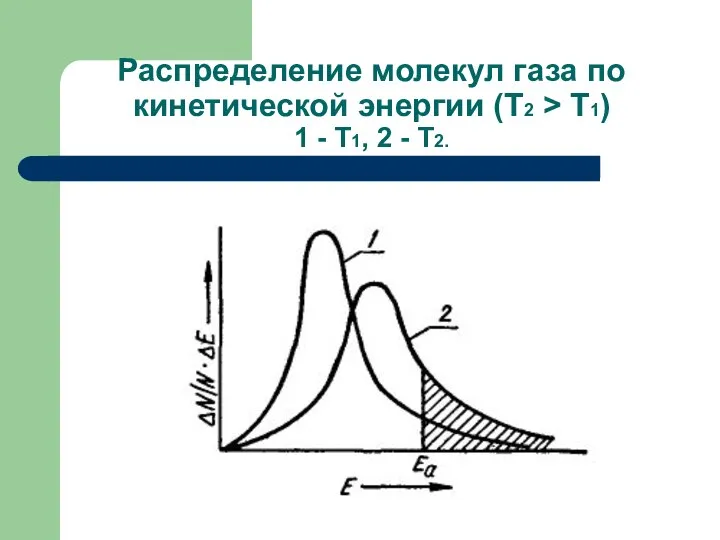
- 45. Распределение молекул газа по кинетической энергии (Т2 > Т1) 1 - Т1, 2 - Т2.
- 46. Уравнение Аррениуса К – константа скорости реакции, е – основание натурального логарифма, Т – температура, в
- 47. Из уравнения Аррениуса видно, что поскольку Т входит в показатель степени, скорость химической реакции очень чувствительна
- 48. Графический метод определения энергии активации Строят график в аррениусовских координатах (ln k – 1/T) ln k
- 49. Скорость химической реакции в значительной мере зависит от энергии активации. Для подавляющего большинства реакций она лежит
- 50. Пример: Энергия активации некоторой реакции при 500 К равна 80 кДж/моль. Определить долю активных молекул. Решение:
- 51. Влияние давления на скорость химической реакции Если в реакции участвуют газообразные вещества, то повышение давления равносильно
- 52. ↑ давления → ↑ конц-ции газа → ↑ v х.р. ↓ давления → ↓ конц-ции газа
- 53. Пример: 2NOгаз + 2H2газ → N2 + 2H2O Как изменится скорость химической реакции при увеличении давления
- 54. Решение: 2NOгаз + 2H2газ → N2 + 2H2O 1) V1 = k · РNO2 · РH22
- 55. КАТАЛИЗ
- 56. Катализ - это один из наиболее распространенных в химической практике методов ускорения химических реакций
- 57. Катализаторы – это вещества, которые ускоряют химические реакции за счет участия в образовании промежуточных соединений, в
- 58. В присутствии катализатора возникают другие активированные комплексы. Для их образования требуется меньше энергии, чем для образования
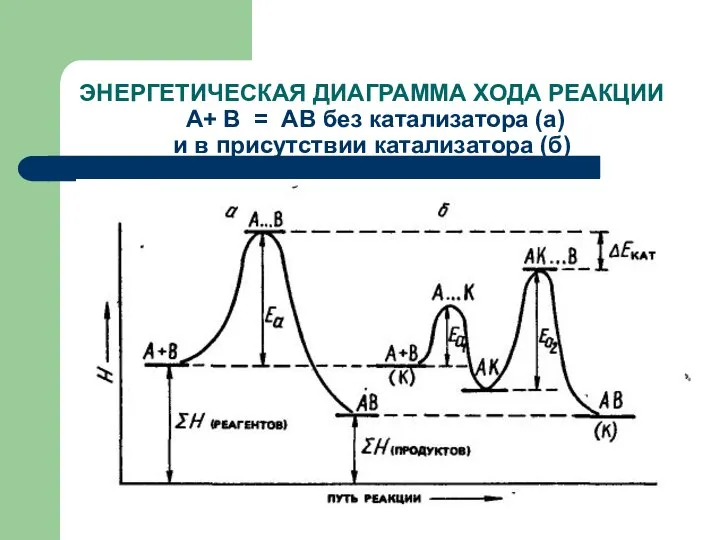
- 59. ЭНЕРГЕТИЧЕСКАЯ ДИАГРАММА ХОДА РЕАКЦИИ А+ В = АВ без катализатора (а) и в присутствии катализатора (б)
- 60. Т. о., в присутствии катализаторов энергия активации реакции понижается. Уменьшение энергии активации приводит к увеличению скорости
- 61. Пример Платина снижает значение Еа реакции Н2 + J2 = 2HJ от Еа =198 кДж/моль до
- 62. Пример Влияние катализатора на снижение энергии активации процесса Еа можно показать на следующих данных для реакции
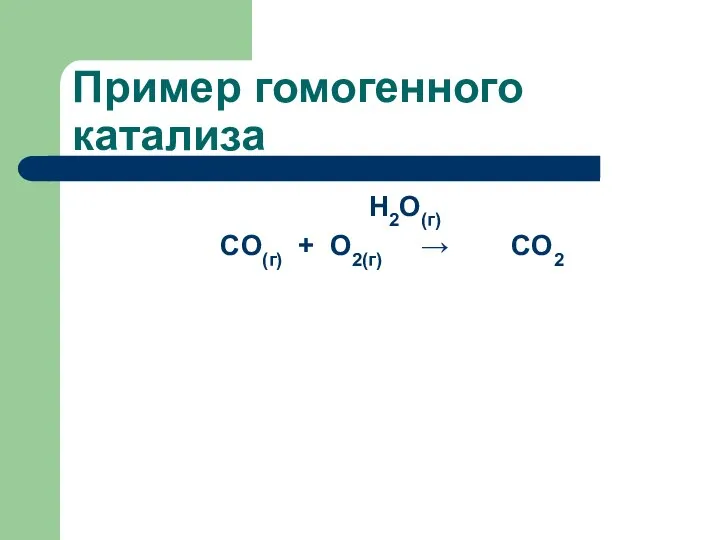
- 64. Пример гомогенного катализа
- 65. Пример гомогенного катализа H2O(г) CO(г) + О2(г) → CO2
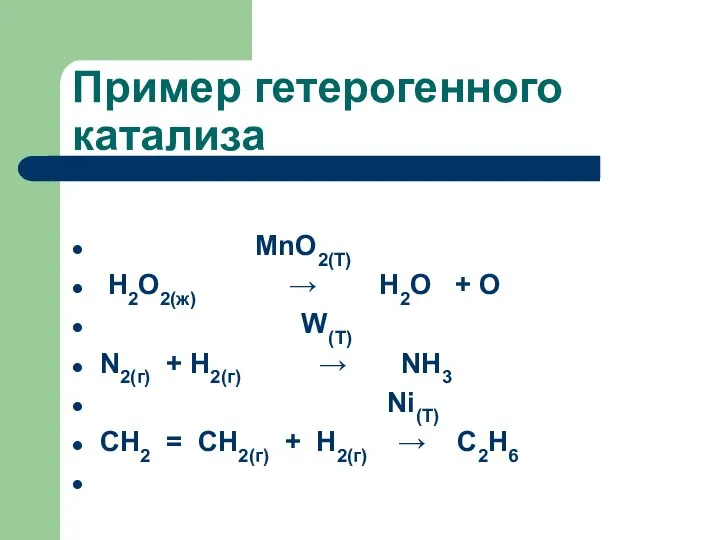
- 66. Пример гетерогенного катализа
- 67. Пример гетерогенного катализа MnO2(T) Н2О2(ж) → Н2О + О W(T) N2(г) + H2(г) → NH3 Ni(T)
- 68. Эффективность гетерогенных катализаторов обычно намного больше чем гомогенных. Скорость реакций в случае гомогенного катализатора зависит от
- 69. Сорбция - поглощение газа или жидкого вещества твердым веществом - сорбентом.
- 70. Различают: Адсорбция – поглощение поверхностью Абсорбция – поглощение всем объемом, поглощение газа жидкостью, или твердым веществом.
- 71. Пример Энергия активации некоторой реакции в отсутствии катализатора равна 75,24 кДж/моль, а с катализатором – 50,14
- 72. Выводы: 1. Скорость химической реакции зависит от температуры, концентрации реагирующих веществ, их природы и наличия катализатора.
- 74. Скачать презентацию































































 Формирование УУД на уроках химии
Формирование УУД на уроках химии Игра по химии Разработала учитель химии МОУ «Яльчикская СОШ» Левая В.Н.
Игра по химии Разработала учитель химии МОУ «Яльчикская СОШ» Левая В.Н. УРОК ПО ТЕМЕ: «ЧИСТАЯ ВОДА»
УРОК ПО ТЕМЕ: «ЧИСТАЯ ВОДА» Материалы будущего
Материалы будущего Строение вещества. Строение атома и периодическая система элементов
Строение вещества. Строение атома и периодическая система элементов Великие учёные Тюменской области
Великие учёные Тюменской области Кислоты. Повторение
Кислоты. Повторение Методы изготовления из резины и латекса
Методы изготовления из резины и латекса Вода. Химические и физические свойства воды
Вода. Химические и физические свойства воды Состав тонких покрытий
Состав тонких покрытий Коррозия и защита строительных материалов
Коррозия и защита строительных материалов Минералы
Минералы Учебно-познавательный проект на тему: «Физико-химические процессы, происходящие при выпечке и хранении хлеба и хлебобулочных изде
Учебно-познавательный проект на тему: «Физико-химические процессы, происходящие при выпечке и хранении хлеба и хлебобулочных изде Растворы. Классификация растворов. (Лекция 5)
Растворы. Классификация растворов. (Лекция 5) Пищевая биотехнология
Пищевая биотехнология Оксиды. Классификация оксидов
Оксиды. Классификация оксидов Выращивание кристаллов Выполнил: ученик 8 класса А Алексеев Ден
Выращивание кристаллов Выполнил: ученик 8 класса А Алексеев Ден Основные объекты исследования биофизики клеточных и мембранных процессов. Лекция 3-1
Основные объекты исследования биофизики клеточных и мембранных процессов. Лекция 3-1 Химия Для студентов I курса специальностей: 2080165 — экология, 08040165 — товароведение и экспертиза товаров, 260800 — технология, конс
Химия Для студентов I курса специальностей: 2080165 — экология, 08040165 — товароведение и экспертиза товаров, 260800 — технология, конс Обмен нуклеотидов
Обмен нуклеотидов Химическая и электрическая работа систем с химическими реакциями. Устройства для проведения электрохимических реакций
Химическая и электрическая работа систем с химическими реакциями. Устройства для проведения электрохимических реакций Классификация химических реакций
Классификация химических реакций Презентация по Химии "Электролиз расплавов и растворов" - скачать смотреть
Презентация по Химии "Электролиз расплавов и растворов" - скачать смотреть  Выполнила студентка ХБ-4 Ширяева София
Выполнила студентка ХБ-4 Ширяева София Презентация по Химии "Нитраты и организм человека" - скачать смотреть
Презентация по Химии "Нитраты и организм человека" - скачать смотреть  Функциональные наноматериалы. (Лекция 1)
Функциональные наноматериалы. (Лекция 1) Оксиды. Номенклатура, классификация, физические свойства
Оксиды. Номенклатура, классификация, физические свойства Концентраційні межі поширення полум'я
Концентраційні межі поширення полум'я