Примеры базовых моделей. Ферментативная кинетика Михаэлиса Ментен. Уравнение Моно. Исследование моделей на устойчивость
Содержание
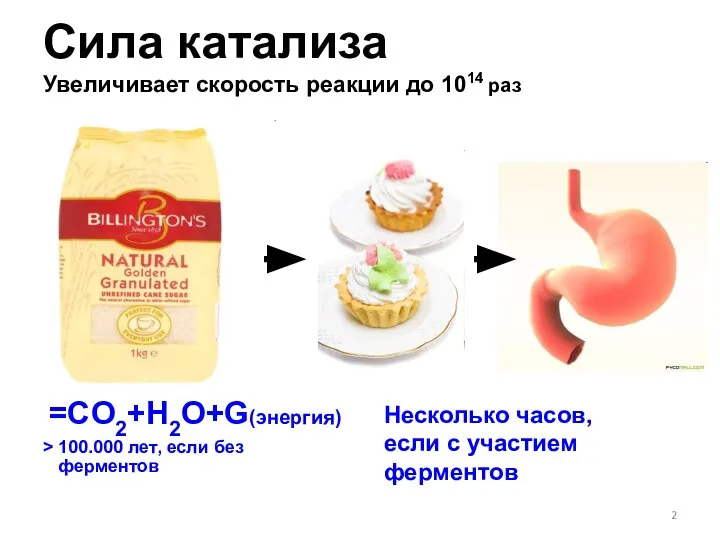
- 2. Сила катализа Увеличивает скорость реакции до 1014 раз =CO2+H2O+G(энергия) > 100.000 лет, если без ферментов Несколько
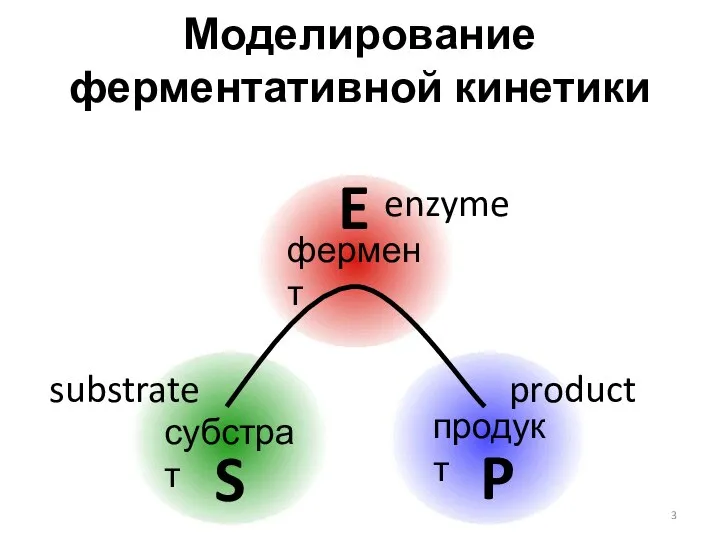
- 3. Моделирование ферментативной кинетики фермент субстрат продукт S E P enzyme substrate product
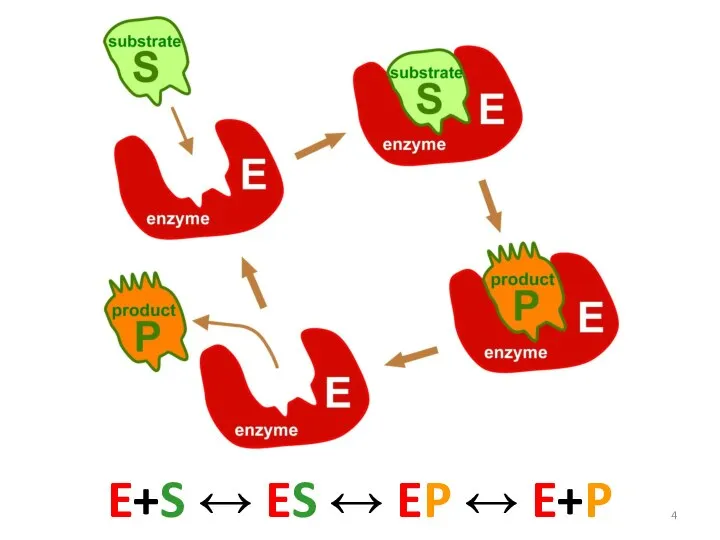
- 4. E+S ↔ ES ↔ EP ↔ E+P
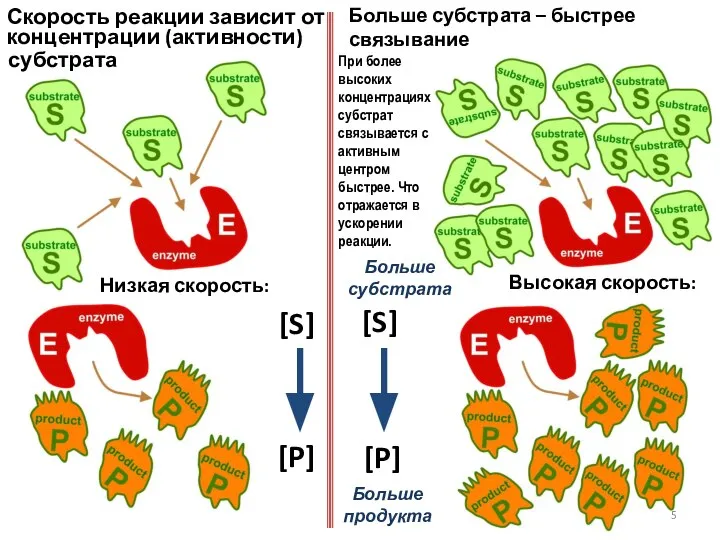
- 5. Больше субстрата – быстрее связывание Низкая скорость: Высокая скорость: Скорость реакции зависит от концентрации (активности) [S]
- 6. Насыщение происходит при какой-то высокой концентрации субстрата [S], когда дальнейшее повышение его уровня уже не приводит
- 7. Наиболее простая ферментативная реакция Е – фермент S – субстрат P – продукт ES – фермент-субстратный
- 8. Система дифференциальных уравнений, отвечающая схеме реакции
- 9. Сложив второе и третье уравнения системы получим или [E] + [ES] = E0 = const, То
- 10. Уравнение для скорости изменения фермент-субстратного комплекса, с использоваванием условия сохранения числа молекул фермента Исходя из третьего
- 11. Величина, Km называемая константой Михаэлиса, по физическому смыслу и числен-ному значению представляет собой концентра-цию субстрата, при
- 12. Из первого уравнения системы можно найти скорости убыли субстрата Когда концентрация фермент-субстратного комплекса не меняется во
- 13. Из четвертого уравнения системы можно найти скорость образования продукта Когда концентрация фермент-субстратного комплекса остается постоянной, Подставляем
- 14. Что дает уравнение Михаэлиса-Ментен Скорость простейшей ферментативной реакции линейно зависит от начальной концентрации фермента . Когда
- 15. Концентрация субстрата велика, S » Km Стационарная скорость ферментативной реакции как функция концентрации субстрата обладает свойством
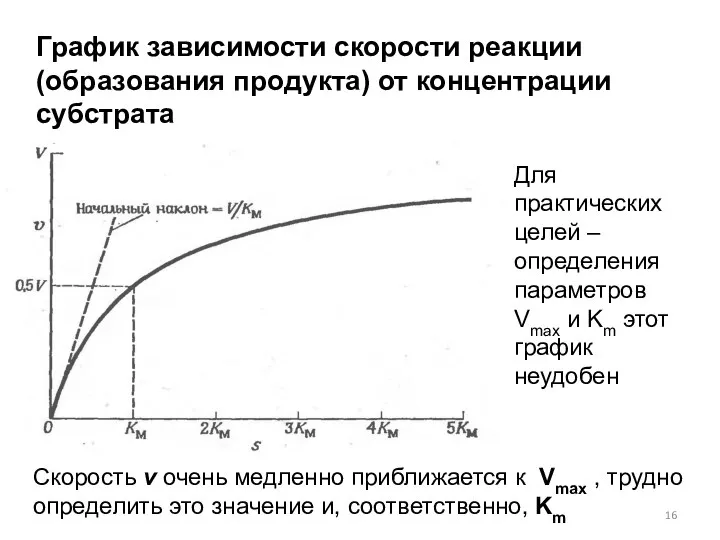
- 16. График зависимости скорости реакции (образования продукта) от концентрации субстрата Для практических целей – определения параметров Vmax
- 17. Концентрация субстрата велика, S » Km Стационарная скорость ферментативной реакции как функция концентрации субстрата обладает свойством
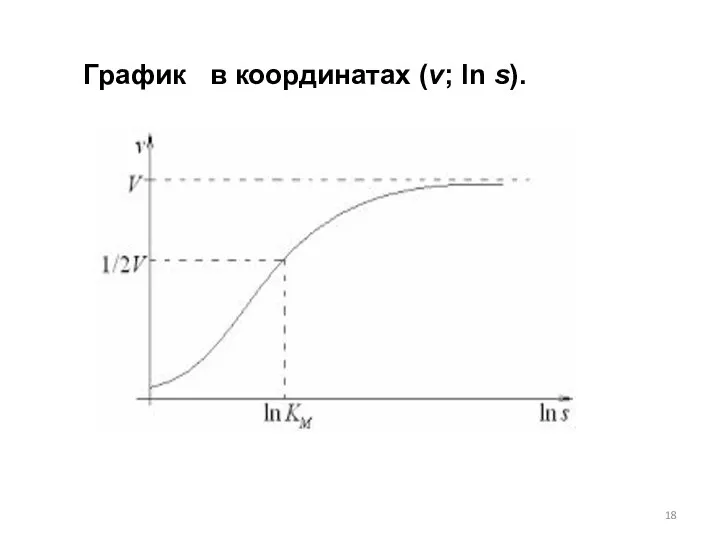
- 18. График в координатах (v; ln s).
- 19. или Варианты линеаризации зависимости скорости реакции от концентрации субстрата Метод Лайнуивера-Берка Метод Хайнса-Вульфа Метод Иди-Хофсти. Метод
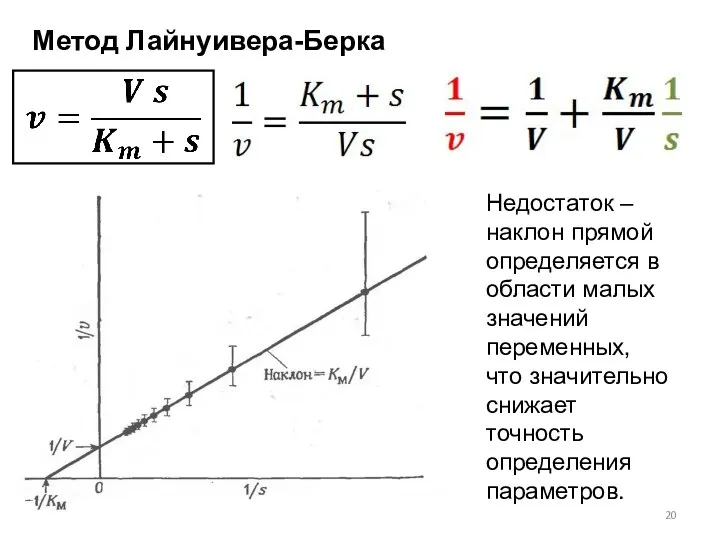
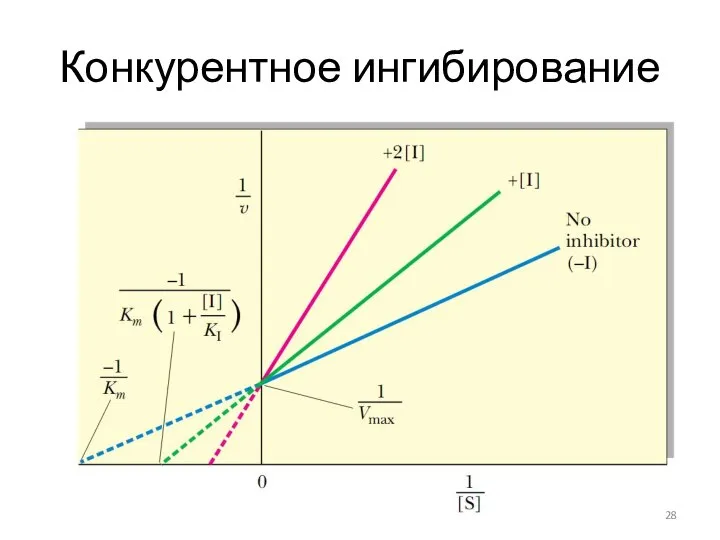
- 20. Метод Лайнуивера-Берка Недостаток – наклон прямой определяется в области малых значений переменных, что значительно снижает точность
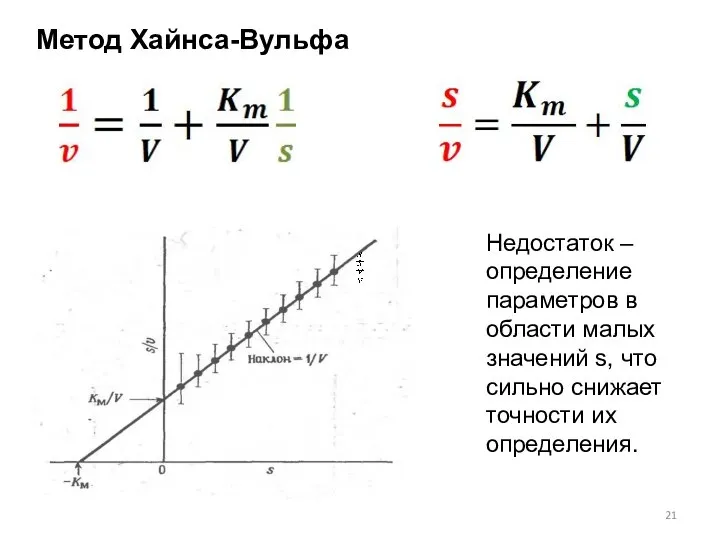
- 21. Метод Хайнса-Вульфа Недостаток – определение параметров в области малых значений s, что сильно снижает точности их
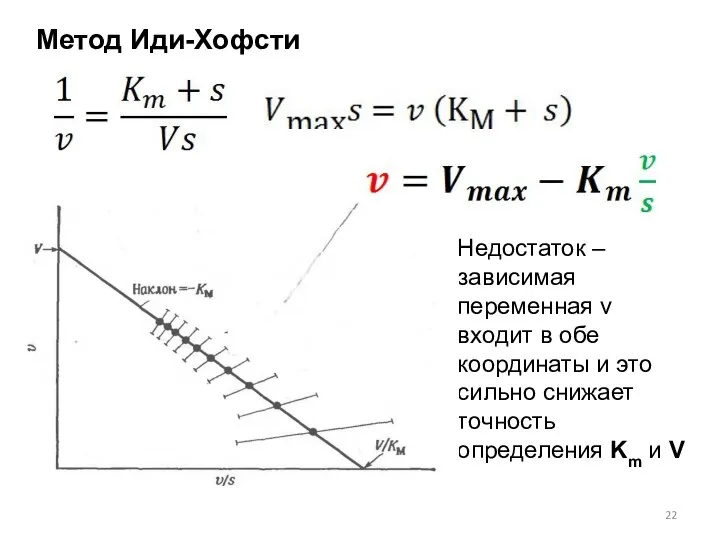
- 22. Метод Иди-Хофсти Недостаток – зависимая переменная v входит в обе координаты и это сильно снижает точность
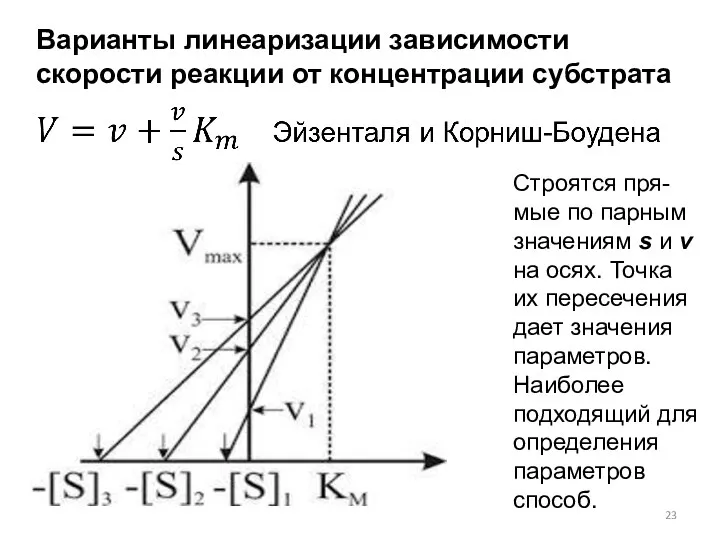
- 23. Варианты линеаризации зависимости скорости реакции от концентрации субстрата Строятся пря-мые по парным значениям s и v
- 24. Ингибирование Необратимое Обратимое: конкурентное неконкурентное бесконкурентное смешанное
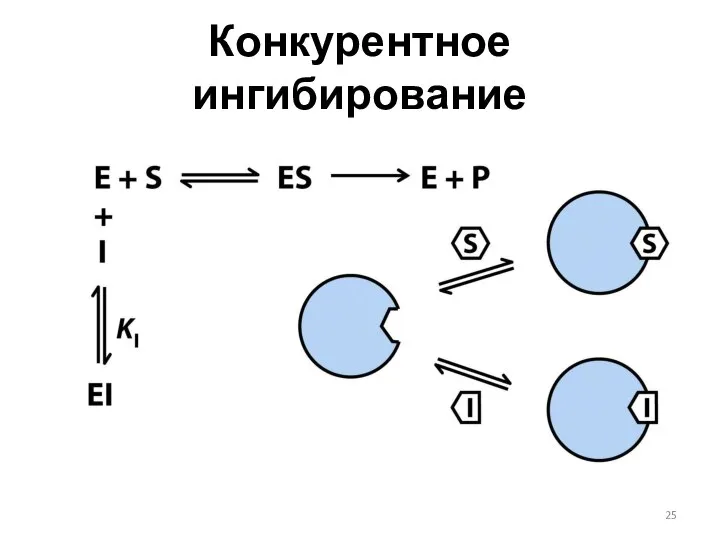
- 25. Конкурентное ингибирование
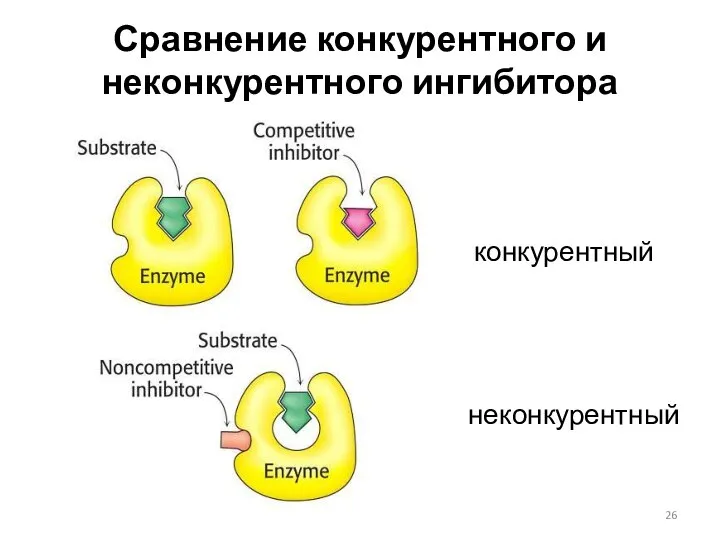
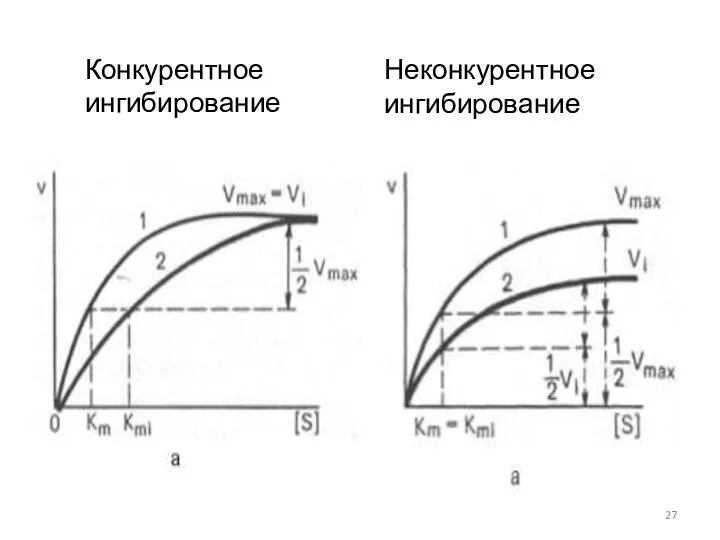
- 26. Сравнение конкурентного и неконкурентного ингибитора конкурентный неконкурентный
- 27. Конкурентное ингибирование Неконкурентное ингибирование
- 28. Конкурентное ингибирование
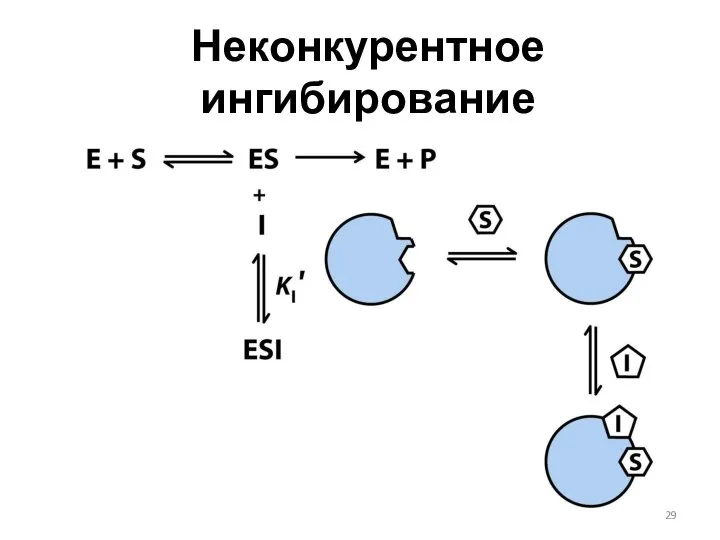
- 29. Неконкурентное ингибирование
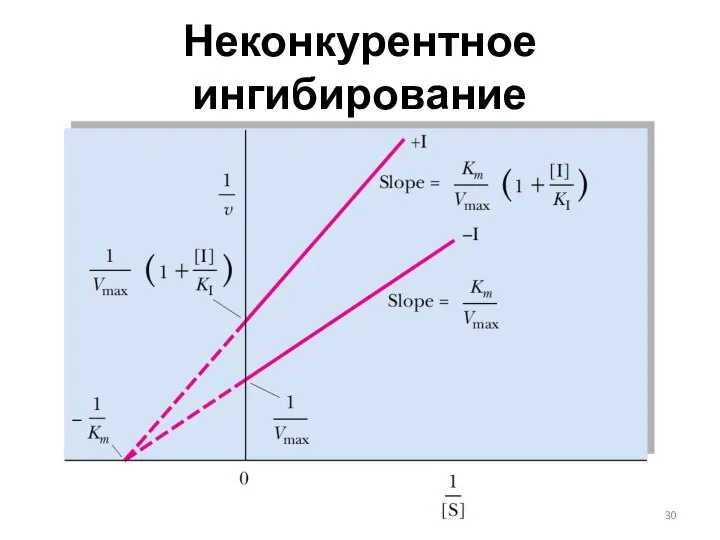
- 30. Неконкурентное ингибирование
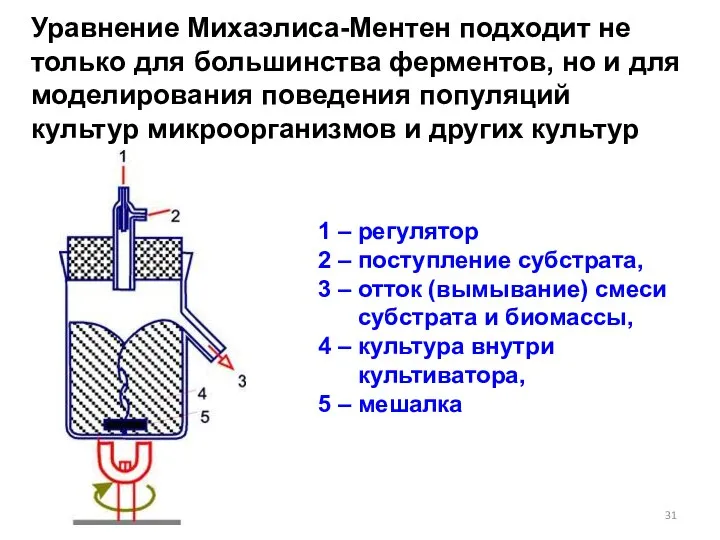
- 31. Уравнение Михаэлиса-Ментен подходит не только для большинства ферментов, но и для моделирования поведения популяций культур микроорганизмов
- 32. Для микробиологических систем обычно величина, лимитирующая рост, это ‑ концентрация субстрата. Наиболее распространенная форма записи, учитывающая
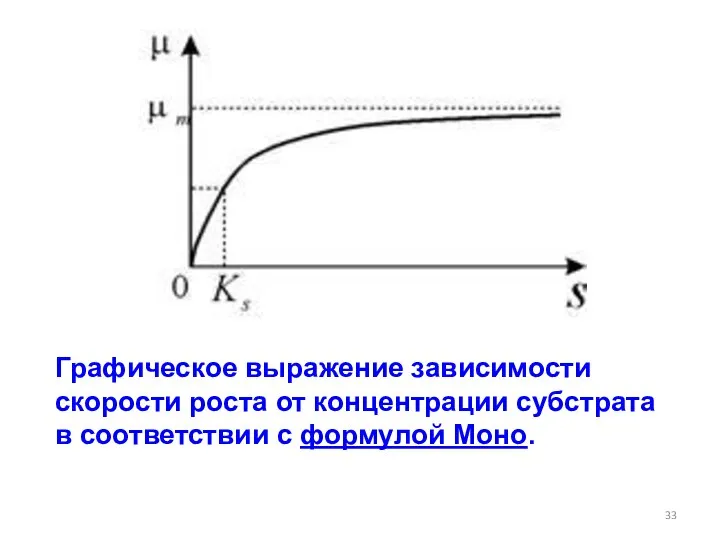
- 33. Графическое выражение зависимости скорости роста от концентрации субстрата в соответствии с формулой Моно.
- 34. При перемешивании можно считать весь объем культиватора однородно заполненным, концентрации субстрата и клеток в каждой точке
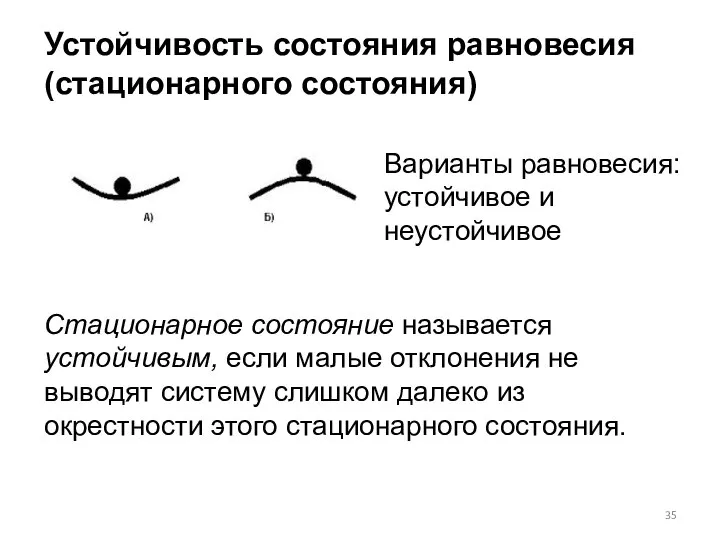
- 35. Устойчивость состояния равновесия (стационарного состояния) Варианты равновесия: устойчивое и неустойчивое Стационарное состояние называется устойчивым, если малые
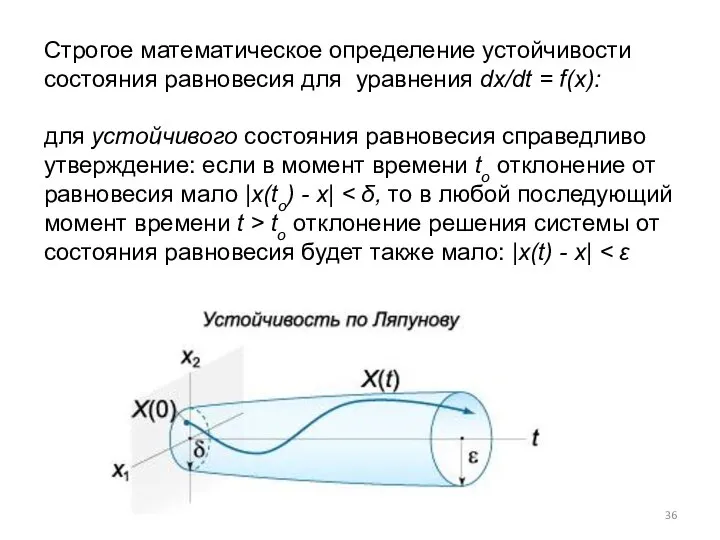
- 36. Строгое математическое определение устойчивости состояния равновесия для уравнения dx/dt = f(x): для устойчивого состояния равновесия справедливо
- 37. Математический метод Ляпунова определения устойчивости состоит в прямом использовании определения устойчивости
- 39. Скачать презентацию
![Насыщение происходит при какой-то высокой концентрации субстрата [S], когда дальнейшее повышение](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1468400/slide-5.jpg)


![Сложив второе и третье уравнения системы получим или [E] + [ES]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1468400/slide-8.jpg)












 Виды многоугольников
Виды многоугольников Связь между автоматами Мили и Мура
Связь между автоматами Мили и Мура Ознаки предметів
Ознаки предметів Применение нескольких способов разложения многочленов на множители
Применение нескольких способов разложения многочленов на множители 1 класс. Математика. Знаки: «>» (больше), «<» (меньше)
1 класс. Математика. Знаки: «>» (больше), «<» (меньше) Математические головоломки
Математические головоломки Решение неравенств второй степени с двумя переменными
Решение неравенств второй степени с двумя переменными Презентация по математике "Нахождение неизвестного слагаемого" - скачать
Презентация по математике "Нахождение неизвестного слагаемого" - скачать  Разработка тестовых материалов по модели SAM
Разработка тестовых материалов по модели SAM Викторина по математике для 5 - 6 классов
Викторина по математике для 5 - 6 классов Тема: «Преобразование графиков функции»
Тема: «Преобразование графиков функции» Дроби и проценты. Сравнение дробей
Дроби и проценты. Сравнение дробей Прямая и обратная пропорциональные зависимости
Прямая и обратная пропорциональные зависимости Презентация по математике "Метод интервалов" - скачать
Презентация по математике "Метод интервалов" - скачать  Логические элементы
Логические элементы  Область определения и множество значений тригонометрических функций
Область определения и множество значений тригонометрических функций Переводы чисел из одной системы счисления в другую
Переводы чисел из одной системы счисления в другую Сумма углов треугольника. Внешний угол треугольника. Математический диктант
Сумма углов треугольника. Внешний угол треугольника. Математический диктант Презентация по математике "Урок математики В 3 классе" - скачать бесплатно
Презентация по математике "Урок математики В 3 классе" - скачать бесплатно Множества. Основные понятия
Множества. Основные понятия Иррациональные уравнения. Задания для устного счета
Иррациональные уравнения. Задания для устного счета Деление
Деление Понятие логарифма
Понятие логарифма Задачі на знаходження суми двох добутків. Задачі, обернені до задач на знаходження суми двох добутків
Задачі на знаходження суми двох добутків. Задачі, обернені до задач на знаходження суми двох добутків Признаки равенства треугольников Третий признак равенства треугольников
Признаки равенства треугольников Третий признак равенства треугольников Класс точности СИ и его обозначение. Погрешности измерений. Источники и классификация погрешностей измерений
Класс точности СИ и его обозначение. Погрешности измерений. Источники и классификация погрешностей измерений статистические методы обработки данных 22 слайда МОУ ДОД ДЮЦ «ЕДИНСТВО»
статистические методы обработки данных 22 слайда МОУ ДОД ДЮЦ «ЕДИНСТВО»  Презентация по математике "Математика - царица всех наук" - скачать бесплатно
Презентация по математике "Математика - царица всех наук" - скачать бесплатно