Содержание
- 2. Введение ГИБП стало главным прорывом в лечении ревматических заболеваний Основные ГИБП: Блокаторы ФНО альфа Блокаторы ИЛ-
- 3. Генно-инженерные биологические препараты (ГИБП) в ревматологии Белковые структуры, полученные при помощи генно-инженерной технологии Разновидности молекул Растворимые
- 4. Эффекты биологических препаратов: 1.Иммунодепрессивный (характерна селективность) 2. Противовоспалительный 3. Антидеструктивный (способны полностью затормозить и даже предотвратить
- 5. Характерные отличительные черты биологических препаратов Быстрое развитие клинического эффекта (ингибиторы ФНО) Способность вызывать стойко низкую активность
- 6. Фармакологические свойства биологических препаратов из группы БПВП
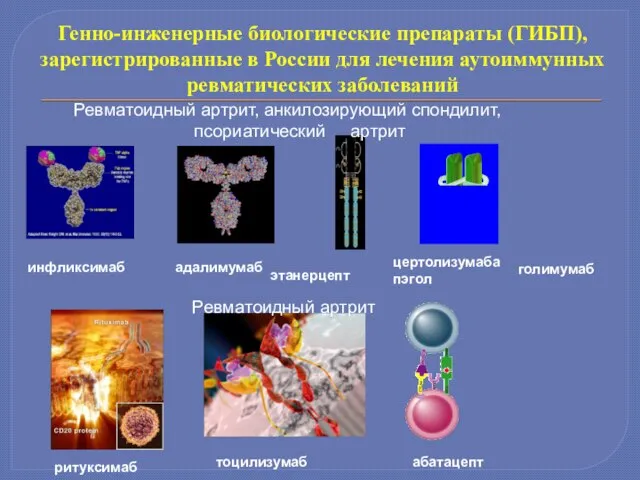
- 7. Генно-инженерные биологические препараты (ГИБП), зарегистрированные в России для лечения аутоиммунных ревматических заболеваний инфликсимаб адалимумаб этанерцепт Ревматоидный
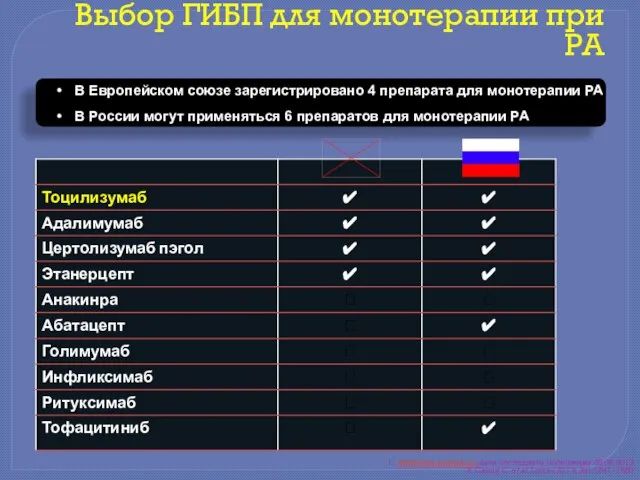
- 8. Выбор ГИБП для монотерапии при РА 1.. www.ema.europa.eu, дата последнего посещения 28.08.2013 2. Gabay C, et
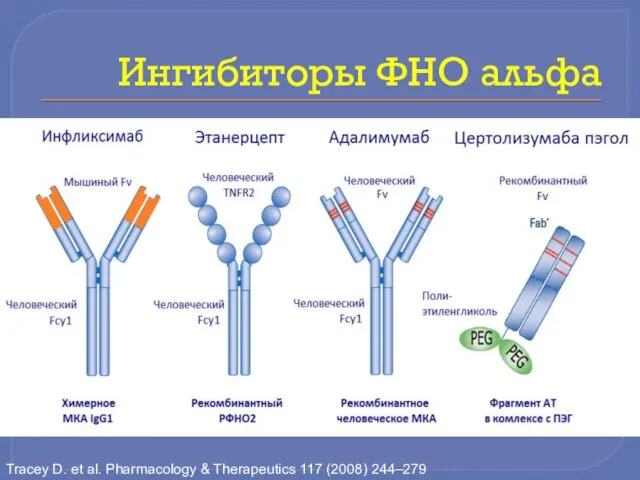
- 9. Ингибиторы ФНО альфа Tracey D. et al. Pharmacology & Therapeutics 117 (2008) 244–279
- 12. Этанерцепт Этанерцепт – единственный растворимый рецептор к ФНО альфа. Первый ингибитор ФНО альфа, зарегистрированный для лечения
- 13. Этанерцепт («Энбрел») Человеческие растворимые рецепторы к ФНО-альфа Показания* Ревматоидный артрит (±метотрексат) Ювенильный идиопатический артрит (с 2-х
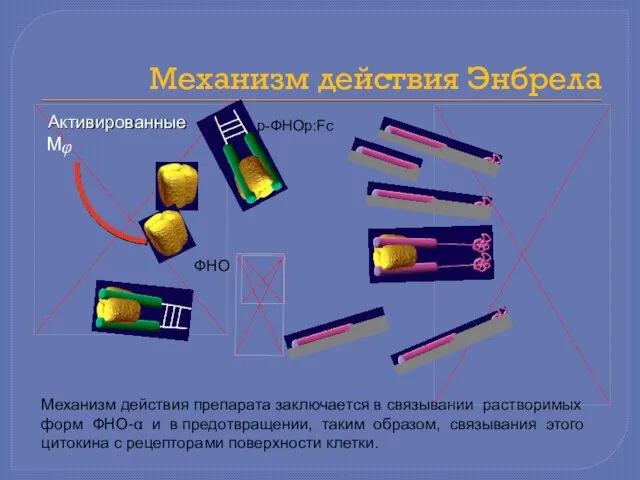
- 14. Механизм действия препарата заключается в связывании растворимых форм ФНО-α и в предотвращении, таким образом, связывания этого
- 15. Этанерцепт («Энбрел») особенности применения Подкожно Дозировка препарата ВЗРОСЛЫЕ: по 50 мг в неделю ИЛИ по 25
- 16. Лиофилизат для приготовления раствора по 10 мг* Лиофилизат для приготовления раствора по 25 мг** Шприц с
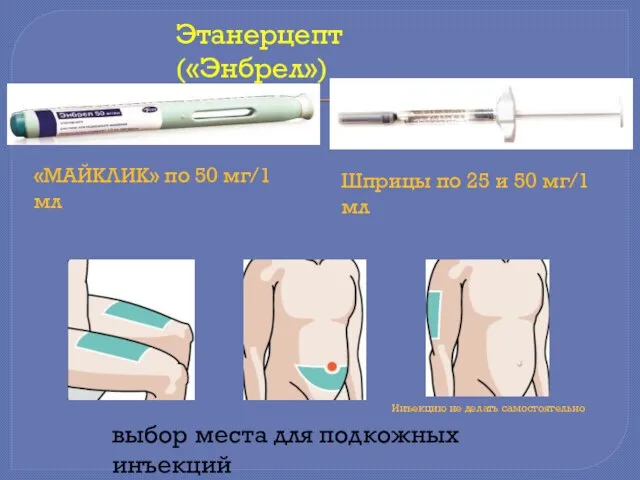
- 17. «МАЙКЛИК» по 50 мг/1 мл Шприцы по 25 и 50 мг/1 мл выбор места для подкожных
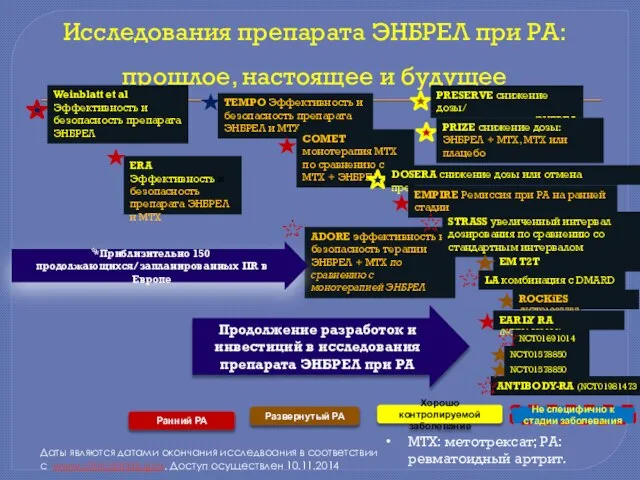
- 19. Исследования препарата ЭНБРЕЛ при РА: прошлое, настоящее и будущее Даты являются датами окончания исследвоания в соответствии
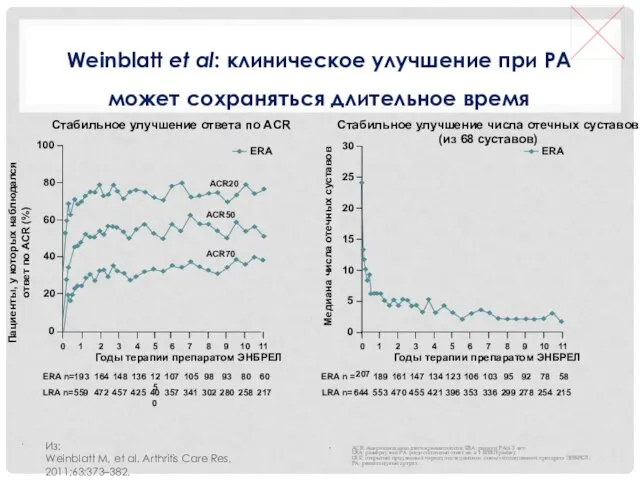
- 20. Weinblatt et al: клиническое улучшение при РА может сохраняться длительное время Из: Weinblatt M, et al.
- 21. PRESERVE: предотвращение рентгенологического прогрессирования у пациентов с РА Smolen J, et al. Lancet. 2013;381:918–929 mITT, модифицированная
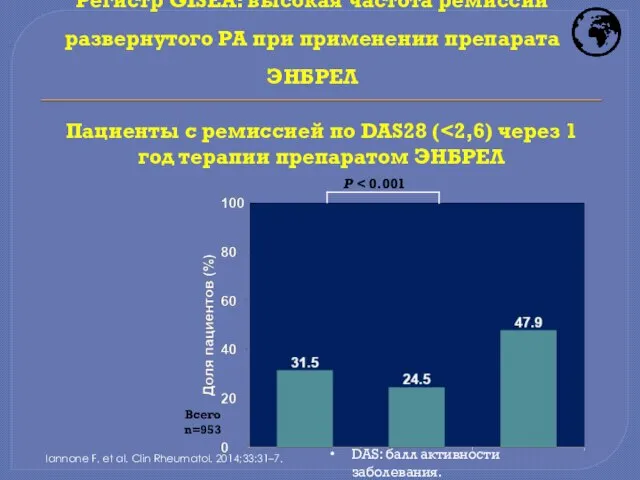
- 22. P Всего n=953 Регистр GISEA: высокая частота ремиссии развернутого РА при применении препарата ЭНБРЕЛ Iannone F,
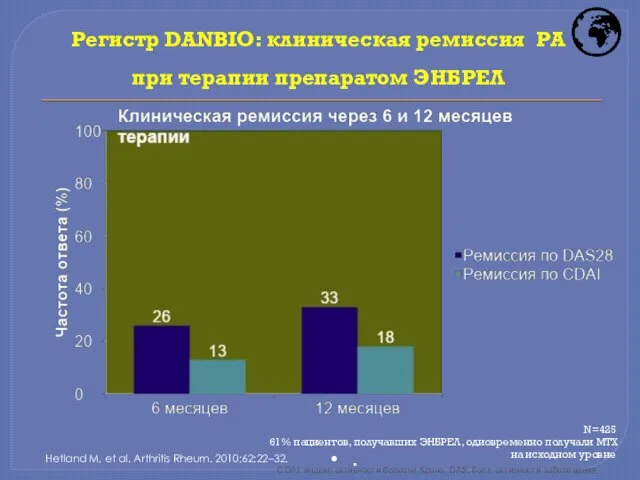
- 23. Регистр DANBIO: клиническая ремиссия РА при терапии препаратом ЭНБРЕЛ Hetland M, et al. Arthritis Rheum. 2010;62:22–32.
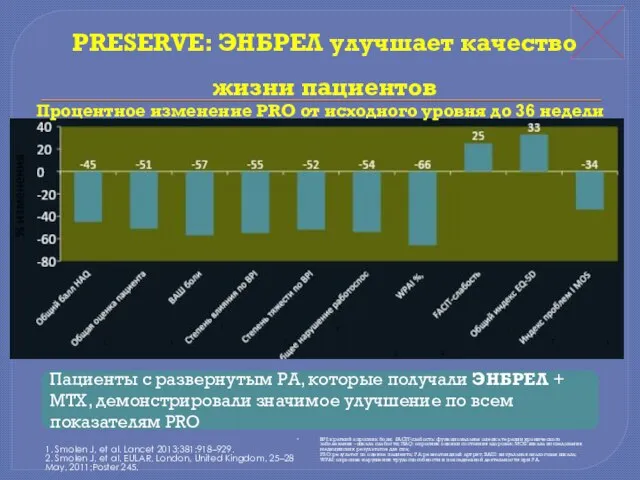
- 24. PRESERVE: ЭНБРЕЛ улучшает качество жизни пациентов 1. Smolen J, et al. Lancet 2013;381:918–929. 2. Smolen J,
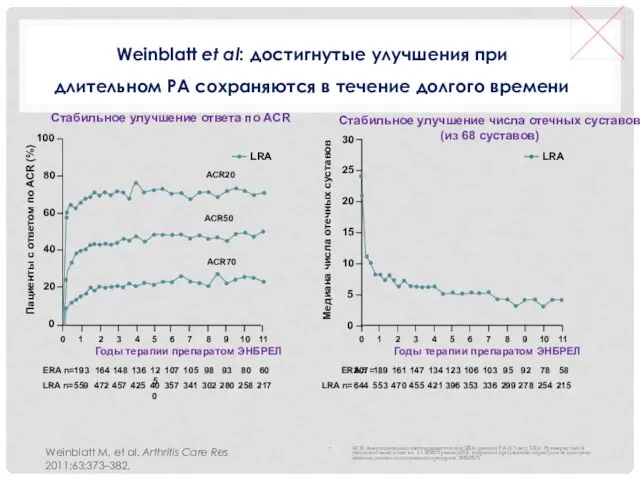
- 25. Weinblatt et al: достигнутые улучшения при длительном РА сохраняются в течение долгого времени Weinblatt M, et
- 26. Эффективность этанерцепта Этанерцепт достоверно снижает скорость рентгенологического прогрессирования суставов при РА Этанерцепт – эффективный препарат для
- 27. Keystone E, et al. Ann Rheum Dis. 2009;68:789-796 Клинический ответ при ревматоидном артрите Этанерцепт в комбинации
- 28. Этанерцепт («Энбрел») противопоказания* Повышенная чувствительность к этанерцепту или любому другому компоненту препарата. Сепсис или риск возникновения
- 29. Лекарственные взаимодействия Не наблюдалось нежелательных взаимодействий при одновременном применении препарата Энбрел® с глюкокортикостероидами, салицилатами (за исключением
- 30. Нежелательные сочетания Сульфасалазин У пациентов, которым на фоне лечения сульфасалазином вводили Энбрел®, описано значительное снижение числа
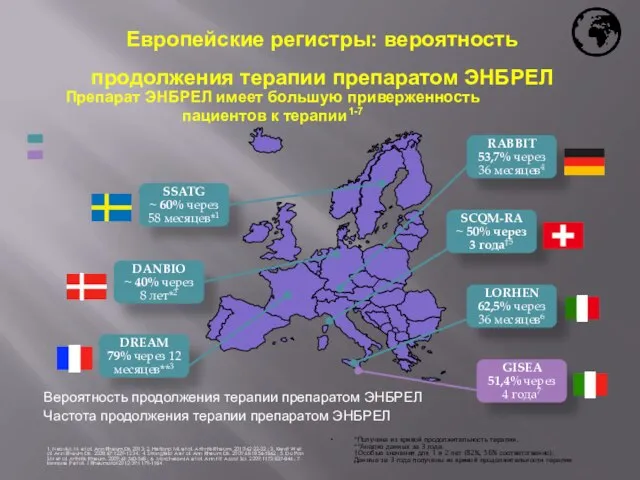
- 31. Европейские регистры: вероятность продолжения терапии препаратом ЭНБРЕЛ 1. Neovius M, et al. Ann Rheum Dis 2013;
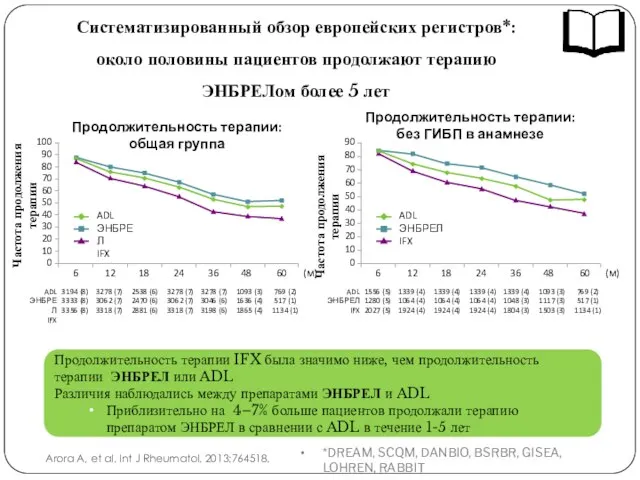
- 32. Систематизированный обзор европейских регистров*: около половины пациентов продолжают терапию ЭНБРЕЛом более 5 лет Arora A, et
- 33. Мета-анализ: ЭНБРЕЛ не обладает клинически значимой иммуногенностью 17 исследований иммуногенности при терапии воспалительных заболеваний ингибиторами ФНО
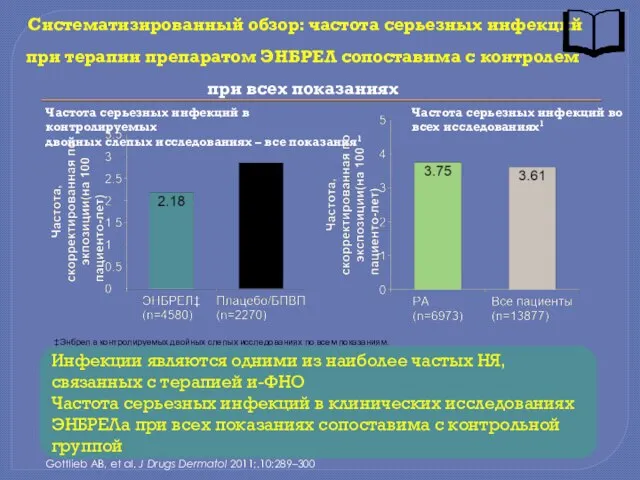
- 34. Систематизированный обзор: частота серьезных инфекций при терапии препаратом ЭНБРЕЛ сопоставима с контролем при всех показаниях Gottlieb
- 35. 0 2 4 6 8 10 0.6 0.7 0.8 0.9 1.0 Регистр BSRBR: более низкая смертность
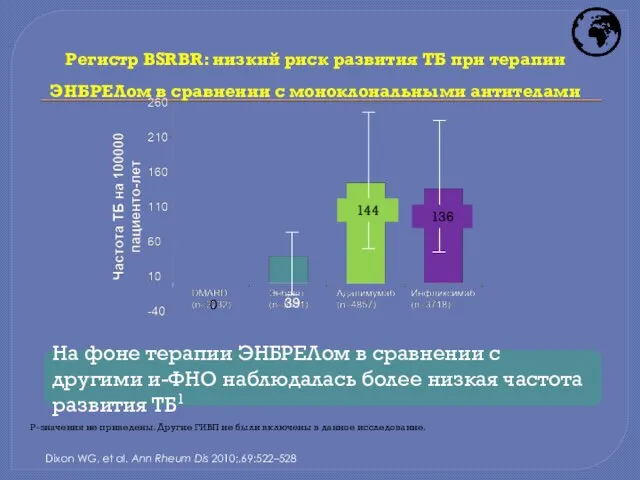
- 36. Регистр BSRBR: низкий риск развития ТБ при терапии ЭНБРЕЛом в сравнении с моноклональными антителами Dixon WG,
- 37. Выводы Этанерцепт – эффективный препарат, который снижает клинико- лабораторную активность, задерживает рентгенологическое прогрессирование поражения суставов, повышает
- 38. ….В 21 веке ЯКВИНУС – первый пероральный ингибитор JAK киназы для лечения ревматоидного артрита 2013г
- 39. ► Тофацитиниб(торговые наименования Xeljanz, Jakvinus) – низкомолекулярный пероральный препарат, блокирующий активность JAK киназы. ► Тофацитиниб обратимо
- 40. Яквинус: общие сведения Международное непатентованное наименование: тофацитиниб Торговое наименование: ЯКВИНУСTM Фармакотерапевтическая группа: селективные иммунодепрессанты Код АТХ:
- 41. ОСНОВНЫЕ ОТЛИЧИЯ ТОФАЦИТИНИБА ОТ ГИБП По сравнению с ГИБП, которые являются белками, тофацитиниб представляет собой простую
- 42. Способ применения и дозы Внутрь вне зависимости от приема пищи Яквинус можно применять в качестве монотерапии
- 43. Яквинус был изучен в рамках масштабной клинической разработки в разных странах мира Масштабная, продолжающаяся программа исследований:
- 44. Выводы Болезнь-модифицирующая терапия с включением Тофацитиниба позволяет существенно снизить активность РА и уменьшить выраженность иммунных сдвигов
- 46. Скачать презентацию

























 Anorexia
Anorexia Планирование семьи. Регулирование рождаемости. Контрацепция
Планирование семьи. Регулирование рождаемости. Контрацепция Переливание крови
Переливание крови Эпидемиологический контроль в родовспомагательных заведениях
Эпидемиологический контроль в родовспомагательных заведениях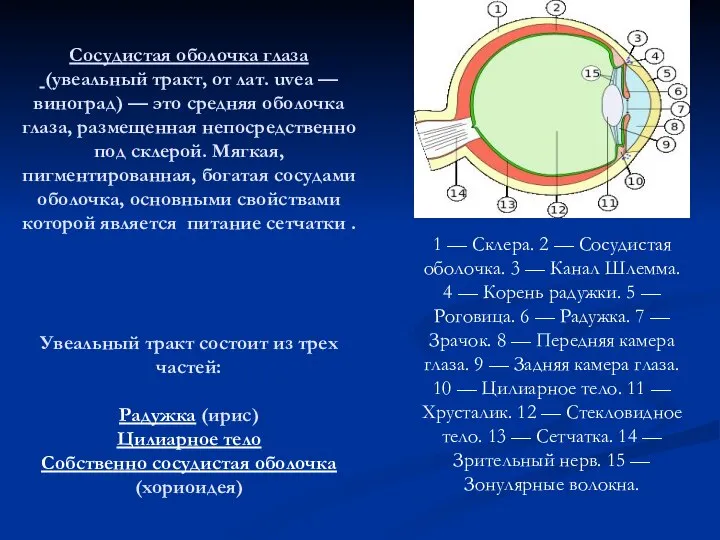 Сосудистая оболочка глаза
Сосудистая оболочка глаза Современные ингаляторы в лечении бронхиальной астмы. Влияние на приверженность терапии
Современные ингаляторы в лечении бронхиальной астмы. Влияние на приверженность терапии Пыль (аэрозоль)
Пыль (аэрозоль) Лазерный термолиз в гинекологии
Лазерный термолиз в гинекологии Туа біткен бұлшықеттік қисық мойын
Туа біткен бұлшықеттік қисық мойын Жыныстық изосексуалдық ерте жетілу
Жыныстық изосексуалдық ерте жетілу Топография таза и операции на органах таза
Топография таза и операции на органах таза Лимфодренажная гимнастика. Лимфодренажный самомассаж. Массаж ложками
Лимфодренажная гимнастика. Лимфодренажный самомассаж. Массаж ложками атерлі ісікті сәулелеік терапиямен негізі. Брахиотерапия мен сәуле терапияның негізі
атерлі ісікті сәулелеік терапиямен негізі. Брахиотерапия мен сәуле терапияның негізі Рожа свиней
Рожа свиней ОСТЕОХОНДРОЗ_ПОЗВОНОЧНИКА
ОСТЕОХОНДРОЗ_ПОЗВОНОЧНИКА Реставрация костного препарата (черепа)
Реставрация костного препарата (черепа) Основные принципы и средства физической реабилитации
Основные принципы и средства физической реабилитации Артериальная аневризма. Артерио-венозная мальформация. Клинические проявления. Лечение
Артериальная аневризма. Артерио-венозная мальформация. Клинические проявления. Лечение Қоғамдық денсаулық сақтаудағы ғылыми зерттеуді жоспарлаудың ерекшелігі
Қоғамдық денсаулық сақтаудағы ғылыми зерттеуді жоспарлаудың ерекшелігі 20 искусственных объектов для улучшения и поддержания здоровья, усовершенствования тела человека
20 искусственных объектов для улучшения и поддержания здоровья, усовершенствования тела человека Алгоритмы диагностики и лечения злокачественных новообразований
Алгоритмы диагностики и лечения злокачественных новообразований Символизация. Виды символизации
Символизация. Виды символизации Почки и артериальная гипертензия
Почки и артериальная гипертензия Основные способы получения клеточного материала для цитологического исследования
Основные способы получения клеточного материала для цитологического исследования Грудное вскармливание - здоровое начало жизни. Помощь и поддержка будущих и кормящих мам
Грудное вскармливание - здоровое начало жизни. Помощь и поддержка будущих и кормящих мам Менструальный цикл
Менструальный цикл Тестостерон. Лекция 9
Тестостерон. Лекция 9 Диагностика психологической готовности ребенка к школе
Диагностика психологической готовности ребенка к школе