Содержание
- 2. Этапы развития иммунологии 1. Период протоиммунологии (от античного периода до 80-х годов XIX века) – связан
- 3. 3. Развитие иммунологии до середины XX века — описание новых иммунологических феноменов, развитие инфекционной иммунологии 4.
- 4. Эдуард Дженнер прививка человеку коровьей оспы Луи Пастер принцип получения живых вакцин Основоположники иммунологии
- 5. Илья Ильич Мечников клеточная теория иммунитета Пауль Эрлих гипотеза об антителах
- 6. Габричевский Георгий Норбертоич описал явления хемотаксиса лейкоцитов Здродовский Павел Феликсович обосновал физиологическое направление в иммунологии
- 7. Н. А. Гайский вакцины против чумы, туляремии Лев Зильбер иммунология рака
- 8. Чумаков Михаил Петрович вакцина против полиомиелита, кори, гриппа, паротита Смородинцев Анатолий Александрович
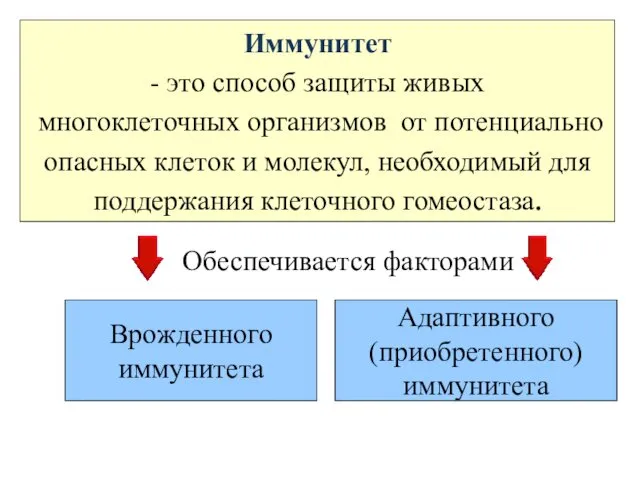
- 9. Иммунитет - это способ защиты живых многоклеточных организмов от потенциально опасных клеток и молекул, необходимый для
- 10. Основные источники экзогенной агрессии (проникающие из внешней среды): 1. микроорганизмы 2. высокомолекулярные продукты биологического происхождения (яды
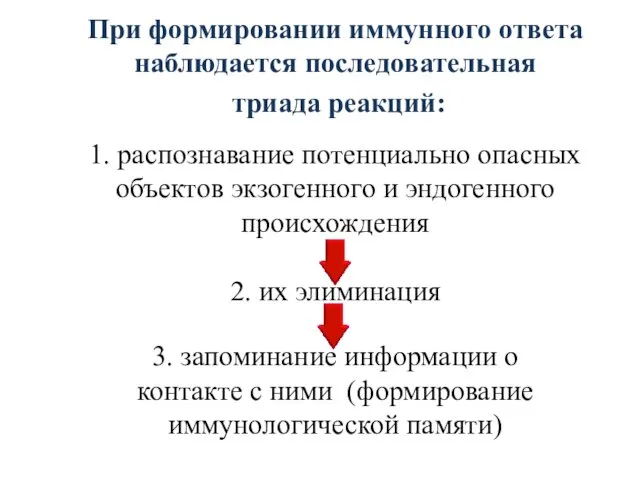
- 11. При формировании иммунного ответа наблюдается последовательная триада реакций: 1. распознавание потенциально опасных объектов экзогенного и эндогенного
- 12. Классификация видов иммунитета по этиологической направленности
- 13. Классификация видов иммунитета по локализации Классификация видов иммунитета по происхождению
- 15. 1. PAMP - образы патогенности, или патогенассоциированные молекулярные паттерны (Pathogen-associated molecular patterns) 2. Антигены 3. Стрессорные
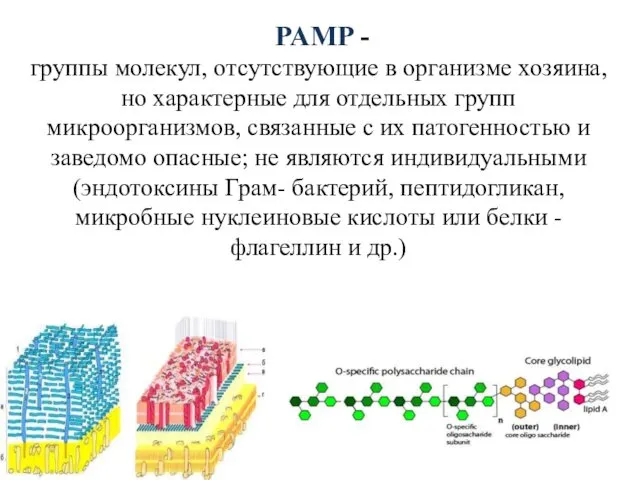
- 16. PAMP - группы молекул, отсутствующие в организме хозяина, но характерные для отдельных групп микроорганизмов, связанные с
- 17. Антигены ― высокомолекулярные соединения, способные специфически стимулировать иммунокомпетентные лимфоидные клетки и обеспечивать тем самым развитие иммунного
- 18. Рецепторы клеток организма, распознающие мишени иммунитета
- 19. Классификация патогенраспознающих рецепторов по функциям 1. эндоцитозные - опосредуют поглощение и доставку патогена к лизосомам, где
- 20. Врожденный иммунитет — наследственно закрепленная система защиты, объектом распознавания для которой являются PAMP и DAMP, формирующаяся
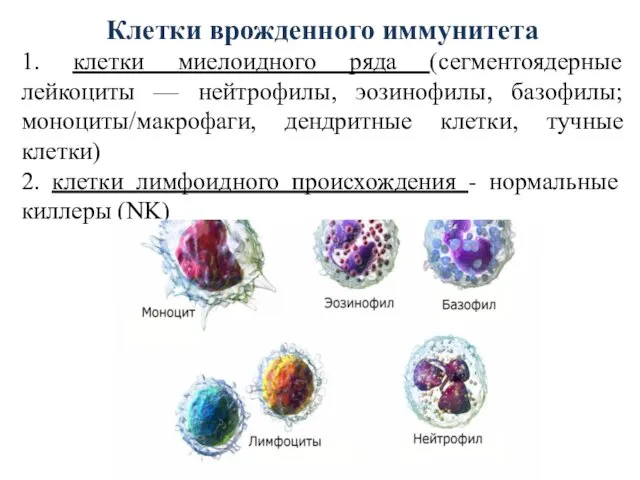
- 21. Клетки врожденного иммунитета 1. клетки миелоидного ряда (сегментоядерные лейкоциты — нейтрофилы, эозинофилы, базофилы; моноциты/макрофаги, дендритные клетки,
- 22. Нейтрофилы - созревают в костном мозге, после чего 70% депонируется на его территории, остальные выходят в
- 23. Эозинофилы гранулярные сегментоядерные лейкоциты крови (0,5-2,0%), после циркуляции в крови мигрирует в ткани, преимущественно пищеварительного тракта.
- 24. Базофилы и тучные клетки (мастоциты) Имеют сегментированное ядро, базофильные гранулы и дополнительные этапы созревания после костного
- 25. Дендритные клетки (ДК) Клетки, преимущественно миелоидного ряда, малая часть — лимфоидного. Имеют характерную отростчатую форму. Незрелые
- 26. Моноциты и макрофаги Моноциты – циркулирующие в крови клетки, при миграции в ткань трансформируются в макрофаги
- 27. Основные функции моноцитов/макрофагов: распознавание всех видов PAMP, фаго- и пиноцитоз клеток-мишеней и клеточных фрагментов с последующим
- 28. Естественные, или нормальные, киллеры большие гранулярные лимфоциты; отделяются в костном мозге от Т-клеточной линии; мигрируют в
- 29. Основные типы рецепторов и других молекул, представленных на клетках врожденного иммунитета: 1. рецепторы , распознающие PAMP
- 30. Основные эффекторные механизмы врожденного иммунитета реализуемые клетками 1. фагоцитоз (внутриклеточный киллинг) 2. контактный цитолиз клеток-мишеней 3.
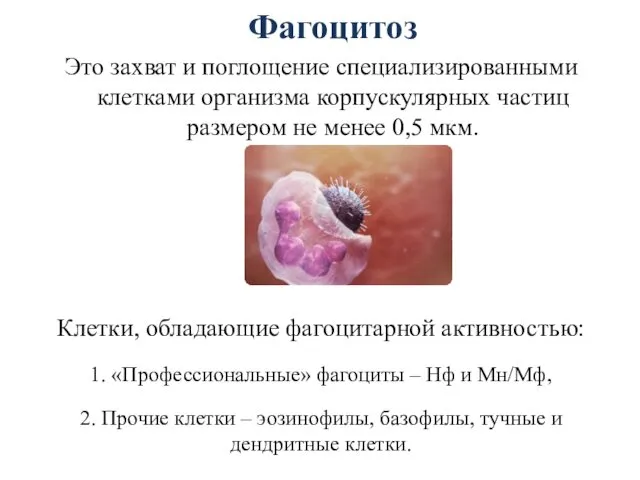
- 31. Фагоцитоз Это захват и поглощение специализированными клетками организма корпускулярных частиц размером не менее 0,5 мкм. Клетки,
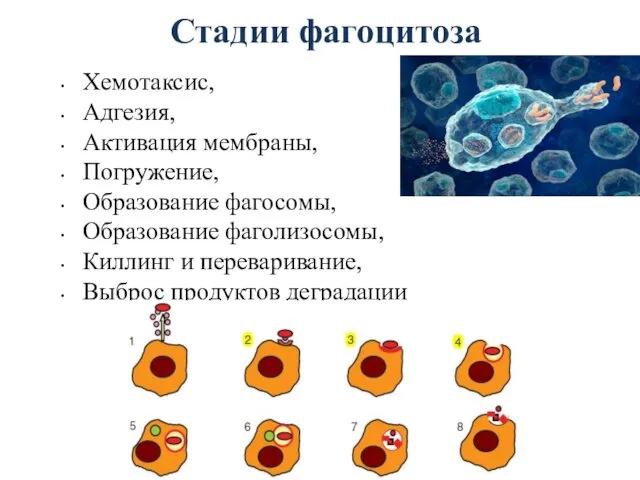
- 32. Стадии фагоцитоза Хемотаксис, Адгезия, Активация мембраны, Погружение, Образование фагосомы, Образование фаголизосомы, Киллинг и переваривание, Выброс продуктов
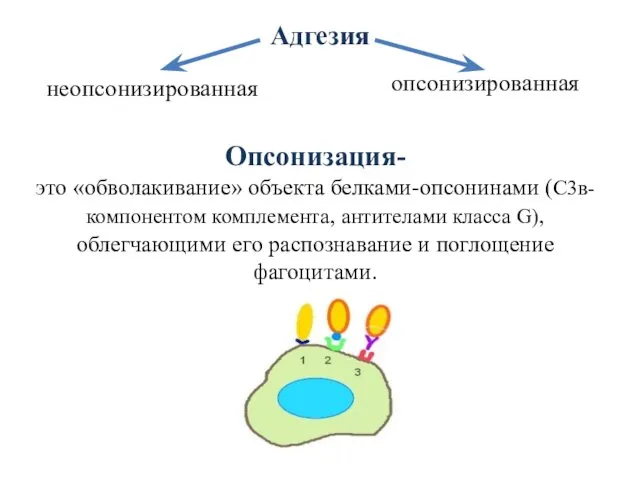
- 33. Адгезия Опсонизация- это «обволакивание» объекта белками-опсонинами (С3в-компонентом комплемента, антителами класса G), облегчающими его распознавание и поглощение
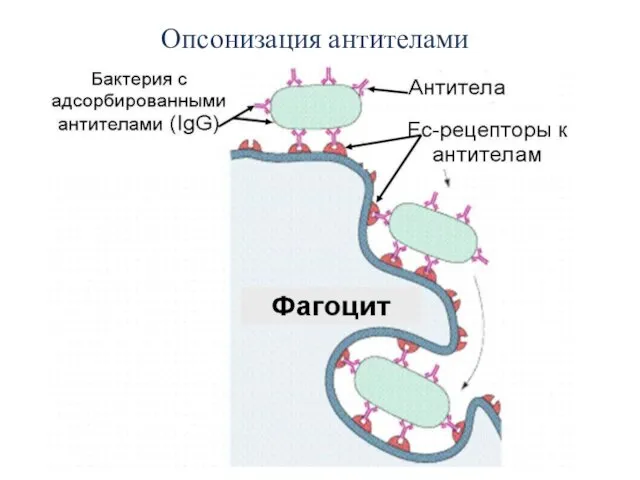
- 34. Опсонизация антителами
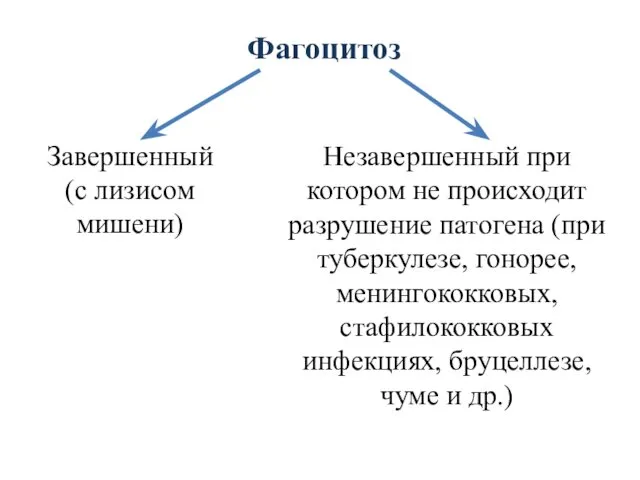
- 35. Фагоцитоз Незавершенный при котором не происходит разрушение патогена (при туберкулезе, гонорее, менингококковых, стафилококковых инфекциях, бруцеллезе, чуме
- 36. Гуморальные факторы врожденного иммунитета Система комплемента Цитокиновая сеть Нормальные антитела Бактерицидные пептиды: дефензины; белок, связывающий ЛПС,
- 37. Система комплемента – это многокомпонентная самособирающаяся система сывороточных белков (более 20), которые в норме находятся в
- 38. Фазы активации комплемента 1. Запуск активации (участвуют факторы С1-С5, конвертазы С3, С5 и ряд других белков)
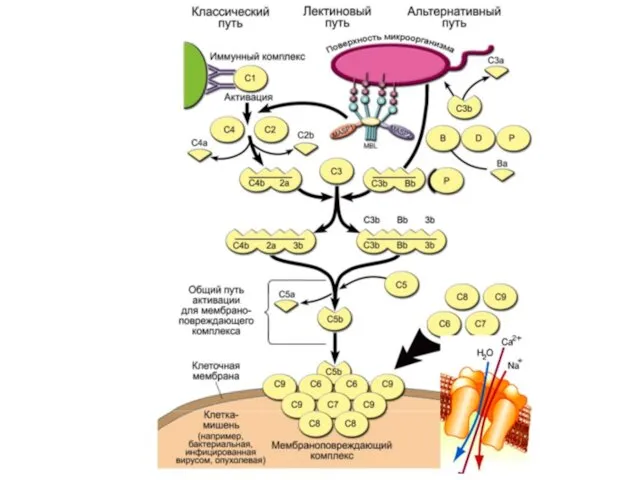
- 39. Классический путь 1. Активатор – иммунный комплекс Аг-Ат, который узнается С1-компонентом; 2. Последующая активация С4 и
- 40. Лектиновый путь 1. Распознавание углеводов на поверхности микробной клетки маннозосвязывающим лектином сыворотки крови. 2. Активация сразу
- 41. Альтернативный путь 1. Гидролиз C3 на поверхности микробной клетки (обычно на ЛПС клеточной стенки Гр- бактерий)
- 42. 3.9.14
- 43. Биологические эффекты комплемента 1. Лизис клеток (все пути активации завершаются образованием мембраноатакующего комплекса); 2. «Анафилотоксическое» действие
- 44. Цитокины Это система низкомолекулярных белков организма, синтезируемых преимущественно активированными клетками иммунной и кроветворной систем, регулирующих межклеточные
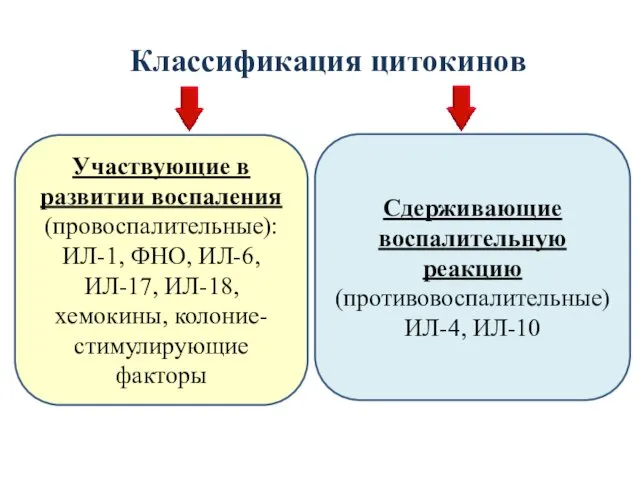
- 45. Классификация цитокинов Участвующие в развитии воспаления (провоспалительные): ИЛ-1, ФНО, ИЛ-6, ИЛ-17, ИЛ-18, хемокины, колоние-стимулирующие факторы Сдерживающие
- 46. Структурно-функциональные семейства цитокинов 1. интерфероны типа I — III (ИФН-α, β, γ и др.); 2. интерлейкины
- 47. Свойства цитокинов Отсутствие специфичности в отношении антигенов, Функционирование по принципу сети, Участие в регуляции межклеточных взаимодействий
- 49. Скачать презентацию































 Бруцеллез. Лабораторная диагностика
Бруцеллез. Лабораторная диагностика Емхана - іс қарекетінің көрсеткіштері
Емхана - іс қарекетінің көрсеткіштері Воспалительное заболевание поджелудочной железы, панкреатит
Воспалительное заболевание поджелудочной железы, панкреатит Миокардиты
Миокардиты Сестринский уход в послеоперационном периоде
Сестринский уход в послеоперационном периоде Современный взгляд на диагностику и лечение остеопороза
Современный взгляд на диагностику и лечение остеопороза Врождённая гиперплазия коры надпочечников
Врождённая гиперплазия коры надпочечников Воспаление. Острое воспаление
Воспаление. Острое воспаление Воспаление. Классификация воспаления
Воспаление. Классификация воспаления Коксартроз & гонартроз
Коксартроз & гонартроз Решение задач по количественным взаимосвязям в энергообеспеченности мышечной деятельности
Решение задач по количественным взаимосвязям в энергообеспеченности мышечной деятельности Методы исследования, патология и лечение органа слуха
Методы исследования, патология и лечение органа слуха Противірусні препарати для лікування гепатитів
Противірусні препарати для лікування гепатитів Физиология сердца
Физиология сердца История сестричества и ухода за больными
История сестричества и ухода за больными Столбняк
Столбняк Морально этические проблемы искусственного аборта
Морально этические проблемы искусственного аборта Наружное применение лекарственных средств
Наружное применение лекарственных средств Метод гирлянд случайностей и ассоциаций
Метод гирлянд случайностей и ассоциаций Патологии кариотипа человека
Патологии кариотипа человека Проблемы и перспективы современной медицины: философский анализ
Проблемы и перспективы современной медицины: философский анализ Воспитание и обучение детей с нарушениями эмоционального развития, с синдромом раннего детского аутизма. (Лекция 9)
Воспитание и обучение детей с нарушениями эмоционального развития, с синдромом раннего детского аутизма. (Лекция 9) Радуйтесь жизни
Радуйтесь жизни Твердые лекарственные формы и их рецептурное оформление
Твердые лекарственные формы и их рецептурное оформление Клиника и лечение. Асфиксии новорожденных
Клиника и лечение. Асфиксии новорожденных Лимфатическая система
Лимфатическая система Возбудитель скарлатины
Возбудитель скарлатины Вітчизняні та зарубіжні теорії мотивації
Вітчизняні та зарубіжні теорії мотивації