Содержание
- 2. КЛАССИФИКАЦИЯ I. Orthomyxoviridae Inluenzavirus (Alphainfluenzavirus, Betainfluenzavirus, Gammainfluenzavirus, Deltainfluenzavirus) В обозначение штаммов вирусов гриппа включают: 1. тип;
- 3. КЛАССИФИКАЦИЯ II. Paramyxoviridae / Paramyxovirinae Род Morbillivirus (7 видов) Measles morbillivirus [syn. Measles virus] — Вирус
- 4. КЛАССИФИКАЦИЯ III. Coronaviridae (HCoV, SARS-CoV, MERS-CoV, SARS-CoV-2 - COVID-19 ) IV. Picornaviridae Rhinovirus — 113 Parechovirus
- 5. Эпидемиология ОРВИ Источник инфекции Больной человек Пути передачи инфекции: Воздушно-капельный Воздушно-пылевой Контактный (адено-, рино-, RS-вирусы)
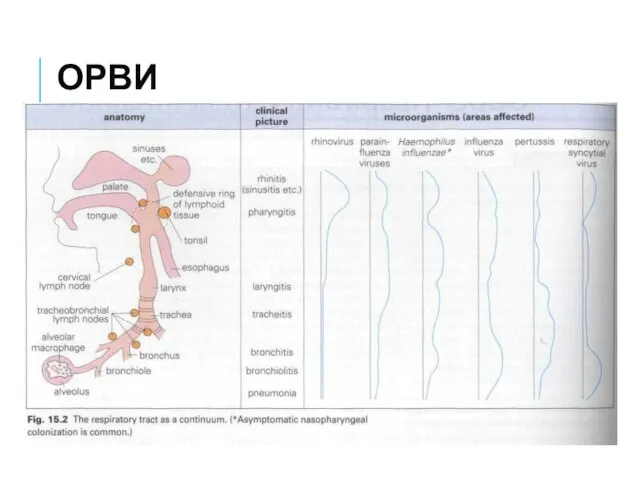
- 6. ОРВИ
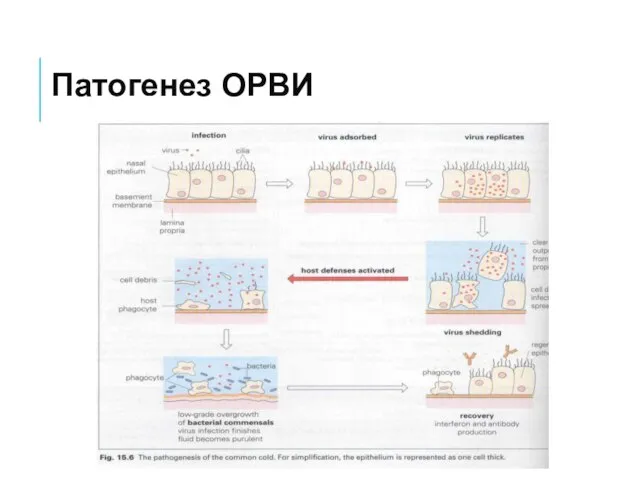
- 7. Патогенез ОРВИ
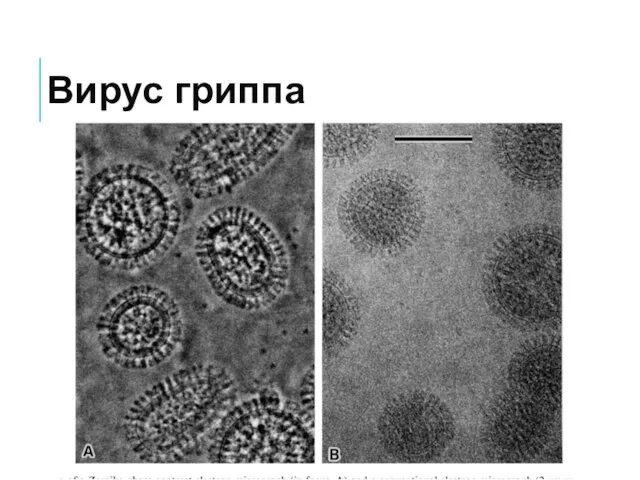
- 8. Вирус гриппа Вирион (инфекционная частица) гриппа имеет форму сферы или приближающуюся к шарообразной, его диаметр 100−120
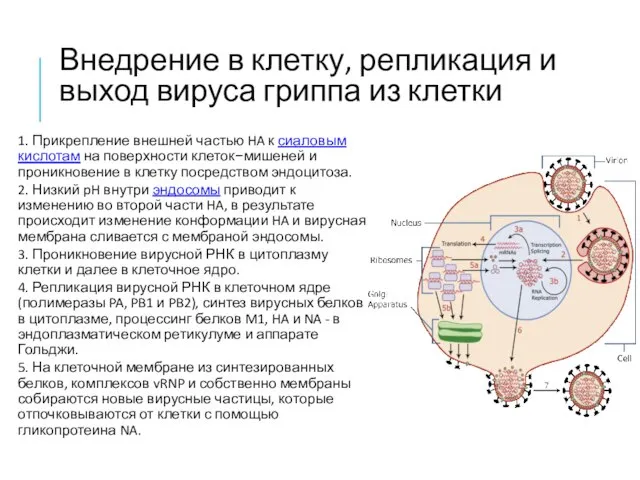
- 9. Внедрение в клетку, репликация и выход вируса гриппа из клетки 1. Прикрепление внешней частью HA к
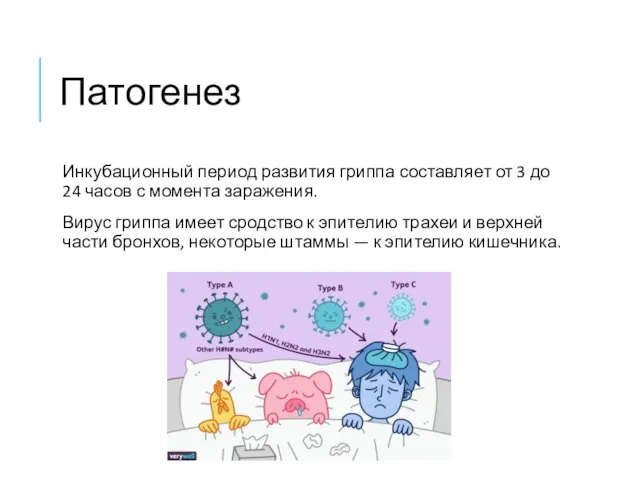
- 10. Патогенез Инкубационный период развития гриппа составляет от 3 до 24 часов с момента заражения. Вирус гриппа
- 11. патогенез 1. Вирусные частицы проникают к клеткам эпителия дыхательных путей, преимущественно цилиндрического эпителия трахеи и бронхов,
- 12. Клинические признаки раздражение верхних дыхательных путей: сильный кашель; заторможенность нервных реакций, мышечная (миалгия) и головная боль
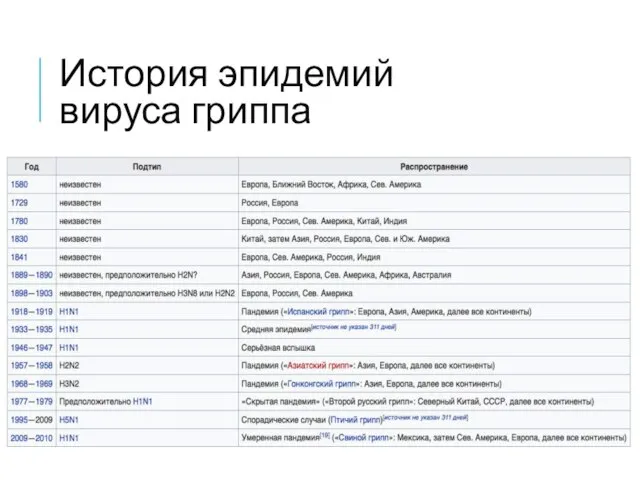
- 13. История эпидемий вируса гриппа
- 14. Вирус гриппа
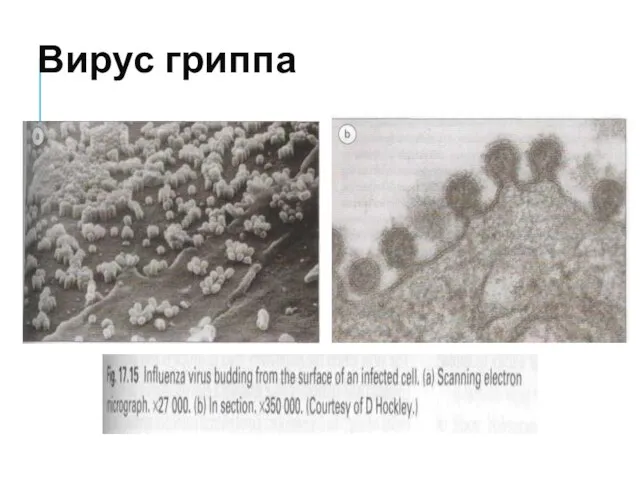
- 15. Вирус гриппа
- 16. специфическая профилактика
- 17. ПАРАМИКСОВИРУСЫ ПАРАГРИПП ПАРОТИТ КОРЬ РЕСПИРАТОРНО-СИНЦИТИАЛЬНЫЙ ВИРУС
- 18. ПАРАМИКСОВИРУСЫ Вирионы имеют сферическую форму, диаметр 150—200 нм. Геном представлен однонитевой нефрагментированной (-)РНК, что сильно ограничивает
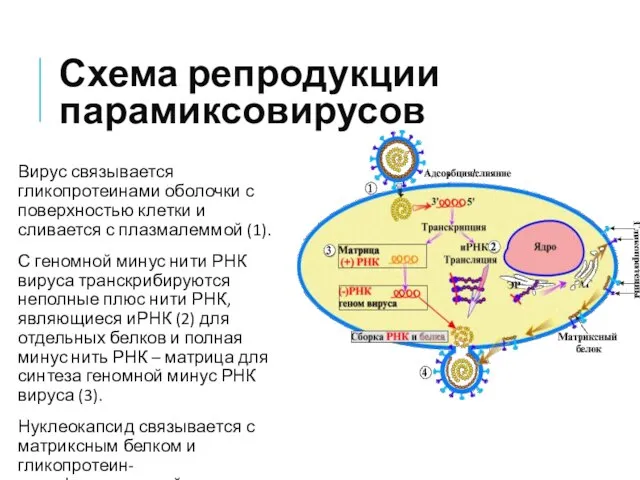
- 19. Схема репродукции парамиксовирусов Вирус связывается гликопротеинами оболочки с поверхностью клетки и сливается с плазмалеммой (1). С
- 20. Парамиксовирусы
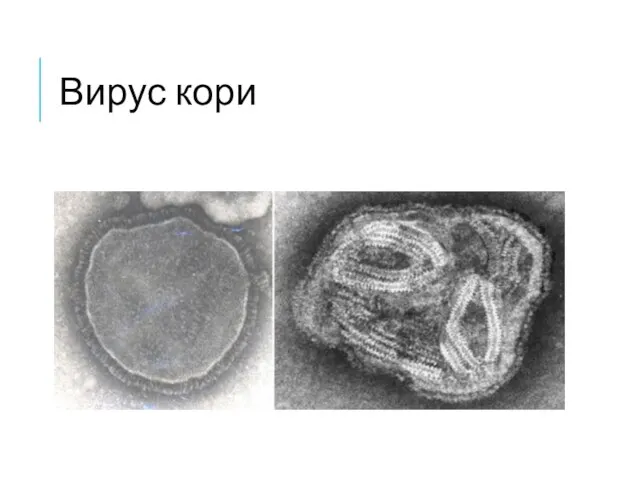
- 22. Вирус кори Корь (Measles morbillivirus) — острое инфекционное вирусное заболевание с очень высоким уровнем контагиозности (90
- 23. Вирус кори Cферическая форма и диаметр 120—230 нм. Вирус состоит из нуклеокапсида — минус-нити РНК, трёх
- 24. Вирус кори
- 25. патогенез кори 1. Проникновение вируса в организм человека происходит через слизистую оболочку верхних дыхательных путей и
- 26. Клиническая картина Инкубационный период 8—14 дней (редко до 17 дней). Острое начало — подъём температуры до
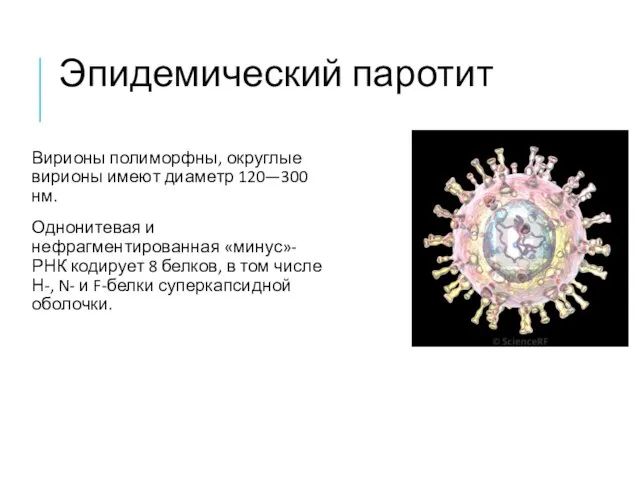
- 27. Эпидемический паротит Вирионы полиморфны, округлые вирионы имеют диаметр 120—300 нм. Однонитевая и нефрагментированная «минус»-РНК кодирует 8
- 28. патогенез паротита Входные ворота инфекции – верхние дыхательные пути Размножение вируса в слизистых оболочках полости рта
- 30. Специфическая профилактика В соответствии с российским национальным календарём прививок, который утверждён приказом Министерства здравоохранения РФ №
- 31. КОРОНАВИРУСЫ Семейство коронавирусов (лат. Coronaviridae) РНК - содержащие вирусы 46 видов
- 32. КОРОНАВИРУСЫ HCoV-229E — Alphacoronavirus, впервые выявлен в середине 1960-х годов; HCoV-NL63 — Alphacoronavirus, возбудитель был выявлен
- 33. COVID-19 (SARS-COV-2) COVID-19 (аббревиатура от англ. COronaVIrus Disease 2019), ранее коронавирусная инфекция 2019-nCoV SARS-CoV-2 (Severe acute
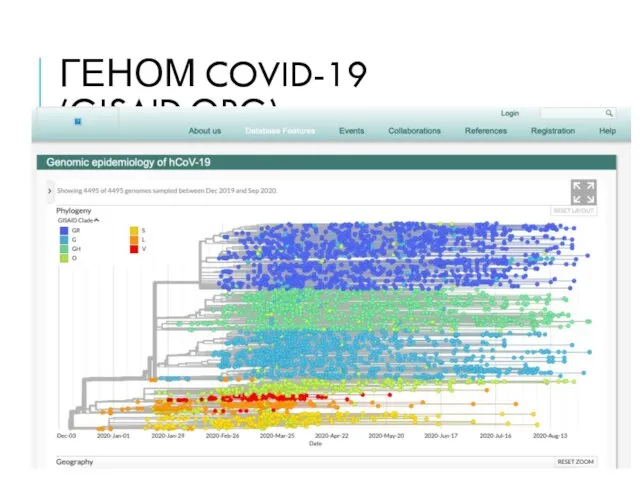
- 34. ГЕНОМ COVID-19 (GISAID.ORG)
- 35. SARS-COV-2 Размер вириона порядка 50-200 нанометров. Белковое моделирование, осуществлённое на основе расшифрованного генома вируса, показало, что
- 36. SARS-COV-2 МОДЕЛЬ ПОПЕРЕЧНОГО СЕЧЕНИЯ БОЛЬШИНСТВА ПРЕДСТАВИТЕЛЕЙ ГРУППЫ BETA-COV B. ОДНАКО У ВИРУСНЫХ ЧАСТИЦ SARS-COV-2 ОТСУТСТВУЕТ БЕЛОК
- 37. SARS-COV-2 SARS-CoV-2 является вирусом с оболочкой. Липидный бислой оболочки таких вирусов довольно чувствителен к высыханию, повышенной
- 38. ПЕРЕДАЧА ИНФЕКЦИИ Вирус передаётся воздушно-капельным путём через вдыхание мелких капель, распылённых в воздухе при кашле, чихании
- 39. КЛИНИЧЕСКАЯ КАРТИНА Инфекция, вызывается вирусом SARS-CoV-2, инкубационный период составляет 1—14 дней, может протекать бессимптомно, в лёгкой
- 40. ВОЗМОЖНЫЕ ОСЛОЖНЕНИЯ COVID-19: острый респираторный дистресс-синдром, от 15 % до 33 %; острая дыхательная недостаточность, 8
- 41. ЛАБОРАТОРНАЯ ДИАГНОСТИКА Диагностировать вирус возможно при помощи полимеразной цепной реакции с обратной транскрипцией в реальном времени
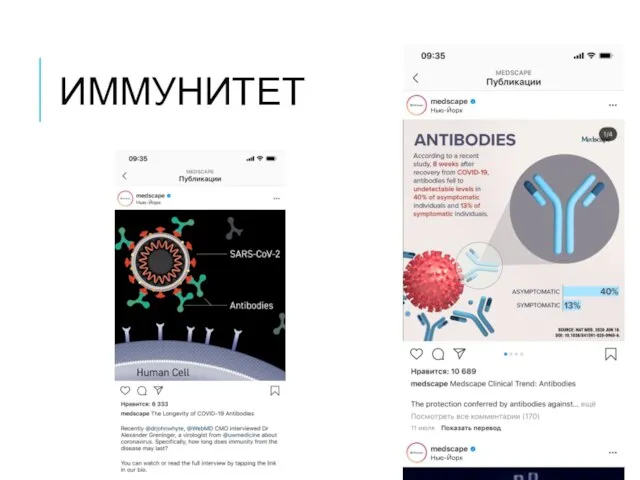
- 42. ИММУНИТЕТ
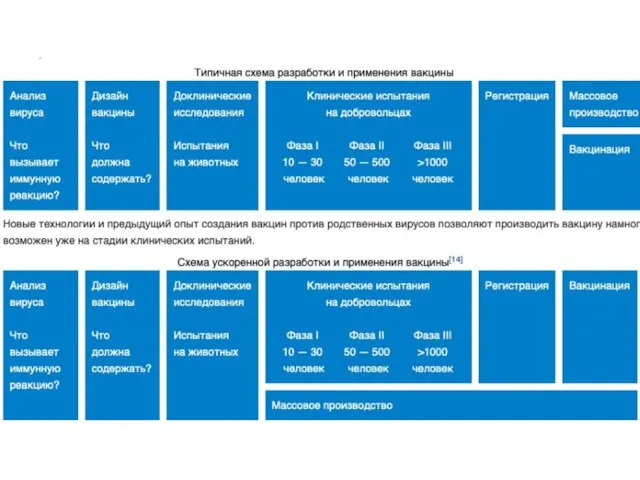
- 43. ВАКЦИНА В работе принимают участие около 35 компаний и академических учреждений Шесть вакцин проходят клинические исследования
- 46. АДЕНОВИРУСНАЯ ИНФЕКЦИЯ Вирус рода Mastadenovirus семейства Adenoviridae Диаметр 70—90 нм, содержат единичную двухцепочечную молекулу ДНК, ассоциированную
- 47. Патогенез В организм инфекция попадает через слизистые оболочки верхних дыхательных путей, реже — кишечник либо конъюнктиву.
- 48. Клиническая картина Инкубационный период от 1 дня до 2 недель. Заболевание начинается остро, с подъёма температуры.
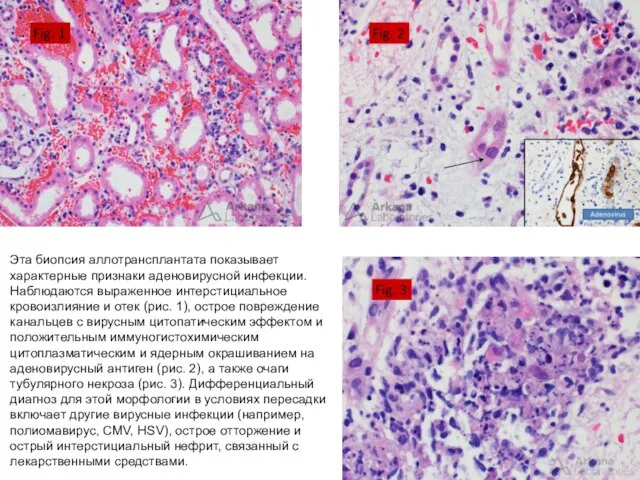
- 49. Эта биопсия аллотрансплантата показывает характерные признаки аденовирусной инфекции. Наблюдаются выраженное интерстициальное кровоизлияние и отек (рис. 1),
- 50. У больного А. 38 лет, внезапно поднялась температура, появи- лась слабость, сильная головная боль, мышечные боли.
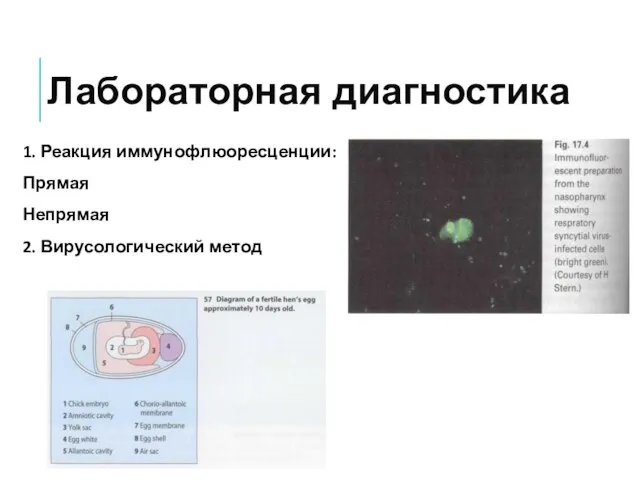
- 51. Лабораторная диагностика 1. Реакция иммунофлюоресценции: Прямая Непрямая 2. Вирусологический метод
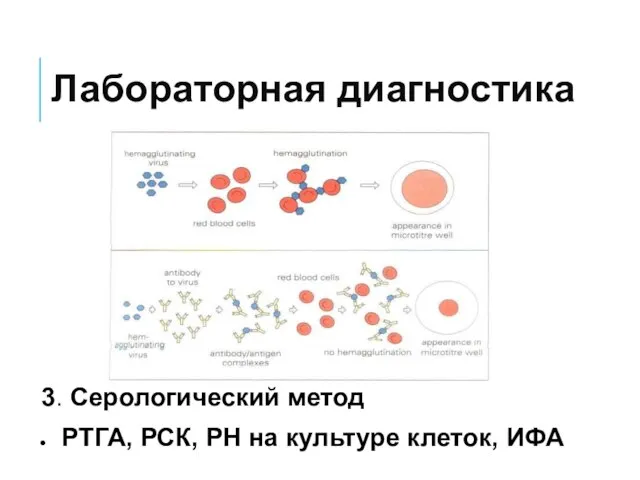
- 52. Лабораторная диагностика 3. Серологический метод РТГА, РСК, РН на культуре клеток, ИФА
- 53. Стадии постановки ПЦР Подготовка пробы биологического материала Амплификация Детекция в агарозном геле
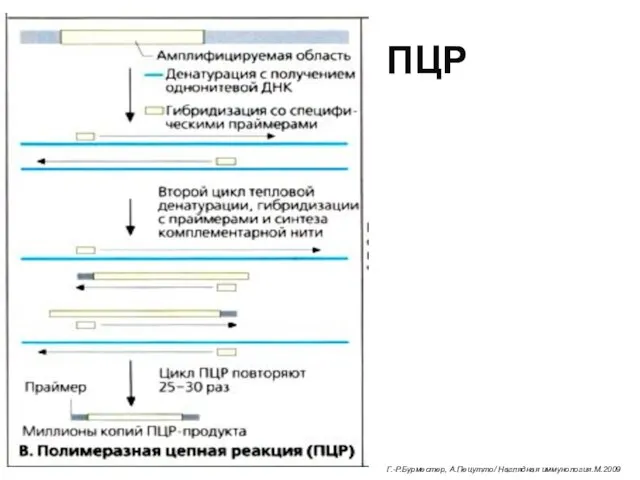
- 54. ПЦР Г.-Р.Бурместер, А.Пецутто/ Наглядная иммунология.М.2009
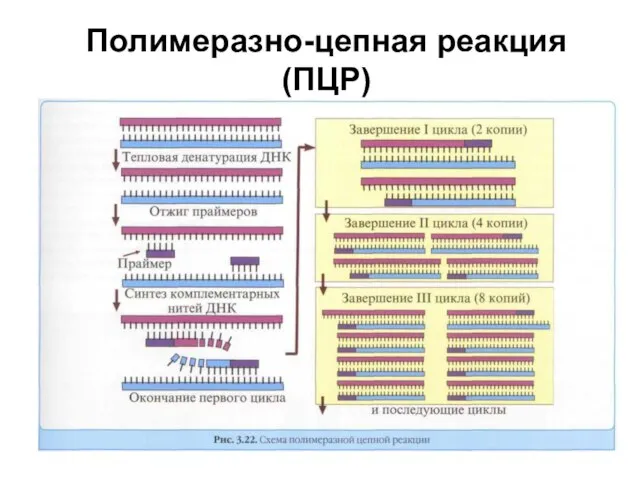
- 55. Полимеразно-цепная реакция (ПЦР)
- 57. Скачать презентацию




































 Поражение нервной системы при воспалительных миопатиях (часть 2)
Поражение нервной системы при воспалительных миопатиях (часть 2) Визуальная диагностика
Визуальная диагностика Профилактика сердечно - сосудистых заболеваний
Профилактика сердечно - сосудистых заболеваний Правила гигиены питания
Правила гигиены питания Сепсис. Классификация и критерии диагностики сепсиса
Сепсис. Классификация и критерии диагностики сепсиса Врожденные аномалии почек
Врожденные аномалии почек Жалпы тәжірибелі дәрiгердiң тұлға аралық қарым-қатынас және емделушiлерімен кеңесуiнiң қағидалары
Жалпы тәжірибелі дәрiгердiң тұлға аралық қарым-қатынас және емделушiлерімен кеңесуiнiң қағидалары Болезни губ, языка
Болезни губ, языка Презентация Красная кровь
Презентация Красная кровь Моя профессия – Моя гордость. Мои профессиональные возможности. Профессия медсестра
Моя профессия – Моя гордость. Мои профессиональные возможности. Профессия медсестра Аденовирусы
Аденовирусы Гонорея
Гонорея Сахарный диабет
Сахарный диабет Неотложная помощь при тяжелой бронхиальной астме и анафилактическом шоке
Неотложная помощь при тяжелой бронхиальной астме и анафилактическом шоке Система органов кроветворения и иммунной защиты. Центральные и периферические органы
Система органов кроветворения и иммунной защиты. Центральные и периферические органы Дифференциальная диагностика кратковременной потери сознании (синкопе)
Дифференциальная диагностика кратковременной потери сознании (синкопе) Вредное влияние алкоголя, курения и наркотиков в период эмбрионального развития
Вредное влияние алкоголя, курения и наркотиков в период эмбрионального развития Холестеатома среднего уха. Этиология. Патогенез
Холестеатома среднего уха. Этиология. Патогенез Вирус иммунодефицита человека. Синдром приобретенного иммунодефицита человека
Вирус иммунодефицита человека. Синдром приобретенного иммунодефицита человека Кровотечение из варикозно-расширенных вен пищевода
Кровотечение из варикозно-расширенных вен пищевода Этика медицинской генетики
Этика медицинской генетики Механизмы компенсации нарушений внешнего дыхания
Механизмы компенсации нарушений внешнего дыхания Нарушения функции почек
Нарушения функции почек Синдромы: Бругада, СРРЖ, удлинненого
Синдромы: Бругада, СРРЖ, удлинненого Оперативные методы лечения в гинекологии
Оперативные методы лечения в гинекологии Роль медицинского брата в предупреждении затяжного течения очаговой пневмонии
Роль медицинского брата в предупреждении затяжного течения очаговой пневмонии Основы медицинской коммуникации
Основы медицинской коммуникации Отечественная заднекамерная факичная интраокулярная линза в коррекции миопии высокой степени
Отечественная заднекамерная факичная интраокулярная линза в коррекции миопии высокой степени