Бета-лактамиды (природные и полусинтетические пенициллины и цефалоспорины) Бета-лактамиды (природные и полусинтетические пен
Содержание
- 2. Цель лекции: Изучить физико-химические и фармакологические свойства, методы оценки качества лекарственных средств указанной группы во взаимосвязи
- 3. План лекции: План излагаемой лекции соответствует всем разделам фармакопейной статьи.
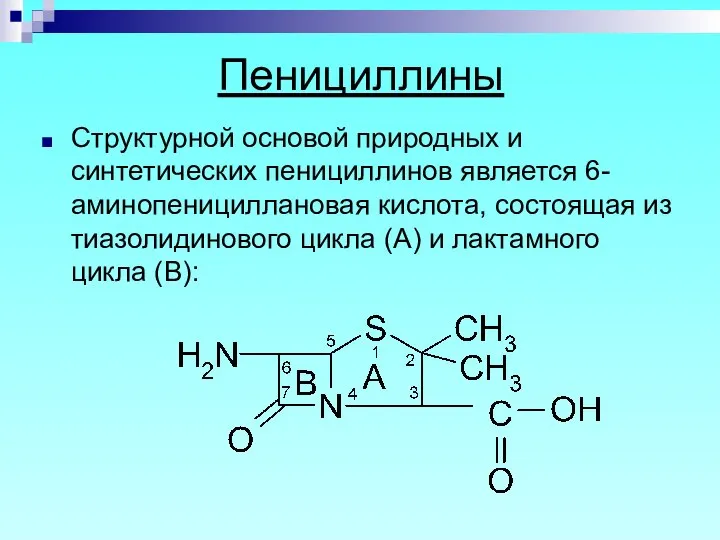
- 4. Пенициллины Структурной основой природных и синтетических пенициллинов является 6-аминопенициллановая кислота, состоящая из тиазолидинового цикла (А) и
- 5. Специфическая биологическая активность обусловлена наличием тиазолидинового и лактамного колец, а также заместителем в 6-ом положении. Биосинтез
- 6. Для выделения и очистки пенициллинов используют хроматографию, ионообменную сорбцию. Природные пенициллины имеют серьезный недостаток – они
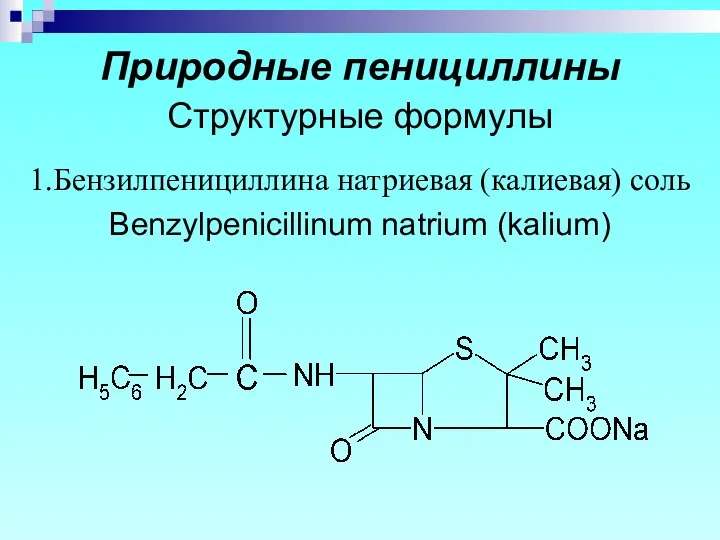
- 7. Природные пенициллины Структурные формулы 1.Бензилпенициллина натриевая (калиевая) соль Benzylpenicillinum natrium (kalium)
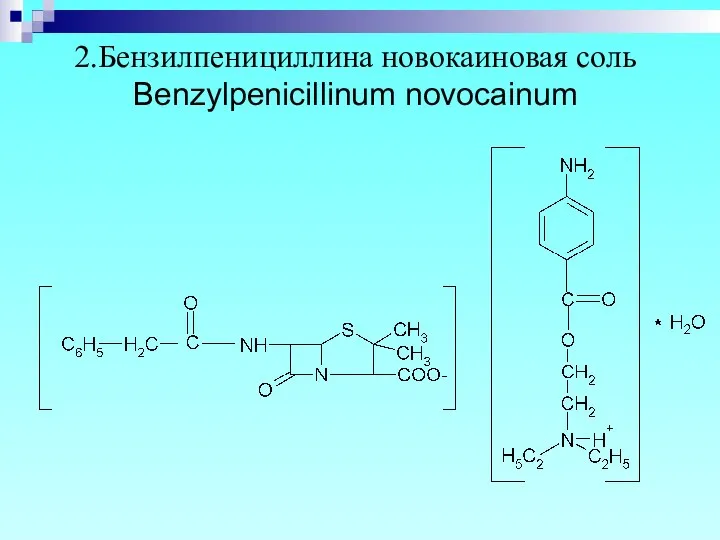
- 8. 2.Бензилпенициллина новокаиновая соль Benzylpenicillinum novocainum
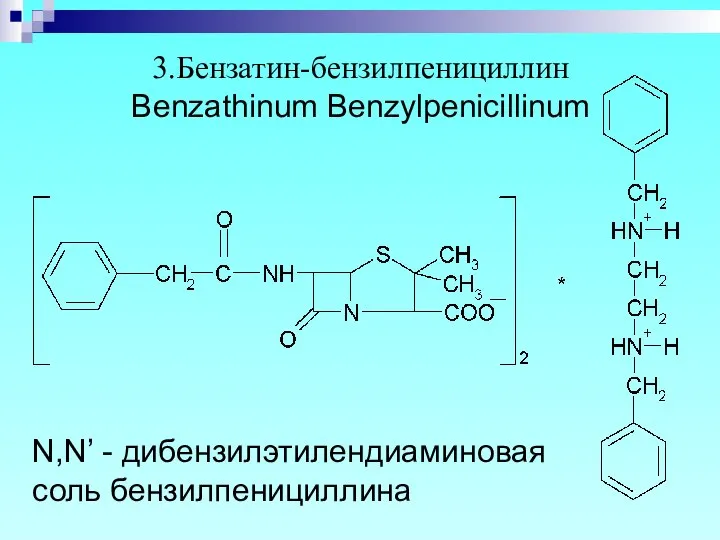
- 9. 3.Бензатин-бензилпенициллин Benzathinum Benzylpenicillinum N,N’ - дибензилэтилендиаминовая соль бензилпенициллина
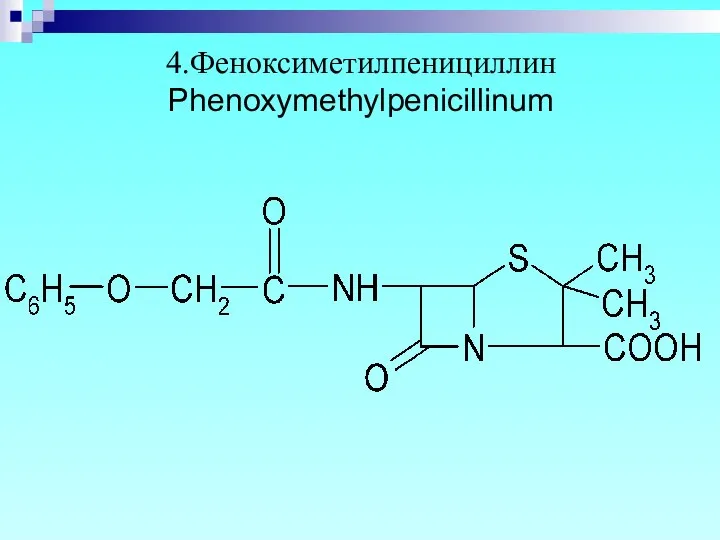
- 10. 4.Феноксиметилпенициллин Phenoxymethylpenicillinum
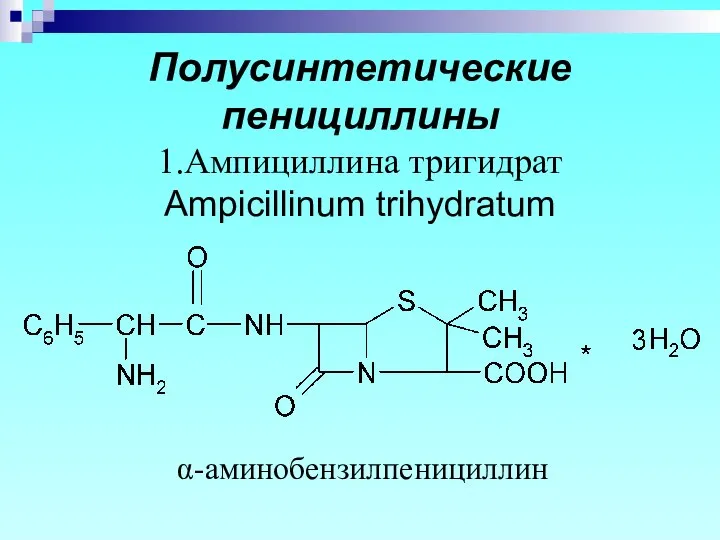
- 11. Полусинтетические пенициллины 1.Ампициллина тригидрат Ampicillinum trihydratum α-аминобензилпенициллин
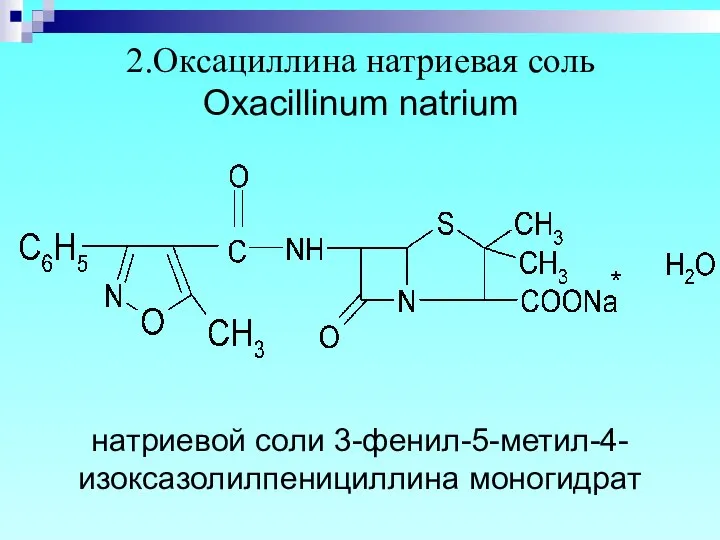
- 12. 2.Оксациллина натриевая соль Oxacillinum natrium натриевой соли 3-фенил-5-метил-4-изоксазолилпенициллина моногидрат
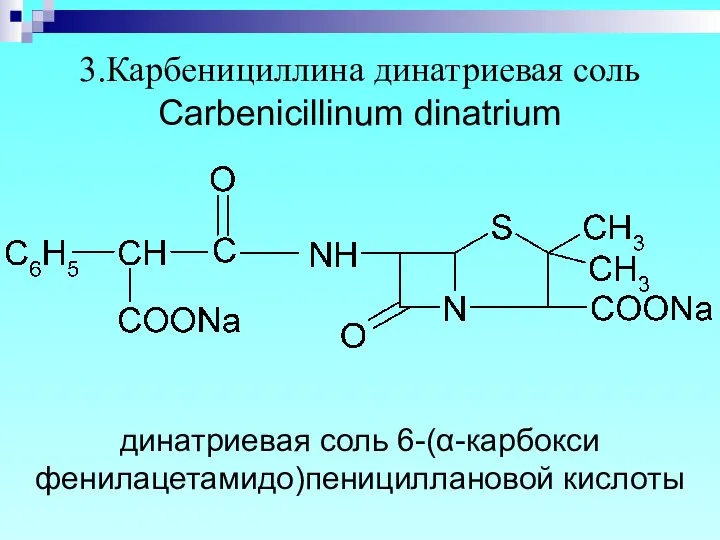
- 13. 3.Карбенициллина динатриевая соль Carbenicillinum dinatrium динатриевая соль 6-(α-карбокси фенилацетамидо)пенициллановой кислоты
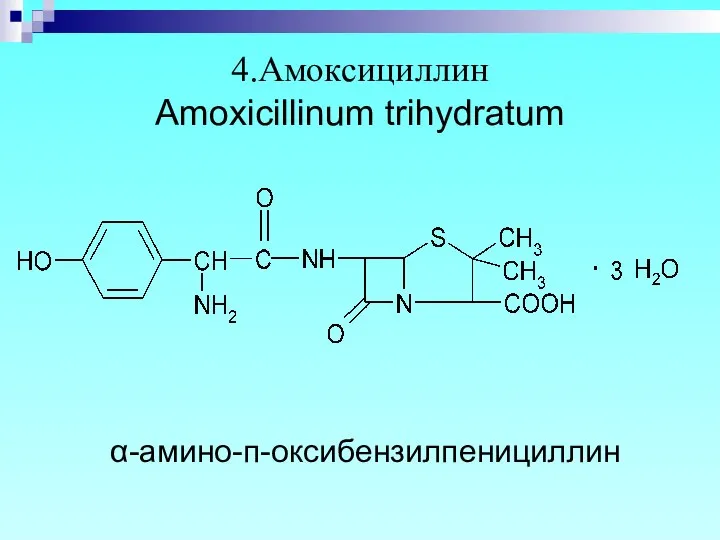
- 14. 4.Амоксициллин Amoxicillinum trihydratum α-амино-п-оксибензилпенициллин
- 15. Физические свойства Препараты – белые кристаллические порошки, без запаха. Натриевые и калиевые соли слегка гигроскопичны, карбенициллина
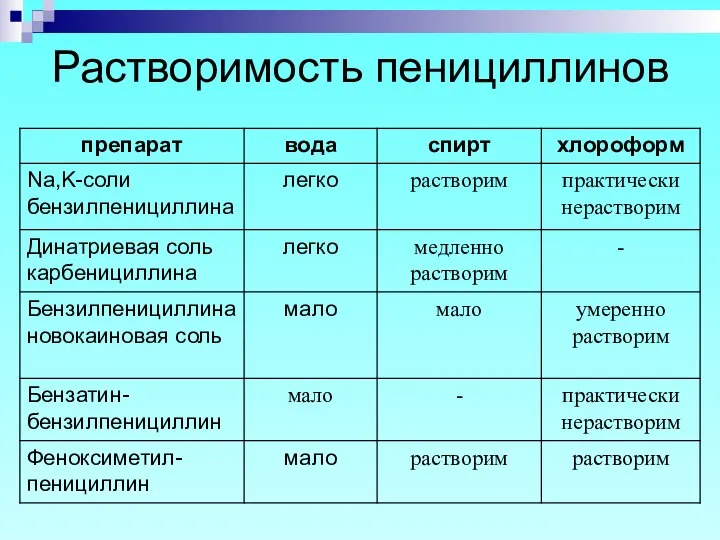
- 16. Растворимость пенициллинов
- 17. Растворимость пенициллинов
- 18. Определение подлинности 1. УФ – спектроскопия: соли бензилпенициллина λ = 280-286 нм. феноксиметилпенициллин λmax= 268-274 нм,
- 19. Определение подлинности 2. ИК - спектроскопия 3. Удельное вращение 4. ВЭЖХ 5. ТСХ
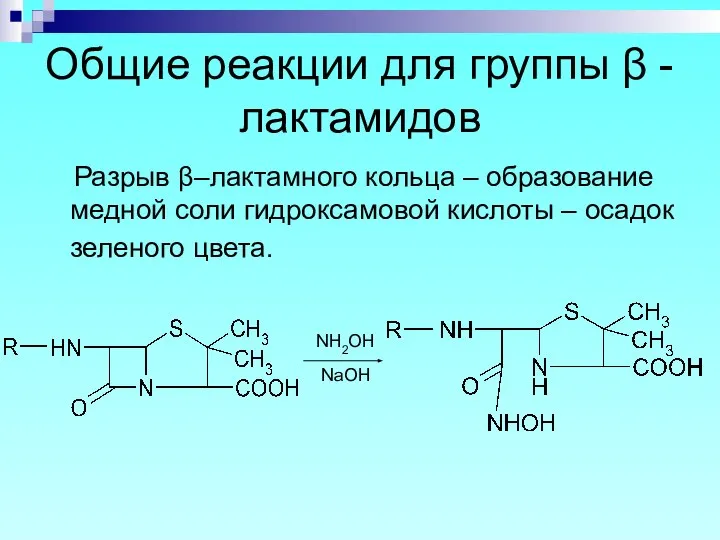
- 20. Общие реакции для группы β - лактамидов Разрыв β–лактамного кольца – образование медной соли гидроксамовой кислоты
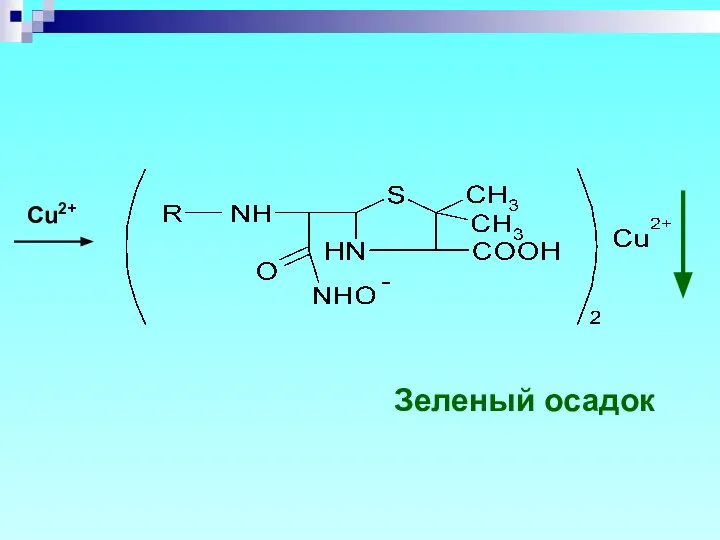
- 21. Cu2+ Зеленый осадок
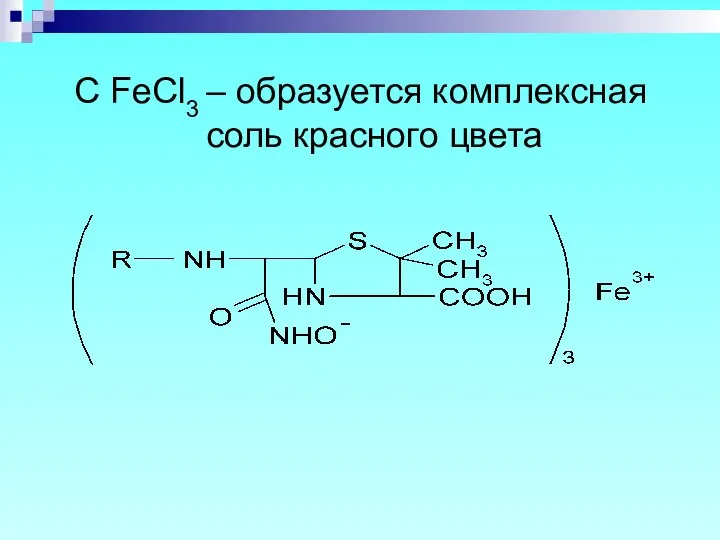
- 22. C FeCl3 – образуется комплексная соль красного цвета
- 23. Обнаружение азотистого основания а) с насыщенным раствором йода – коричневый осадок; б) с реактивом Майера –
- 24. Проба Лассеня для обнаружения N и S Препарат прокаливают с солями Na, фильтруют: а) к части
- 25. Окислительная минерализация а) сплавление со щелочью с образованием S2- иона: S2- + Pb2+ → PbS или
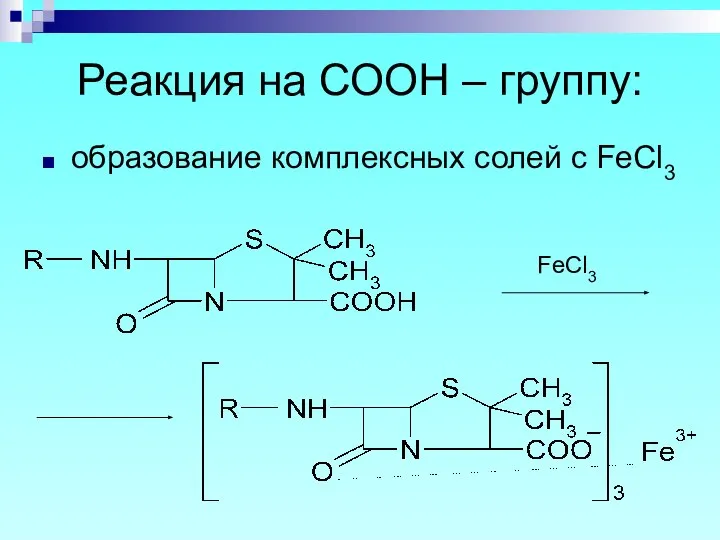
- 26. Реакция на СООН – группу: образование комплексных солей с FeCl3 FeCl3
- 27. ампициллин – желтое окрашивание; бензилпенициллин (Na, K) – желтый осадок; феноксиметилпенициллин – желто-зеленый осадок.
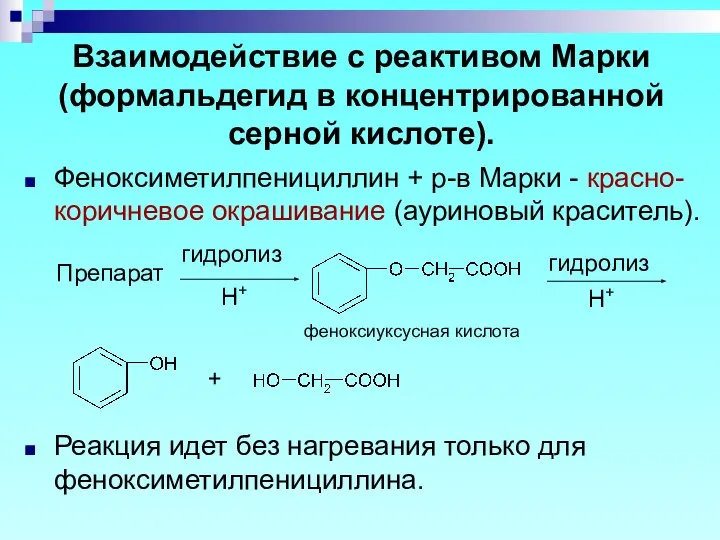
- 28. Взаимодействие с реактивом Марки (формальдегид в концентрированной серной кислоте). Феноксиметилпенициллин + р-в Марки - красно-коричневое окрашивание
- 29. Взаимодействие с реактивом Марки (формальдегид в концентрированной серной кислоте). Соли бензилпенициллина + р-в Марки - красно-коричневое
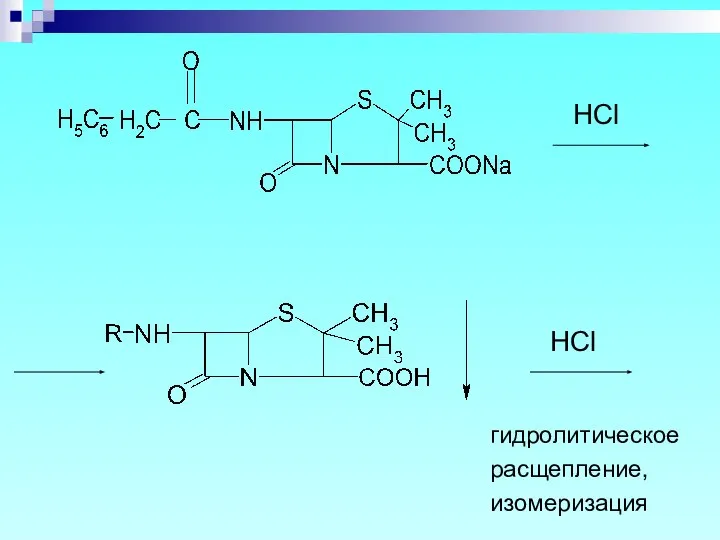
- 30. Частные реакции 1. Бензилпенициллина Na и K соли Осаждение свободной кислоты при добавлении соляной кислоты –
- 31. HCl HCl гидролитическое расщепление, изомеризация
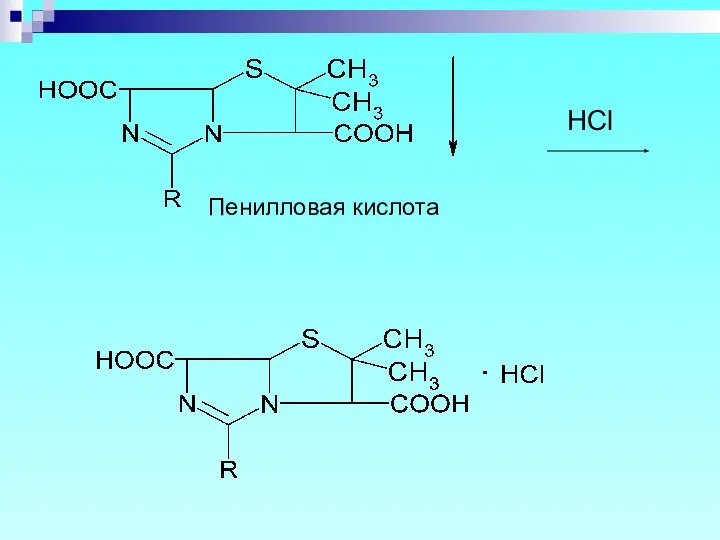
- 32. Пенилловая кислота HCl
- 33. Обнаружение катионов Na и K 1) окраска пламени 2) с кобальтинитритом Na на К+ - оранжево-желтый
- 34. Реакция Витали-Морена: Препарат выпаривают в смеси с дымящей HNO3, а затем прибавляют спиртовый раствор KOH и
- 35. Выделение фенилуксусной кислоты после кипячения в 4% NaOH и последующего добавления избытка разбавленной H2SO4 (по запаху)
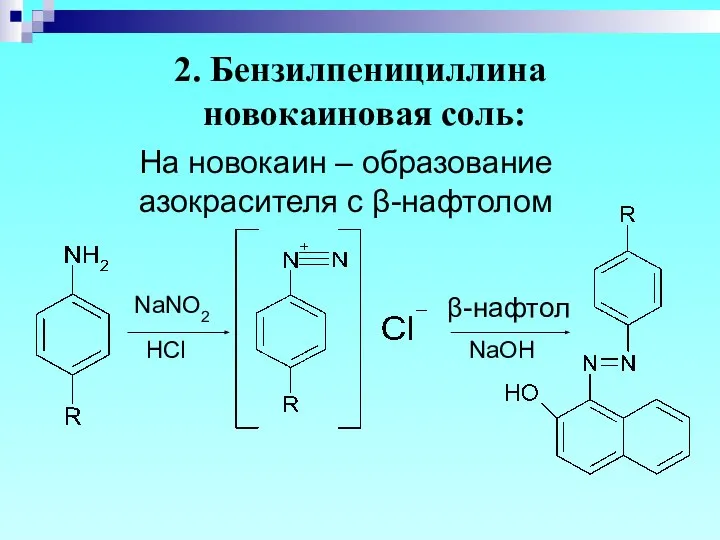
- 36. 2. Бензилпенициллина новокаиновая соль: На новокаин – образование азокрасителя с β-нафтолом NaOH HCl β-нафтол NaNO2
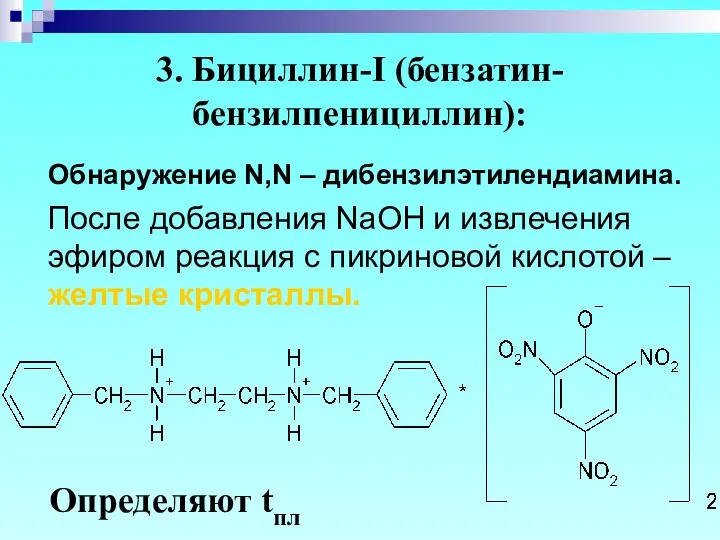
- 37. 3. Бициллин-I (бензатин-бензилпенициллин): Обнаружение N,N – дибензилэтилендиамина. После добавления NaOH и извлечения эфиром реакция с пикриновой
- 38. Окислительное разложение: Препарат + NaOH + KMnO4 – зеленое окрашивание При нагревании появляется запах бензальдегида. Действуют
- 39. 4. Ампициллина тригидрат: с реактивом Фелинга – красно-фиолетовое окрашивание (образование медных комплексов). нагревание с нингидрином –
- 40. 5. Карбенициллина натриевая соль: реакция декарбоксилирования: добавляют Na2CO3 и фенолфталеин – розовое окрашивание, нагревают - окраска
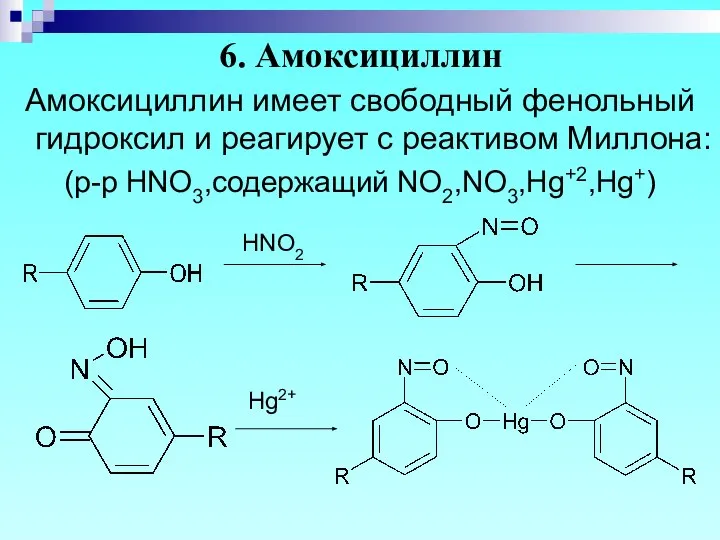
- 41. 6. Амоксициллин Амоксициллин имеет свободный фенольный гидроксил и реагирует с реактивом Миллона: (р-р HNO3,содержащий NO2,NO3,Hg+2,Hg+) Hg2+
- 42. Чистота: кислотность или щелочность (рН = 5,5; 7,5); потеря в массе при высушивании; испытания на токсичность,
- 43. Чистота: светопоглощающие примеси; йодсорбирующие примеси не более 6% (обратная йодметрия); остаточные растворители - ГЖХ; триметиламин, диметиланилин
- 44. Устойчивость бензилпенициллина устойчив на холоду только в сухом состоянии, при повышенной температуре в присутствии влаги, следов
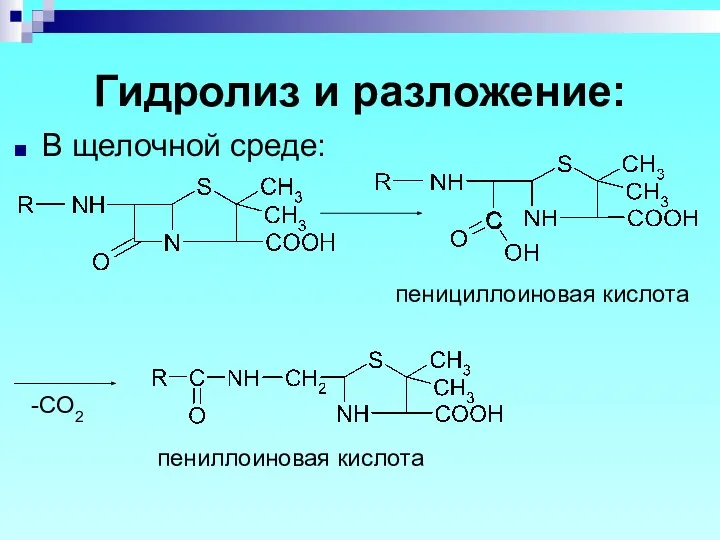
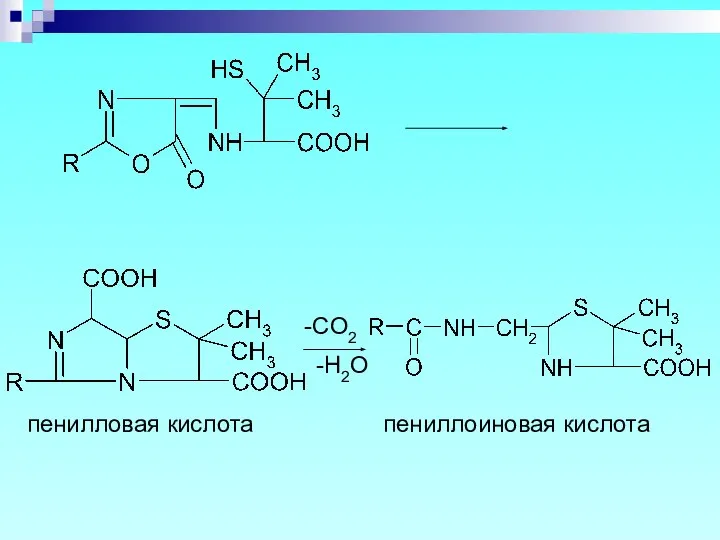
- 45. Гидролиз и разложение: В щелочной среде: пенициллоиновая кислота пениллоиновая кислота -CO2
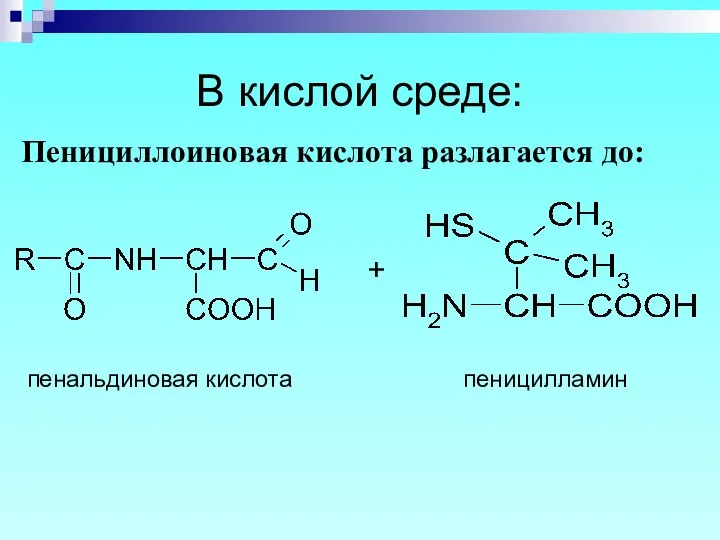
- 46. В кислой среде: Пенициллоиновая кислота разлагается до: + пенальдиновая кислота пеницилламин
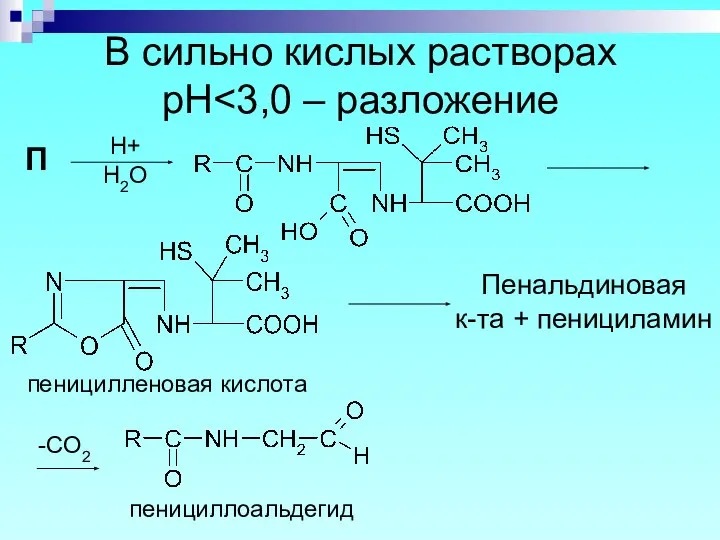
- 47. В сильно кислых растворах рН П Пенальдиновая к-та + пенициламин H+ H2O -CO2 пенициллоальдегид пеницилленовая кислота
- 48. пениллоиновая кислота пенилловая кислота -CO2 -H2O
- 49. Количественное определение Состоит из двух этапов: определение суммы пенициллинов и определение соответствующего препарата. 1. Обратная йодометрия
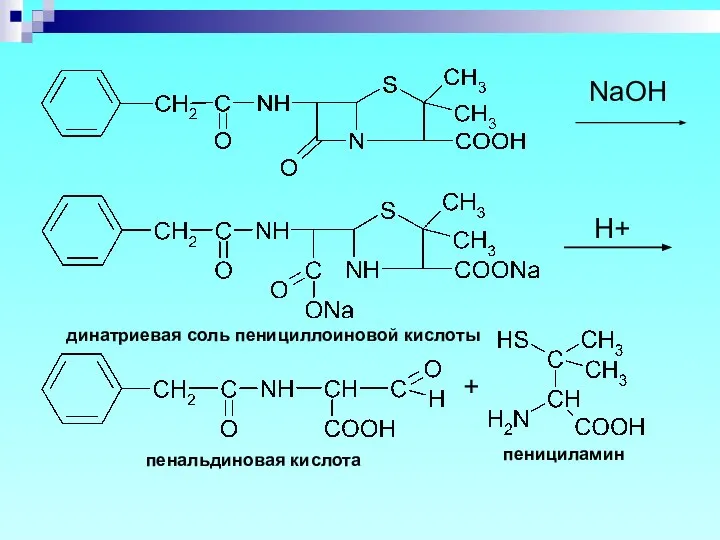
- 50. H+ пенициламин пенальдиновая кислота + динатриевая соль пенициллоиновой кислоты NaOH
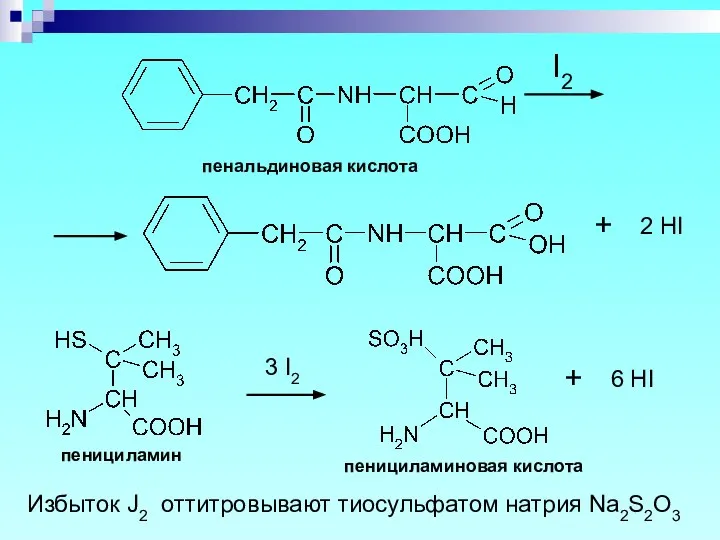
- 51. пенальдиновая кислота пенициламин пенициламиновая кислота Избыток J2 оттитровывают тиосульфатом натрия Na2S2O3 + I2 2 HI +
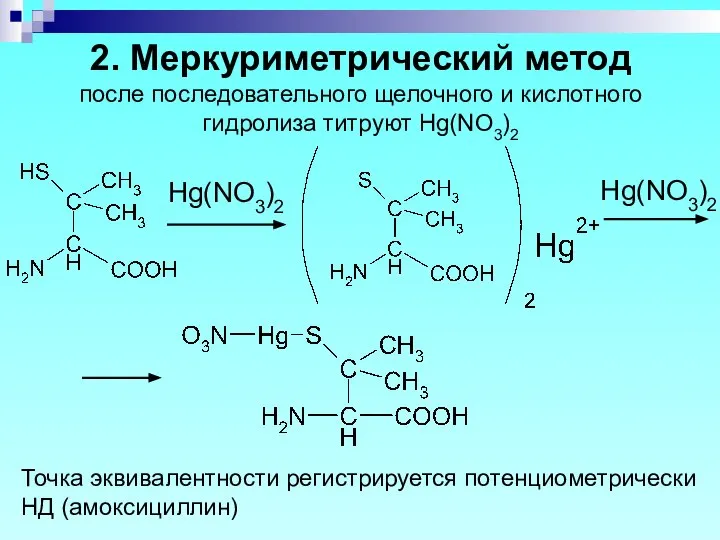
- 52. 2. Меркуриметрический метод после последовательного щелочного и кислотного гидролиза титруют Hg(NO3)2 Точка эквивалентности регистрируется потенциометрически НД
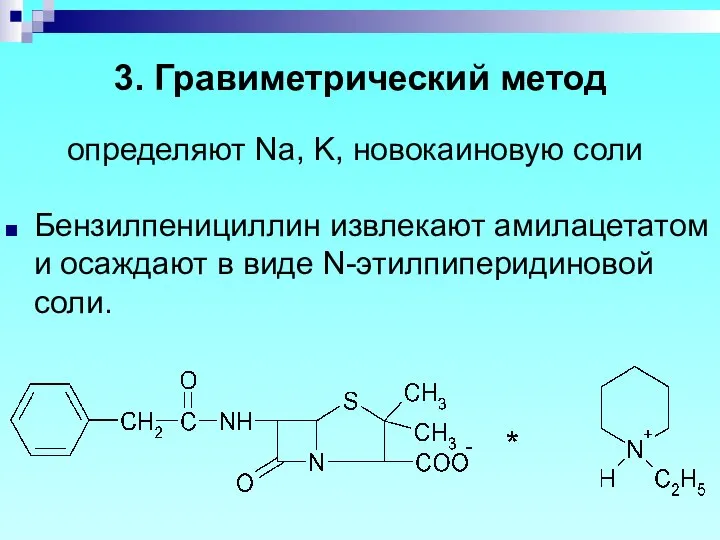
- 53. определяют Na, K, новокаиновую соли Бензилпенициллин извлекают амилацетатом и осаждают в виде N-этилпиперидиновой соли. 3. Гравиметрический
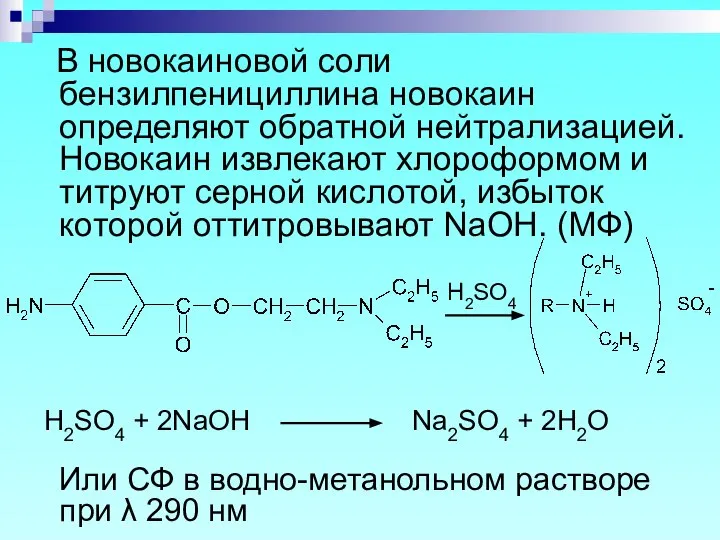
- 54. В новокаиновой соли бензилпенициллина новокаин определяют обратной нейтрализацией. Новокаин извлекают хлороформом и титруют серной кислотой, избыток
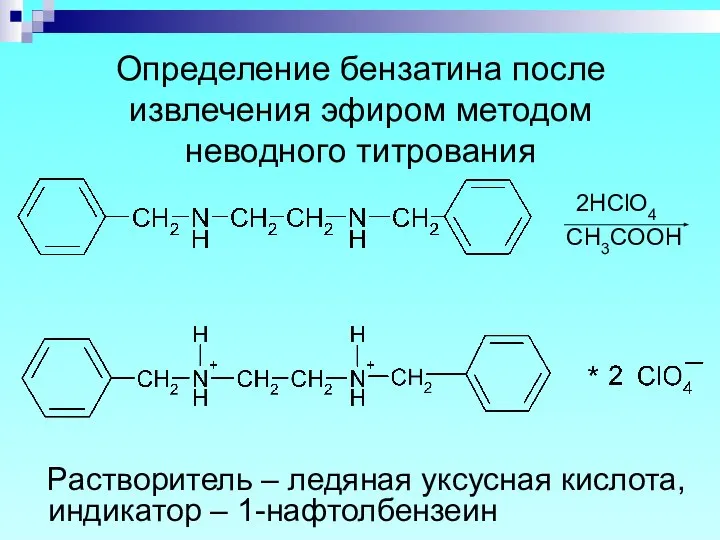
- 55. Определение бензатина после извлечения эфиром методом неводного титрования 2HClO4 СH3COOH Растворитель – ледяная уксусная кислота, индикатор
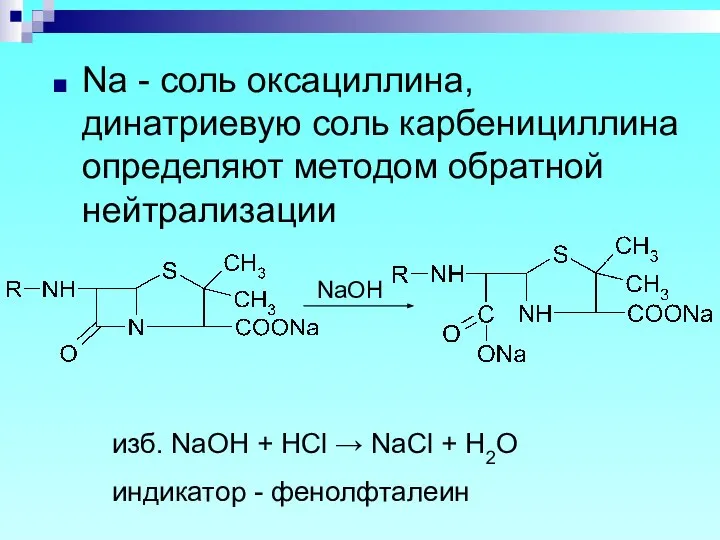
- 56. Na - соль оксациллина, динатриевую соль карбенициллина определяют методом обратной нейтрализации NaOH изб. NaOH + HCl
- 57. Спектрофотометрический метод (ФС, МФ) а) Феноксиметилпенициллин в NaOH при λ 269 нм б) МФ – (препарат
- 58. Активность пенициллинов – метод диффузии в агар 1 ЕД = 0,5988 мкг химически чистой Na-соли бензилпенициллина
- 59. Применение: антибактериальные препараты. Совместимость: пенициллины нельзя объединять с аминогликозидами в одном шприце, т.к. образующиеся пенициллоиновые кислоты
- 60. Фармакокинетика: выводятся с мочой 90% в неизменном виде, остальное в виде неактивных продуктов: пенициллоиновая кислота и
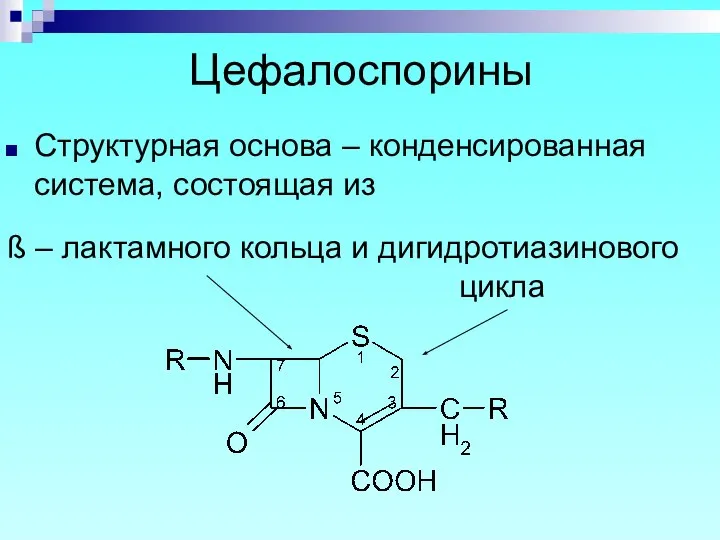
- 61. Цефалоспорины Структурная основа – конденсированная система, состоящая из ß – лактамного кольца и дигидротиазинового цикла
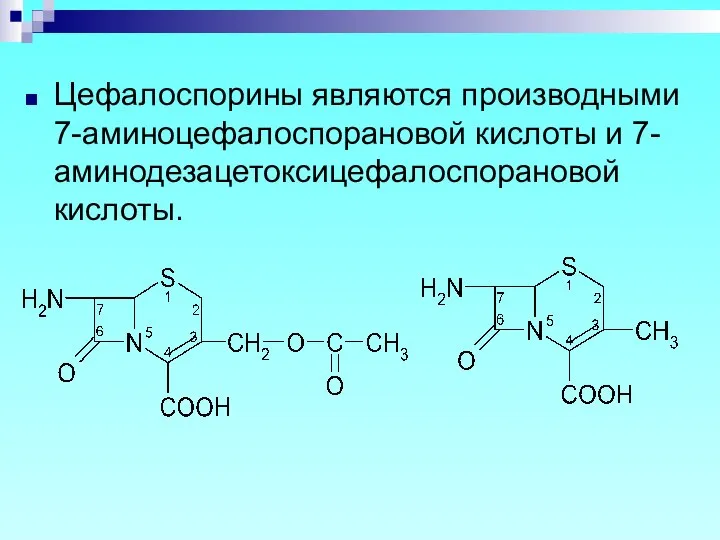
- 62. Цефалоспорины являются производными 7-аминоцефалоспорановой кислоты и 7-аминодезацетоксицефалоспорановой кислоты.
- 63. Получение: природный цефалоспорин С – продукт жизнедеятельности плесневого гриба Cephalosporium salmosynnematum. Цефалоспорин С – токсичен и
- 64. Из пенициллинов с помощью химической трансформации можно получить 7 –аминодезацетоксицефалоспорановую кислоту. [O] 7АДЦК
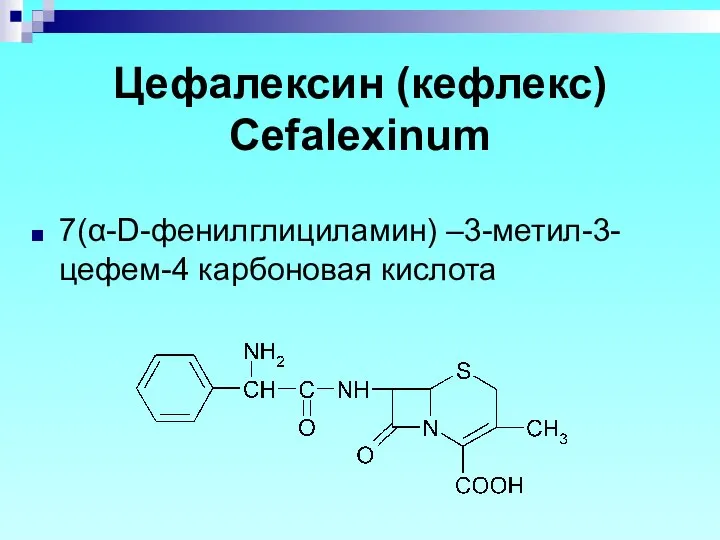
- 65. Цефалексин (кефлекс) Cefalexinum 7(α-D-фенилглициламин) –3-метил-3-цефем-4 карбоновая кислота
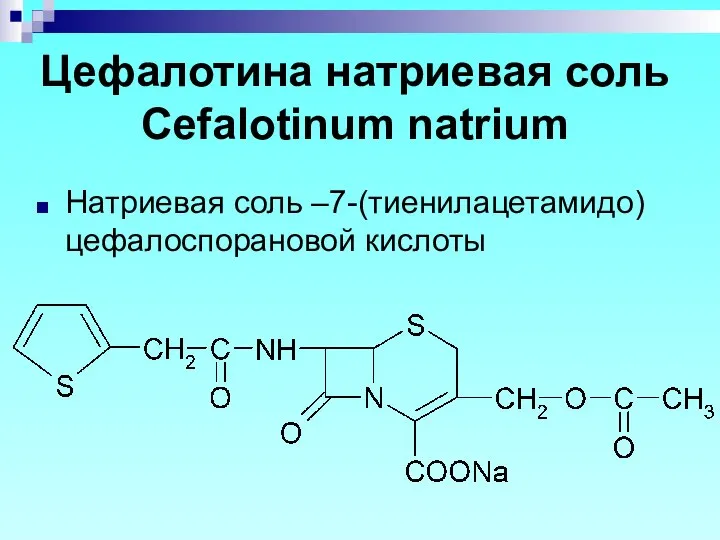
- 66. Цефалотина натриевая соль Cefalotinum natrium Натриевая соль –7-(тиенилацетамидо) цефалоспорановой кислоты
- 67. Описание: белые кристаллические порошки, практически не растворимы в хлороформе и эфире. Цефалотина натриевая соль – легко
- 68. Идентификация 1.Спектрофотометрия в УФ и ИК областях. λ = 260 нм, 4000-400 см-1, ЯМР. 2.ТСХ. 3.Удельное
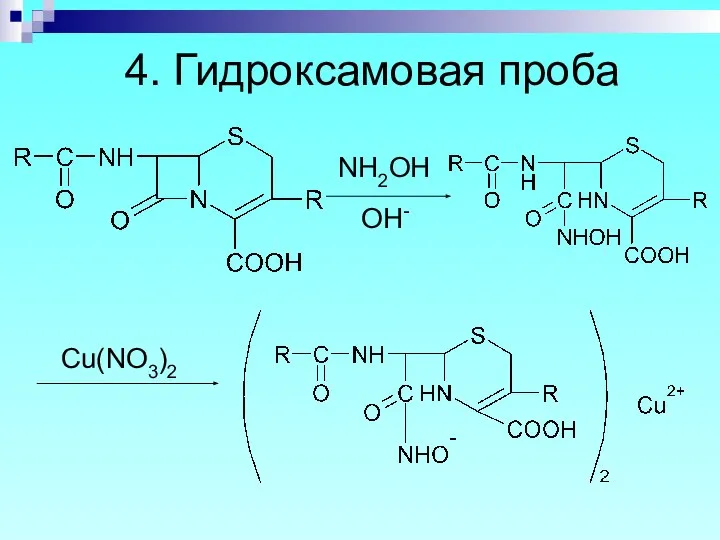
- 69. 4. Гидроксамовая проба Cu(NO3)2 NH2OH OH-
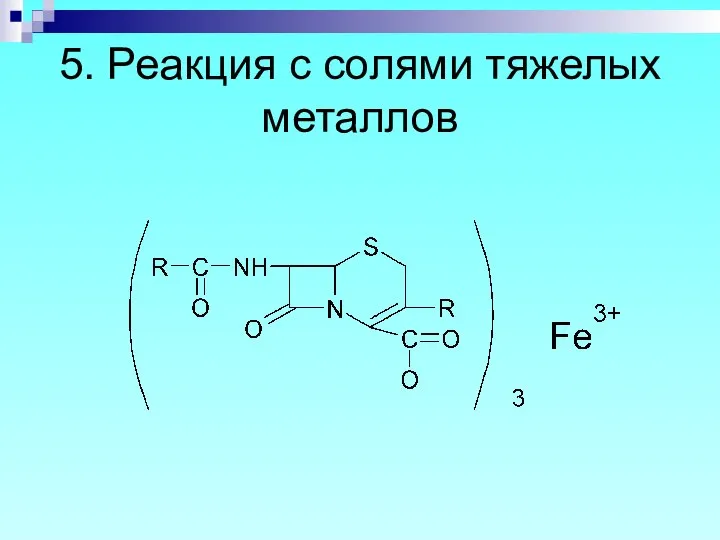
- 70. 5. Реакция с солями тяжелых металлов
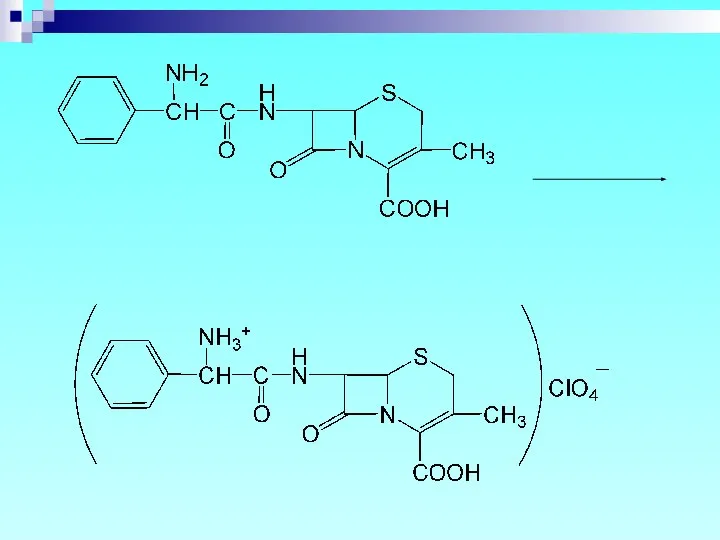
- 71. 6. Цефалексин - на аминокислоту: нингидриновая проба и реакция комплексообразования с ионами Cu2+ в среде уксусной
- 72. Чистота: примеси – ВЭЖХ; наличие специфических примесей – ГЖХ.
- 73. Количественное определение: 1. Обратная йодометрия: 1 эквивалент цефалоспорина требует 4 эквивалента J2. 2. Меркуриметрия. 3. Цефалоспорин
- 75. Хранение: в хорошо укупоренной таре. Применение: антибактериальные (грамположительные и грамотрицательные микроорганизмы).
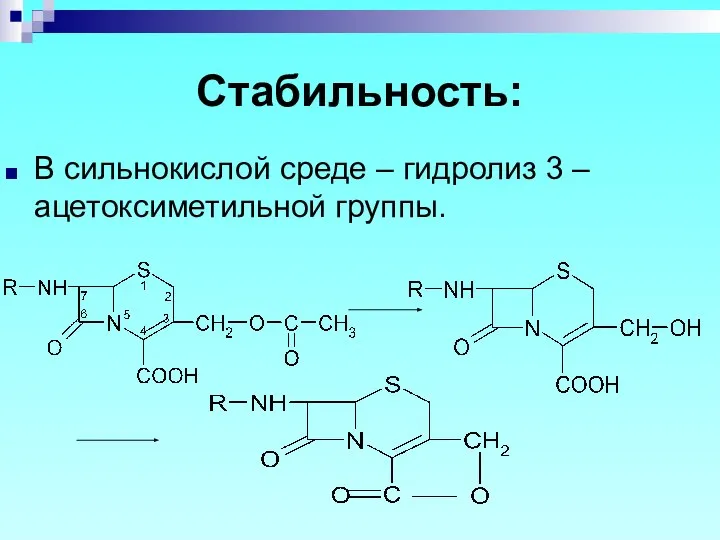
- 76. Стабильность: В сильнокислой среде – гидролиз 3 –ацетоксиметильной группы.
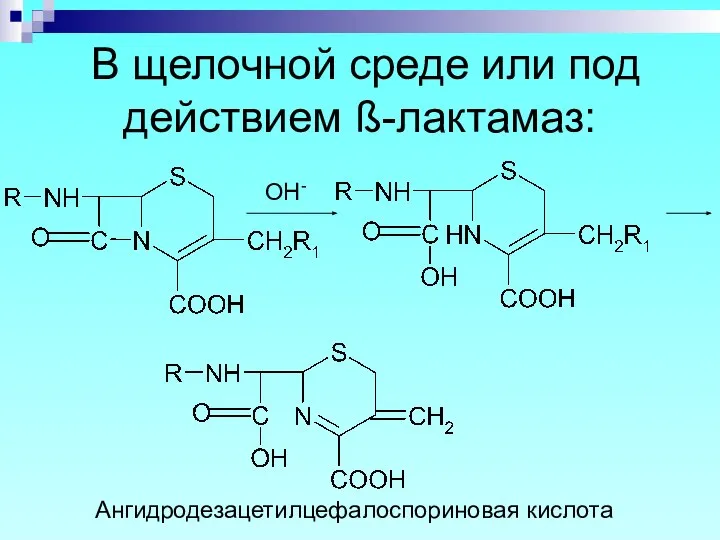
- 77. В щелочной среде или под действием ß-лактамаз: OH- Ангидродезацетилцефалоспориновая кислота
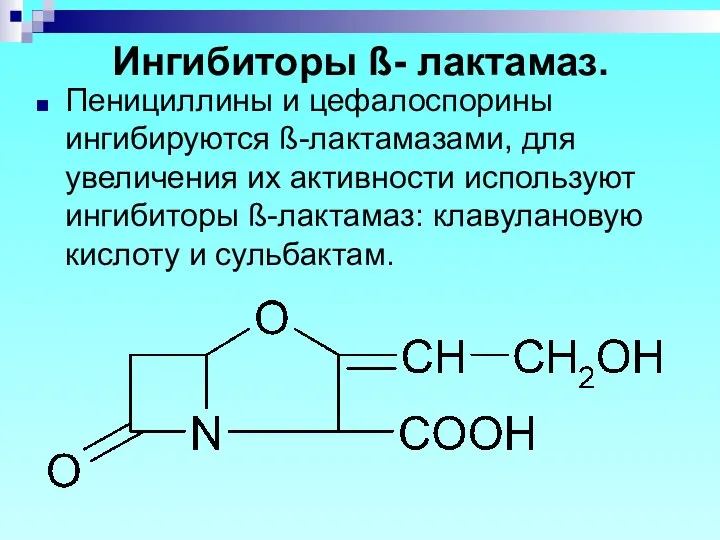
- 78. Ингибиторы ß- лактамаз. Пенициллины и цефалоспорины ингибируются ß-лактамазами, для увеличения их активности используют ингибиторы ß-лактамаз: клавулановую
- 79. Выделяется определенными штаммами микроорганизмов, обладает слабой антибактериальной активностью, но эффективно угнетает ß-лактамазы. В медицине часто применяется
- 80. Калиевая соль клавулановой кислоты. 3-(2-оксилиден)-7-оксо-4-окса-1-азобицикло [3.2.0] гептан-2 карбоксилат калия
- 81. Описание: белый кристаллический порошок, гигроскопичен, легко растворим в воде, мало растворим в этаноле, очень мало растворим
- 82. Идентификация: ИК-спектроскопия; ВЭЖХ; реакция на К+.
- 83. Испытание на чистоту и количественное определение проводят методом ВЭЖХ. Стабильность: водные растворы разлагаются при рН 6,0-6,3.
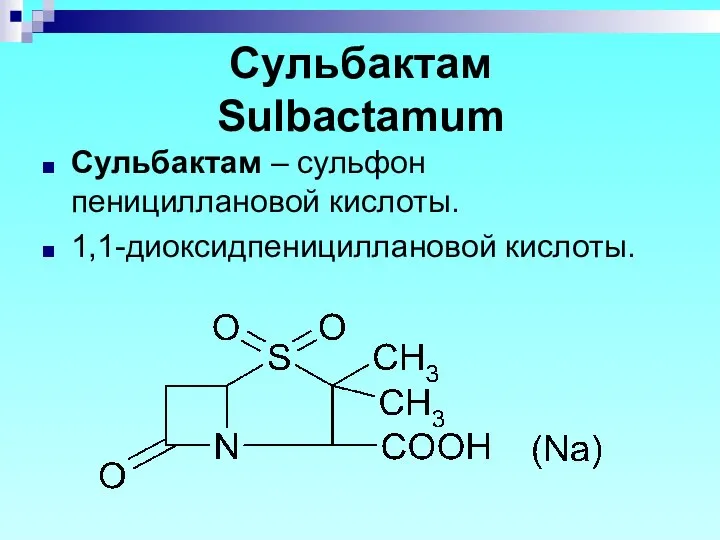
- 84. Сульбактам Sulbactamum Сульбактам – сульфон пенициллановой кислоты. 1,1-диоксидпенициллановой кислоты.
- 85. Описание: белый кристаллический порошок, хорошо растворим в воде, натриевая соль легко растворима в воде, кислотах, мало
- 86. Анализ аналогичен пенициллинам Идентификация: 1. ТСХ 2. Обнаружение Na+ Чистота: ВЭЖХ, прозрачность, цветность
- 87. Количественное определение 1. Спектрофотометрия 2. ВЭЖХ Хранение в сухом, защищённом от света месте
- 88. Уназин Unasyn Уназин состоит из ампициллина натрия и сульбактама натрия (2:1).
- 90. Скачать презентацию




























![Из пенициллинов с помощью химической трансформации можно получить 7 –аминодезацетоксицефалоспорановую кислоту. [O] 7АДЦК](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1241148/slide-63.jpg)







![Калиевая соль клавулановой кислоты. 3-(2-оксилиден)-7-оксо-4-окса-1-азобицикло [3.2.0] гептан-2 карбоксилат калия](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1241148/slide-79.jpg)







 Делимость чисел
Делимость чисел  Vocabulaire. Vidéo deuxième partie. Discussion. Le nouvel édito B1 Leçon 8
Vocabulaire. Vidéo deuxième partie. Discussion. Le nouvel édito B1 Leçon 8 Здоровьесберегающая деятельность в образовательном процессе: проблемы и пути их решения
Здоровьесберегающая деятельность в образовательном процессе: проблемы и пути их решения Разработка бизнес-плана инновационного проекта КОТОВА ОЛЬГА ИВАНОВНА
Разработка бизнес-плана инновационного проекта КОТОВА ОЛЬГА ИВАНОВНА Процессы поддержки и предоставления ИТ-сервисов. (Лекция 3)
Процессы поддержки и предоставления ИТ-сервисов. (Лекция 3) Презентация "Происхождение искусства и формирование основ художественного мышления" - скачать презентации по МХК
Презентация "Происхождение искусства и формирование основ художественного мышления" - скачать презентации по МХК George Bernard Shaw
George Bernard Shaw Командный вид спорта мини-футбол
Командный вид спорта мини-футбол Язык программирования JavaScript
Язык программирования JavaScript Методология научных исследований
Методология научных исследований Товарищество собственников жилья «Вайнера 60»
Товарищество собственников жилья «Вайнера 60» Библейские сюжеты в творчестве русских художников
Библейские сюжеты в творчестве русских художников Cristiano Ronaldo
Cristiano Ronaldo Изучение влияния физической культуры и спорта на формирование ЗОЖ у подростков
Изучение влияния физической культуры и спорта на формирование ЗОЖ у подростков Устройство систем теплоснабжения зданий
Устройство систем теплоснабжения зданий Обязательственное право. Судебное разбирательство
Обязательственное право. Судебное разбирательство Муниципальное учреждение «Управление образования» Нурлатского муниципального района РТ МОУ «Средняя общеобразовательная школа
Муниципальное учреждение «Управление образования» Нурлатского муниципального района РТ МОУ «Средняя общеобразовательная школа  Презентация мероприятия по совершенствованию системы управления
Презентация мероприятия по совершенствованию системы управления  Казахстанско-Российский медицинский университет Кафедра общей и клинической фармакологии
Казахстанско-Российский медицинский университет Кафедра общей и клинической фармакологии  Пока горит свеча - презентация для начальной школы
Пока горит свеча - презентация для начальной школы «МАТЕРИАЛЫ ДЛЯ ПЛОМБИРОВАНИЯ КОРНЕВЫХ КАНАЛОВ»
«МАТЕРИАЛЫ ДЛЯ ПЛОМБИРОВАНИЯ КОРНЕВЫХ КАНАЛОВ» ЗОЖ презентация_
ЗОЖ презентация_ Проект практической эстонско-белорусской транскрипции
Проект практической эстонско-белорусской транскрипции Повреждение костей предплечья, запястья и кисти
Повреждение костей предплечья, запястья и кисти Museo del Prado
Museo del Prado Урок №3 Рисование по представлению. Осенние деревья Изобразительное искусство 2 класс
Урок №3 Рисование по представлению. Осенние деревья Изобразительное искусство 2 класс Pressure
Pressure  Принятие управленческих решений
Принятие управленческих решений