Содержание
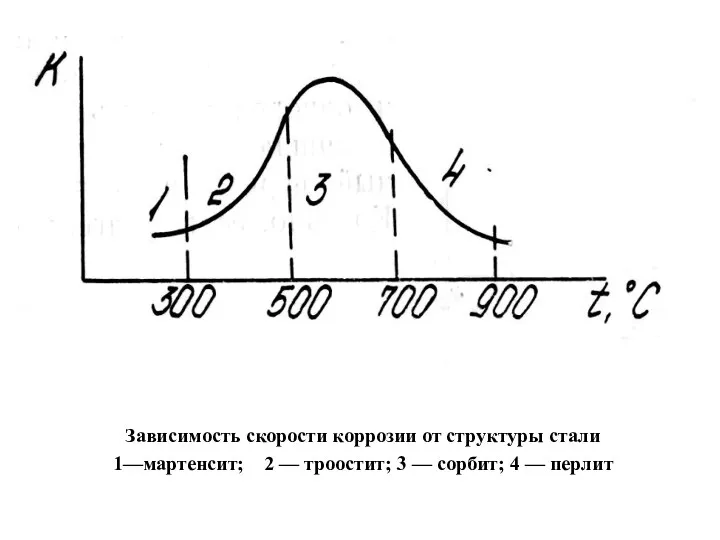
- 2. Зависимость скорости коррозии от структуры стали 1—мартенсит; 2 — троостит; 3 — сорбит; 4 — перлит
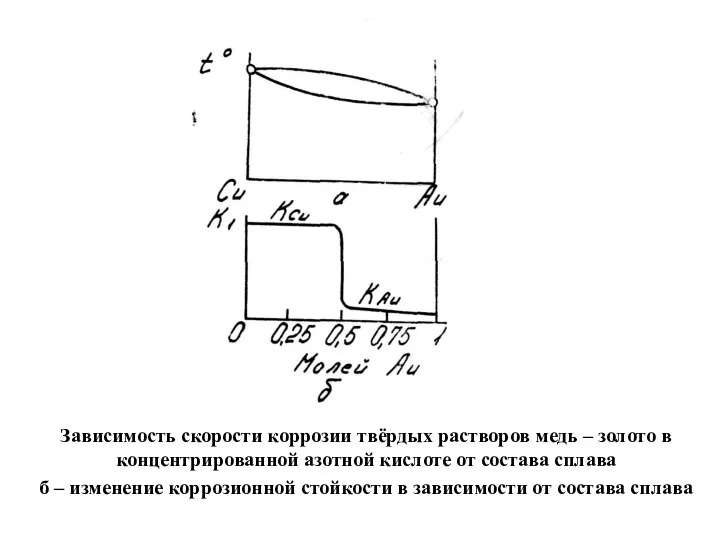
- 3. Зависимость скорости коррозии твёрдых растворов медь – золото в концентрированной азотной кислоте от состава сплава б
- 4. Зависимость скорости коррозии от рН среды а – благородные металлы Ag, Au, Pt; б – малостойкие
- 5. Зависимость скорости коррозии железа от концентрации кислорода (а) и температуры (б)
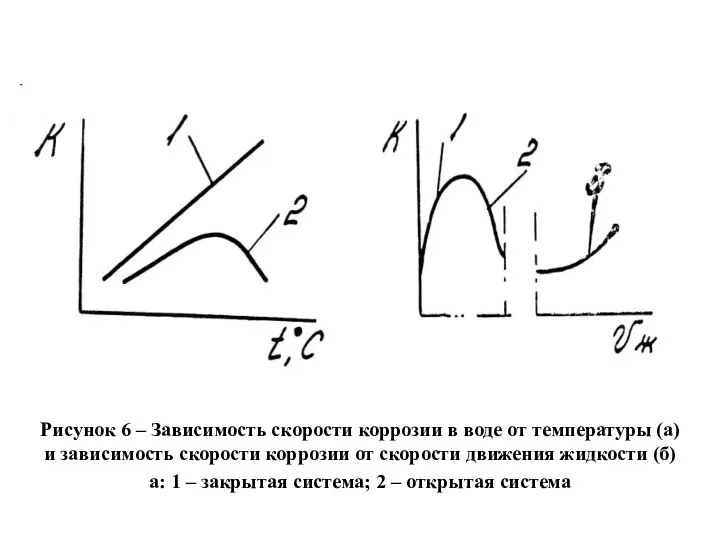
- 6. Рисунок 6 – Зависимость скорости коррозии в воде от температуры (а) и зависимость скорости коррозии от
- 7. Схема газовой коррозии
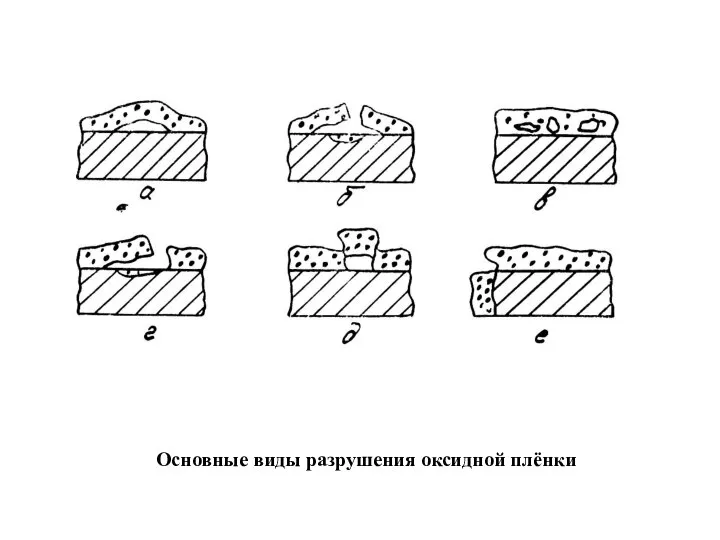
- 8. Основные виды разрушения оксидной плёнки
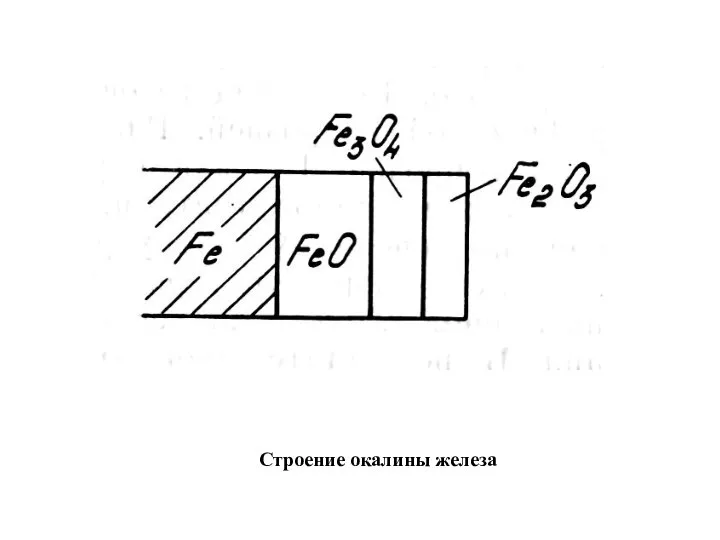
- 9. Строение окалины железа
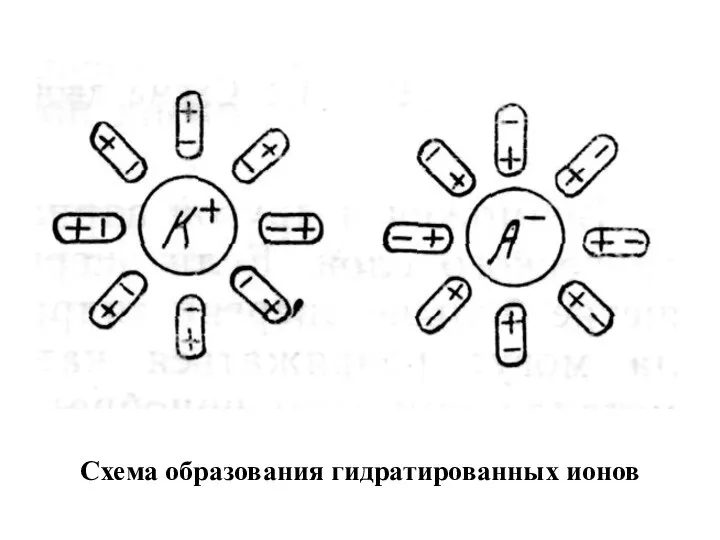
- 10. Схема образования гидратированных ионов
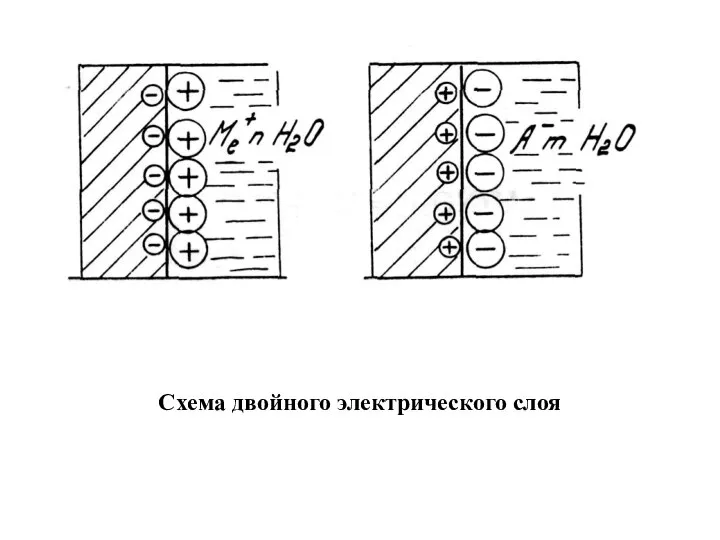
- 11. Схема двойного электрического слоя
- 12. Стандартные электродные потенциалы
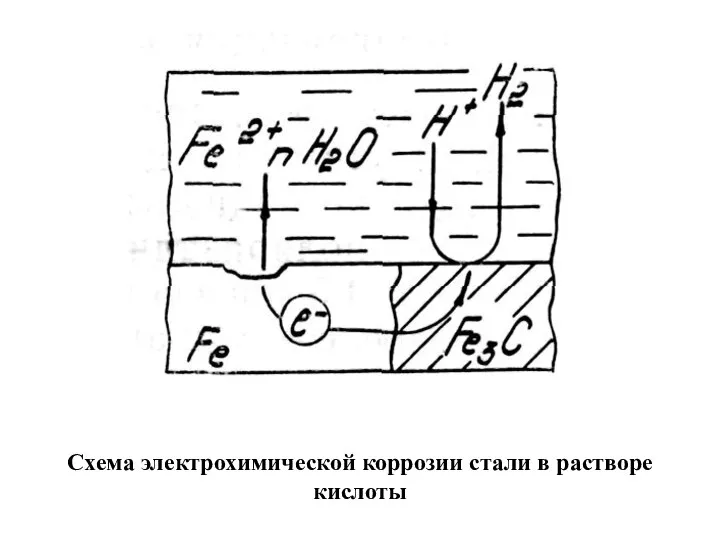
- 13. Схема электрохимической коррозии стали в растворе кислоты
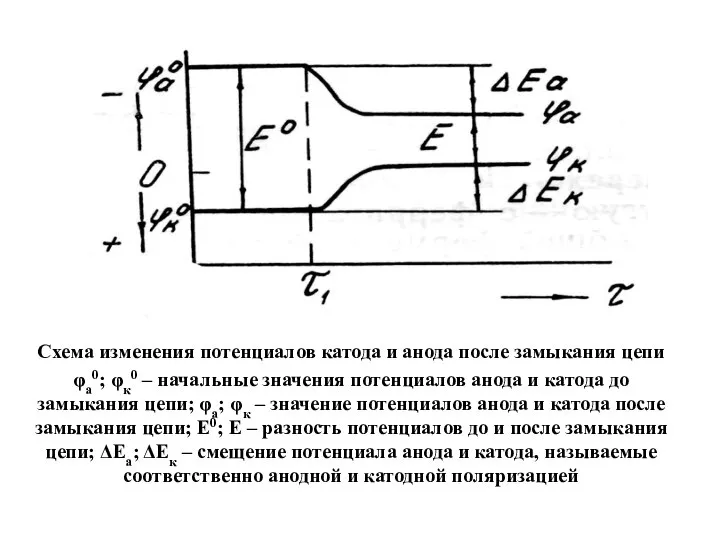
- 14. Схема изменения потенциалов катода и анода после замыкания цепи φа0; φк0 – начальные значения потенциалов анода
- 15. Потенциал водородного и кислородного электродов в зависимости от рН среды
- 16. Коррозионная диаграмма Эванса φа; φк – начальное положение потенциалов анода и катода (бесконечное сопротивление, ток отсутствует);
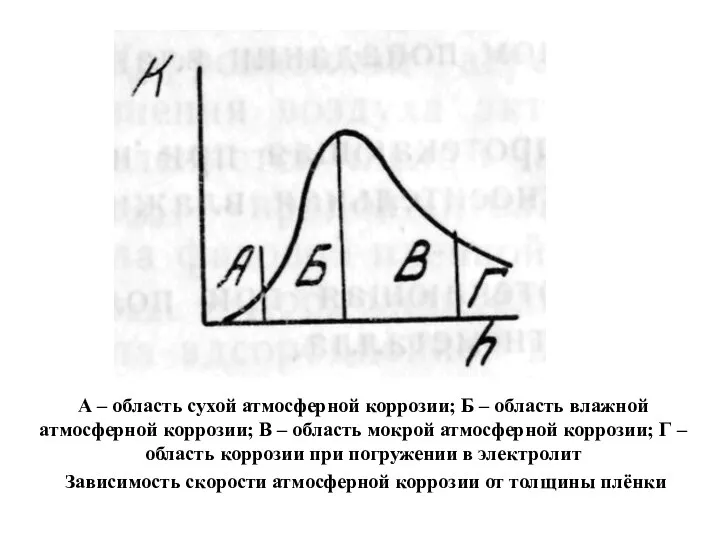
- 17. А – область сухой атмосферной коррозии; Б – область влажной атмосферной коррозии; В – область мокрой
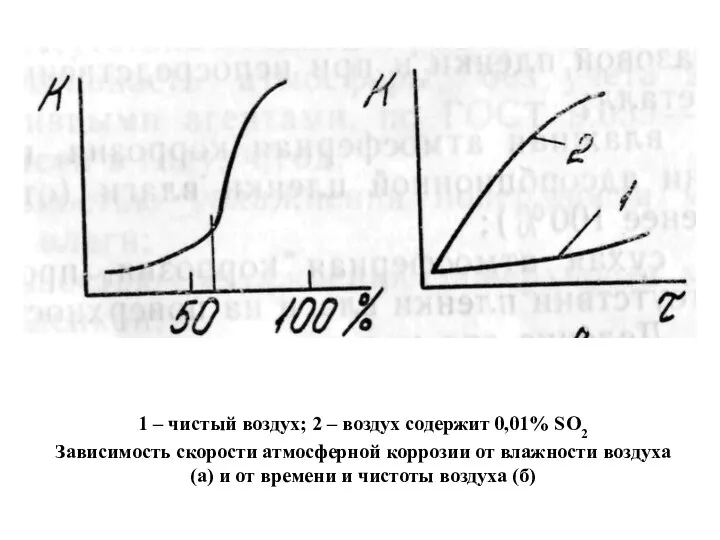
- 18. 1 – чистый воздух; 2 – воздух содержит 0,01% SO2 Зависимость скорости атмосферной коррозии от влажности
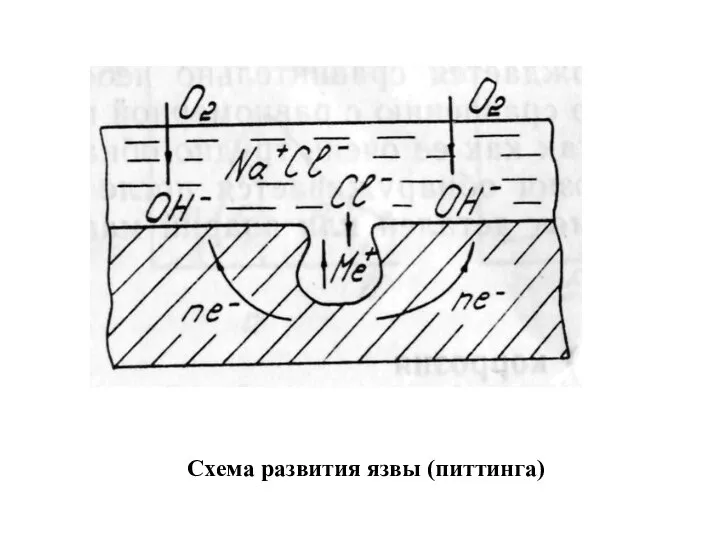
- 19. Схема развития язвы (питтинга)
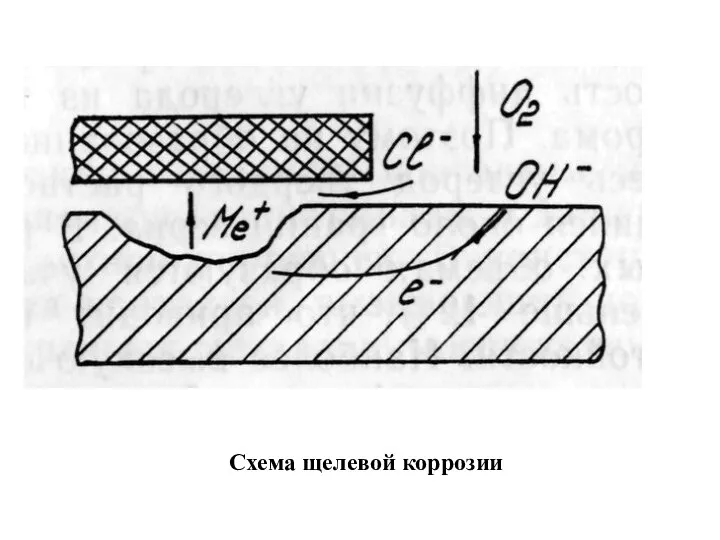
- 20. Схема щелевой коррозии
- 21. Образование ножевой коррозии
- 22. Заклёпочные соединения а – соединение медных листов стальными заклёпками; б – соединениестальных листов медными заклёпками
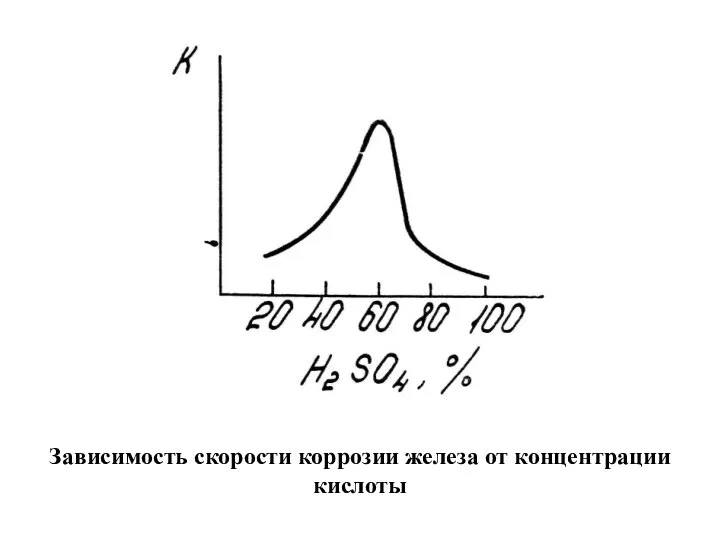
- 23. Зависимость скорости коррозии железа от концентрации кислоты
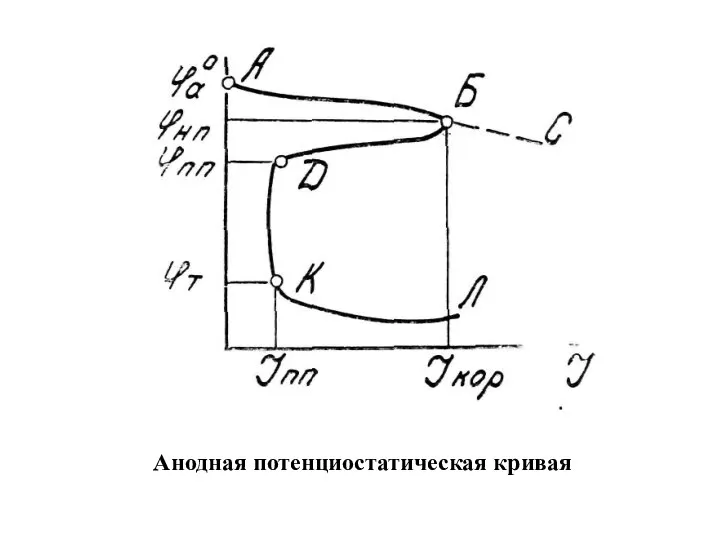
- 24. Анодная потенциостатическая кривая
- 26. Скачать презентацию








 Государственная служба в системе управления
Государственная служба в системе управления Структура поверхности и ее физические свойства
Структура поверхности и ее физические свойства  Археологічний музей Іракліону
Археологічний музей Іракліону Основы языка Visual Basic. Выражения
Основы языка Visual Basic. Выражения Франсиско де Гойя Биография и творчество художника
Франсиско де Гойя Биография и творчество художника Благотворительный забег "достигая цели!" В честь дня железнодорожника
Благотворительный забег "достигая цели!" В честь дня железнодорожника Профессиональная этика таможенника
Профессиональная этика таможенника Проект новых стандартов: компетентностный подход
Проект новых стандартов: компетентностный подход Спорт в СПбГУ
Спорт в СПбГУ Сортувальна Гірка. АССКРП
Сортувальна Гірка. АССКРП Торговые организации Башкортостана
Торговые организации Башкортостана Современные системы физического воспитания
Современные системы физического воспитания ФГОС СО
ФГОС СО Инструменты для продвижения и популяризации ВФСК ГТО на территории Красноярского края
Инструменты для продвижения и популяризации ВФСК ГТО на территории Красноярского края ДЕЙСТВИЯ И РЕШЕНИЯ ПРОКУРОРА
ДЕЙСТВИЯ И РЕШЕНИЯ ПРОКУРОРА Урок в соответствии с ФГОС Н.А. Разагатова, МОУ ДПО (ПК) «Центр развития образования г.о. Самара»
Урок в соответствии с ФГОС Н.А. Разагатова, МОУ ДПО (ПК) «Центр развития образования г.о. Самара»  Инновационная модель управления таможенными органами. Тема 10
Инновационная модель управления таможенными органами. Тема 10 Булки не растут на деревьях
Булки не растут на деревьях Воздействие электрического тока на организм человека Выполнила ученица 8 а класса МОУ «СОШ № 57», г. Оренбург Кисе
Воздействие электрического тока на организм человека Выполнила ученица 8 а класса МОУ «СОШ № 57», г. Оренбург Кисе Языки, компиляторы, эмуляторы
Языки, компиляторы, эмуляторы закалдованые цыфры - презентация для начальной школы
закалдованые цыфры - презентация для начальной школы Теория локальных цивилизаций Освальда Шпенглера
Теория локальных цивилизаций Освальда Шпенглера Острый коронарный синдром
Острый коронарный синдром Налогообложение природопользования Доц. Каширина М.В. Цель дисциплины – дать специальные знания в области системы налогообл
Налогообложение природопользования Доц. Каширина М.В. Цель дисциплины – дать специальные знания в области системы налогообл Язык C++
Язык C++ Реалізація державної політики у сфері державної реєстрації фізичних осіб, департаментом реєстраційних послуг Запорізької ради
Реалізація державної політики у сфері державної реєстрації фізичних осіб, департаментом реєстраційних послуг Запорізької ради Методические рекомендации по проведению мероприятий благоустройства дворовых территорий. Программа «Башкирские дворики»
Методические рекомендации по проведению мероприятий благоустройства дворовых территорий. Программа «Башкирские дворики» причины финансового кризиса 2008 года в РФ и пути выхода Карташова Галина Т-093
причины финансового кризиса 2008 года в РФ и пути выхода Карташова Галина Т-093